12.1人类重要的营养物质同步练习-2021-2022学年九年级化学人教版下册(含解析)
文档属性
| 名称 | 12.1人类重要的营养物质同步练习-2021-2022学年九年级化学人教版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 280.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-02 00:00:00 | ||
图片预览



文档简介
12.1、人类重要的营养物质
一、选择题(共16题)
1.下列食物中,富含糖类的是( )
A.鸡蛋
B.豆油
C.黄瓜
D.馒头
2.杜阮凉瓜是江门市乃至省、港、澳地区知名的农产品,该美食主要富含的营养素是( )
A.糖类 B.油脂 C.无机盐 D.维生素
3.哈尔滨老鼎丰糕点中含有最多的营养素是( )
A.糖类 B.蛋白质
C.维生素 D.无机盐
4.在端午节我们包粽子时准备了如下食材:糯米、瘦肉、绿豆、花生,其中瘦肉富含的营养素主要是( )
A.维生素 B.蛋白质 C.油脂 D.糖类
5.化学元素与人体健康息息相关。下列关于元素影响人体健康的表述不正确的是( )
A.缺氟易产生龋齿
B.缺硒会引起甲状腺肿大
C.老年人缺钙会导致骨质疏松
D.长期缺铁会引发缺铁性贫血
6.下列食物中富含糖类的是( )
A.大米 B.花生油 C.白菜 D.牛肉
7.“我可喜欢吃虾了”,因为它们富含( )
A.蛋白质 B.维生素 C.油脂 D.糖
8.下列有关实验的现象描述正确的是( )
A.向加碘食盐溶液中滴加淀粉,溶液变蓝
B.打开浓盐酸的瓶塞时,瓶口冒白烟
C.在鸡蛋清溶液中加几滴浓硝酸,微热,出现白色沉淀
D.10%葡萄糖溶液中加入新制的氢氧化铜加热至沸,出现砖红色沉淀
9.利用化学知识对下列说法进行判断,其中正确的是( )
A.油脂会让人长胖,应禁止食用
B.绿色植物合成葡萄糖的过程中将太阳能转化为化学能
C.取样尿液与硫酸铜溶液混合煮沸,可以检验尿液中是否含有葡萄糖
D.向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀是化学变化
10.下列人体所必需的元素中,缺乏会引起贫血的是( )
A.铁 B.钙 C.碘 D.锌
11.根据你所学的化学知识和生活经验,下列说法中错误的是( )
A.滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂具有乳化功能
B.利用中和反应的原理,可用含有氢氧化铝、氢氧化镁、碳酸氢钠等的药物除去过多的胃酸
C.蛋白质、糖类和油脂都是人体内的供能物质
D.做饭时,燃气灶的火焰呈黄色或橙色,此时需要调节炉具的进风口
12.河南美食誉天下,下列食品或食材富含蛋白质的是( )
A.灵宝苹果 B.禹州粉条 C.怀庆驴肉 D.淮阳黄花菜
13.下列富含淀粉的食物是( )
A.猪肉 B.白菜 C.菜籽油 D.米饭
14.平时要常吃一些糙米的主要原因是为了摄取 ( )
A.油脂 B.葡萄糖 C.维生素 D.蛋白质
15.除了茶文化以外,中国其他饮食文化同样博大精深,“狮子头”是中国八大菜系之苏中典的菜品,观察图片,选出下列关于狮子头的描述中错误的一项( )
A.青菜心可以为人体提供维生素
B.狮子头的主要营养蛋白质在肠胃中被人体直接吸收
C.减肥期间不宜多食狮子头
D.狮子头中的精瘦肉、鸡蛋,淀粉等都能为人体提供能量
16.下列原因解释不正确的是( )
A.豆浆中加盐卤或石膏制成豆腐,因为豆浆中的蛋白质发生了变性
B.水体发生赤潮现象,因为水体中氮、磷元素含量增高
C.打开啤酒瓶盖,有大量泡沫溢出,因为气体的溶解度随着压强的减小而减小
D.食盐在热水中比在冷水中溶解得快,因为温度越高,微粒运动越快
二、非选择题(共8题)
17.米、面、蔬菜、肉、植物油是烹饪食品时的主要原料。
(1)以上原料中富含蛋白质的是_______。
(2)大米、面粉等在温度和湿度较高的环境下容易滋生对人体有危害的_______(填序号)。
A.黄曲霉素 B.甲醛 C.一氧化碳
18.某品牌“自热米饭”的食品成分包括:米饭、鸡肉、胡萝卜等。“自热米饭”的自加热原理为:饭盒夹层的水与生石灰接触,反应放出大量的热。
(1)米饭、鸡肉、胡萝卜中富含糖类的是______。
(2)写出自加热原理的化学方程式______。
19.生活中处处有化学。
(1)人类六大营养素中,能供给人体能量的有油脂、蛋白质和________。
(2)化肥可提供农作物生长需要的营养元素,尿素[化学式为CO(NH2)2]属于______(选填“氮”、“磷”或“钾”或“复合”)肥。
20.化学与人类的生产、生活密切相关。
(1)化学与健康。
①钙能强壮骨骼,在人体中属于__________(填“常量元素”或“微量元素”)。
②在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,该反应的化学方程式为______________________。
(2)化学与资源。
①在空气的成分中,稀有气体所占比率虽然很小,但有广泛的用途。写出氦气的化学式,并标出氦元素的化合价:__________。
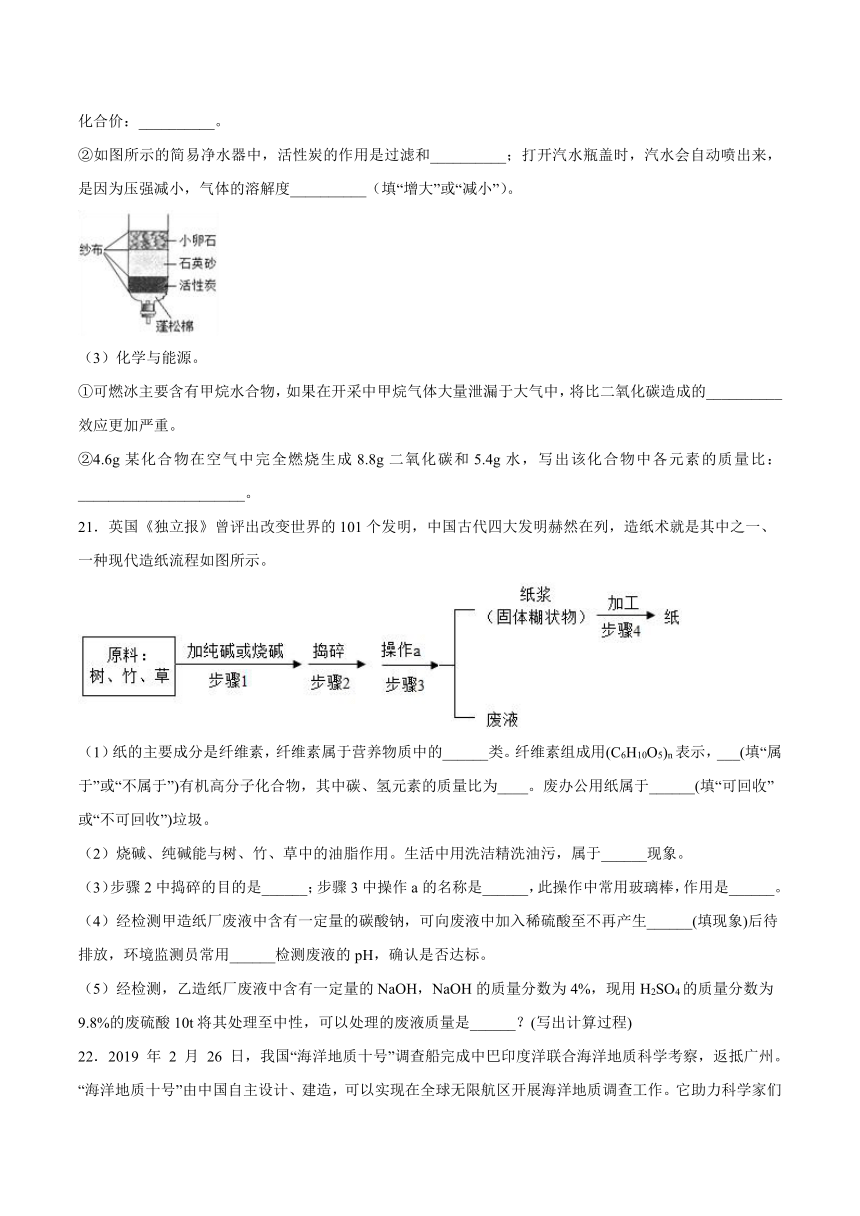
②如图所示的简易净水器中,活性炭的作用是过滤和__________;打开汽水瓶盖时,汽水会自动喷出来,是因为压强减小,气体的溶解度__________(填“增大”或“减小”)。
(3)化学与能源。
①可燃冰主要含有甲烷水合物,如果在开采中甲烷气体大量泄漏于大气中,将比二氧化碳造成的__________效应更加严重。
②4.6g某化合物在空气中完全燃烧生成8.8g二氧化碳和5.4g水,写出该化合物中各元素的质量比:______________________。
21.英国《独立报》曾评出改变世界的101个发明,中国古代四大发明赫然在列,造纸术就是其中之一、一种现代造纸流程如图所示。
(1)纸的主要成分是纤维素,纤维素属于营养物质中的______类。纤维素组成用(C6H10O5)n表示,___(填“属于”或“不属于”)有机高分子化合物,其中碳、氢元素的质量比为____。废办公用纸属于______(填“可回收”或“不可回收”)垃圾。
(2)烧碱、纯碱能与树、竹、草中的油脂作用。生活中用洗洁精洗油污,属于______现象。
(3)步骤2中捣碎的目的是______;步骤3中操作a的名称是______,此操作中常用玻璃棒,作用是______。
(4)经检测甲造纸厂废液中含有一定量的碳酸钠,可向废液中加入稀硫酸至不再产生______(填现象)后待排放,环境监测员常用______检测废液的pH,确认是否达标。
(5)经检测,乙造纸厂废液中含有一定量的NaOH,NaOH的质量分数为4%,现用H2SO4的质量分数为9.8%的废硫酸10t将其处理至中性,可以处理的废液质量是______?(写出计算过程)
22.2019 年 2 月 26 日,我国“海洋地质十号”调查船完成中巴印度洋联合海洋地质科学考察,返抵广州。“海洋地质十号”由中国自主设计、建造,可以实现在全球无限航区开展海洋地质调查工作。它助力科学家们对海底世界的新认知,新发现与新开发。
(1)人类正在运用各种方法,开采、提取多种海洋资源。
①海水化学资源:工业上常采用___法从海水中获取大量淡水,解决淡水危机。利用_______的基本原理从海水中提取大量盐类,用作化工原料。
②海底矿产资源:海底蕴含着煤、石油、天然气等数百种矿产资源。
③海洋鱼类、海参、龙虾富含的营养素是_______________。
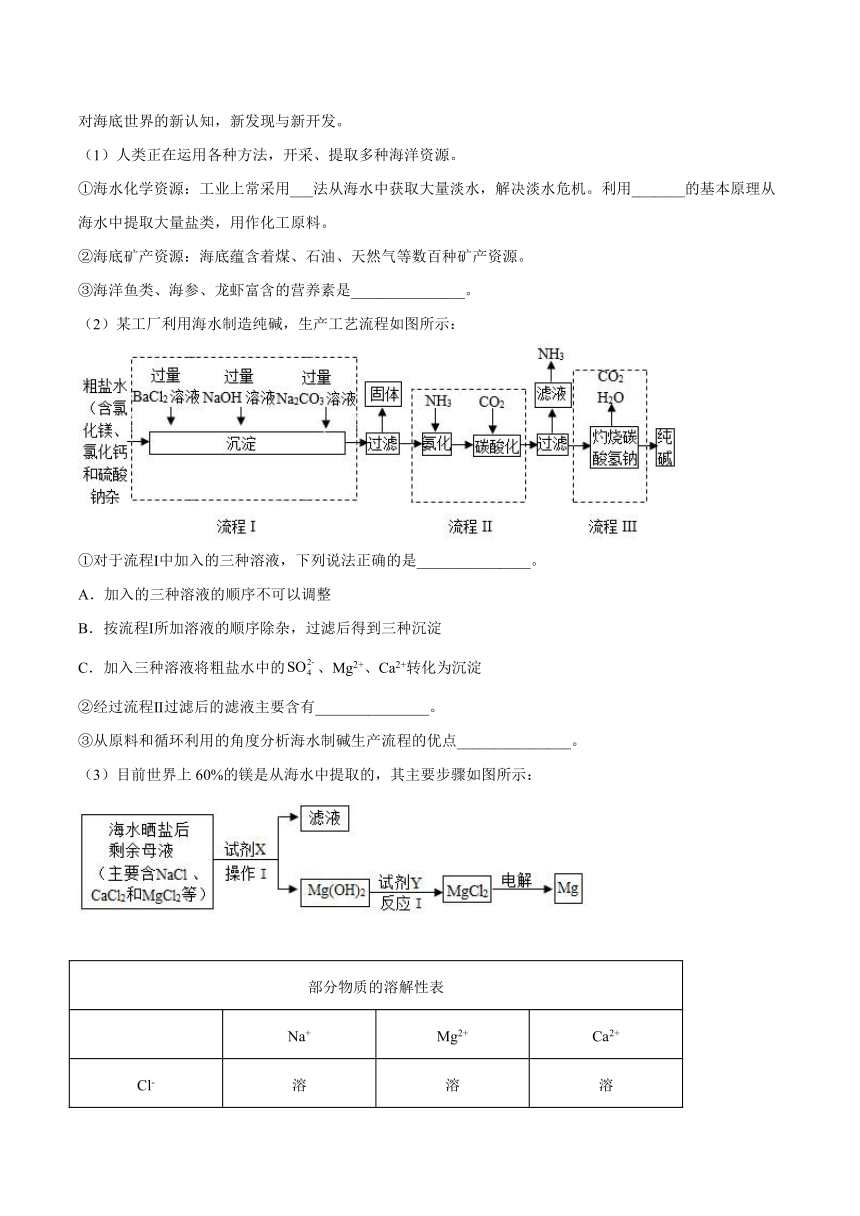
(2)某工厂利用海水制造纯碱,生产工艺流程如图所示:
①对于流程Ⅰ中加入的三种溶液,下列说法正确的是_______________。
A.加入的三种溶液的顺序不可以调整
B.按流程Ⅰ所加溶液的顺序除杂,过滤后得到三种沉淀
C.加入三种溶液将粗盐水中的、Mg2+、Ca2+转化为沉淀
②经过流程Ⅱ过滤后的滤液主要含有_______________。
③从原料和循环利用的角度分析海水制碱生产流程的优点_______________。
(3)目前世界上60%的镁是从海水中提取的,其主要步骤如图所示:
部分物质的溶解性表
Na+ Mg2+ Ca2+
Cl- 溶 溶 溶
OH- 溶 不 微
溶 微 不
①已知部分化工原料的市场价格为:烧碱3200元/吨,熟石灰1200元/吨。工业上为了达到更高的生产效率效益,你认为如图中的试剂X应该选择上述化工原料中的____更适宜。
②加入试剂X后,发生反应的化学方程式为_______。
③综合如图和表中的信息,试分析工业上通常不选择碳酸钠作试剂X的理由___。
23.(1)目前,新冠肺炎疫情全球蔓延,消毒剂的使用在防疫过程中起着重要作用。
①75%酒精溶液。请用学过的知识解释75%酒精溶液能杀死冠状病毒的原因:________。
②威王消毒液。威王消毒液的主要成分是对氯间二甲苯酚,对氯间二甲苯酚的化学式是C8H9ClO,对氯间二甲苯酚属于______(填“无机物”或“有机物”)。
③84消毒液。84消毒液的主要成分是次氯酸钠NaClO,标出次氯酸钠中氯元素的化合价_______。
④过氧乙酸溶液。0.2%的过氧乙酸溶液常用于空气和地面消毒。某校要配制0.2%的过氧乙酸消毒溶液100kg,需要10%的过氧乙酸溶液_______kg。
(2)小明同学向石灰石和稀盐酸制备CO2后过滤得到的滤液中滴加5.3%的Na2CO3溶液,得到的沉淀质量随碳酸钠溶液的质量的变化如图所示:
①过滤所得滤液中的阳离子______。
②a点对应的溶液pH_____7(填“>”、“=”或“<”)。
③产生沉淀所消耗的碳酸钠溶液质量是_______g。
④求m的值。_____(写出计算过程)
24.中国有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。
(1)海洋为我们提供了营养丰富的食材。鱼虾富含的 ________ (填一种营养素)是机体生长及修补受损组织的主要原料,海带富含的 _____ (填元素符号)可以预防甲状腺肿大。
(2)我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于 _______ (选填“纯净物”或“混合物”)。有科学家开采得到一种天然气水合物样品。取50.0克样品放置在一密闭容器内,该样品迅速转化为甲烷气体和水,将甲烷气体分离并完全燃烧,得到17.6克二氧化碳。该天然气水合物样品中甲烷的质量分数为 _____ 。(写出完整的计算过程)
(3)海水淡化可缓解淡水资源匮乏问题。
①水变成水蒸气的过程中,发生变化的是 _______ (填字母序号)。
A分子个数 B分子质量 C分子间隔 D分子种类
②从海水中获得淡水可采取的方法是 ________________ (填“过滤”“吸附”或“蒸馏”)。
(4)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减小。
①根据海水pH变化趋势判断:2000年时海水呈 ________ 性。
②“海洋酸化”的原因可用化学方程式表示为 ____ 。
参考答案
1.D
【详解】
A、鸡蛋中富含有蛋白质,不符合题意;
B、豆油中富含有油脂,不符合题意;
C、黄瓜中富含有维生素,不符合题意;
D、馒头中富含有淀粉,属于糖类,符合题意。
故选:D。
2.D
【详解】
蔬菜水果中主要营养素是维生素,所以杜阮凉瓜主要富含的营养素是维生素。
故选:D。
3.A
【详解】
哈尔滨老鼎丰糕点的主要成分是面粉,其中含有淀粉,属于糖类,且糕点中的食品添加剂也有糖类,故哈尔滨老鼎丰糕点中含有最多的营养素是糖类,故选A。
4.B
【详解】
瘦肉中富含蛋白质,故选B。
5.B
【详解】
A、缺氟易产生龋齿,A正确;
B、缺硒会引起表皮角质化和癌症,缺碘才会引起甲状腺肿大,B不正确;
C、老年人缺钙会导致骨质疏松,C正确;
D、长期缺铁会引发缺铁性贫血,D正确。故选B。
6.A
【详解】
A、大米中富含糖类;
B、花生油中富含油脂;
C、白菜中富含维生素;
D、牛肉干中富含蛋白质。
故选:A。
7.A
【详解】
A、蛋白质主要存在于动物肌肉、奶类、蛋类、鱼类及花生和豆类的种子或制品中,虾中主要含蛋白质,所以正确;
B、维生素主要存在于蔬菜和水果中,所以错误;
C、油脂主要存在于动物脂肪和花生、大豆、芝麻和种子中,所以错误;
D、糖类主要存在于植物的种子和块茎中,所以错误。
故选A。
8.D
【详解】
A、淀粉遇碘单质变蓝色,而加碘食盐溶液中不含碘单质,向加碘食盐溶液中滴加淀粉,无明显变化,故选项A错误;
B、浓盐酸具有挥发性,打开浓盐酸的瓶塞时,瓶口冒白雾,而不是白烟,故选项B错误;
C、鸡蛋清溶液中含有蛋白质,加入浓硝酸,微热后,出现黄色沉淀,故选项C错误;
D、在新配制的氢氧化铜中加入葡萄糖溶液,加热到沸腾,生成有砖红色的氧化亚铜沉淀,会观察到产生红色沉淀,故选项D正确。
故选D。
9.B
【详解】
A、油脂是人体的营养素之一,要合理食用,故此答案错误。
B、植物的光合作用是能量转化过程,是太阳能转化为化学能,故此答案正确。
C、葡萄糖与新制的氢氧化铜在加热的条件下,可生成葡萄糖酸和水,同时生成砖红色沉淀氧化亚铜,据此可以检验葡萄糖的存在,故此选项错误。
D、向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀是盐析现象,不是蛋白质变性导致,故此选项错误。
故选:B。
10.A
【详解】
人体必须的元素中,缺铁容易引起贫血,缺少钙元素会引起骨质疏松症;缺少碘元素会造成甲状腺肿大;缺少锌元素会发育迟缓,食欲不振;故答案选择A。
11.B
【详解】
A、滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂具有乳化功能,不符合题意;
B、中和反应是酸和碱反应生成盐和水的反应,碳酸氢钠是盐,不是中和反应,符合题意;
C、蛋白质、糖类和油脂都是人体内的供能物质,不符合题意;
D、做饭时,燃气灶的火焰呈黄色或橙色,是氧气不足的表现,此时需要调节炉具的进风口,增大氧气的进入量,不符合题意。故选B。
12.C
【解析】
A、水果富含维生素;B、粉条的主要成分是淀粉,淀粉为糖类物质;C、驴肉富含蛋白质;D、蔬菜富含维生素。故选C。
13.D
【详解】
富含淀粉的食物是D. 米饭。A. 猪肉富含,蛋白质。B. 白菜,富含维生素。 C. 菜籽油,富含脂肪。
14.C
【详解】
一些糙米中含有维生素,故选C。
15.B
【详解】
A、青菜心富含维生素,故选项正确;
B、胃中含有胃蛋白酶,能初步分解蛋白质,蛋白质不能在肠胃中被人体直接吸收,故选项错误;
C、狮子头富含 蛋白质和油脂,减肥期间不宜多食狮子头,故选项正确;
D、狮子头中的精瘦肉、鸡蛋,淀粉等都能为人体提供能量,故选项正确。
故选:B。
16.A
【详解】
A、向蛋白质溶液中加入浓的无机盐溶液,可使蛋白质的溶解度降低而从溶液中析出,这种作用叫做盐析;这样析出的蛋白质在继续加水时,仍能溶解,并不影响原来蛋白质的性质,蛋白质并没有失去活性,选项说法错误;
B、水体中氮磷元素含量过多会造成水生藻类的疯狂生长,导致水质恶化,造成“水华”或“赤潮”现象的发生,选项说法正确;
C、打开啤酒瓶盖,压强变小,有大量泡沫溢出,这是因为气体的溶解度随着压强的减小而减小,选项说法正确;
D、粒子是在不断运动的,温度越高,粒子运动速率越快,所以食盐在热水中比在冷水中溶解得快,选项说法正确。
故选A。
17. 肉 A
【解析】(1)根据蛋白质的食物来源分析;
(2)根据潮湿环境下容易发生霉变分析。
解:(1)动物肌肉、皮肤、毛发、蹄、角、蛋清、大豆、花生富含蛋白质。故填:肉;
(2)大米、面粉等在温度和湿度较高的环境下容易发生霉变,滋生含有黄曲霉素的黄曲霉菌,故填:A。
18.
(1)米饭
(2)
【分析】
本题考查营养物质。
(1)米饭中富含糖类、鸡肉红富含蛋白质、胡萝卜中富含维生素,故填:米饭;
(2)氧化钙和水反应生成氢氧化钙:。
19.糖类 氮
【详解】
(1)人类六大营养素中,能供给人体能量的有蛋白质、糖类、油脂,故填糖类;
(2)从尿素的化学式中看出,尿素中含有氮元素,尿素属于氮肥,故填氮。
20. 常量元素 C6H12O6 + 6O26H2O + 6CO2 吸附 减小 温室 碳、氢、氧元素的质量比等于12︰3︰8(合理叙述均可)
【解析】(1)化学与健康。①钙能强壮骨骼,在人体中属于常量元素。 ②在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,该反应的化学方程式为C6H12O6 + 6O26H2O + 6CO2 。(2)化学与资源。①在空气的成分中,稀有气体所占比率虽然很小,但有广泛的用途。写出氦气的化学式,并标出氦元素的化合价: 。②如图所示的简易净水器中,活性炭的作用是过滤和吸附;打开汽水瓶盖时,汽水会自动喷出来,是因为压强减小,气体的溶解度减小。(3)化学与能源。①可燃冰主要含有甲烷水合物,如果在开采中甲烷气体大量泄漏于大气中,将比二氧化碳造成的温室效应更加严重。②4.6g某化合物在空气中完全燃烧生成8.8g二氧化碳和5.4g水,写出该化合物中各元素的质量比:8.8g× ×100%=2.4g. 5.4g××100%=0.6g. 4.6g-2.4g-0.6g=1.6g. 该化合物中碳、氢、氧元素各元素的质量比:2.4∶0.6∶1.6=12︰3︰8.
21.
(1) 糖类 属于 36:5 可回收
(2)乳化
(3) 增大反应物的接触面积 过滤 引流
(4) 气泡 pH试纸或pH计
(5)20t
解:设处理废液的质量为x。
x=20t
答:可处理20t。
【分析】
(1)
纤维素属于糖类;纤维素的相对分子质量达到几万、甚至几十万,所以属于有机高分子化合物;纤维素由碳、氢、氧三种元素组成;其中碳、氢元素的质量之比=(12×6×n):(1×10×n)=36:5;废办公用纸可以再利用,属于可回收垃圾;故填:糖类;属于;36:5;可回收。
(2)
洗洁精能将油污乳化,属于乳化现象;故填:乳化。
(3)
步骤2中捣碎的目的是增大反应物的接触面积;步骤3中操作a是将固体和液体分离,因此是过滤操作;此操作中常用玻璃棒,作用是引流;故填:增大反应物的接触面积;过滤;引流。
(4)
碳酸钠与硫酸反应生成硫酸钠钠、水二氧化碳,因此可向废液中加入稀硫酸至不再产生气泡后待排放;检测pH常用pH试纸或pH计;故填:气泡;pH试纸或pH计。
(5)
见答案。
22.
(1) 蒸馏 蒸发结晶 蛋白质
(2) C 氯化铵4Cl 原料易得,经济,且氨气、二氧化碳可循环利用
(3) 熟石灰
碳酸钠会与母液中的氯化钙、氯化镁反应生成难溶于水的碳酸钙和微溶于水的碳酸镁,导致镁元素的沉淀富集效率降低,且混合沉淀难以分离
【分析】
(1)
①工业上常采用蒸馏法从海水中获取大量淡水,解决淡水危机;利用蒸发结晶的基本原理从海水中提取大量盐类,用作化工原料;
③海洋鱼类、海参、龙虾富含的营养素是蛋白质;
(2)
①A、加入过量的氯化钡溶液,氯化钡和硫酸钠反应生成硫酸钡和氯化钠,加入过量的氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,加入过量的碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和过量的氯化钡反应生成碳酸钡和氯化钠,故加入的三种溶液的顺序可以调整,但是加入碳酸钠一定要在加入氯化钡之后,才能将氯化钡除去,不符合题意;
B、由以上分析可知,按流程Ⅰ所加溶液的顺序除杂,过滤后得到碳酸钙、碳酸钡、氢氧化镁、硫酸钡四种沉淀,不符合题意;
C、由以上分析可知,加入三种溶液将粗盐水中的、Mg2+、Ca2+转化为沉淀,符合题意。
故选C;
②流程Ⅱ中,氯化钠、氨气、二氧化碳和水反应生成碳酸氢钠和氯化铵,碳酸氢钠结晶析出,过滤后的滤液主要含有氯化铵;
③从原料和循环利用的角度分析,海水制碱是以氯化钠溶液、氨气、二氧化碳为原料,原料易得,经济,且氨气、二氧化碳可循环利用;
(3)
①假设用氢氧化钠和氢氧化钙分别制取m吨氢氧化镁,所需氢氧化钠的质量为:
所需氢氧化钙的质量为:
购买氢氧化钠的价格为:;
购买氢氧化钙的价格为:
故试剂X应该选择上述化工原料中的熟石灰更适宜;
②加入试剂X后,氢氧化钙和氯化镁反应生成氢氧化镁和氯化钙,该反应的化学方程式为:;
③碳酸钠会与母液中的氯化钙、氯化镁反应生成难溶于水的碳酸钙和微溶于水的碳酸镁,导致镁元素的沉淀富集效率降低,且混合沉淀难以分离。故不选择碳酸钠。
23.酒精使蛋白质变性 有机物 2 H+、Ca2+ = 100 解:产生沉淀所消耗的碳酸钠的质量为5.3%×100g=5.3g
解得
答:m的值为5。
【详解】
(1)①75%酒精溶液能杀死冠状病毒是因为酒精使蛋白质变性;
②因为对氯间二甲苯酚的化学式是C8H9ClO,是含碳元素的化合物,属于有机物;
③钠显+1价,氧显-2价,设氯的化合价为x,根据化合物化合价代数和为零,则(+1)+x+(-2)=0,x=+1,表示为:;
④由题可知,需要10%的过氧乙酸溶液;
(2)①石灰石和盐酸反应生成氯化钙、水和二氧化碳,向反应后的滤液中加碳酸钠溶液开始没有沉淀生成后来有沉淀生成,说明制取二氧化碳的实验中盐酸是过量的,碳酸钠加进来先和盐酸反应,待盐酸反应完后再和氯化钙反应。过滤所得滤液中含有过量的盐酸和生成的氯化钙,对应的阳离子有H+、Ca2+;
②a点盐酸已经被反应完,发生的反应是碳酸钠和氯化钙反应生成碳酸钙沉淀、氯化钠,对应的溶液pH=7;
③产生沉淀所消耗的碳酸钠溶液质量是120g-20g=100g;
④见答案。
24.蛋白质 碘 混合物 12.8% C 蒸馏 碱
【分析】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的碘元素可以预防甲状腺肿大。
(2)含有两种或两种以上物质的物质属于混合物;根据生成的二氧化碳的质量和对应的化学方程式求算参加反应的甲烷的质量,进而求算其质量分数。
(3)水变成水蒸气的过程中,水分子之间的间隔变大;通过蒸馏可以得到蒸馏水;
(4)显酸性溶液的pH小于7,显中性溶液的pH等于7,显碱性溶液的pH大于7;
水和二氧化碳反应生成碳酸。
【详解】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的 碘可以预防甲状脚肿大。故填:蛋白质;碘;
(2)可燃冰主要含有甲烷水合物,还含少量CO2等气体,属于混合物;
设生成17.6g二氧化碳需要的甲烷的质量为x。
x=6.4g
该天然气水合物样品中甲烷的质量分数为:。
故答案为混合物; 12.8%。
(3)①水变成水蒸气的过程中,发生变化的是水分子间隔,故填:C;
②从海水中获得淡水可采取的方法是蒸馏,故填:蒸馏。
(4)①根据海水pH变化趋势判断:2000年时海水的pH应该是介于8.1和8.2之间,呈碱性;②“海洋酸化”的原因是二氧化碳和水反应生成碳酸,反应的化学方程式表示为:。故填:碱;。
一、选择题(共16题)
1.下列食物中,富含糖类的是( )
A.鸡蛋
B.豆油
C.黄瓜
D.馒头
2.杜阮凉瓜是江门市乃至省、港、澳地区知名的农产品,该美食主要富含的营养素是( )
A.糖类 B.油脂 C.无机盐 D.维生素
3.哈尔滨老鼎丰糕点中含有最多的营养素是( )
A.糖类 B.蛋白质
C.维生素 D.无机盐
4.在端午节我们包粽子时准备了如下食材:糯米、瘦肉、绿豆、花生,其中瘦肉富含的营养素主要是( )
A.维生素 B.蛋白质 C.油脂 D.糖类
5.化学元素与人体健康息息相关。下列关于元素影响人体健康的表述不正确的是( )
A.缺氟易产生龋齿
B.缺硒会引起甲状腺肿大
C.老年人缺钙会导致骨质疏松
D.长期缺铁会引发缺铁性贫血
6.下列食物中富含糖类的是( )
A.大米 B.花生油 C.白菜 D.牛肉
7.“我可喜欢吃虾了”,因为它们富含( )
A.蛋白质 B.维生素 C.油脂 D.糖
8.下列有关实验的现象描述正确的是( )
A.向加碘食盐溶液中滴加淀粉,溶液变蓝
B.打开浓盐酸的瓶塞时,瓶口冒白烟
C.在鸡蛋清溶液中加几滴浓硝酸,微热,出现白色沉淀
D.10%葡萄糖溶液中加入新制的氢氧化铜加热至沸,出现砖红色沉淀
9.利用化学知识对下列说法进行判断,其中正确的是( )
A.油脂会让人长胖,应禁止食用
B.绿色植物合成葡萄糖的过程中将太阳能转化为化学能
C.取样尿液与硫酸铜溶液混合煮沸,可以检验尿液中是否含有葡萄糖
D.向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀是化学变化
10.下列人体所必需的元素中,缺乏会引起贫血的是( )
A.铁 B.钙 C.碘 D.锌
11.根据你所学的化学知识和生活经验,下列说法中错误的是( )
A.滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂具有乳化功能
B.利用中和反应的原理,可用含有氢氧化铝、氢氧化镁、碳酸氢钠等的药物除去过多的胃酸
C.蛋白质、糖类和油脂都是人体内的供能物质
D.做饭时,燃气灶的火焰呈黄色或橙色,此时需要调节炉具的进风口
12.河南美食誉天下,下列食品或食材富含蛋白质的是( )
A.灵宝苹果 B.禹州粉条 C.怀庆驴肉 D.淮阳黄花菜
13.下列富含淀粉的食物是( )
A.猪肉 B.白菜 C.菜籽油 D.米饭
14.平时要常吃一些糙米的主要原因是为了摄取 ( )
A.油脂 B.葡萄糖 C.维生素 D.蛋白质
15.除了茶文化以外,中国其他饮食文化同样博大精深,“狮子头”是中国八大菜系之苏中典的菜品,观察图片,选出下列关于狮子头的描述中错误的一项( )
A.青菜心可以为人体提供维生素
B.狮子头的主要营养蛋白质在肠胃中被人体直接吸收
C.减肥期间不宜多食狮子头
D.狮子头中的精瘦肉、鸡蛋,淀粉等都能为人体提供能量
16.下列原因解释不正确的是( )
A.豆浆中加盐卤或石膏制成豆腐,因为豆浆中的蛋白质发生了变性
B.水体发生赤潮现象,因为水体中氮、磷元素含量增高
C.打开啤酒瓶盖,有大量泡沫溢出,因为气体的溶解度随着压强的减小而减小
D.食盐在热水中比在冷水中溶解得快,因为温度越高,微粒运动越快
二、非选择题(共8题)
17.米、面、蔬菜、肉、植物油是烹饪食品时的主要原料。
(1)以上原料中富含蛋白质的是_______。
(2)大米、面粉等在温度和湿度较高的环境下容易滋生对人体有危害的_______(填序号)。
A.黄曲霉素 B.甲醛 C.一氧化碳
18.某品牌“自热米饭”的食品成分包括:米饭、鸡肉、胡萝卜等。“自热米饭”的自加热原理为:饭盒夹层的水与生石灰接触,反应放出大量的热。
(1)米饭、鸡肉、胡萝卜中富含糖类的是______。
(2)写出自加热原理的化学方程式______。
19.生活中处处有化学。
(1)人类六大营养素中,能供给人体能量的有油脂、蛋白质和________。
(2)化肥可提供农作物生长需要的营养元素,尿素[化学式为CO(NH2)2]属于______(选填“氮”、“磷”或“钾”或“复合”)肥。
20.化学与人类的生产、生活密切相关。
(1)化学与健康。
①钙能强壮骨骼,在人体中属于__________(填“常量元素”或“微量元素”)。
②在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,该反应的化学方程式为______________________。
(2)化学与资源。
①在空气的成分中,稀有气体所占比率虽然很小,但有广泛的用途。写出氦气的化学式,并标出氦元素的化合价:__________。
②如图所示的简易净水器中,活性炭的作用是过滤和__________;打开汽水瓶盖时,汽水会自动喷出来,是因为压强减小,气体的溶解度__________(填“增大”或“减小”)。
(3)化学与能源。
①可燃冰主要含有甲烷水合物,如果在开采中甲烷气体大量泄漏于大气中,将比二氧化碳造成的__________效应更加严重。
②4.6g某化合物在空气中完全燃烧生成8.8g二氧化碳和5.4g水,写出该化合物中各元素的质量比:______________________。
21.英国《独立报》曾评出改变世界的101个发明,中国古代四大发明赫然在列,造纸术就是其中之一、一种现代造纸流程如图所示。
(1)纸的主要成分是纤维素,纤维素属于营养物质中的______类。纤维素组成用(C6H10O5)n表示,___(填“属于”或“不属于”)有机高分子化合物,其中碳、氢元素的质量比为____。废办公用纸属于______(填“可回收”或“不可回收”)垃圾。
(2)烧碱、纯碱能与树、竹、草中的油脂作用。生活中用洗洁精洗油污,属于______现象。
(3)步骤2中捣碎的目的是______;步骤3中操作a的名称是______,此操作中常用玻璃棒,作用是______。
(4)经检测甲造纸厂废液中含有一定量的碳酸钠,可向废液中加入稀硫酸至不再产生______(填现象)后待排放,环境监测员常用______检测废液的pH,确认是否达标。
(5)经检测,乙造纸厂废液中含有一定量的NaOH,NaOH的质量分数为4%,现用H2SO4的质量分数为9.8%的废硫酸10t将其处理至中性,可以处理的废液质量是______?(写出计算过程)
22.2019 年 2 月 26 日,我国“海洋地质十号”调查船完成中巴印度洋联合海洋地质科学考察,返抵广州。“海洋地质十号”由中国自主设计、建造,可以实现在全球无限航区开展海洋地质调查工作。它助力科学家们对海底世界的新认知,新发现与新开发。
(1)人类正在运用各种方法,开采、提取多种海洋资源。
①海水化学资源:工业上常采用___法从海水中获取大量淡水,解决淡水危机。利用_______的基本原理从海水中提取大量盐类,用作化工原料。
②海底矿产资源:海底蕴含着煤、石油、天然气等数百种矿产资源。
③海洋鱼类、海参、龙虾富含的营养素是_______________。
(2)某工厂利用海水制造纯碱,生产工艺流程如图所示:
①对于流程Ⅰ中加入的三种溶液,下列说法正确的是_______________。
A.加入的三种溶液的顺序不可以调整
B.按流程Ⅰ所加溶液的顺序除杂,过滤后得到三种沉淀
C.加入三种溶液将粗盐水中的、Mg2+、Ca2+转化为沉淀
②经过流程Ⅱ过滤后的滤液主要含有_______________。
③从原料和循环利用的角度分析海水制碱生产流程的优点_______________。
(3)目前世界上60%的镁是从海水中提取的,其主要步骤如图所示:
部分物质的溶解性表
Na+ Mg2+ Ca2+
Cl- 溶 溶 溶
OH- 溶 不 微
溶 微 不
①已知部分化工原料的市场价格为:烧碱3200元/吨,熟石灰1200元/吨。工业上为了达到更高的生产效率效益,你认为如图中的试剂X应该选择上述化工原料中的____更适宜。
②加入试剂X后,发生反应的化学方程式为_______。
③综合如图和表中的信息,试分析工业上通常不选择碳酸钠作试剂X的理由___。
23.(1)目前,新冠肺炎疫情全球蔓延,消毒剂的使用在防疫过程中起着重要作用。
①75%酒精溶液。请用学过的知识解释75%酒精溶液能杀死冠状病毒的原因:________。
②威王消毒液。威王消毒液的主要成分是对氯间二甲苯酚,对氯间二甲苯酚的化学式是C8H9ClO,对氯间二甲苯酚属于______(填“无机物”或“有机物”)。
③84消毒液。84消毒液的主要成分是次氯酸钠NaClO,标出次氯酸钠中氯元素的化合价_______。
④过氧乙酸溶液。0.2%的过氧乙酸溶液常用于空气和地面消毒。某校要配制0.2%的过氧乙酸消毒溶液100kg,需要10%的过氧乙酸溶液_______kg。
(2)小明同学向石灰石和稀盐酸制备CO2后过滤得到的滤液中滴加5.3%的Na2CO3溶液,得到的沉淀质量随碳酸钠溶液的质量的变化如图所示:
①过滤所得滤液中的阳离子______。
②a点对应的溶液pH_____7(填“>”、“=”或“<”)。
③产生沉淀所消耗的碳酸钠溶液质量是_______g。
④求m的值。_____(写出计算过程)
24.中国有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。
(1)海洋为我们提供了营养丰富的食材。鱼虾富含的 ________ (填一种营养素)是机体生长及修补受损组织的主要原料,海带富含的 _____ (填元素符号)可以预防甲状腺肿大。
(2)我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于 _______ (选填“纯净物”或“混合物”)。有科学家开采得到一种天然气水合物样品。取50.0克样品放置在一密闭容器内,该样品迅速转化为甲烷气体和水,将甲烷气体分离并完全燃烧,得到17.6克二氧化碳。该天然气水合物样品中甲烷的质量分数为 _____ 。(写出完整的计算过程)
(3)海水淡化可缓解淡水资源匮乏问题。
①水变成水蒸气的过程中,发生变化的是 _______ (填字母序号)。
A分子个数 B分子质量 C分子间隔 D分子种类
②从海水中获得淡水可采取的方法是 ________________ (填“过滤”“吸附”或“蒸馏”)。
(4)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减小。
①根据海水pH变化趋势判断:2000年时海水呈 ________ 性。
②“海洋酸化”的原因可用化学方程式表示为 ____ 。
参考答案
1.D
【详解】
A、鸡蛋中富含有蛋白质,不符合题意;
B、豆油中富含有油脂,不符合题意;
C、黄瓜中富含有维生素,不符合题意;
D、馒头中富含有淀粉,属于糖类,符合题意。
故选:D。
2.D
【详解】
蔬菜水果中主要营养素是维生素,所以杜阮凉瓜主要富含的营养素是维生素。
故选:D。
3.A
【详解】
哈尔滨老鼎丰糕点的主要成分是面粉,其中含有淀粉,属于糖类,且糕点中的食品添加剂也有糖类,故哈尔滨老鼎丰糕点中含有最多的营养素是糖类,故选A。
4.B
【详解】
瘦肉中富含蛋白质,故选B。
5.B
【详解】
A、缺氟易产生龋齿,A正确;
B、缺硒会引起表皮角质化和癌症,缺碘才会引起甲状腺肿大,B不正确;
C、老年人缺钙会导致骨质疏松,C正确;
D、长期缺铁会引发缺铁性贫血,D正确。故选B。
6.A
【详解】
A、大米中富含糖类;
B、花生油中富含油脂;
C、白菜中富含维生素;
D、牛肉干中富含蛋白质。
故选:A。
7.A
【详解】
A、蛋白质主要存在于动物肌肉、奶类、蛋类、鱼类及花生和豆类的种子或制品中,虾中主要含蛋白质,所以正确;
B、维生素主要存在于蔬菜和水果中,所以错误;
C、油脂主要存在于动物脂肪和花生、大豆、芝麻和种子中,所以错误;
D、糖类主要存在于植物的种子和块茎中,所以错误。
故选A。
8.D
【详解】
A、淀粉遇碘单质变蓝色,而加碘食盐溶液中不含碘单质,向加碘食盐溶液中滴加淀粉,无明显变化,故选项A错误;
B、浓盐酸具有挥发性,打开浓盐酸的瓶塞时,瓶口冒白雾,而不是白烟,故选项B错误;
C、鸡蛋清溶液中含有蛋白质,加入浓硝酸,微热后,出现黄色沉淀,故选项C错误;
D、在新配制的氢氧化铜中加入葡萄糖溶液,加热到沸腾,生成有砖红色的氧化亚铜沉淀,会观察到产生红色沉淀,故选项D正确。
故选D。
9.B
【详解】
A、油脂是人体的营养素之一,要合理食用,故此答案错误。
B、植物的光合作用是能量转化过程,是太阳能转化为化学能,故此答案正确。
C、葡萄糖与新制的氢氧化铜在加热的条件下,可生成葡萄糖酸和水,同时生成砖红色沉淀氧化亚铜,据此可以检验葡萄糖的存在,故此选项错误。
D、向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀是盐析现象,不是蛋白质变性导致,故此选项错误。
故选:B。
10.A
【详解】
人体必须的元素中,缺铁容易引起贫血,缺少钙元素会引起骨质疏松症;缺少碘元素会造成甲状腺肿大;缺少锌元素会发育迟缓,食欲不振;故答案选择A。
11.B
【详解】
A、滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂具有乳化功能,不符合题意;
B、中和反应是酸和碱反应生成盐和水的反应,碳酸氢钠是盐,不是中和反应,符合题意;
C、蛋白质、糖类和油脂都是人体内的供能物质,不符合题意;
D、做饭时,燃气灶的火焰呈黄色或橙色,是氧气不足的表现,此时需要调节炉具的进风口,增大氧气的进入量,不符合题意。故选B。
12.C
【解析】
A、水果富含维生素;B、粉条的主要成分是淀粉,淀粉为糖类物质;C、驴肉富含蛋白质;D、蔬菜富含维生素。故选C。
13.D
【详解】
富含淀粉的食物是D. 米饭。A. 猪肉富含,蛋白质。B. 白菜,富含维生素。 C. 菜籽油,富含脂肪。
14.C
【详解】
一些糙米中含有维生素,故选C。
15.B
【详解】
A、青菜心富含维生素,故选项正确;
B、胃中含有胃蛋白酶,能初步分解蛋白质,蛋白质不能在肠胃中被人体直接吸收,故选项错误;
C、狮子头富含 蛋白质和油脂,减肥期间不宜多食狮子头,故选项正确;
D、狮子头中的精瘦肉、鸡蛋,淀粉等都能为人体提供能量,故选项正确。
故选:B。
16.A
【详解】
A、向蛋白质溶液中加入浓的无机盐溶液,可使蛋白质的溶解度降低而从溶液中析出,这种作用叫做盐析;这样析出的蛋白质在继续加水时,仍能溶解,并不影响原来蛋白质的性质,蛋白质并没有失去活性,选项说法错误;
B、水体中氮磷元素含量过多会造成水生藻类的疯狂生长,导致水质恶化,造成“水华”或“赤潮”现象的发生,选项说法正确;
C、打开啤酒瓶盖,压强变小,有大量泡沫溢出,这是因为气体的溶解度随着压强的减小而减小,选项说法正确;
D、粒子是在不断运动的,温度越高,粒子运动速率越快,所以食盐在热水中比在冷水中溶解得快,选项说法正确。
故选A。
17. 肉 A
【解析】(1)根据蛋白质的食物来源分析;
(2)根据潮湿环境下容易发生霉变分析。
解:(1)动物肌肉、皮肤、毛发、蹄、角、蛋清、大豆、花生富含蛋白质。故填:肉;
(2)大米、面粉等在温度和湿度较高的环境下容易发生霉变,滋生含有黄曲霉素的黄曲霉菌,故填:A。
18.
(1)米饭
(2)
【分析】
本题考查营养物质。
(1)米饭中富含糖类、鸡肉红富含蛋白质、胡萝卜中富含维生素,故填:米饭;
(2)氧化钙和水反应生成氢氧化钙:。
19.糖类 氮
【详解】
(1)人类六大营养素中,能供给人体能量的有蛋白质、糖类、油脂,故填糖类;
(2)从尿素的化学式中看出,尿素中含有氮元素,尿素属于氮肥,故填氮。
20. 常量元素 C6H12O6 + 6O26H2O + 6CO2 吸附 减小 温室 碳、氢、氧元素的质量比等于12︰3︰8(合理叙述均可)
【解析】(1)化学与健康。①钙能强壮骨骼,在人体中属于常量元素。 ②在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,该反应的化学方程式为C6H12O6 + 6O26H2O + 6CO2 。(2)化学与资源。①在空气的成分中,稀有气体所占比率虽然很小,但有广泛的用途。写出氦气的化学式,并标出氦元素的化合价: 。②如图所示的简易净水器中,活性炭的作用是过滤和吸附;打开汽水瓶盖时,汽水会自动喷出来,是因为压强减小,气体的溶解度减小。(3)化学与能源。①可燃冰主要含有甲烷水合物,如果在开采中甲烷气体大量泄漏于大气中,将比二氧化碳造成的温室效应更加严重。②4.6g某化合物在空气中完全燃烧生成8.8g二氧化碳和5.4g水,写出该化合物中各元素的质量比:8.8g× ×100%=2.4g. 5.4g××100%=0.6g. 4.6g-2.4g-0.6g=1.6g. 该化合物中碳、氢、氧元素各元素的质量比:2.4∶0.6∶1.6=12︰3︰8.
21.
(1) 糖类 属于 36:5 可回收
(2)乳化
(3) 增大反应物的接触面积 过滤 引流
(4) 气泡 pH试纸或pH计
(5)20t
解:设处理废液的质量为x。
x=20t
答:可处理20t。
【分析】
(1)
纤维素属于糖类;纤维素的相对分子质量达到几万、甚至几十万,所以属于有机高分子化合物;纤维素由碳、氢、氧三种元素组成;其中碳、氢元素的质量之比=(12×6×n):(1×10×n)=36:5;废办公用纸可以再利用,属于可回收垃圾;故填:糖类;属于;36:5;可回收。
(2)
洗洁精能将油污乳化,属于乳化现象;故填:乳化。
(3)
步骤2中捣碎的目的是增大反应物的接触面积;步骤3中操作a是将固体和液体分离,因此是过滤操作;此操作中常用玻璃棒,作用是引流;故填:增大反应物的接触面积;过滤;引流。
(4)
碳酸钠与硫酸反应生成硫酸钠钠、水二氧化碳,因此可向废液中加入稀硫酸至不再产生气泡后待排放;检测pH常用pH试纸或pH计;故填:气泡;pH试纸或pH计。
(5)
见答案。
22.
(1) 蒸馏 蒸发结晶 蛋白质
(2) C 氯化铵4Cl 原料易得,经济,且氨气、二氧化碳可循环利用
(3) 熟石灰
碳酸钠会与母液中的氯化钙、氯化镁反应生成难溶于水的碳酸钙和微溶于水的碳酸镁,导致镁元素的沉淀富集效率降低,且混合沉淀难以分离
【分析】
(1)
①工业上常采用蒸馏法从海水中获取大量淡水,解决淡水危机;利用蒸发结晶的基本原理从海水中提取大量盐类,用作化工原料;
③海洋鱼类、海参、龙虾富含的营养素是蛋白质;
(2)
①A、加入过量的氯化钡溶液,氯化钡和硫酸钠反应生成硫酸钡和氯化钠,加入过量的氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,加入过量的碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和过量的氯化钡反应生成碳酸钡和氯化钠,故加入的三种溶液的顺序可以调整,但是加入碳酸钠一定要在加入氯化钡之后,才能将氯化钡除去,不符合题意;
B、由以上分析可知,按流程Ⅰ所加溶液的顺序除杂,过滤后得到碳酸钙、碳酸钡、氢氧化镁、硫酸钡四种沉淀,不符合题意;
C、由以上分析可知,加入三种溶液将粗盐水中的、Mg2+、Ca2+转化为沉淀,符合题意。
故选C;
②流程Ⅱ中,氯化钠、氨气、二氧化碳和水反应生成碳酸氢钠和氯化铵,碳酸氢钠结晶析出,过滤后的滤液主要含有氯化铵;
③从原料和循环利用的角度分析,海水制碱是以氯化钠溶液、氨气、二氧化碳为原料,原料易得,经济,且氨气、二氧化碳可循环利用;
(3)
①假设用氢氧化钠和氢氧化钙分别制取m吨氢氧化镁,所需氢氧化钠的质量为:
所需氢氧化钙的质量为:
购买氢氧化钠的价格为:;
购买氢氧化钙的价格为:
故试剂X应该选择上述化工原料中的熟石灰更适宜;
②加入试剂X后,氢氧化钙和氯化镁反应生成氢氧化镁和氯化钙,该反应的化学方程式为:;
③碳酸钠会与母液中的氯化钙、氯化镁反应生成难溶于水的碳酸钙和微溶于水的碳酸镁,导致镁元素的沉淀富集效率降低,且混合沉淀难以分离。故不选择碳酸钠。
23.酒精使蛋白质变性 有机物 2 H+、Ca2+ = 100 解:产生沉淀所消耗的碳酸钠的质量为5.3%×100g=5.3g
解得
答:m的值为5。
【详解】
(1)①75%酒精溶液能杀死冠状病毒是因为酒精使蛋白质变性;
②因为对氯间二甲苯酚的化学式是C8H9ClO,是含碳元素的化合物,属于有机物;
③钠显+1价,氧显-2价,设氯的化合价为x,根据化合物化合价代数和为零,则(+1)+x+(-2)=0,x=+1,表示为:;
④由题可知,需要10%的过氧乙酸溶液;
(2)①石灰石和盐酸反应生成氯化钙、水和二氧化碳,向反应后的滤液中加碳酸钠溶液开始没有沉淀生成后来有沉淀生成,说明制取二氧化碳的实验中盐酸是过量的,碳酸钠加进来先和盐酸反应,待盐酸反应完后再和氯化钙反应。过滤所得滤液中含有过量的盐酸和生成的氯化钙,对应的阳离子有H+、Ca2+;
②a点盐酸已经被反应完,发生的反应是碳酸钠和氯化钙反应生成碳酸钙沉淀、氯化钠,对应的溶液pH=7;
③产生沉淀所消耗的碳酸钠溶液质量是120g-20g=100g;
④见答案。
24.蛋白质 碘 混合物 12.8% C 蒸馏 碱
【分析】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的碘元素可以预防甲状腺肿大。
(2)含有两种或两种以上物质的物质属于混合物;根据生成的二氧化碳的质量和对应的化学方程式求算参加反应的甲烷的质量,进而求算其质量分数。
(3)水变成水蒸气的过程中,水分子之间的间隔变大;通过蒸馏可以得到蒸馏水;
(4)显酸性溶液的pH小于7,显中性溶液的pH等于7,显碱性溶液的pH大于7;
水和二氧化碳反应生成碳酸。
【详解】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的 碘可以预防甲状脚肿大。故填:蛋白质;碘;
(2)可燃冰主要含有甲烷水合物,还含少量CO2等气体,属于混合物;
设生成17.6g二氧化碳需要的甲烷的质量为x。
x=6.4g
该天然气水合物样品中甲烷的质量分数为:。
故答案为混合物; 12.8%。
(3)①水变成水蒸气的过程中,发生变化的是水分子间隔,故填:C;
②从海水中获得淡水可采取的方法是蒸馏,故填:蒸馏。
(4)①根据海水pH变化趋势判断:2000年时海水的pH应该是介于8.1和8.2之间,呈碱性;②“海洋酸化”的原因是二氧化碳和水反应生成碳酸,反应的化学方程式表示为:。故填:碱;。
同课章节目录
