8.3 金属资源的利用和保护同步练习—2021-2022学年九年级化学人教版下册(word版 含解析)
文档属性
| 名称 | 8.3 金属资源的利用和保护同步练习—2021-2022学年九年级化学人教版下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 295.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-03 00:00:00 | ||
图片预览




文档简介
8.3、金属资源的利用和保护
一、选择题(共16题)
1.下列实验操作正确的是
A.用玻璃棒搅拌加快过滤
B.用镊子取用二氧化锰
C.用量筒量取液体时最后改用胶头滴管加至刻度
D.实验室模拟炼铁时先加热氧化铁再通一氧化碳
2.中央电视台春节联欢晚会上,甘肃省向观众拜年的对联是:“金银铜铁铬镍铅锌”。针对此联,下列说法正确的是
A.这八种金属单质颜色是相同的
B.合金的制造大大拓宽了这八种金属的应用范围和使用价值
C.这八种金属均可与稀盐酸反应产生氢气
D.这八种金属在矿物中均以单质形式存在
3.下列图标中,表示可回收物品的标志是
A. B.C.D.
4.下列实验中,铁片最容易发生锈蚀的是
A. B.C.D.
5.下列关于资源、能源和环境的叙述不正确的是
A.陆地储水约占全球水储量的2.53%
B.改进发动机的燃烧方式,使汽油充分燃烧,可减少汽车尾气对空气的污染
C.在生活和生产中,人们经常利用的能源有化石能源、水能等
D.金属的回收利用,既能降低生产成本,又能节约金属资源和能源
6.用如图所示装置进行实验。下列说法不正确的是
A.直玻璃管内红棕色粉末变为黑色
B.可利用点燃的方法处理尾气
C.试管中澄清石灰水变浑浊证明有CO2生成
D.直玻璃管内反应的化学方程式为3CO + Fe2O3 =3CO2 + 2Fe
7.下列说法正确的是
A.所有金属都呈银白色
B.铁制品部分浸入食盐水中不易生锈
C.铁在氧气中燃烧,剧烈燃烧火星四射,生成一种红色固体
D.工业炼铁的主要原理是用一氧化碳与铁矿石在高温条件下反应生成铁
8.下列做法不是为了隔绝空气中的氧气的是
A.石灰水密封保存 B.白磷浸没在水中保存
C.暖气片表面刷“银粉”漆 D.用灯帽盖灭酒精灯
9.下列关于资源、能源的叙述正确的是
A.回收利用废旧金属,虽不能减少对环境的污染,却可以节约金属资源
B.目前人类制得的纯金属只有80余种,合金却高达几千种
C.我国矿物储量比较丰富,其中钨、钛、锡等储量居世界前列
D.金属资源只有金、银以单质的形式存在,其余都以化合物形式存在
10.下列说法不正确的是
A.回收一个铝饮料罐比制造一个新饮料罐要贵
B.回收铝饮料罐可以节约金属资源
C.回收铝饮料罐可以节约能源
D.回收铝饮料罐可以减少对环境的污染
11.生活中处处有化学,以下说法正确的是
①煤和石油是不可再生资源,通过综合利用以提高其利用率
②发现家中煤气泄漏应立即打开排气扇换气
③油锅着火,立即用大量的水救火
④为保护赖以生存的水资源,生活污水、工业废水要处理达标后再排放
⑤除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发
⑥铁锈是一层氧化物保护膜,铁锈最好不要除去
A.①②⑤ B.①④⑤ C.③④ D.⑤⑥
12.“暖宝宝”放热的反应可看作是铁粉与空气中的水和氧气相互作用,产生氢氧化亚铁 Fe(OH)2,最终转化为氢氧化铁 Fe(OH)3.下列说法中不正确的是
A.总反应为:2Fe+3H2O=2Fe(OH)3
B.“暖宝宝”放出的热量是由化学反应产生的
C.上述含铁的物质中铁元素的化合价有 0、+2、+3
D.“暖宝宝”使用前必须密封保存
13.下列实验不能达到实验目的的是
A.
B.
C.
D.
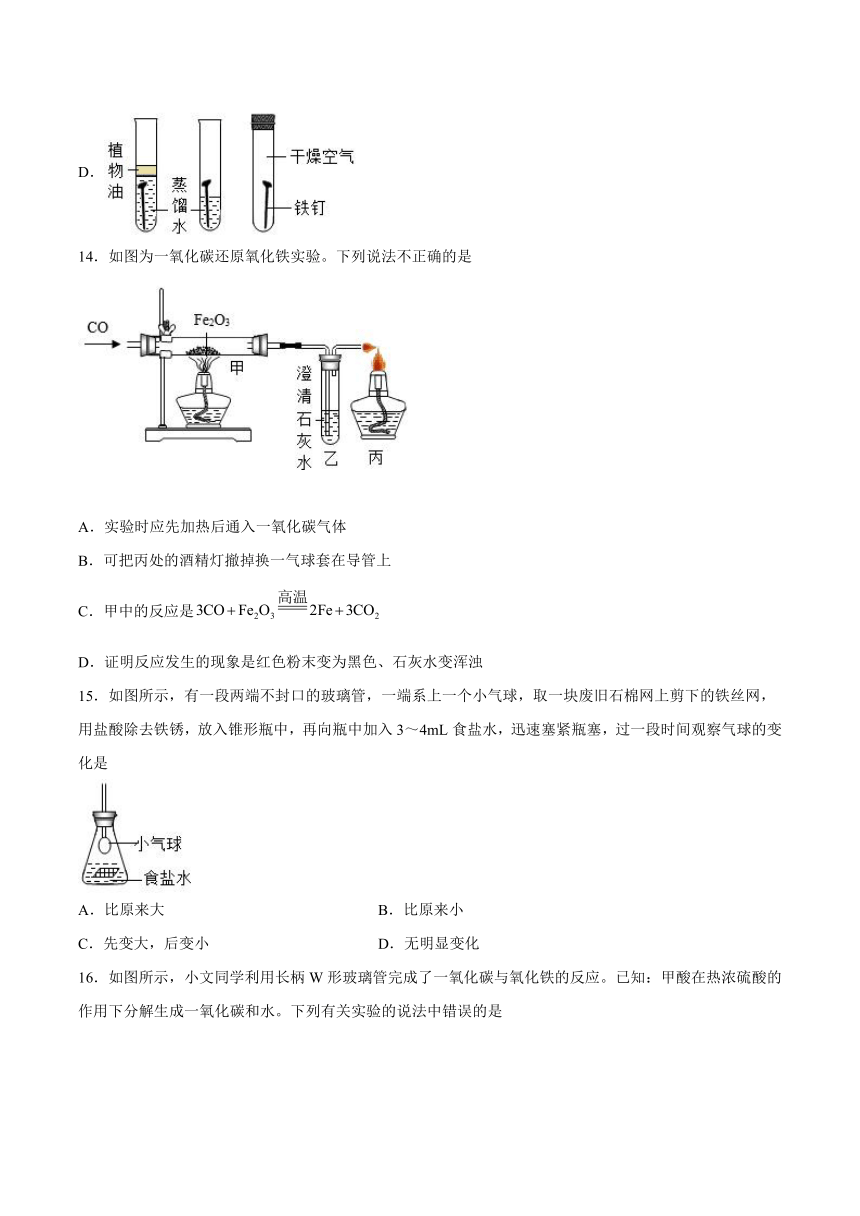
14.如图为一氧化碳还原氧化铁实验。下列说法不正确的是
A.实验时应先加热后通入一氧化碳气体
B.可把丙处的酒精灯撤掉换一气球套在导管上
C.甲中的反应是
D.证明反应发生的现象是红色粉末变为黑色、石灰水变浑浊
15.如图所示,有一段两端不封口的玻璃管,一端系上一个小气球,取一块废旧石棉网上剪下的铁丝网,用盐酸除去铁锈,放入锥形瓶中,再向瓶中加入3~4mL食盐水,迅速塞紧瓶塞,过一段时间观察气球的变化是
A.比原来大 B.比原来小
C.先变大,后变小 D.无明显变化
16.如图所示,小文同学利用长柄W形玻璃管完成了一氧化碳与氧化铁的反应。已知:甲酸在热浓硫酸的作用下分解生成一氧化碳和水。下列有关实验的说法中错误的是
A.该微型实验具有药品用量少、清洁环保、操作简单等优点
B.灯罩的作用是,集中火焰,提高酒精灯火焰的温度
C.A处发生的反应中,一氧化碳夺取氧化铁中的氧,发生还原反应
D.A处可观察到的实验现象是:红色粉末变成黑色
二、非选择题(共8题)
17.按要求填空:
(1)硬水与软水相比,硬水中含有较多的可溶性_________化合物。在净水器中装 有活性炭,这是利用了活性炭的_________性。
(2)要除去硫酸亚铁溶液中混有的硫酸铜杂质,可加入的试剂为_________,主要操作方法为_________。
(3)防止金属腐蚀是保护金属资源的有效途经之一,写出一种防止铁制品生锈的具体方法____。
18.化学与生活密切相关,学好化学可以帮助我们分析、解决生产生活中的问题。铝、铁、铜是我们生活中常见的金属,请按要求回答下列问题:
(1)铝块能制成铝箔是利用了铝的______性。
(2)铁锅易生锈,通常用完后擦干并保持干燥以防止生锈。自行车的支架刷有油漆,以防生锈,是因为油漆可以使铁与空气中的______和______隔绝。
(3)在高温下,利用焦炭和氧气反应生成的一氧化碳可把铁从赤铁矿石里还原出来,用化学方程式表示该炼铁反应的原理______。
(4)黄铜是铜锌合金,其硬度比纯铜______(填“大”或“小”)。
(5)将铁粉投入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若溶液中只含一种溶质,这种溶质是______,过滤后的滤渣中一定含有______,可能含有______。
19.从生活走进化学,从化学走向社会.请从化学的视角认识生活中的有关问题.
家里炒菜时油锅着火,最好的灭火方法是________;
某同学的午餐食谱如下:“主食:米饭;副食:豆腐、红烧肉”.其中富含淀粉的是________;
食盐是最重要的调味品.下表为食盐在不同温度下的溶解度,结合表内信息回答下列问题:
温度
溶解度
①构成食盐的微粒是________;
②从接近饱和的食盐溶液中获得食盐晶体,应采取的方法是________;
③时,向水中加入 食盐,充分搅拌,所得溶液的质量是________;
铁制品长期使用容易生锈,铁生锈的条件是________;
日常生活中防止铁制品锈蚀的方法有________;
自来水厂净水过程中常用活性炭,活性炭的主要作用是________.
工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中发生反应的化学方程式为________.
20.金属钛(Ti)因常温下不与酸、碱反应等优良性能,被誉为“未来金属”。提取钛的主要反应原理。请回答:
(1)该反应属于基本反应类型中的_____反应。
(2)反应前后,钛元素化合价的变化为_____→_____。
(3)95KgTiCl4能生产含杂质4%的金属钛_____kg。
(4)上述反应得到的金属钛中混有少量金属杂质,可加入_____除去。
21.钢铁在生产生活中有广泛应用。工业用铁矿石炼铁,实验室也可模拟炼铁。
Ⅰ.工业炼铁
(1)工业炼铁的主要设备为___________。
(2)上述设备中焦炭的作用___________,___________。
Ⅱ.实验室模拟炼铁
(3)实验室模拟炼铁的装置如图所示。
①反应前先通一氧化碳的目的___________。
②硬质玻璃管内发生反应的化学方程式为___________。
③该装置的缺陷是___________。
(4)小华同学查阅资料得知:铁的氧化物除氧化铁外,其余均为黑色;而且除了铁能够被磁铁吸引外,四氧化三铁也能够被磁铁吸引;铁的氧化物均能和稀硫酸或稀盐酸反应生成相应的铁的化合物和水,没有气体生成;氧化铁转化为铁的具体过程是: Fe2O3Fe3O4FeOFe
①小华认为:用磁铁来检验反应后生成了铁是不够科学的,他的依据是___________。
②小华同学为了验证黑色的生成物中含有铁,他取少量黑色生成物样品于试管中,加入___________,如果观察到有___________产生,则生成物中一定有铁。
22.化学与生活息息相关 请利用所学知识回答下列问题。
(1)我们日常生活中常用的“加铁酱油”“高钙牛奶”等生活用品,这里提到的铁、钙指的是_______(填“单质”“原子”或“元素”)。
(2)氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,可为氢动力汽车提供能源。写出该反应的化学方程式:________
(3)目前汽车的燃料主要是汽油,汽油是从石油中分离得到的,石油、煤和_______都是化石燃料,汽车生产中使用了大量钢材和塑料,在钢表面喷漆可防止其锈蚀,该方法的防锈原理是_______
(4)竹炭是竹子经过碳化后形成的多孔性材料,具有极强的_______性,可除去冰箱中的异味。
23.(1) 为庆祝中国人民海军成立70周年,2019年4月23日在青岛海域举行了海上阅兵活动。70年来人民海军在党的坚强领导下,一路劈波斩浪,纵横万里海疆,取得举世瞩目的伟大成就,正以全新资态屹立于世界的东方!中方参阅舰艇和飞机包括航母辽宁舰、新型核潜艇、新型驱逐舰、战机等在内,有些舰艇是第一次亮相。
①军舰外壳需要涂防锈漆,目的是为了防止铁与空气中的_____发生反应而生锈。
②核潜艇上一般备有的氧气再生药板,是由一片片涂有过氧化钠(Na2O2)的薄板组成,使用时过氧化钠与二氧化碳反应生成氧气和碳酸钠,请写出该反应的化学方程式_____。
(2)工业上采用氨碱法生产纯碱(Na2CO3) ,主要流程如图:
其生产过程中有下列反应:①;②;碳酸氢钠和氯化铵的溶解度曲线如图所示。
请回答下列问题:
①30℃时, NH4Cl饱和溶液的溶质质量分数_____NaHCO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②30℃时,将25gNH4Cl加入到50g水中,所得溶液的溶质质量分数为_____(计算结果精确到0.1%)。
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,请根据它们的溶解度曲线,从溶解度角度分析原因是_____。
24.金属材料在人类发展的历史长河中起着非常重要的作用。
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的______(填“高”或“低”)。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:
①实验甲中铝丝会出现的现象是______,该反应的化学方程式为______。
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是______(填字母代号)。
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式______。
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?______。
③a处尾气被点燃,写出反应的化学方程式______。
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?______(反应方程式:)
参考答案
1.C
【详解】
A、用玻璃棒搅拌过滤器中的液体可能将滤纸弄破,使实验失败,故错误;
B、二氧化锰是粉末状的固体,用药匙来取用;故错误;
C、向量筒中倾倒液体至接近刻度线时,再改用胶头滴管加液到刻度线,故正确;
D、实验室炼铁的过程中,防止气体不纯引起爆炸,要先通入CO排出空气,再加热,故顺序错误;
故选:C。
2.B
【详解】
A.金为黄色,铜为紫红色,所以选项说法错误。
B.合金的制造大大拓宽了这八种金属的应用范围和使用价值,选项说法正确。
C.只有氢前金属会与稀盐酸反应产生氢气,即金银铜不会与稀盐酸反应,选项说法错误。
D.金银活性较弱以单质形式存在,而活性强的铁锌等是以化合物的形式存在,选项说法错误。
故选:B。
3.B
【详解】
A、表示当心火灾---易燃物质标志,与消防安全有关,选项A不正确;
B、表示可回收标志,选项B正确;
C、表示交通标志,选项C不正确;
D、表示燃烧标志,选项D不正确;
故选B。
4.C
【详解】
A、铁与水接触,与氧气不接触,只能与水中溶解的少量氧气接触,不易生锈,不符合题意;
B、铁与氧气直接接触,没有和水蒸气接触,不易生锈,不符合题意;
C、铁能与氧气和水接触,比较容易生锈,符合题意;
D、铁只能与水接触,与氧气不接触,不易生锈,不符合题意。
故选C。
5.A
【详解】
A、陆地淡水约占全球水储量的2.53%;故选项错误,但符合题意;
B、改进发动机的燃烧方式,使汽油充分燃烧,高效利用能源,可减少汽车尾气对空气的污染;故选项正确,但不符合题意;
C、在生活和生产中,人们经常利用的能源有化石能源、水能等;故选项正确,但不符合题意;
D、金属的回收利用,既能降低生产成本,又能节约金属资源和能源;故选项正确,但不符合题意;
故选:A。
6.D
【详解】
A、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,直玻璃管中出现的现象是红棕色粉末逐渐变黑,故选项说法正确。
B、一氧化碳有毒,直接排放到空气中会污染环境,可利用点燃的方法进行尾气处理,故选项说法正确。
C、二氧化碳能使澄清的石灰水变浑浊,试管中澄清石灰水变浑浊证明有二氧化碳生成,故选项说法正确。
D、一氧化碳与氧化铁高温条件下反应生成铁和二氧化碳,反应方程式为:,故选项错误;
故选D。
7.D
【详解】
A、并不是所有金属都呈银白色,铜是红色的,故A不正确;
B、食盐水能促进铁生锈的速率,则铁制品部分浸入食盐水中易生锈,故B不正确;
C、铁在氧气中燃烧,剧烈燃烧火星四射,生成一种黑色固体,故C不正确;
D、工业炼铁的主要原理是用一氧化碳与铁矿石在高温条件下反应生成铁,故D正确。
故选D。
8.A
【详解】
A、石灰水密封保存,是为了防止与空气中的二氧化碳反应而变质,不是为了隔绝空气中的氧气,故A符合题意;
B、白磷易自燃,白磷浸没在水中保存,是为了隔绝空气中的氧气,故B不符合题意;
C、暖气片表面刷“银粉”漆,是为了防止铁与空气中与氧气、水分反应而生锈,是为了隔绝空气中的氧气,故C不符合题意;
D、用灯帽盖灭酒精等,是为了隔绝氧气,故D不符合题意。
故选A。
9.C
【详解】
A、回收利用废旧金属,既可以减少对环境的污染,又可以节约金属资源,错误;
B、目前人类制得的纯金属只有90余种,合金却高达几千种,错误;
C、我国矿物储量比较丰富,其中钨、钛、锡等储量居世界前列,正确;
D、除少数很不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在,错误。
故选C。
10.A
【详解】
因为回收一个铝饮料罐比制造一个新饮料罐要便宜20%,而且还节约金属资源和95%的能源,所以A的说法错误,BCD的说法正确.故选A.
11.B
【详解】
①煤和石油是不可再生资源,通过综合利用以提高其利用率,单纯作为燃料使用是一种浪费,说法正确;
②发现家中煤气泄漏不能立即打开排气扇换气,因为会产生电火花点燃气体发生爆炸和火灾,说法错误;
③油锅着火,不能用水救火,油的密度小会浮在水面继续燃烧,说法错误;
④生活污水、工业废水要处理达标后再排放,有利于保护水资源,说法正确;
⑤除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,说法正确;
⑥铁锈是一层氧化物保护膜,铁锈疏松多孔,会吸收水和氧气,最好除去,说法错误;
故选:B。
12.A
【详解】
A、总反应可表示为:4Fe+3O2+6H2O=4Fe(OH)3,错误;
B、热敷袋放出的热量是由化学反应产生的,正确;
C、铁属于单质,铁单质中铁元素的化合价是 0,氢氧化亚铁中铁元素的化合价是+2,氢氧化铁中铁元素的化合价是+3,该选项说法正确;
D、热敷袋中的铁粉与水在未使用时要分别密封保存,以防过早发生化学反应,该选项说法正确。
故选:A。
13.A
【详解】
带火星的木条在呼出气体中和在空气中都不能复燃,所以A不能达到实验目的。故选A.
14.A
【详解】
A、实验时,应先通一氧化碳气体,将装置内空气排尽,然后加热,因为一氧化碳具有可燃性,混有一定量的空气,遇到明火,容易发生爆炸,不符合题意;
B、丙处酒精灯的作用是处理尾气,也可将丙处的酒精灯撤掉,换一气球套在导管上,收集尾气,不符合题意;
C、甲中的反应是一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,该反应的化学方程式为:,不符合题意;
D、红色粉末变成黑色,说明氧化铁被还原为了铁,石灰水变浑浊,说明有二氧化碳生成,可证明反应的发生,不符合题意。
故选A。
15.A
【分析】
根据金属的性质以及物质间反应的现象结合物理压强的知识进行分析解答即可。
【详解】
铁在水与氧气并存的情况下易生锈,食盐能加速铁的锈蚀,铁生锈需要消耗氧气,导致锥形瓶内的压强减小,故气球会变大。故选A。
16.C
【详解】
A、该微型实验,能节约药品,具有药品用量少、清洁环保、操作简单等优点,故选项说法正确。
B、灯罩的作用是集中火焰,提高酒精灯火焰的温度,故选项说法正确。
C、A处发生的反应中,一氧化碳夺取氧化铁中的氧,发生氧化反应,故选项说法错误。
D、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,A处可观察到的实验现象是红色粉末变成黑色,故选项说法正确。
故选C。
17.钙、镁 吸附 铁粉(或 Fe) 过滤 刷漆(或涂油或保持表面洁净、干燥或制成合金)(其他合理答案均可)
【详解】
(1)含有较多可溶性钙镁化合物的水叫硬水,不含或含较少可溶性钙、镁化合物的水叫软水;活性炭具有疏松多孔的结构,具有吸附性,可以除去色素和异味;
(2)铁与硫酸铜反应生成硫酸亚铁和铜。要除去硫酸亚铁溶液中混有的硫酸铜杂质,可加入铁粉,将不溶性杂质除去,常用过滤的方法;
(3)为了防止钢铁的锈蚀,人们常采用在其表面刷漆、涂油或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水。
18.延展 氧气 水 Fe2O3+3CO2Fe+3CO2 大 硝酸亚铁 铜、银 铁
【详解】
(1)利用金属铝具有良好的延展性可把金属铝制成片;故答案为延展;
(2)铁生锈是铁与氧气、水同时接触,自行车的支架刷有油漆用以防锈,是因为油漆可以使铁与空气中的氧气、水隔绝。故填:氧气、水;
(3)在高温下,氧化铁和一氧化碳反应的化学方程式为:Fe2O3+3CO2Fe+3CO2。故填:Fe2O3+3CO2Fe+3CO2。
(4)由于合金的硬度比组成它的纯金属的硬度大,因此由铜锌组成的黄铜合金的硬度比纯铜的硬度大。故填:大;
(5)金属活动性顺序中,排在前面的金属能将排在后面的金属从其化合物的水溶液中置换出来,且金属活动性差距越大,越易反应,首先发生反应: Fe+2AgNO3=2Ag+ Fe(NO3)2,当AgNO3反应完以后,铁与Cu(NO3)2溶液反应,Fe+Cu(NO3)2= Fe(NO3)2 + Cu。溶液中只有一种溶质,则为硝酸亚铁;银和铜已经被完全置换出来,铁可能有剩余.
故答案为硝酸亚铁;铜、银;铁。
19.用锅盖盖灭 米饭 、 蒸发结晶 与氧气和水接触 刷漆或涂油 吸附
【详解】
(1)油锅着火时,用锅盖盖灭是最好的处理办法;
(2)米饭中富含淀粉;
(3)①食盐的主要成分是氯化钠,氯化钠是离子型化合物,因此构成氯化钠的最小微粒是钠离子和氯离子;
②氯化钠的溶解度随温度变化较小,因此从接近饱和的食盐溶液中获得食盐晶体,应采取的方法是蒸发结晶;
③20 C时,氯化钠的溶解度是36g,因此向100g水中加入40g食盐,充分搅拌,最多可溶解氯化钠36g,所得溶液的质量是136g。
(4)铁与氧气和水同时接触时会生锈,可以通过刷油漆的方式来隔绝铁与氧气和水解除;
(5)活性炭的主要作用是吸附水中的异味和色素;
(6)该过程中,硫酸铜与铁发生反应,反应方程式是,红色的线是析出的铜单质。
20.置换 +4 0 13.3 稀盐酸
【详解】
(1)该反应是单质和化合物反应生成单质和化合物,属于基本反应类型中的置换反应。
故填:置换。
(2)反应前四氯化钛中氯元素显-1价,根据化合物中元素化合价代数和为0可知,四氯化钛中钛元素的化合价为+4价,反应后生成金属钛单质,化合价为0,钛元素化合价的变化为+4→0。
故填:+4;0。
(3)95kgTiCl4能生产含杂质4%金属钛质量:95kg×÷(1-4%)=25kg。
故填:25。
(4)上述反应得到的金属钛中混有少量金属杂质,可加入稀盐酸除去,这是因为稀盐酸能和镁反应生成氯化镁和氢气。
故填:稀盐酸。
21.
(1)高炉
(2) 提供热量 制还原剂CO
(3) 排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸
没有尾气处理装置
(4) 四氧化三铁也能被磁铁吸引 稀盐酸(或稀硫酸) 气泡
【分析】
(1)
工业炼铁的主要设备为高炉,故填:高炉。
(2)
上述设备中焦炭与空气中氧气反应放出大量的热,可以提供热量;碳与二氧化碳在高温条件下生成还原剂一氧化碳,所以上述设备中焦炭的作用是提供热量;制还原剂CO,故填;提供热量;制还原剂CO。
(3)
①反应前先通一氧化碳的目的是:排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸,故填:排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸;
②硬质玻璃管内发生反应是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,该反应的化学方程式为,故填: 。
③一氧化碳有毒,未反应的一氧化碳未进行处理,所以该装置的缺陷是没有尾气处理装置,故填:没有尾气处理装置。
(4)
①由资料可知:四氧化三铁也能够被磁铁吸引,所以用磁铁吸用来检验反应后产物中生成了铁是不够科学的,故填:四氧化三铁也能够被磁铁吸引;
②铁能与稀盐酸或稀硫酸反应生成氢气,所以为了验证黑色的生成物中含有铁,取少量黑色生成物样品于试管中,加入稀盐酸或稀硫酸,如果观察到有少量气泡产生,则产物中一定有铁生成,故填:稀盐酸(或稀硫酸);气泡
22.元素 天然气 与氧气和水隔绝 吸附
【详解】
(1)我们日常生活中常用的“加铁酱油”“高钙牛奶”等,这里提到的铁、钙不是以单质、分子、原子等形式存在,这里所指的“铁、钙”是强调存在的元素,与具体形态无关;(2)氢化镁固体与水反应的化学方程式为:MgH2+2H2O=Mg(OH)2+2H2↑;(3)煤、石油、天然气是三大化石燃料;铁生锈的条件是与空气和水接触,所以喷漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝空气和水;(4)竹炭是竹子经过碳化后形成的多孔性材料,具有极强的吸附性,可除去冰箱中的异味。
23.氧气、水 大于 28.6% 相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量
【详解】
(1)①军舰外壳需要涂防锈漆,目的是为了防止铁与空气中的氧气、水发生反应而生锈,防止锈蚀的原理是隔绝氧气和水。
②过氧化钠与二氧化碳反应生成氧气和碳酸钠,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。
故答案为:①氧气、水;②2Na2O2+2CO2=2Na2CO3+O2。
(2)①由溶解度曲线可知,30℃时,氯化铵的溶解度大于碳酸氢钠的溶解度,由饱和溶液中溶质质量分数的计算公式×100%可知,30℃时,NH4Cl饱和溶液的溶质质量分数大于NaHCO3饱和溶液的溶质质量分数;故填:大于;
②30℃时,氯化铵的溶解度为40g,则在该温度下,将25gNH4Cl加入到50g水中,只能溶解20g氯化铵,所得溶液为该温度下饱和溶液,其中溶质的质量分数为×100%≈28.6%;故填:28.6%;
③氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是碳酸氨钠,原因是相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量。
故填:相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量。
24.高 有红色固体析出,溶液由蓝色变为无色 C 澄清石灰水变浑浊 解:设用13.5kg铝粉可制取铁的质量是x
x=28kg
答:用13.5kg铝粉可制取铁的质量是28kg。
【详解】
(1)合金比组成它的纯金属的硬度大,故铝合金的强度和硬度比纯铝的高;
(2)①实验甲中,铝与硫酸铜反应生成硫酸铝和铜,故有红色固体析出,溶液由蓝色变为无色;该反应的化学方程式为;
②铝能与硫酸铜反应生成硫酸铝和铜,有红色固体析出,说明铝比铜活泼,铝与硫酸镁不反应,无明显现象,说明镁比铝活泼,铜与硫酸铝不反应,无明显现象,说明铝比铜活泼,故丙可以省去,乙不能省去。故选C;
(3)①玻璃管内,一氧化碳能与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为;
②一氧化碳还原氧化铁生成的气体是二氧化碳,通常用澄清石灰水来检验二氧化碳,二氧化碳能与氢氧化钙反应生成碳酸钙和水,故实验现象是:产生白色沉淀;
③a处的尾气是一氧化碳,一氧化碳具有可燃性,一氧化碳燃烧生成二氧化碳,该反应的化学方程式为;
(4)见答案。
一、选择题(共16题)
1.下列实验操作正确的是
A.用玻璃棒搅拌加快过滤
B.用镊子取用二氧化锰
C.用量筒量取液体时最后改用胶头滴管加至刻度
D.实验室模拟炼铁时先加热氧化铁再通一氧化碳
2.中央电视台春节联欢晚会上,甘肃省向观众拜年的对联是:“金银铜铁铬镍铅锌”。针对此联,下列说法正确的是
A.这八种金属单质颜色是相同的
B.合金的制造大大拓宽了这八种金属的应用范围和使用价值
C.这八种金属均可与稀盐酸反应产生氢气
D.这八种金属在矿物中均以单质形式存在
3.下列图标中,表示可回收物品的标志是
A. B.C.D.
4.下列实验中,铁片最容易发生锈蚀的是
A. B.C.D.
5.下列关于资源、能源和环境的叙述不正确的是
A.陆地储水约占全球水储量的2.53%
B.改进发动机的燃烧方式,使汽油充分燃烧,可减少汽车尾气对空气的污染
C.在生活和生产中,人们经常利用的能源有化石能源、水能等
D.金属的回收利用,既能降低生产成本,又能节约金属资源和能源
6.用如图所示装置进行实验。下列说法不正确的是
A.直玻璃管内红棕色粉末变为黑色
B.可利用点燃的方法处理尾气
C.试管中澄清石灰水变浑浊证明有CO2生成
D.直玻璃管内反应的化学方程式为3CO + Fe2O3 =3CO2 + 2Fe
7.下列说法正确的是
A.所有金属都呈银白色
B.铁制品部分浸入食盐水中不易生锈
C.铁在氧气中燃烧,剧烈燃烧火星四射,生成一种红色固体
D.工业炼铁的主要原理是用一氧化碳与铁矿石在高温条件下反应生成铁
8.下列做法不是为了隔绝空气中的氧气的是
A.石灰水密封保存 B.白磷浸没在水中保存
C.暖气片表面刷“银粉”漆 D.用灯帽盖灭酒精灯
9.下列关于资源、能源的叙述正确的是
A.回收利用废旧金属,虽不能减少对环境的污染,却可以节约金属资源
B.目前人类制得的纯金属只有80余种,合金却高达几千种
C.我国矿物储量比较丰富,其中钨、钛、锡等储量居世界前列
D.金属资源只有金、银以单质的形式存在,其余都以化合物形式存在
10.下列说法不正确的是
A.回收一个铝饮料罐比制造一个新饮料罐要贵
B.回收铝饮料罐可以节约金属资源
C.回收铝饮料罐可以节约能源
D.回收铝饮料罐可以减少对环境的污染
11.生活中处处有化学,以下说法正确的是
①煤和石油是不可再生资源,通过综合利用以提高其利用率
②发现家中煤气泄漏应立即打开排气扇换气
③油锅着火,立即用大量的水救火
④为保护赖以生存的水资源,生活污水、工业废水要处理达标后再排放
⑤除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发
⑥铁锈是一层氧化物保护膜,铁锈最好不要除去
A.①②⑤ B.①④⑤ C.③④ D.⑤⑥
12.“暖宝宝”放热的反应可看作是铁粉与空气中的水和氧气相互作用,产生氢氧化亚铁 Fe(OH)2,最终转化为氢氧化铁 Fe(OH)3.下列说法中不正确的是
A.总反应为:2Fe+3H2O=2Fe(OH)3
B.“暖宝宝”放出的热量是由化学反应产生的
C.上述含铁的物质中铁元素的化合价有 0、+2、+3
D.“暖宝宝”使用前必须密封保存
13.下列实验不能达到实验目的的是
A.
B.
C.
D.
14.如图为一氧化碳还原氧化铁实验。下列说法不正确的是
A.实验时应先加热后通入一氧化碳气体
B.可把丙处的酒精灯撤掉换一气球套在导管上
C.甲中的反应是
D.证明反应发生的现象是红色粉末变为黑色、石灰水变浑浊
15.如图所示,有一段两端不封口的玻璃管,一端系上一个小气球,取一块废旧石棉网上剪下的铁丝网,用盐酸除去铁锈,放入锥形瓶中,再向瓶中加入3~4mL食盐水,迅速塞紧瓶塞,过一段时间观察气球的变化是
A.比原来大 B.比原来小
C.先变大,后变小 D.无明显变化
16.如图所示,小文同学利用长柄W形玻璃管完成了一氧化碳与氧化铁的反应。已知:甲酸在热浓硫酸的作用下分解生成一氧化碳和水。下列有关实验的说法中错误的是
A.该微型实验具有药品用量少、清洁环保、操作简单等优点
B.灯罩的作用是,集中火焰,提高酒精灯火焰的温度
C.A处发生的反应中,一氧化碳夺取氧化铁中的氧,发生还原反应
D.A处可观察到的实验现象是:红色粉末变成黑色
二、非选择题(共8题)
17.按要求填空:
(1)硬水与软水相比,硬水中含有较多的可溶性_________化合物。在净水器中装 有活性炭,这是利用了活性炭的_________性。
(2)要除去硫酸亚铁溶液中混有的硫酸铜杂质,可加入的试剂为_________,主要操作方法为_________。
(3)防止金属腐蚀是保护金属资源的有效途经之一,写出一种防止铁制品生锈的具体方法____。
18.化学与生活密切相关,学好化学可以帮助我们分析、解决生产生活中的问题。铝、铁、铜是我们生活中常见的金属,请按要求回答下列问题:
(1)铝块能制成铝箔是利用了铝的______性。
(2)铁锅易生锈,通常用完后擦干并保持干燥以防止生锈。自行车的支架刷有油漆,以防生锈,是因为油漆可以使铁与空气中的______和______隔绝。
(3)在高温下,利用焦炭和氧气反应生成的一氧化碳可把铁从赤铁矿石里还原出来,用化学方程式表示该炼铁反应的原理______。
(4)黄铜是铜锌合金,其硬度比纯铜______(填“大”或“小”)。
(5)将铁粉投入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若溶液中只含一种溶质,这种溶质是______,过滤后的滤渣中一定含有______,可能含有______。
19.从生活走进化学,从化学走向社会.请从化学的视角认识生活中的有关问题.
家里炒菜时油锅着火,最好的灭火方法是________;
某同学的午餐食谱如下:“主食:米饭;副食:豆腐、红烧肉”.其中富含淀粉的是________;
食盐是最重要的调味品.下表为食盐在不同温度下的溶解度,结合表内信息回答下列问题:
温度
溶解度
①构成食盐的微粒是________;
②从接近饱和的食盐溶液中获得食盐晶体,应采取的方法是________;
③时,向水中加入 食盐,充分搅拌,所得溶液的质量是________;
铁制品长期使用容易生锈,铁生锈的条件是________;
日常生活中防止铁制品锈蚀的方法有________;
自来水厂净水过程中常用活性炭,活性炭的主要作用是________.
工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中发生反应的化学方程式为________.
20.金属钛(Ti)因常温下不与酸、碱反应等优良性能,被誉为“未来金属”。提取钛的主要反应原理。请回答:
(1)该反应属于基本反应类型中的_____反应。
(2)反应前后,钛元素化合价的变化为_____→_____。
(3)95KgTiCl4能生产含杂质4%的金属钛_____kg。
(4)上述反应得到的金属钛中混有少量金属杂质,可加入_____除去。
21.钢铁在生产生活中有广泛应用。工业用铁矿石炼铁,实验室也可模拟炼铁。
Ⅰ.工业炼铁
(1)工业炼铁的主要设备为___________。
(2)上述设备中焦炭的作用___________,___________。
Ⅱ.实验室模拟炼铁
(3)实验室模拟炼铁的装置如图所示。
①反应前先通一氧化碳的目的___________。
②硬质玻璃管内发生反应的化学方程式为___________。
③该装置的缺陷是___________。
(4)小华同学查阅资料得知:铁的氧化物除氧化铁外,其余均为黑色;而且除了铁能够被磁铁吸引外,四氧化三铁也能够被磁铁吸引;铁的氧化物均能和稀硫酸或稀盐酸反应生成相应的铁的化合物和水,没有气体生成;氧化铁转化为铁的具体过程是: Fe2O3Fe3O4FeOFe
①小华认为:用磁铁来检验反应后生成了铁是不够科学的,他的依据是___________。
②小华同学为了验证黑色的生成物中含有铁,他取少量黑色生成物样品于试管中,加入___________,如果观察到有___________产生,则生成物中一定有铁。
22.化学与生活息息相关 请利用所学知识回答下列问题。
(1)我们日常生活中常用的“加铁酱油”“高钙牛奶”等生活用品,这里提到的铁、钙指的是_______(填“单质”“原子”或“元素”)。
(2)氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,可为氢动力汽车提供能源。写出该反应的化学方程式:________
(3)目前汽车的燃料主要是汽油,汽油是从石油中分离得到的,石油、煤和_______都是化石燃料,汽车生产中使用了大量钢材和塑料,在钢表面喷漆可防止其锈蚀,该方法的防锈原理是_______
(4)竹炭是竹子经过碳化后形成的多孔性材料,具有极强的_______性,可除去冰箱中的异味。
23.(1) 为庆祝中国人民海军成立70周年,2019年4月23日在青岛海域举行了海上阅兵活动。70年来人民海军在党的坚强领导下,一路劈波斩浪,纵横万里海疆,取得举世瞩目的伟大成就,正以全新资态屹立于世界的东方!中方参阅舰艇和飞机包括航母辽宁舰、新型核潜艇、新型驱逐舰、战机等在内,有些舰艇是第一次亮相。
①军舰外壳需要涂防锈漆,目的是为了防止铁与空气中的_____发生反应而生锈。
②核潜艇上一般备有的氧气再生药板,是由一片片涂有过氧化钠(Na2O2)的薄板组成,使用时过氧化钠与二氧化碳反应生成氧气和碳酸钠,请写出该反应的化学方程式_____。
(2)工业上采用氨碱法生产纯碱(Na2CO3) ,主要流程如图:
其生产过程中有下列反应:①;②;碳酸氢钠和氯化铵的溶解度曲线如图所示。
请回答下列问题:
①30℃时, NH4Cl饱和溶液的溶质质量分数_____NaHCO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②30℃时,将25gNH4Cl加入到50g水中,所得溶液的溶质质量分数为_____(计算结果精确到0.1%)。
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,请根据它们的溶解度曲线,从溶解度角度分析原因是_____。
24.金属材料在人类发展的历史长河中起着非常重要的作用。
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的______(填“高”或“低”)。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:
①实验甲中铝丝会出现的现象是______,该反应的化学方程式为______。
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是______(填字母代号)。
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式______。
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?______。
③a处尾气被点燃,写出反应的化学方程式______。
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?______(反应方程式:)
参考答案
1.C
【详解】
A、用玻璃棒搅拌过滤器中的液体可能将滤纸弄破,使实验失败,故错误;
B、二氧化锰是粉末状的固体,用药匙来取用;故错误;
C、向量筒中倾倒液体至接近刻度线时,再改用胶头滴管加液到刻度线,故正确;
D、实验室炼铁的过程中,防止气体不纯引起爆炸,要先通入CO排出空气,再加热,故顺序错误;
故选:C。
2.B
【详解】
A.金为黄色,铜为紫红色,所以选项说法错误。
B.合金的制造大大拓宽了这八种金属的应用范围和使用价值,选项说法正确。
C.只有氢前金属会与稀盐酸反应产生氢气,即金银铜不会与稀盐酸反应,选项说法错误。
D.金银活性较弱以单质形式存在,而活性强的铁锌等是以化合物的形式存在,选项说法错误。
故选:B。
3.B
【详解】
A、表示当心火灾---易燃物质标志,与消防安全有关,选项A不正确;
B、表示可回收标志,选项B正确;
C、表示交通标志,选项C不正确;
D、表示燃烧标志,选项D不正确;
故选B。
4.C
【详解】
A、铁与水接触,与氧气不接触,只能与水中溶解的少量氧气接触,不易生锈,不符合题意;
B、铁与氧气直接接触,没有和水蒸气接触,不易生锈,不符合题意;
C、铁能与氧气和水接触,比较容易生锈,符合题意;
D、铁只能与水接触,与氧气不接触,不易生锈,不符合题意。
故选C。
5.A
【详解】
A、陆地淡水约占全球水储量的2.53%;故选项错误,但符合题意;
B、改进发动机的燃烧方式,使汽油充分燃烧,高效利用能源,可减少汽车尾气对空气的污染;故选项正确,但不符合题意;
C、在生活和生产中,人们经常利用的能源有化石能源、水能等;故选项正确,但不符合题意;
D、金属的回收利用,既能降低生产成本,又能节约金属资源和能源;故选项正确,但不符合题意;
故选:A。
6.D
【详解】
A、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,直玻璃管中出现的现象是红棕色粉末逐渐变黑,故选项说法正确。
B、一氧化碳有毒,直接排放到空气中会污染环境,可利用点燃的方法进行尾气处理,故选项说法正确。
C、二氧化碳能使澄清的石灰水变浑浊,试管中澄清石灰水变浑浊证明有二氧化碳生成,故选项说法正确。
D、一氧化碳与氧化铁高温条件下反应生成铁和二氧化碳,反应方程式为:,故选项错误;
故选D。
7.D
【详解】
A、并不是所有金属都呈银白色,铜是红色的,故A不正确;
B、食盐水能促进铁生锈的速率,则铁制品部分浸入食盐水中易生锈,故B不正确;
C、铁在氧气中燃烧,剧烈燃烧火星四射,生成一种黑色固体,故C不正确;
D、工业炼铁的主要原理是用一氧化碳与铁矿石在高温条件下反应生成铁,故D正确。
故选D。
8.A
【详解】
A、石灰水密封保存,是为了防止与空气中的二氧化碳反应而变质,不是为了隔绝空气中的氧气,故A符合题意;
B、白磷易自燃,白磷浸没在水中保存,是为了隔绝空气中的氧气,故B不符合题意;
C、暖气片表面刷“银粉”漆,是为了防止铁与空气中与氧气、水分反应而生锈,是为了隔绝空气中的氧气,故C不符合题意;
D、用灯帽盖灭酒精等,是为了隔绝氧气,故D不符合题意。
故选A。
9.C
【详解】
A、回收利用废旧金属,既可以减少对环境的污染,又可以节约金属资源,错误;
B、目前人类制得的纯金属只有90余种,合金却高达几千种,错误;
C、我国矿物储量比较丰富,其中钨、钛、锡等储量居世界前列,正确;
D、除少数很不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在,错误。
故选C。
10.A
【详解】
因为回收一个铝饮料罐比制造一个新饮料罐要便宜20%,而且还节约金属资源和95%的能源,所以A的说法错误,BCD的说法正确.故选A.
11.B
【详解】
①煤和石油是不可再生资源,通过综合利用以提高其利用率,单纯作为燃料使用是一种浪费,说法正确;
②发现家中煤气泄漏不能立即打开排气扇换气,因为会产生电火花点燃气体发生爆炸和火灾,说法错误;
③油锅着火,不能用水救火,油的密度小会浮在水面继续燃烧,说法错误;
④生活污水、工业废水要处理达标后再排放,有利于保护水资源,说法正确;
⑤除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,说法正确;
⑥铁锈是一层氧化物保护膜,铁锈疏松多孔,会吸收水和氧气,最好除去,说法错误;
故选:B。
12.A
【详解】
A、总反应可表示为:4Fe+3O2+6H2O=4Fe(OH)3,错误;
B、热敷袋放出的热量是由化学反应产生的,正确;
C、铁属于单质,铁单质中铁元素的化合价是 0,氢氧化亚铁中铁元素的化合价是+2,氢氧化铁中铁元素的化合价是+3,该选项说法正确;
D、热敷袋中的铁粉与水在未使用时要分别密封保存,以防过早发生化学反应,该选项说法正确。
故选:A。
13.A
【详解】
带火星的木条在呼出气体中和在空气中都不能复燃,所以A不能达到实验目的。故选A.
14.A
【详解】
A、实验时,应先通一氧化碳气体,将装置内空气排尽,然后加热,因为一氧化碳具有可燃性,混有一定量的空气,遇到明火,容易发生爆炸,不符合题意;
B、丙处酒精灯的作用是处理尾气,也可将丙处的酒精灯撤掉,换一气球套在导管上,收集尾气,不符合题意;
C、甲中的反应是一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,该反应的化学方程式为:,不符合题意;
D、红色粉末变成黑色,说明氧化铁被还原为了铁,石灰水变浑浊,说明有二氧化碳生成,可证明反应的发生,不符合题意。
故选A。
15.A
【分析】
根据金属的性质以及物质间反应的现象结合物理压强的知识进行分析解答即可。
【详解】
铁在水与氧气并存的情况下易生锈,食盐能加速铁的锈蚀,铁生锈需要消耗氧气,导致锥形瓶内的压强减小,故气球会变大。故选A。
16.C
【详解】
A、该微型实验,能节约药品,具有药品用量少、清洁环保、操作简单等优点,故选项说法正确。
B、灯罩的作用是集中火焰,提高酒精灯火焰的温度,故选项说法正确。
C、A处发生的反应中,一氧化碳夺取氧化铁中的氧,发生氧化反应,故选项说法错误。
D、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,A处可观察到的实验现象是红色粉末变成黑色,故选项说法正确。
故选C。
17.钙、镁 吸附 铁粉(或 Fe) 过滤 刷漆(或涂油或保持表面洁净、干燥或制成合金)(其他合理答案均可)
【详解】
(1)含有较多可溶性钙镁化合物的水叫硬水,不含或含较少可溶性钙、镁化合物的水叫软水;活性炭具有疏松多孔的结构,具有吸附性,可以除去色素和异味;
(2)铁与硫酸铜反应生成硫酸亚铁和铜。要除去硫酸亚铁溶液中混有的硫酸铜杂质,可加入铁粉,将不溶性杂质除去,常用过滤的方法;
(3)为了防止钢铁的锈蚀,人们常采用在其表面刷漆、涂油或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水。
18.延展 氧气 水 Fe2O3+3CO2Fe+3CO2 大 硝酸亚铁 铜、银 铁
【详解】
(1)利用金属铝具有良好的延展性可把金属铝制成片;故答案为延展;
(2)铁生锈是铁与氧气、水同时接触,自行车的支架刷有油漆用以防锈,是因为油漆可以使铁与空气中的氧气、水隔绝。故填:氧气、水;
(3)在高温下,氧化铁和一氧化碳反应的化学方程式为:Fe2O3+3CO2Fe+3CO2。故填:Fe2O3+3CO2Fe+3CO2。
(4)由于合金的硬度比组成它的纯金属的硬度大,因此由铜锌组成的黄铜合金的硬度比纯铜的硬度大。故填:大;
(5)金属活动性顺序中,排在前面的金属能将排在后面的金属从其化合物的水溶液中置换出来,且金属活动性差距越大,越易反应,首先发生反应: Fe+2AgNO3=2Ag+ Fe(NO3)2,当AgNO3反应完以后,铁与Cu(NO3)2溶液反应,Fe+Cu(NO3)2= Fe(NO3)2 + Cu。溶液中只有一种溶质,则为硝酸亚铁;银和铜已经被完全置换出来,铁可能有剩余.
故答案为硝酸亚铁;铜、银;铁。
19.用锅盖盖灭 米饭 、 蒸发结晶 与氧气和水接触 刷漆或涂油 吸附
【详解】
(1)油锅着火时,用锅盖盖灭是最好的处理办法;
(2)米饭中富含淀粉;
(3)①食盐的主要成分是氯化钠,氯化钠是离子型化合物,因此构成氯化钠的最小微粒是钠离子和氯离子;
②氯化钠的溶解度随温度变化较小,因此从接近饱和的食盐溶液中获得食盐晶体,应采取的方法是蒸发结晶;
③20 C时,氯化钠的溶解度是36g,因此向100g水中加入40g食盐,充分搅拌,最多可溶解氯化钠36g,所得溶液的质量是136g。
(4)铁与氧气和水同时接触时会生锈,可以通过刷油漆的方式来隔绝铁与氧气和水解除;
(5)活性炭的主要作用是吸附水中的异味和色素;
(6)该过程中,硫酸铜与铁发生反应,反应方程式是,红色的线是析出的铜单质。
20.置换 +4 0 13.3 稀盐酸
【详解】
(1)该反应是单质和化合物反应生成单质和化合物,属于基本反应类型中的置换反应。
故填:置换。
(2)反应前四氯化钛中氯元素显-1价,根据化合物中元素化合价代数和为0可知,四氯化钛中钛元素的化合价为+4价,反应后生成金属钛单质,化合价为0,钛元素化合价的变化为+4→0。
故填:+4;0。
(3)95kgTiCl4能生产含杂质4%金属钛质量:95kg×÷(1-4%)=25kg。
故填:25。
(4)上述反应得到的金属钛中混有少量金属杂质,可加入稀盐酸除去,这是因为稀盐酸能和镁反应生成氯化镁和氢气。
故填:稀盐酸。
21.
(1)高炉
(2) 提供热量 制还原剂CO
(3) 排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸
没有尾气处理装置
(4) 四氧化三铁也能被磁铁吸引 稀盐酸(或稀硫酸) 气泡
【分析】
(1)
工业炼铁的主要设备为高炉,故填:高炉。
(2)
上述设备中焦炭与空气中氧气反应放出大量的热,可以提供热量;碳与二氧化碳在高温条件下生成还原剂一氧化碳,所以上述设备中焦炭的作用是提供热量;制还原剂CO,故填;提供热量;制还原剂CO。
(3)
①反应前先通一氧化碳的目的是:排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸,故填:排尽装置内的空气,防止一氧化碳与空气的混合气体在加热时发生爆炸;
②硬质玻璃管内发生反应是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,该反应的化学方程式为,故填: 。
③一氧化碳有毒,未反应的一氧化碳未进行处理,所以该装置的缺陷是没有尾气处理装置,故填:没有尾气处理装置。
(4)
①由资料可知:四氧化三铁也能够被磁铁吸引,所以用磁铁吸用来检验反应后产物中生成了铁是不够科学的,故填:四氧化三铁也能够被磁铁吸引;
②铁能与稀盐酸或稀硫酸反应生成氢气,所以为了验证黑色的生成物中含有铁,取少量黑色生成物样品于试管中,加入稀盐酸或稀硫酸,如果观察到有少量气泡产生,则产物中一定有铁生成,故填:稀盐酸(或稀硫酸);气泡
22.元素 天然气 与氧气和水隔绝 吸附
【详解】
(1)我们日常生活中常用的“加铁酱油”“高钙牛奶”等,这里提到的铁、钙不是以单质、分子、原子等形式存在,这里所指的“铁、钙”是强调存在的元素,与具体形态无关;(2)氢化镁固体与水反应的化学方程式为:MgH2+2H2O=Mg(OH)2+2H2↑;(3)煤、石油、天然气是三大化石燃料;铁生锈的条件是与空气和水接触,所以喷漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝空气和水;(4)竹炭是竹子经过碳化后形成的多孔性材料,具有极强的吸附性,可除去冰箱中的异味。
23.氧气、水 大于 28.6% 相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量
【详解】
(1)①军舰外壳需要涂防锈漆,目的是为了防止铁与空气中的氧气、水发生反应而生锈,防止锈蚀的原理是隔绝氧气和水。
②过氧化钠与二氧化碳反应生成氧气和碳酸钠,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。
故答案为:①氧气、水;②2Na2O2+2CO2=2Na2CO3+O2。
(2)①由溶解度曲线可知,30℃时,氯化铵的溶解度大于碳酸氢钠的溶解度,由饱和溶液中溶质质量分数的计算公式×100%可知,30℃时,NH4Cl饱和溶液的溶质质量分数大于NaHCO3饱和溶液的溶质质量分数;故填:大于;
②30℃时,氯化铵的溶解度为40g,则在该温度下,将25gNH4Cl加入到50g水中,只能溶解20g氯化铵,所得溶液为该温度下饱和溶液,其中溶质的质量分数为×100%≈28.6%;故填:28.6%;
③氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是碳酸氨钠,原因是相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量。
故填:相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量。
24.高 有红色固体析出,溶液由蓝色变为无色 C 澄清石灰水变浑浊 解:设用13.5kg铝粉可制取铁的质量是x
x=28kg
答:用13.5kg铝粉可制取铁的质量是28kg。
【详解】
(1)合金比组成它的纯金属的硬度大,故铝合金的强度和硬度比纯铝的高;
(2)①实验甲中,铝与硫酸铜反应生成硫酸铝和铜,故有红色固体析出,溶液由蓝色变为无色;该反应的化学方程式为;
②铝能与硫酸铜反应生成硫酸铝和铜,有红色固体析出,说明铝比铜活泼,铝与硫酸镁不反应,无明显现象,说明镁比铝活泼,铜与硫酸铝不反应,无明显现象,说明铝比铜活泼,故丙可以省去,乙不能省去。故选C;
(3)①玻璃管内,一氧化碳能与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为;
②一氧化碳还原氧化铁生成的气体是二氧化碳,通常用澄清石灰水来检验二氧化碳,二氧化碳能与氢氧化钙反应生成碳酸钙和水,故实验现象是:产生白色沉淀;
③a处的尾气是一氧化碳,一氧化碳具有可燃性,一氧化碳燃烧生成二氧化碳,该反应的化学方程式为;
(4)见答案。
同课章节目录
