第九单元课题2溶解度课后练习2-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元课题2溶解度课后练习2-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 130.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-06 00:00:00 | ||
图片预览


文档简介
2021——2022学年度人教版九年级化学下册 第九单元 溶液 课题2 溶解度课后练习2
一、选择题
1.下列说法正确的是
A.CO2可用于人工降雨,CO可用于光合作用 B.铝元素在地壳中含量最多,使用也最早
C.增加溶质可使不饱和溶液变为饱和溶液 D.鱼类能在水中生存,证明氧气易溶于水
2.下列说法正确的是
A.所有的变化一定符合质量守恒定律
B.氧化物一定是含有氧元素的纯净物
C.在化学反应中催化剂性质和质量一定不变
D.在一定温度下,饱和溶液一定比不饱和溶液浓
3.有关溶液的说法正确的是
A.溶液一定是液态的
B.所有溶质都以分子形式溶解在溶剂里
C.溶液具有均一性和稳定性
D.一定温度下,压强减小时,气体的溶解度会增大
4.谚语和诗词中蕴含着科学道理。下列说法正确的是
A.“冬天捞碱,夏天晒盐”—纯碱的溶解度随温度变化不大
B.“众人拾柴火焰高”—可燃物越多,着火点越低,越容易着火
C.“百炼成钢”和“只要功夫深,铁杵磨成针”—化学原理相同
D.“满架蔷薇一院香”—分子在不停地运动
5.下列事实的结论或解释不正确的是
A.变瘪的乒乓球遇到热水复原——温度升高,分子间隔变大
B.CO能燃烧,CO2不能燃烧——构成物质分子的原子种类不同
C.真金不怕火炼——金的化学性质稳定
D.打开汽水瓶盖冒出大量气泡——气体的溶解度随压强减小而减小
6.溶液与人们的生活息息相关。下列有关溶液的说法正确的是
A.均一、稳定的液体都是溶液
B.同一温度下,硝酸铵的饱和溶液比不饱和溶液浓
C.溶液中都存在大量自由移动的离子
D.饱和溶液析出晶体后溶质质量分数一定变小
7.有一杯t℃时的硝酸钾溶液,在该溶液中加入27克硝酸钾晶体,充分搅拌后有11克没有溶解;若将原溶液加热蒸发掉40克水再冷却至原温度,溶液恰好达到饱和,则t℃时硝酸钾的溶解度为
A.50 克 B.28 C.36克 D.40克
8.NaCl 和 KNO3 在不同温度时的溶解度如下表。下列说法正确的是
温度/C 0 20 40 60
NaCI的溶解度/g 35.7 36.0 36.6 37.3
KNO3的溶解度/g 13.3 31.6 63.9 110
A.20℃时,100 g氯化钠溶液中最多能溶解36.0g NaCl
B.40℃时,KNO3饱和溶液的溶质质量分数等于63.9%
C.可用冷却海水的方法获取大量食盐
D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
9.提纯含少量NaCl杂质的KNO3,部分实验过程如下。相关物质的溶解度曲线如图所示。下列说法正确的是
A.①→②,KNO3的溶解度不变
B.①→②,溶液中KNO3的质量分数不变
C.②→③,溶液中NaCl的质量增大
D.②→③,溶液中KNO3的质量减小
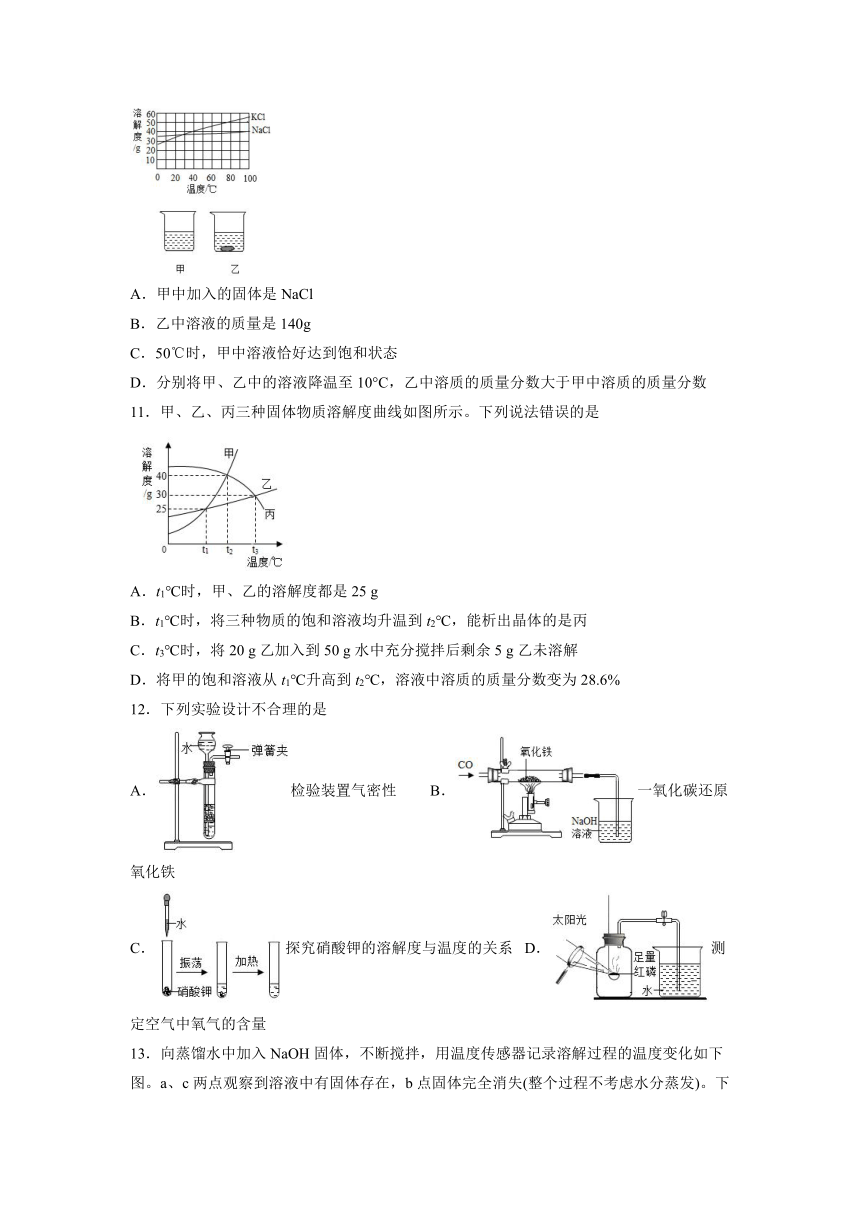
10.两种固体物质NaCl和KCl的溶解度曲线如图所示,现有40gNaC1、40gKCl两份固体,分别置于两只烧杯中,各倒入100g50°C蒸馏水充分溶解,实验现象如下图所示,下列推断正确的是
A.甲中加入的固体是NaCl
B.乙中溶液的质量是140g
C.50℃时,甲中溶液恰好达到饱和状态
D.分别将甲、乙中的溶液降温至10°C,乙中溶质的质量分数大于甲中溶质的质量分数
11.甲、乙、丙三种固体物质溶解度曲线如图所示。下列说法错误的是
A.t1℃时,甲、乙的溶解度都是25 g
B.t1℃时,将三种物质的饱和溶液均升温到t2℃,能析出晶体的是丙
C.t3℃时,将20 g乙加入到50 g水中充分搅拌后剩余5 g乙未溶解
D.将甲的饱和溶液从t1℃升高到t2℃,溶液中溶质的质量分数变为28.6%
12.下列实验设计不合理的是
A.检验装置气密性 B.一氧化碳还原氧化铁
C.探究硝酸钾的溶解度与温度的关系 D.测定空气中氧气的含量
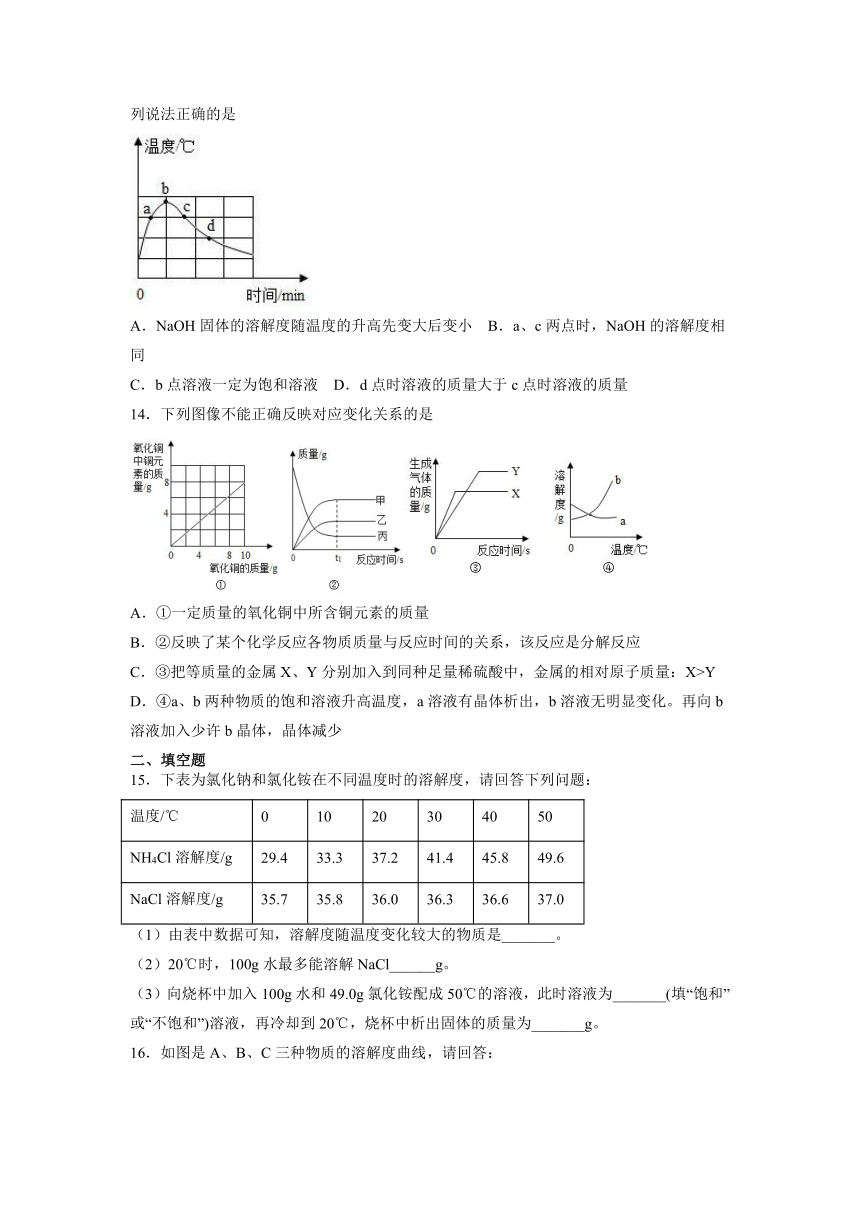
13.向蒸馏水中加入NaOH固体,不断搅拌,用温度传感器记录溶解过程的温度变化如下图。a、c两点观察到溶液中有固体存在,b点固体完全消失(整个过程不考虑水分蒸发)。下列说法正确的是
A.NaOH固体的溶解度随温度的升高先变大后变小 B.a、c两点时,NaOH的溶解度相同
C.b点溶液一定为饱和溶液 D.d点时溶液的质量大于c点时溶液的质量
14.下列图像不能正确反映对应变化关系的是
A.①一定质量的氧化铜中所含铜元素的质量
B.②反映了某个化学反应各物质质量与反应时间的关系,该反应是分解反应
C.③把等质量的金属X、Y分别加入到同种足量稀硫酸中,金属的相对原子质量:X>Y
D.④a、b两种物质的饱和溶液升高温度,a溶液有晶体析出,b溶液无明显变化。再向b溶液加入少许b晶体,晶体减少
二、填空题
15.下表为氯化钠和氯化铵在不同温度时的溶解度,请回答下列问题:
温度/℃ 0 10 20 30 40 50
NH4Cl溶解度/g 29.4 33.3 37.2 41.4 45.8 49.6
NaCl溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0
(1)由表中数据可知,溶解度随温度变化较大的物质是_______。
(2)20℃时,100g水最多能溶解NaCl______g。
(3)向烧杯中加入100g水和49.0g氯化铵配成50℃的溶液,此时溶液为_______(填“饱和”或“不饱和”)溶液,再冷却到20℃,烧杯中析出固体的质量为_______g。
16.如图是A、B、C三种物质的溶解度曲线,请回答:
(1)m点的含义是 ________
(2)t3℃时,A B C三种物质的溶解度由小到大的顺序是________。
(3)t3℃时,45克A物质放于50克水中,所得溶液为________溶液(填饱和或不饱和),所得溶液质量为_________。
(4)t3℃时,C物质的不饱和溶液500克,蒸发50克水或增加5克溶质,溶液都刚好达到饱和则该温度下该物质的溶解度为________g。
17.溶解是生活中常见的现象,下表是KNO3、NaC1在不同温度下的溶解度。请回答:
温度(℃) 0 10 20 30 40 50 60 70 80 90 100
KNO3/g 13.3 20.9 32 45.8 64 85.5 110 138 169 202 246
NaCl/g 35.7 35.8 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8
(1)20℃时,NaCl的溶解度是__________。
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为_________。
(3)60℃时,KNO3的饱和溶液中含有少量NaC1,通过__________方法获得较纯净的KNO3晶体。
(4)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则是蒸发前原溶液是_________(填“饱和”或“不饱和”)溶液,n的数值是________。
18.已知40℃时氯化钾的溶解度为40g,如图,甲中盛放的是20℃时的氯化钾溶液,其溶剂为100g。(忽略实验过程中水的损失)
请回答:
(1)甲中溶液是_______(填“饱和”或“不饱和”)溶液。
(2)乙中溶液溶质的质量是_______g。
(3)20℃时氯化钾的溶解度是________g。
(4)上述实验说明,氯化钾的溶解度随温度的升高而____(填“增大”或“减小”)。
19.如图是X、Y、Z三种固体物质的溶解度曲线。
(1)t2℃时,将35gX加入50g水中,充分搅拌,得到的溶液是______(填“饱和”或“不饱和”)溶液。
(2)将 X、Y、Z 三种物质的饱和溶液,由t2℃降温到t1℃没有固体析出的是______。
20.下图是a、b、C三种固体物质的溶解度曲线。
(1)根据图中C物质的溶解度曲线说明,C物质的溶解度的变化趋势是_______;
(2)配制浓的C溶液比配制稀的C溶液,选择的温度要_______(填:高或低)。
(3)20℃时,50g水中最多能溶解的a物质的质量是_______g,所得溶液的质量是_______g。
三、简答题
21.按照要求回答下列问题
(1)运用溶解度相关知识,回答打开可乐的瓶盖立即冒出大量气泡的原因是什么 ______
(2)小明在做饭时不慎将豆油滴在衣服上,他发现用洗洁精和汽油都能洗去,请解释这两种方法洗去豆油的原理分别是什么 ______
22.通过学习化学你会发现化学与生活息息相关。请回答:
(1)不能用铁质易拉罐盛放食醋,其原因是什么?______。
(2)喝雪碧等含有二氧化碳的汽水后会打嗝。能解释这一现象的化学原理是什么?______。
(3)用水后及时关闭水龙头是一种节约用水的做法。除了这种做法,说说你在生活中节约用水的另一种做法______。
23.控制变量是科学探究的重要方法之一。小华同学实验中发现:把质量相等的不同物质放入同样一杯水中,有的溶解快,有的溶解多,有的溶解又快又多。是哪些因素影响着物质溶解的快慢与多少呢
请你参考下表硝酸钾的溶解度随温度的变化关系,以硝酸钾为例,选择一种可能影响硝酸钾溶解快慢的因素设计实验进行探究:
温度(℃) 20 30 40 50 60 70 80
溶解度(g) 31.6 45.8 63.9 85.5 110 138 168
①影响因素:_____;
②实施方案:_____;
③通过实验得出_____。
24.如图为A、B、C三种物质的溶解度曲线,回答下列问题。
(1)当温度在t1℃(2) t1℃时,若要将210克B物质的饱和溶液稀释成溶质质量分数为10%的溶液,需要加水的质量为_____。
(3)分别将A、B、C的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系是_____。
四、综合应用题
25.人类的日常生活和工农业生产离不开水和溶液。请回答下列问题:
(1)如图所示,三个实验分别用到水。
请回答:
①实验A中热水的作用是提供热量和 ________ 。
②实验B能说明CO2可溶于水,同时发生的化学反应方程式为 ______ 。
③实验C,滴加水后看到U型管中 ______ (填“左边”或“右边”)液面升高。
(2)如图D是甲乙两种物质的溶解度曲线(不含结晶水)请回答下列问题:
①t1℃时,甲的溶解度是 _____ 。 ②下列说法一定正确的是 _______
A.甲的溶解度比乙的溶解度大
B.t1℃时,甲、乙的饱和溶液的溶质的质量分数相等
C.常温下,乙易溶于水
D.从t2℃降至t1℃,甲、乙溶液中均有晶体析出
③某同学设计的鉴别甲、乙固体的方案如下:t2℃时,取4.0g甲和4.0g乙分别放入两只小烧杯中,各加入10mL水(水的密度为1g/mL),用玻璃棒充分搅拌后,观察现象。你认为此方案是否可行?并说明理由 ____ 。
④甲中混有少量的乙,要提纯甲,实验步骤:加水溶解,蒸发浓缩, __________ ,然后过滤。
【参考答案】
1.C 2.B 3.C 4.D 5.B 6.B 7.D 8.D 9.D 10.D 11.D 12.B 13.B 14.C
15.(1)NH4Cl(2)36.0(3) 不饱和 11.8
16.(1)t2℃时,A、B物质的溶解度相等(2)A>B>C(3) 饱和 90g (4)10
17.(1)36g(2)164g(3)降温结晶(4) 不饱和 9
18.(1)不饱和(2)30(3)34(4)增大
19.(1)饱和(2)Z
20.(1)C物质溶解度随温度升高,逐渐降低(2)低(3) 5 55
21.气体的溶解度随着压强的减小而减小 洗洁精去除豆油是乳化,汽油去除豆油是溶解
22.食醋中的醋酸会和铁发生化学反反应,使食醋变质,铁质易拉罐被腐蚀(答出醋酸会和铁发生化学反应即可) 气体溶解度随温度的升高而减小 洗衣服水冲厕所或洗菜水浇花等(合理即可)
23.温度 取两只小烧杯,分别加入2g硝酸钾;在其中一只烧杯中倒入10ml冷水,另一只烧杯中加入10ml热水 硝酸钾在热水中溶解快,在冷水中溶解慢
24.能 390g B>A>C
25.隔绝氧气 CO2+H2O=H2CO3 左边 20g BC 可行,t2℃时4g甲能溶解在10g水中形成溶液,而4g乙不能全部溶解在10g水中形成溶液 降温结晶
一、选择题
1.下列说法正确的是
A.CO2可用于人工降雨,CO可用于光合作用 B.铝元素在地壳中含量最多,使用也最早
C.增加溶质可使不饱和溶液变为饱和溶液 D.鱼类能在水中生存,证明氧气易溶于水
2.下列说法正确的是
A.所有的变化一定符合质量守恒定律
B.氧化物一定是含有氧元素的纯净物
C.在化学反应中催化剂性质和质量一定不变
D.在一定温度下,饱和溶液一定比不饱和溶液浓
3.有关溶液的说法正确的是
A.溶液一定是液态的
B.所有溶质都以分子形式溶解在溶剂里
C.溶液具有均一性和稳定性
D.一定温度下,压强减小时,气体的溶解度会增大
4.谚语和诗词中蕴含着科学道理。下列说法正确的是
A.“冬天捞碱,夏天晒盐”—纯碱的溶解度随温度变化不大
B.“众人拾柴火焰高”—可燃物越多,着火点越低,越容易着火
C.“百炼成钢”和“只要功夫深,铁杵磨成针”—化学原理相同
D.“满架蔷薇一院香”—分子在不停地运动
5.下列事实的结论或解释不正确的是
A.变瘪的乒乓球遇到热水复原——温度升高,分子间隔变大
B.CO能燃烧,CO2不能燃烧——构成物质分子的原子种类不同
C.真金不怕火炼——金的化学性质稳定
D.打开汽水瓶盖冒出大量气泡——气体的溶解度随压强减小而减小
6.溶液与人们的生活息息相关。下列有关溶液的说法正确的是
A.均一、稳定的液体都是溶液
B.同一温度下,硝酸铵的饱和溶液比不饱和溶液浓
C.溶液中都存在大量自由移动的离子
D.饱和溶液析出晶体后溶质质量分数一定变小
7.有一杯t℃时的硝酸钾溶液,在该溶液中加入27克硝酸钾晶体,充分搅拌后有11克没有溶解;若将原溶液加热蒸发掉40克水再冷却至原温度,溶液恰好达到饱和,则t℃时硝酸钾的溶解度为
A.50 克 B.28 C.36克 D.40克
8.NaCl 和 KNO3 在不同温度时的溶解度如下表。下列说法正确的是
温度/C 0 20 40 60
NaCI的溶解度/g 35.7 36.0 36.6 37.3
KNO3的溶解度/g 13.3 31.6 63.9 110
A.20℃时,100 g氯化钠溶液中最多能溶解36.0g NaCl
B.40℃时,KNO3饱和溶液的溶质质量分数等于63.9%
C.可用冷却海水的方法获取大量食盐
D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
9.提纯含少量NaCl杂质的KNO3,部分实验过程如下。相关物质的溶解度曲线如图所示。下列说法正确的是
A.①→②,KNO3的溶解度不变
B.①→②,溶液中KNO3的质量分数不变
C.②→③,溶液中NaCl的质量增大
D.②→③,溶液中KNO3的质量减小
10.两种固体物质NaCl和KCl的溶解度曲线如图所示,现有40gNaC1、40gKCl两份固体,分别置于两只烧杯中,各倒入100g50°C蒸馏水充分溶解,实验现象如下图所示,下列推断正确的是
A.甲中加入的固体是NaCl
B.乙中溶液的质量是140g
C.50℃时,甲中溶液恰好达到饱和状态
D.分别将甲、乙中的溶液降温至10°C,乙中溶质的质量分数大于甲中溶质的质量分数
11.甲、乙、丙三种固体物质溶解度曲线如图所示。下列说法错误的是
A.t1℃时,甲、乙的溶解度都是25 g
B.t1℃时,将三种物质的饱和溶液均升温到t2℃,能析出晶体的是丙
C.t3℃时,将20 g乙加入到50 g水中充分搅拌后剩余5 g乙未溶解
D.将甲的饱和溶液从t1℃升高到t2℃,溶液中溶质的质量分数变为28.6%
12.下列实验设计不合理的是
A.检验装置气密性 B.一氧化碳还原氧化铁
C.探究硝酸钾的溶解度与温度的关系 D.测定空气中氧气的含量
13.向蒸馏水中加入NaOH固体,不断搅拌,用温度传感器记录溶解过程的温度变化如下图。a、c两点观察到溶液中有固体存在,b点固体完全消失(整个过程不考虑水分蒸发)。下列说法正确的是
A.NaOH固体的溶解度随温度的升高先变大后变小 B.a、c两点时,NaOH的溶解度相同
C.b点溶液一定为饱和溶液 D.d点时溶液的质量大于c点时溶液的质量
14.下列图像不能正确反映对应变化关系的是
A.①一定质量的氧化铜中所含铜元素的质量
B.②反映了某个化学反应各物质质量与反应时间的关系,该反应是分解反应
C.③把等质量的金属X、Y分别加入到同种足量稀硫酸中,金属的相对原子质量:X>Y
D.④a、b两种物质的饱和溶液升高温度,a溶液有晶体析出,b溶液无明显变化。再向b溶液加入少许b晶体,晶体减少
二、填空题
15.下表为氯化钠和氯化铵在不同温度时的溶解度,请回答下列问题:
温度/℃ 0 10 20 30 40 50
NH4Cl溶解度/g 29.4 33.3 37.2 41.4 45.8 49.6
NaCl溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0
(1)由表中数据可知,溶解度随温度变化较大的物质是_______。
(2)20℃时,100g水最多能溶解NaCl______g。
(3)向烧杯中加入100g水和49.0g氯化铵配成50℃的溶液,此时溶液为_______(填“饱和”或“不饱和”)溶液,再冷却到20℃,烧杯中析出固体的质量为_______g。
16.如图是A、B、C三种物质的溶解度曲线,请回答:
(1)m点的含义是 ________
(2)t3℃时,A B C三种物质的溶解度由小到大的顺序是________。
(3)t3℃时,45克A物质放于50克水中,所得溶液为________溶液(填饱和或不饱和),所得溶液质量为_________。
(4)t3℃时,C物质的不饱和溶液500克,蒸发50克水或增加5克溶质,溶液都刚好达到饱和则该温度下该物质的溶解度为________g。
17.溶解是生活中常见的现象,下表是KNO3、NaC1在不同温度下的溶解度。请回答:
温度(℃) 0 10 20 30 40 50 60 70 80 90 100
KNO3/g 13.3 20.9 32 45.8 64 85.5 110 138 169 202 246
NaCl/g 35.7 35.8 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8
(1)20℃时,NaCl的溶解度是__________。
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为_________。
(3)60℃时,KNO3的饱和溶液中含有少量NaC1,通过__________方法获得较纯净的KNO3晶体。
(4)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则是蒸发前原溶液是_________(填“饱和”或“不饱和”)溶液,n的数值是________。
18.已知40℃时氯化钾的溶解度为40g,如图,甲中盛放的是20℃时的氯化钾溶液,其溶剂为100g。(忽略实验过程中水的损失)
请回答:
(1)甲中溶液是_______(填“饱和”或“不饱和”)溶液。
(2)乙中溶液溶质的质量是_______g。
(3)20℃时氯化钾的溶解度是________g。
(4)上述实验说明,氯化钾的溶解度随温度的升高而____(填“增大”或“减小”)。
19.如图是X、Y、Z三种固体物质的溶解度曲线。
(1)t2℃时,将35gX加入50g水中,充分搅拌,得到的溶液是______(填“饱和”或“不饱和”)溶液。
(2)将 X、Y、Z 三种物质的饱和溶液,由t2℃降温到t1℃没有固体析出的是______。
20.下图是a、b、C三种固体物质的溶解度曲线。
(1)根据图中C物质的溶解度曲线说明,C物质的溶解度的变化趋势是_______;
(2)配制浓的C溶液比配制稀的C溶液,选择的温度要_______(填:高或低)。
(3)20℃时,50g水中最多能溶解的a物质的质量是_______g,所得溶液的质量是_______g。
三、简答题
21.按照要求回答下列问题
(1)运用溶解度相关知识,回答打开可乐的瓶盖立即冒出大量气泡的原因是什么 ______
(2)小明在做饭时不慎将豆油滴在衣服上,他发现用洗洁精和汽油都能洗去,请解释这两种方法洗去豆油的原理分别是什么 ______
22.通过学习化学你会发现化学与生活息息相关。请回答:
(1)不能用铁质易拉罐盛放食醋,其原因是什么?______。
(2)喝雪碧等含有二氧化碳的汽水后会打嗝。能解释这一现象的化学原理是什么?______。
(3)用水后及时关闭水龙头是一种节约用水的做法。除了这种做法,说说你在生活中节约用水的另一种做法______。
23.控制变量是科学探究的重要方法之一。小华同学实验中发现:把质量相等的不同物质放入同样一杯水中,有的溶解快,有的溶解多,有的溶解又快又多。是哪些因素影响着物质溶解的快慢与多少呢
请你参考下表硝酸钾的溶解度随温度的变化关系,以硝酸钾为例,选择一种可能影响硝酸钾溶解快慢的因素设计实验进行探究:
温度(℃) 20 30 40 50 60 70 80
溶解度(g) 31.6 45.8 63.9 85.5 110 138 168
①影响因素:_____;
②实施方案:_____;
③通过实验得出_____。
24.如图为A、B、C三种物质的溶解度曲线,回答下列问题。
(1)当温度在t1℃
(3)分别将A、B、C的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系是_____。
四、综合应用题
25.人类的日常生活和工农业生产离不开水和溶液。请回答下列问题:
(1)如图所示,三个实验分别用到水。
请回答:
①实验A中热水的作用是提供热量和 ________ 。
②实验B能说明CO2可溶于水,同时发生的化学反应方程式为 ______ 。
③实验C,滴加水后看到U型管中 ______ (填“左边”或“右边”)液面升高。
(2)如图D是甲乙两种物质的溶解度曲线(不含结晶水)请回答下列问题:
①t1℃时,甲的溶解度是 _____ 。 ②下列说法一定正确的是 _______
A.甲的溶解度比乙的溶解度大
B.t1℃时,甲、乙的饱和溶液的溶质的质量分数相等
C.常温下,乙易溶于水
D.从t2℃降至t1℃,甲、乙溶液中均有晶体析出
③某同学设计的鉴别甲、乙固体的方案如下:t2℃时,取4.0g甲和4.0g乙分别放入两只小烧杯中,各加入10mL水(水的密度为1g/mL),用玻璃棒充分搅拌后,观察现象。你认为此方案是否可行?并说明理由 ____ 。
④甲中混有少量的乙,要提纯甲,实验步骤:加水溶解,蒸发浓缩, __________ ,然后过滤。
【参考答案】
1.C 2.B 3.C 4.D 5.B 6.B 7.D 8.D 9.D 10.D 11.D 12.B 13.B 14.C
15.(1)NH4Cl(2)36.0(3) 不饱和 11.8
16.(1)t2℃时,A、B物质的溶解度相等(2)A>B>C(3) 饱和 90g (4)10
17.(1)36g(2)164g(3)降温结晶(4) 不饱和 9
18.(1)不饱和(2)30(3)34(4)增大
19.(1)饱和(2)Z
20.(1)C物质溶解度随温度升高,逐渐降低(2)低(3) 5 55
21.气体的溶解度随着压强的减小而减小 洗洁精去除豆油是乳化,汽油去除豆油是溶解
22.食醋中的醋酸会和铁发生化学反反应,使食醋变质,铁质易拉罐被腐蚀(答出醋酸会和铁发生化学反应即可) 气体溶解度随温度的升高而减小 洗衣服水冲厕所或洗菜水浇花等(合理即可)
23.温度 取两只小烧杯,分别加入2g硝酸钾;在其中一只烧杯中倒入10ml冷水,另一只烧杯中加入10ml热水 硝酸钾在热水中溶解快,在冷水中溶解慢
24.能 390g B>A>C
25.隔绝氧气 CO2+H2O=H2CO3 左边 20g BC 可行,t2℃时4g甲能溶解在10g水中形成溶液,而4g乙不能全部溶解在10g水中形成溶液 降温结晶
同课章节目录
