13.1食物中的营养物质-2021-2022学年九年级化学京改版(2013)九年级下册(word版 含解析)
文档属性
| 名称 | 13.1食物中的营养物质-2021-2022学年九年级化学京改版(2013)九年级下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 133.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-06 00:00:00 | ||
图片预览




文档简介
13.1食物中的营养物质
一、选择题(共16题)
1.甘蔗中含有丰富的糖类、水,此外,还含有对人体新陈代谢非常有益的各种维生素、有机酸、钙、铁等物质,经常食用有益人体健康。下列甘蔗中含有的营养物质主要能提供能量的是
A.糖类 B.有机酸 C.钙、铁元素 D.维生素
2.长期受电磁辐射可引起人头昏、头痛、失眠等症状,科学家发现富含维生素的食物具有较好的防辐射损伤功能。下列食物中富含维生素的是
A.豆腐 B.西红柿 C.鸡蛋 D.牛肉
3.糖类是能为人体提供能量的重要营养成分之一。下列食物中,富含糖类物质的是
A.鸡蛋 B.面包 C.青菜 D.花生油
4.民生热词:“舌尖上的安全”。下列做法符合食品安全要求的是
A.甲醛浸泡水产品保鲜
B.为了促进消化,牛奶发酵后制成酸奶再食用
C.亚硝酸钠代替食盐烹调食物
D.为了防止骨质疏松,长期摄入过量的钙元素
5.中原大地盛产小麦,面条是中原人家餐桌上的主食。面条为人们提供的营养素为
A.蛋白质 B.维生素 C.油脂 D.糖类
6.下列疾病可能与缺锌有关的是
A.佝偻病 B.侏儒症 C.贫血症 D.甲状腺肿大
7.人类的健康离不开化学,下列说法合理的是
A.不食用富含蛋白质的食品
B.发霉食品不可食用
C.长期饮用纯净水有利于人体健康
D.食用大米可以补充油脂
8.青少年身体生长发育需要蛋白质,下列广东美食中富含蛋白质的是
A.客家娘酒 B.潮汕卤鹅 C.广式叉烧包 D.陈村米粉
9.2016年7月河北普降大暴雨,造成较大的人员伤亡和财产损失,在救援过程中,医护人员向受伤人群输送大量营养液。该营养液中主要供能物质是
A.水 B.葡萄糖 C.维生素 D.氯化钠
10.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。近年来科学家还发现维生素C有防癌作用。下列关于维生素C的说法中正确的是
A.维生素C是氧化物
B.青少年应多吃蔬菜水果,切勿偏食
C.维生素是由6个碳元素、8个氢元素和15个氧元素组成的
D.维生素C中C、H、O三种元素的原子个数比为9:1:2
11.推理是一种常用的化学学习方法.下列各推理中,正确的是
A.燃烧时发光发热,所以发光发热的变化一定是燃烧
B.氧化物含氧元素,所以含氧元素的物质一定是氧化物
C.碘元素可预防甲状腺疾病,所以需尽可能多补充碘元素
D.单质只含有一种元素,所以只含有一种元素的纯净物一定是单质
12.下列说法正确的是
A.生成盐和水的反应不一定是中和反应
B.Ca、Cr、Se 都是人体必需微量元素
C.水变成冰后体积变大,是因为水分子变大了
D.有机物一定含碳元素,无机物一定不含碳元素
13.下列我市特产中,维生素含量最高的是
A.阜宁大糕 B.龙冈茌梨 C.滨海香肠 D.伍佑糖麻花
14.由于受日本大地震的影响,国内出现了抢购“加碘食盐”的现象,加碘食盐中的“碘”指的是
A.单质 B.分子 C.原子 D.元素
15.下列现象的描述正确的是
A.打开浓盐酸试剂瓶,瓶口出现大量白烟
B.加碘盐的溶液滴到米汤中会出现蓝色
C.铜绿加热后生成黑色固体,管口有水珠,产生能使澄清石灰水变浑浊的气体
D.紫色石蕊试液中通入二氧化碳变红,加热溶液变成无色
16.下列归类不正确的是
选 项 归 类 内容
A 清洁能源 风能、氢能、太阳能
B 常见合金 黄铜、硬铝、磁铁矿
C 碳水化合物 淀粉、葡萄糖、纤维素
D 常见氮肥 碳铵、氨水、尿素
A.A B.B C.C D.D
二、综合题(共8题)
17.化学与生活密切相关,在厨房里蕴藏着许多化学知识。
(1)下列食物中,能提供大量维生素的是_______(填字母序号);
A蔬菜 B牛奶 C大米
(2)加钙牛奶是为了补充钙质,中老年人身体中一旦缺钙,可能患有的疾病是_______;
(3)厨房中用来做面包的发酵粉的主要成分为________(填化学式)。
18.学好化学有助于我们科学地处理和解决生活中的问题。
(1)净水器中可以用______有效地除去水中的异味。
(2)厨房里可以用______来洗涤水壶中的水垢(主要成分是CaCO3和Mg(OH)2)。
(3)利用洗涤剂的______功能来除去衣物上的油污。
(4)青少年多食用豆类、虾皮等富含______元素的食物可以有效预防佝偻病。
19.2018年12月11日是广西壮族自治区成立60周年纪念日,人民日报微信公众号发布了一则微视频《广西一分钟》。
(1)一分钟,184人在桂林山水间自在畅游。漓江的水清澈透明,若想鉴别漓江水属于硬水或软水,可以使用_____。
(2)一分钟,556袋柳州螺蛳粉通过电商售出。螺蛳粉的主要成分﹣﹣粉属于六大营养素中的_____。
(3)一分钟,产出33.4吨糖。榨糖中用到活性炭,主要是利用其_____。
(4)一分钟,完成植树造林4491平方米。绿色植物在光合作用中可以把_____能转化为_____能。
(5)一分钟,体会壮乡美味。品尝美食后用洗洁精清洗碗盘,属于_____作用。
20.酱油是中国的传统调味品。下表是某酱油油膏的部分营养成分列表,根据所学知识回答。
酱油膏的部分营养成分列表(每100克中含)
成分名称 含量 成分名称 含量 成分名称 含量
水分(克) 54.7 蛋白质(克) 13 脂肪(克) 0.7
糖类(克) 10.2 钠(毫克) 7700 钙(毫克) 46
铁(克) 8.6 硒(微克) 2.96 …… ……
(1)上表中不含六大基本营养素中_____________;
(2)上表中“钠”、“钙”等指是___________(填“单质”“分子”“原子”或“元素”);
(3)老年人每天都要摄入足量的钙,有利于防止___________________;
(4)糖类主要是给人体提供能量,写出葡萄糖(C6H12O6)在酶的作用下进行呼吸作用的化学方程式______________。
21.⑴ 请从下列物质中选择适当的物质填空(填序号):
A.干冰 B.盐酸 C.明矾 D.生石灰 E.葡萄糖
①能被人体直接吸收的营养物质是________; ②可用于人工降雨的物质是________; ③可用于净水的物质是________; ④常用作袋装食品的干燥剂________。
⑵ 根据题意用下列选项的字母填空:A.熔点 B.沸点 C.硬度
①工业制氧气和石油分馏都是利用混合物中各成分的________不同;
②武德合金用作保险丝比用纯铜丝更安全,是因为前者的________低。
22.金属材料的应用推动了社会的发展。
(1)铁是年产量最高的金属。中国人烹饪常使用铁锅,铁做炊具主要利用了其_______性,铁锅炒菜时少量铁元素会随着烹饪进人食物,有利于预防_______(填疾病名称)。某混合物由铁、锌、铝、镁中的两种组成,取2.4g该混合物与足量的稀硫酸反应,生成0.2g气体,则该混合物中一定含有的金属是_____
(2)用足量的细铁丝进行如图所示实验,放置足够长的时间后,观察到试管中的水面上升至1处,请解释原因_______。
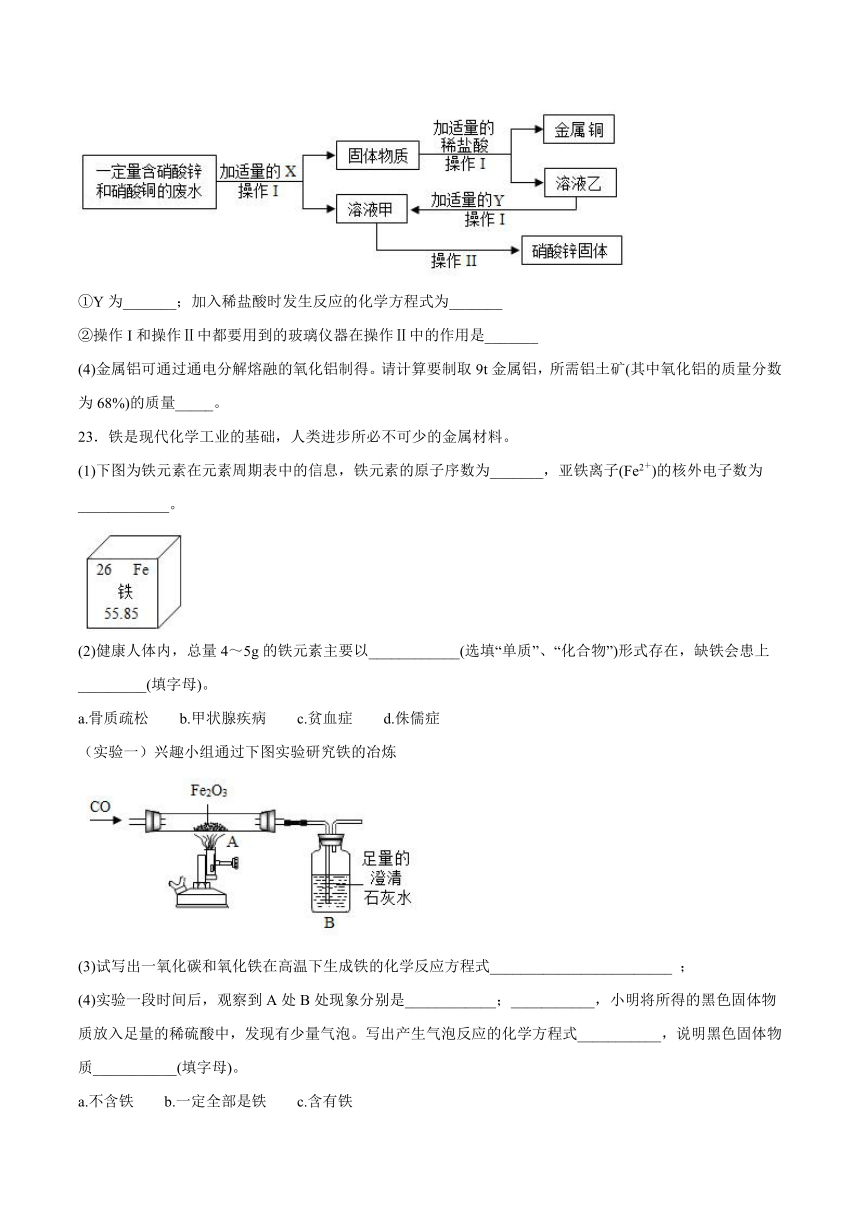
(3)为实现工业废水的综合利用、回收金属资源,某化学小组进行了以下探究:
①Y为_______;加入稀盐酸时发生反应的化学方程式为_______
②操作I和操作Ⅱ中都要用到的玻璃仪器在操作Ⅱ中的作用是_______
(4)金属铝可通过通电分解熔融的氧化铝制得。请计算要制取9t金属铝,所需铝土矿(其中氧化铝的质量分数为68%)的质量_____。
23.铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)下图为铁元素在元素周期表中的信息,铁元素的原子序数为_______,亚铁离子(Fe2+)的核外电子数为____________。
(2)健康人体内,总量4~5g的铁元素主要以____________(选填“单质”、“化合物”)形式存在,缺铁会患上_________(填字母)。
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
(实验一)兴趣小组通过下图实验研究铁的冶炼
(3)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式________________________ ;
(4)实验一段时间后,观察到A处B处现象分别是____________;___________,小明将所得的黑色固体物质放入足量的稀硫酸中,发现有少量气泡。写出产生气泡反应的化学方程式___________,说明黑色固体物质___________(填字母)。
a.不含铁 b.一定全部是铁 c.含有铁
(资料1)已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
(资料2)实验研究表明:该实验得到的是四氧化三铁与铁粉的混合物
(实验二)兴趣小组用下图实验研究实验一所得黑色粉末中单质铁的质量分数
(资料3)氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,且吸收能力比石灰水强
(5)从安全与规范的角度考虑,装置C后面应连接__________(选填装置序号D或E),B装置的作用是___________。
(6)铁与四氧化三铁的混合物10 g充分反应后,玻璃管中剩余固体(单质铁)的质量为8.4g。请计算10 g黑色粉末中单质铁的质量分数________ 。
(实验三)兴趣小组为探究生铁中铁的含量(生铁中只考虑铁,碳),设计有关方案,取0.58克生铁放于试管中,实验中将注射器内76毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为300毫升。已知实验条件下氢气的密度为0.09g/L。
(7)计算生铁中铁的质量分数为_______ (写出计算过程,氢气质量保留两位小数,结果保留到0.1℅)
(8)上述方法测得的生铁中铁的质量分数偏小,可能的原因是_______
A.没等装置冷却就读数 B.生铁中含有少量锌
C.试管中有氢气没有排出 D.将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
24.(1)水是宝贵的自然资源,我国南海海域海洋资源极其丰富。
①2017年5月18日,南海可燃冰试采成功,可燃冰主要含有甲烷水合物。甲烷中碳元素的化合价是______价,甲烷充分燃烧的化学方程式是__________________。
②渔民常在这一带从事捕鱼作业,鱼肉中含量最多的营养素是_____(填序号)。
A.糖类 B.油脂 C.蛋白质 D.维生素
③科学研究证明,水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气,反应的化学方程式是____________________。
④河水和海水一样都是混合物。自来水厂利用河水生产饮用水的过程中常用活性炭的_____性来除去水中的色素和异味。检验饮用水是软水还是硬水,可用___来检验。
(2)能源利用和环境保护是人类共同关注的问题。
①下列说法中正确的是______(填字母)。
A.煤、石油和天然气都属于可再生能源 B.氢气是理想的“绿色能源”
C.人类使用的能源绝大部分来自太阳能 D.废弃电池可以填埋在土壤里
②煤燃烧时排放出的二氧化硫等污染物,有可能会导致降雨的酸性增强。我们把pH_____5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石浆来吸收二氧化硫,其反应的化学方程式为:2CaCO3+2SO2+O2=2CaSO4+2x,则x的化学式为______。
③研究发现,二氧化碳和氢气在催化剂作用下转化为甲醇(CH3OH)和水。该反应的化学方程式为______________________。
④将一定质量的甲醇与8.8g氧气混合于密闭容器内,在一定条件下,发生如下反应:8CH3OH+xO2 一定条件 mCO2+nCO+16H2O。当反应物完全耗尽且全部转化为生成物时,有7.2g水生成,同时生成二氧化碳的质量为______g。
参考答案
1.A
【详解】
能提供能量的主要营养物质是糖类、油脂,总能量中有60%~70%来自糖类,故选A。
2.B
【详解】
A、豆腐中富含蛋白质,故选项错误。
B、西红柿中富含维生素,故选项正确。
C、鸡蛋中富含蛋白质,故选项错误。
D、牛肉中富含蛋白质,故选项错误。
故选:B。
3.B
【详解】
A、鸡蛋中富含有蛋白质,故A错;
B、面包中富含有淀粉,属于糖类,故B正确;
C、青菜中富含有维生素,故C错;
D、花生油中富含有油脂,故D错。
故选:B。
4.B
【详解】
A、甲醛具有毒性,不得浸泡海鲜保鲜,选项A错误;
B、酸奶更利于人体吸收,可促进消化,所以可以将牛奶发酵制成酸奶食用,选项B正确;
C、亚硝酸钠有毒,不得食用,选项C错误;
D、摄入过量的钙元素容易造成结石、高钙血症等病症,所以需要适当补钙,选项D错误。故选B。
5.D
【详解】
面条的主要成分是淀粉,淀粉属于糖类,故选D。
6.B
【详解】
A. 缺钙易患佝偻病,此选项不符合题意;
B. 严重缺锌会导致蛋白质合成障碍,从而引起体内生长激素分泌不足而诱发侏儒症,此选项符合题意;
C. 缺铁会患缺铁性贫血,此选项不符合题意;
D. 缺碘易患甲状腺肿大疾病,此选项不符合题意。
故选B。
7.B
【详解】
A.蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料,故应食用含蛋白质的食物,且一日三餐应该包含六大营养素, 使营养均衡,A错误;
B.霉变食物中含有黄曲霉素,有剧毒,不可食用,B正确;
C.纯净水几乎不含矿物质,长期饮用不利于身体健康,C错误;
D.大米中含有丰富的糖类,D错误。
故选:B。
8.B
【详解】
A、客家娘酒富含水和酒精,不符合题意;
B、潮汕卤鹅富含蛋白质,符合题意;
C、广式叉烧包富含淀粉,淀粉属于糖类,不符合题意;
D、陈村米粉富含淀粉,淀粉属于糖类,不符合题意。
故选B。
9.B
【详解】
A. 水不能提供能量,不符合题意 ;B. 葡萄糖 属于糖类,是人体最直接的供能物质 ,不需要消化,能直接被人吸收,所以常用于给病人输液;C. 维生素主要功能是调节新陈代谢,不能提供能量,不符合题意; D. 氯化钠,属于无机盐,不能提供能量,不符合题意。故选B。
10.B
【详解】
A. 氧化物是由两种元素组成的化合物,其中一种元素是氧元素。维生素C含有三种元素,不是氧化物,此选项错误;
B. 蔬菜水果富含维生素,青少年应多吃蔬菜水果,切勿偏食,此选项正确;
C. 维生素C是由维生素C分子构成的,每个维生素C分子是由6个碳原子、8个氢原子和6个氧原子构成的,此选项错误;
D. 维生素C中C、H、O三种元素的原子个数比为6:8:6=3:4:3,此选项错误。
故选B。
11.D
【详解】
单质只含有一种元素,所以只含有一种元素的纯净物一定是单质;燃烧时发光发热,但是发光发热的变化不一定是燃烧,比如灯泡的发光灯;氧化物含氧元素,含氧元素的物质不一定是氧化物,比如氧气;碘元素可预防甲状腺疾病,但不能多补充碘元素,碘是一种微粒元素。故选D.
12.A
【详解】
A、中和反应指的是酸和碱反应生成盐和水的反应,但是生成盐和水的反应不一定是中和反应,例如金属氧化物和酸反应生成盐和水,不属于中和反应,A选项说法正确,符合题意;
B、Ca是人体必需常量元素,Cr、Se 是人体必需微量元素,B选项说法不正确,不符合题意;
C、水变成冰后体积变大,是因为水分子之间的间隔变大了,C选项说法不正确,不符合题意;
D、有机物一定含碳元素,无机物可能含碳元素,例如碳酸钙、二氧化碳等无机物含有碳元素,D选项说法不正确,不符合题意。故选A。
13.B
【详解】
A、阜宁大糕富含糖类和油脂;
B、龙冈茌梨是一种富含维生素的水果;
C、滨海香肠中富含蛋白质和油脂;
D、伍佑糖麻花含有丰富的糖类和油脂;
故选B.
14.D
【详解】
加碘食盐中的“碘”存在于无机盐中,有利于人体吸收,则碘是指元素.
故选D.
15.C
【详解】
A、浓盐酸具有挥发性,打开浓盐酸的瓶塞,挥发出的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,从而形成白雾,故瓶口出现白雾,而不是白烟,故选项说法错误;
B、淀粉遇碘变蓝色,米汤中富含淀粉,但加碘盐中不含碘单质,加碘盐的溶液滴到米汤中不会出现蓝色,故选项说法错误;
C、铜绿加热生成氧化铜、水和二氧化碳,铜绿加热后生成黑色固体,管口有水珠,产生能使澄清石灰水变浑浊的气体,故选项说法正确;
D、紫色石蕊试液中通入二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色;加热溶液,碳酸分解生成水和二氧化碳,溶液变成紫色,故选项说法错误。
故选:C。
16.B
【详解】
A、风能、氢能、太阳能均属于清洁能源,不符合题意;
B、黄铜、硬铝都属于合金,磁铁矿属于铁矿石,不属于合金,符合题意;
C、淀粉、葡萄糖、纤维素都属于糖类,属于碳水化合物,不符合题意;
D、碳铵、氨水和尿素中均含有氮元素,属于氮肥,不符合题意。故选B。
17.A 骨质疏松 NaHCO3
【详解】
(1)蔬菜水果富含维生素,故选A。
(2)加钙牛奶是为了补充钙质,中老年人身体中一旦缺钙,可能患有的疾病是骨质疏松;
(3)厨房中用来做面包的发酵粉的主要成分为NaHCO3。
18.活性炭 食醋 乳化 钙
【详解】
(1)活性炭具有吸附性,净水器中可以用活性炭有效地去除水中的异味。
(2)水垢的主要成分是CaCO3和Mg(OH)2,能与酸反应,可以利用厨房中的食醋清洗水壶中的水垢。
(3)洗涤剂具有乳化作用,将大分子团油污分成小分子团油滴,能除去衣物上的油污;
(4)豆类、虾皮中富含钙元素,青少年多食用豆类、虾皮等富含钙元素的食物可以有效预防佝偻病。
19.肥皂水 糖类 吸附性 太阳 化学 乳化
【详解】
(1)硬水中加入肥皂水产生泡沫少,软水中加入肥皂水产生泡沫多,可用肥皂水来检验硬水或软水;
(2)螺蛳粉的主要成分﹣﹣粉属于六大营养素中的糖类;
(3)活性炭具有吸附性,可以除去色素;
(4)绿色植物在光合作用中可以把太阳能转化为化学能;
(5)洗洁精对油污起到了乳化作用,所以可用洗洁精清洗碗盘。
20.维生素 元素 骨质疏松
【详解】
(1)人体所需的六大营养素是:蛋白质、糖类、油脂、维生素、无机盐和水,从表中提供的营养成分可知,表中含蛋白质、水、糖类、无机盐、油脂,故表中不含六大基本营养素中的维生素;
(2)上表中“钠”“钙”等不是指以单质、分子、原子等形式存在,这里所指的“钠、钙”是强调存在的元素,与具体形态无关,故填:元素;
(3)老年人缺钙容易患骨质疏松,故老年人每天都要摄入足量的钙,有利于防止骨质疏松;
(4)葡萄糖(C6H12O6)在酶的作用下进行呼吸作用生成二氧化碳和水,该反应的化学方程式为:。
21.E A C D B A
【详解】
(1) ①能被人体直接吸收的营养物质是葡萄糖;②干冰升华吸热,可用于人工降雨;③可用于净水的物质是明矾;④常用作装食品的干燥剂生石灰;(2)①工业制氧气和工业石油分馏都是利用混合物中各成分的沸点不同;②武德合金用作保险丝比用纯铜丝更安全,是因为前者的熔点低。
22.导热 缺铁性贫血 铝 细铁丝与空气中的氧气反应(也就是生锈),氧气被消耗完之后,外界大气压与内部产生压强差 硝酸银 HCl+AgNO3=AgCl↓+HNO3 搅拌以防止液体局部温度过高造成液滴飞溅 可知该反应的方程式为,
设需要氧化铝的质量为 x。
解得 x=17t,
铝土矿中氧化铝的质量分数为68%,17t为氧化铝的质量铝士矿质量为
【详解】
(1)铁做炊具主要利用了其导热性,铁锅炒菜时少量铁元素会随着烹饪进人食物,有利于预防缺铁性贫血,锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑,铁和稀硫酸Fe+H2SO4=FeSO4+H2↑;镁和稀硫酸Mg+H2SO4=MgSO4+H2↑,铝和稀硫酸2A1+3H2SO4=Al2(SO4)3+3H2↑,若四种金属分别产生 0. 2g气体,需要铁5. 6g、锌6. 5g、铝1. 8g、镁2. 4g由于混合物由两种金属组成,则所需金属质量一个得大于2. 4g,一个得小于2. 4g大于2. 4g的铁、锌小于2. 4g的只有铝,故合物中一定含有铝;
(2)细铁丝在空气中放置足够长的时间之后会与空气中的氧气反应(也就是生锈),氧气被消耗完之后,外界大气压与内部产生压强差,所以水面会上升;
(3)锌能和硝酸铜反应生成硝酸锌和铜,X为锌,溶液甲为硝酸锌,溶液乙为氯化锌,硝酸银和氯化锌反应生成硝酸锌和氯化银沉淀,Y为硝酸银。
①根据分析可知,Y为硝酸银,硝酸银和稀盐酸反应生成氯化银和硝酸,反应的化学方程式为:HCl+AgNO3=AgCl↓+HNO3;
②操作I和操作II分别是过滤操作和蒸发操作,其中都要用到的玻璃仪器是玻璃棒,玻璃棒在蒸发操作中的作用是搅拌以防止液体局部温度过高造成液滴飞溅;
(4)见答案。
23.26 24 化合物 c 红棕色固体变黑 澄清石灰水变浑浊 c E 防止倒吸,安全瓶 42% 96.6% BD
【详解】
(1)铁的原子序数为26;在原子中原子序数=质子数=核外电子数,故铁原子有26个电子,形成亚铁离子时失去了2个电子,故亚铁离子还有24个电子;(2)元素在人体内主要是以化合物的形式存在的,缺铁易患贫血;(3)一氧化碳还原氧化铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为;(4)由化学反应的化学方程式可知,红棕色的氧化铁被还原成黑色的铁,同时生成能使澄清石灰水变浑浊的二氧化碳气体,实验一段时间后,观察到A处B处现象分别是红棕色固体变黑;澄清石灰水变浑浊;铁能与稀硫酸反应生成硫酸亚铁和氢气,此现象说明黑色固体中含有铁,但不一定全部是铁。故化学方程式为:;(5)氢氧化钠溶液具有强烈的腐蚀性,且会从C中溢出,从安全与规范的角度考虑,装置C后面应连接E,B装置是安全瓶,防止溶液倒吸;(6)设四氧化三铁的质量为,由四氧化三铁和一氧化碳反应的化学方程式可知固体减少的质量就是四氧化三铁中氧元素的质量可知:
固体减少的质量
232 232-168=64
10g-8.4g=1.6g
=5.8g
则混合物中铁的质量分数为:
答:10g黑色粉末中单质铁的质量分数为42%。
(7)生成氢气的质量为(0.3L 0.076L)×0.09g/L=0.02g
设铁的质量为。
56 2
0.02g
=0.56g
生铁中铁的质量分数为;
(8)A、没等装置冷却就读数,气体膨胀,气体的体积较大,测得的铁的质量分数偏大;B、相同质量锌和铁与足量的酸反应,铁生成的氢气的质量大,生铁中含有少量锌,生成氢气的质量偏小,测得的铁的质量分数偏小;C、试管中有气体没有排出,排入集气瓶中,正好等于产生氢气的体积,对结果没影响。D、将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹,少量气体从注射器中逸出,导致压过去的水的体积减小,使测量到的氢气体积减小,测得的铁的质量分数会偏小。故选BD。
24.-4 CH4+2O2 CO2+2H2O C 2H2O2H2↑+O2↑ 吸附 肥皂水 BC < CO2 CO2+3H2 CH3OH+H2O 6.6
【解析】
(1) ①根据根据化合物中各元素正负化合价代数和为0及甲烷燃烧生成二氧化碳和水解答;②根据肉类主要富含蛋白质解答;③根据水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气解答;④根据活性炭有吸附性及用肥皂水检验软水和硬水解答;(2)①根据能源的分类及其对环境的影响来分析;②根据酸雨的形成与质量守恒定律来分析;③根据反应物和生成物书写有关反应的化学方程式;④依据质量守恒定律的有关应用解答即可;依据已知的化学方程式利用水的质量可以求出生成的二氧化碳质量。(1) ①甲烷中氢元素显+1价,碳元素的化合价是[0-(+1×4)]=-4;甲烷和氧气在点燃条件下生成二氧化碳和水,的化学方程式是CH4+2O2 点燃 2H2O+CO2;②肉、蛋、奶、大豆类食品给人提供丰富的蛋白质,故选C;(3)水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气,反应的化学方程式是2H2O2H2↑+O2↑ ;(4)活性炭结构疏松多孔,有吸附性,常用活性炭除去水中的色素和异味;检验饮用水是软水还是硬水,可用肥皂水来检验;加肥皂水后,泡沫少、浮渣多的为硬水,反之,为软水;(2)①A、煤、石油和天然气都属于不可再生能源,错误;B、氢气燃烧的错误是水,是理想的“绿色能源”,正确;C、人类使用的能源绝大部分来自太阳能,正确;D、废弃电池填埋在土壤里会造成土壤污染,错误。故选BC。②我们把pH<5.6的雨水称为酸雨;由反应的化学方程式2CaCO3+2SO2+O2=2CaSO4+2x,可知反应前后各原子的个数为反应前Ca原子2个、C原子 2个、O原子12个、S原子2个;反应后Ca原子2个、C原子0个、O原子8个、S原子2个。根据化学变化前后原子的种类、数目不变,可判断生成物x的2个分子中含有2个C原子和4个O原子,则每个x分子由1个C原子和2个O原子构成,物质x的化学式为CO2;③氢气和二氧化碳在催化剂和一定温度下反应生成甲醇和水,反应的化学方程式为CO2+3H2 CH3OH+H2O;④依据化学反应前后各原子的个数不会变化对x、m进行计算;反应前碳原子的个数是8,故反应后碳原子个数也是8,则有m+n=8;由题意可知:
8CH3OH+xO2mCO2+nCO+16H2O
32x 288
8.8g 7.2g
x=11
该化学方程式为8CH3OH+11O26CO2+2CO+16H2O
设生成的二氧化碳质量是y
8CH3OH+11O26CO2+2CO+16H2O
264 288
y 7.2g
y=6.6g
一、选择题(共16题)
1.甘蔗中含有丰富的糖类、水,此外,还含有对人体新陈代谢非常有益的各种维生素、有机酸、钙、铁等物质,经常食用有益人体健康。下列甘蔗中含有的营养物质主要能提供能量的是
A.糖类 B.有机酸 C.钙、铁元素 D.维生素
2.长期受电磁辐射可引起人头昏、头痛、失眠等症状,科学家发现富含维生素的食物具有较好的防辐射损伤功能。下列食物中富含维生素的是
A.豆腐 B.西红柿 C.鸡蛋 D.牛肉
3.糖类是能为人体提供能量的重要营养成分之一。下列食物中,富含糖类物质的是
A.鸡蛋 B.面包 C.青菜 D.花生油
4.民生热词:“舌尖上的安全”。下列做法符合食品安全要求的是
A.甲醛浸泡水产品保鲜
B.为了促进消化,牛奶发酵后制成酸奶再食用
C.亚硝酸钠代替食盐烹调食物
D.为了防止骨质疏松,长期摄入过量的钙元素
5.中原大地盛产小麦,面条是中原人家餐桌上的主食。面条为人们提供的营养素为
A.蛋白质 B.维生素 C.油脂 D.糖类
6.下列疾病可能与缺锌有关的是
A.佝偻病 B.侏儒症 C.贫血症 D.甲状腺肿大
7.人类的健康离不开化学,下列说法合理的是
A.不食用富含蛋白质的食品
B.发霉食品不可食用
C.长期饮用纯净水有利于人体健康
D.食用大米可以补充油脂
8.青少年身体生长发育需要蛋白质,下列广东美食中富含蛋白质的是
A.客家娘酒 B.潮汕卤鹅 C.广式叉烧包 D.陈村米粉
9.2016年7月河北普降大暴雨,造成较大的人员伤亡和财产损失,在救援过程中,医护人员向受伤人群输送大量营养液。该营养液中主要供能物质是
A.水 B.葡萄糖 C.维生素 D.氯化钠
10.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。近年来科学家还发现维生素C有防癌作用。下列关于维生素C的说法中正确的是
A.维生素C是氧化物
B.青少年应多吃蔬菜水果,切勿偏食
C.维生素是由6个碳元素、8个氢元素和15个氧元素组成的
D.维生素C中C、H、O三种元素的原子个数比为9:1:2
11.推理是一种常用的化学学习方法.下列各推理中,正确的是
A.燃烧时发光发热,所以发光发热的变化一定是燃烧
B.氧化物含氧元素,所以含氧元素的物质一定是氧化物
C.碘元素可预防甲状腺疾病,所以需尽可能多补充碘元素
D.单质只含有一种元素,所以只含有一种元素的纯净物一定是单质
12.下列说法正确的是
A.生成盐和水的反应不一定是中和反应
B.Ca、Cr、Se 都是人体必需微量元素
C.水变成冰后体积变大,是因为水分子变大了
D.有机物一定含碳元素,无机物一定不含碳元素
13.下列我市特产中,维生素含量最高的是
A.阜宁大糕 B.龙冈茌梨 C.滨海香肠 D.伍佑糖麻花
14.由于受日本大地震的影响,国内出现了抢购“加碘食盐”的现象,加碘食盐中的“碘”指的是
A.单质 B.分子 C.原子 D.元素
15.下列现象的描述正确的是
A.打开浓盐酸试剂瓶,瓶口出现大量白烟
B.加碘盐的溶液滴到米汤中会出现蓝色
C.铜绿加热后生成黑色固体,管口有水珠,产生能使澄清石灰水变浑浊的气体
D.紫色石蕊试液中通入二氧化碳变红,加热溶液变成无色
16.下列归类不正确的是
选 项 归 类 内容
A 清洁能源 风能、氢能、太阳能
B 常见合金 黄铜、硬铝、磁铁矿
C 碳水化合物 淀粉、葡萄糖、纤维素
D 常见氮肥 碳铵、氨水、尿素
A.A B.B C.C D.D
二、综合题(共8题)
17.化学与生活密切相关,在厨房里蕴藏着许多化学知识。
(1)下列食物中,能提供大量维生素的是_______(填字母序号);
A蔬菜 B牛奶 C大米
(2)加钙牛奶是为了补充钙质,中老年人身体中一旦缺钙,可能患有的疾病是_______;
(3)厨房中用来做面包的发酵粉的主要成分为________(填化学式)。
18.学好化学有助于我们科学地处理和解决生活中的问题。
(1)净水器中可以用______有效地除去水中的异味。
(2)厨房里可以用______来洗涤水壶中的水垢(主要成分是CaCO3和Mg(OH)2)。
(3)利用洗涤剂的______功能来除去衣物上的油污。
(4)青少年多食用豆类、虾皮等富含______元素的食物可以有效预防佝偻病。
19.2018年12月11日是广西壮族自治区成立60周年纪念日,人民日报微信公众号发布了一则微视频《广西一分钟》。
(1)一分钟,184人在桂林山水间自在畅游。漓江的水清澈透明,若想鉴别漓江水属于硬水或软水,可以使用_____。
(2)一分钟,556袋柳州螺蛳粉通过电商售出。螺蛳粉的主要成分﹣﹣粉属于六大营养素中的_____。
(3)一分钟,产出33.4吨糖。榨糖中用到活性炭,主要是利用其_____。
(4)一分钟,完成植树造林4491平方米。绿色植物在光合作用中可以把_____能转化为_____能。
(5)一分钟,体会壮乡美味。品尝美食后用洗洁精清洗碗盘,属于_____作用。
20.酱油是中国的传统调味品。下表是某酱油油膏的部分营养成分列表,根据所学知识回答。
酱油膏的部分营养成分列表(每100克中含)
成分名称 含量 成分名称 含量 成分名称 含量
水分(克) 54.7 蛋白质(克) 13 脂肪(克) 0.7
糖类(克) 10.2 钠(毫克) 7700 钙(毫克) 46
铁(克) 8.6 硒(微克) 2.96 …… ……
(1)上表中不含六大基本营养素中_____________;
(2)上表中“钠”、“钙”等指是___________(填“单质”“分子”“原子”或“元素”);
(3)老年人每天都要摄入足量的钙,有利于防止___________________;
(4)糖类主要是给人体提供能量,写出葡萄糖(C6H12O6)在酶的作用下进行呼吸作用的化学方程式______________。
21.⑴ 请从下列物质中选择适当的物质填空(填序号):
A.干冰 B.盐酸 C.明矾 D.生石灰 E.葡萄糖
①能被人体直接吸收的营养物质是________; ②可用于人工降雨的物质是________; ③可用于净水的物质是________; ④常用作袋装食品的干燥剂________。
⑵ 根据题意用下列选项的字母填空:A.熔点 B.沸点 C.硬度
①工业制氧气和石油分馏都是利用混合物中各成分的________不同;
②武德合金用作保险丝比用纯铜丝更安全,是因为前者的________低。
22.金属材料的应用推动了社会的发展。
(1)铁是年产量最高的金属。中国人烹饪常使用铁锅,铁做炊具主要利用了其_______性,铁锅炒菜时少量铁元素会随着烹饪进人食物,有利于预防_______(填疾病名称)。某混合物由铁、锌、铝、镁中的两种组成,取2.4g该混合物与足量的稀硫酸反应,生成0.2g气体,则该混合物中一定含有的金属是_____
(2)用足量的细铁丝进行如图所示实验,放置足够长的时间后,观察到试管中的水面上升至1处,请解释原因_______。
(3)为实现工业废水的综合利用、回收金属资源,某化学小组进行了以下探究:
①Y为_______;加入稀盐酸时发生反应的化学方程式为_______
②操作I和操作Ⅱ中都要用到的玻璃仪器在操作Ⅱ中的作用是_______
(4)金属铝可通过通电分解熔融的氧化铝制得。请计算要制取9t金属铝,所需铝土矿(其中氧化铝的质量分数为68%)的质量_____。
23.铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)下图为铁元素在元素周期表中的信息,铁元素的原子序数为_______,亚铁离子(Fe2+)的核外电子数为____________。
(2)健康人体内,总量4~5g的铁元素主要以____________(选填“单质”、“化合物”)形式存在,缺铁会患上_________(填字母)。
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
(实验一)兴趣小组通过下图实验研究铁的冶炼
(3)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式________________________ ;
(4)实验一段时间后,观察到A处B处现象分别是____________;___________,小明将所得的黑色固体物质放入足量的稀硫酸中,发现有少量气泡。写出产生气泡反应的化学方程式___________,说明黑色固体物质___________(填字母)。
a.不含铁 b.一定全部是铁 c.含有铁
(资料1)已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
(资料2)实验研究表明:该实验得到的是四氧化三铁与铁粉的混合物
(实验二)兴趣小组用下图实验研究实验一所得黑色粉末中单质铁的质量分数
(资料3)氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,且吸收能力比石灰水强
(5)从安全与规范的角度考虑,装置C后面应连接__________(选填装置序号D或E),B装置的作用是___________。
(6)铁与四氧化三铁的混合物10 g充分反应后,玻璃管中剩余固体(单质铁)的质量为8.4g。请计算10 g黑色粉末中单质铁的质量分数________ 。
(实验三)兴趣小组为探究生铁中铁的含量(生铁中只考虑铁,碳),设计有关方案,取0.58克生铁放于试管中,实验中将注射器内76毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为300毫升。已知实验条件下氢气的密度为0.09g/L。
(7)计算生铁中铁的质量分数为_______ (写出计算过程,氢气质量保留两位小数,结果保留到0.1℅)
(8)上述方法测得的生铁中铁的质量分数偏小,可能的原因是_______
A.没等装置冷却就读数 B.生铁中含有少量锌
C.试管中有氢气没有排出 D.将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
24.(1)水是宝贵的自然资源,我国南海海域海洋资源极其丰富。
①2017年5月18日,南海可燃冰试采成功,可燃冰主要含有甲烷水合物。甲烷中碳元素的化合价是______价,甲烷充分燃烧的化学方程式是__________________。
②渔民常在这一带从事捕鱼作业,鱼肉中含量最多的营养素是_____(填序号)。
A.糖类 B.油脂 C.蛋白质 D.维生素
③科学研究证明,水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气,反应的化学方程式是____________________。
④河水和海水一样都是混合物。自来水厂利用河水生产饮用水的过程中常用活性炭的_____性来除去水中的色素和异味。检验饮用水是软水还是硬水,可用___来检验。
(2)能源利用和环境保护是人类共同关注的问题。
①下列说法中正确的是______(填字母)。
A.煤、石油和天然气都属于可再生能源 B.氢气是理想的“绿色能源”
C.人类使用的能源绝大部分来自太阳能 D.废弃电池可以填埋在土壤里
②煤燃烧时排放出的二氧化硫等污染物,有可能会导致降雨的酸性增强。我们把pH_____5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石浆来吸收二氧化硫,其反应的化学方程式为:2CaCO3+2SO2+O2=2CaSO4+2x,则x的化学式为______。
③研究发现,二氧化碳和氢气在催化剂作用下转化为甲醇(CH3OH)和水。该反应的化学方程式为______________________。
④将一定质量的甲醇与8.8g氧气混合于密闭容器内,在一定条件下,发生如下反应:8CH3OH+xO2 一定条件 mCO2+nCO+16H2O。当反应物完全耗尽且全部转化为生成物时,有7.2g水生成,同时生成二氧化碳的质量为______g。
参考答案
1.A
【详解】
能提供能量的主要营养物质是糖类、油脂,总能量中有60%~70%来自糖类,故选A。
2.B
【详解】
A、豆腐中富含蛋白质,故选项错误。
B、西红柿中富含维生素,故选项正确。
C、鸡蛋中富含蛋白质,故选项错误。
D、牛肉中富含蛋白质,故选项错误。
故选:B。
3.B
【详解】
A、鸡蛋中富含有蛋白质,故A错;
B、面包中富含有淀粉,属于糖类,故B正确;
C、青菜中富含有维生素,故C错;
D、花生油中富含有油脂,故D错。
故选:B。
4.B
【详解】
A、甲醛具有毒性,不得浸泡海鲜保鲜,选项A错误;
B、酸奶更利于人体吸收,可促进消化,所以可以将牛奶发酵制成酸奶食用,选项B正确;
C、亚硝酸钠有毒,不得食用,选项C错误;
D、摄入过量的钙元素容易造成结石、高钙血症等病症,所以需要适当补钙,选项D错误。故选B。
5.D
【详解】
面条的主要成分是淀粉,淀粉属于糖类,故选D。
6.B
【详解】
A. 缺钙易患佝偻病,此选项不符合题意;
B. 严重缺锌会导致蛋白质合成障碍,从而引起体内生长激素分泌不足而诱发侏儒症,此选项符合题意;
C. 缺铁会患缺铁性贫血,此选项不符合题意;
D. 缺碘易患甲状腺肿大疾病,此选项不符合题意。
故选B。
7.B
【详解】
A.蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料,故应食用含蛋白质的食物,且一日三餐应该包含六大营养素, 使营养均衡,A错误;
B.霉变食物中含有黄曲霉素,有剧毒,不可食用,B正确;
C.纯净水几乎不含矿物质,长期饮用不利于身体健康,C错误;
D.大米中含有丰富的糖类,D错误。
故选:B。
8.B
【详解】
A、客家娘酒富含水和酒精,不符合题意;
B、潮汕卤鹅富含蛋白质,符合题意;
C、广式叉烧包富含淀粉,淀粉属于糖类,不符合题意;
D、陈村米粉富含淀粉,淀粉属于糖类,不符合题意。
故选B。
9.B
【详解】
A. 水不能提供能量,不符合题意 ;B. 葡萄糖 属于糖类,是人体最直接的供能物质 ,不需要消化,能直接被人吸收,所以常用于给病人输液;C. 维生素主要功能是调节新陈代谢,不能提供能量,不符合题意; D. 氯化钠,属于无机盐,不能提供能量,不符合题意。故选B。
10.B
【详解】
A. 氧化物是由两种元素组成的化合物,其中一种元素是氧元素。维生素C含有三种元素,不是氧化物,此选项错误;
B. 蔬菜水果富含维生素,青少年应多吃蔬菜水果,切勿偏食,此选项正确;
C. 维生素C是由维生素C分子构成的,每个维生素C分子是由6个碳原子、8个氢原子和6个氧原子构成的,此选项错误;
D. 维生素C中C、H、O三种元素的原子个数比为6:8:6=3:4:3,此选项错误。
故选B。
11.D
【详解】
单质只含有一种元素,所以只含有一种元素的纯净物一定是单质;燃烧时发光发热,但是发光发热的变化不一定是燃烧,比如灯泡的发光灯;氧化物含氧元素,含氧元素的物质不一定是氧化物,比如氧气;碘元素可预防甲状腺疾病,但不能多补充碘元素,碘是一种微粒元素。故选D.
12.A
【详解】
A、中和反应指的是酸和碱反应生成盐和水的反应,但是生成盐和水的反应不一定是中和反应,例如金属氧化物和酸反应生成盐和水,不属于中和反应,A选项说法正确,符合题意;
B、Ca是人体必需常量元素,Cr、Se 是人体必需微量元素,B选项说法不正确,不符合题意;
C、水变成冰后体积变大,是因为水分子之间的间隔变大了,C选项说法不正确,不符合题意;
D、有机物一定含碳元素,无机物可能含碳元素,例如碳酸钙、二氧化碳等无机物含有碳元素,D选项说法不正确,不符合题意。故选A。
13.B
【详解】
A、阜宁大糕富含糖类和油脂;
B、龙冈茌梨是一种富含维生素的水果;
C、滨海香肠中富含蛋白质和油脂;
D、伍佑糖麻花含有丰富的糖类和油脂;
故选B.
14.D
【详解】
加碘食盐中的“碘”存在于无机盐中,有利于人体吸收,则碘是指元素.
故选D.
15.C
【详解】
A、浓盐酸具有挥发性,打开浓盐酸的瓶塞,挥发出的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,从而形成白雾,故瓶口出现白雾,而不是白烟,故选项说法错误;
B、淀粉遇碘变蓝色,米汤中富含淀粉,但加碘盐中不含碘单质,加碘盐的溶液滴到米汤中不会出现蓝色,故选项说法错误;
C、铜绿加热生成氧化铜、水和二氧化碳,铜绿加热后生成黑色固体,管口有水珠,产生能使澄清石灰水变浑浊的气体,故选项说法正确;
D、紫色石蕊试液中通入二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色;加热溶液,碳酸分解生成水和二氧化碳,溶液变成紫色,故选项说法错误。
故选:C。
16.B
【详解】
A、风能、氢能、太阳能均属于清洁能源,不符合题意;
B、黄铜、硬铝都属于合金,磁铁矿属于铁矿石,不属于合金,符合题意;
C、淀粉、葡萄糖、纤维素都属于糖类,属于碳水化合物,不符合题意;
D、碳铵、氨水和尿素中均含有氮元素,属于氮肥,不符合题意。故选B。
17.A 骨质疏松 NaHCO3
【详解】
(1)蔬菜水果富含维生素,故选A。
(2)加钙牛奶是为了补充钙质,中老年人身体中一旦缺钙,可能患有的疾病是骨质疏松;
(3)厨房中用来做面包的发酵粉的主要成分为NaHCO3。
18.活性炭 食醋 乳化 钙
【详解】
(1)活性炭具有吸附性,净水器中可以用活性炭有效地去除水中的异味。
(2)水垢的主要成分是CaCO3和Mg(OH)2,能与酸反应,可以利用厨房中的食醋清洗水壶中的水垢。
(3)洗涤剂具有乳化作用,将大分子团油污分成小分子团油滴,能除去衣物上的油污;
(4)豆类、虾皮中富含钙元素,青少年多食用豆类、虾皮等富含钙元素的食物可以有效预防佝偻病。
19.肥皂水 糖类 吸附性 太阳 化学 乳化
【详解】
(1)硬水中加入肥皂水产生泡沫少,软水中加入肥皂水产生泡沫多,可用肥皂水来检验硬水或软水;
(2)螺蛳粉的主要成分﹣﹣粉属于六大营养素中的糖类;
(3)活性炭具有吸附性,可以除去色素;
(4)绿色植物在光合作用中可以把太阳能转化为化学能;
(5)洗洁精对油污起到了乳化作用,所以可用洗洁精清洗碗盘。
20.维生素 元素 骨质疏松
【详解】
(1)人体所需的六大营养素是:蛋白质、糖类、油脂、维生素、无机盐和水,从表中提供的营养成分可知,表中含蛋白质、水、糖类、无机盐、油脂,故表中不含六大基本营养素中的维生素;
(2)上表中“钠”“钙”等不是指以单质、分子、原子等形式存在,这里所指的“钠、钙”是强调存在的元素,与具体形态无关,故填:元素;
(3)老年人缺钙容易患骨质疏松,故老年人每天都要摄入足量的钙,有利于防止骨质疏松;
(4)葡萄糖(C6H12O6)在酶的作用下进行呼吸作用生成二氧化碳和水,该反应的化学方程式为:。
21.E A C D B A
【详解】
(1) ①能被人体直接吸收的营养物质是葡萄糖;②干冰升华吸热,可用于人工降雨;③可用于净水的物质是明矾;④常用作装食品的干燥剂生石灰;(2)①工业制氧气和工业石油分馏都是利用混合物中各成分的沸点不同;②武德合金用作保险丝比用纯铜丝更安全,是因为前者的熔点低。
22.导热 缺铁性贫血 铝 细铁丝与空气中的氧气反应(也就是生锈),氧气被消耗完之后,外界大气压与内部产生压强差 硝酸银 HCl+AgNO3=AgCl↓+HNO3 搅拌以防止液体局部温度过高造成液滴飞溅 可知该反应的方程式为,
设需要氧化铝的质量为 x。
解得 x=17t,
铝土矿中氧化铝的质量分数为68%,17t为氧化铝的质量铝士矿质量为
【详解】
(1)铁做炊具主要利用了其导热性,铁锅炒菜时少量铁元素会随着烹饪进人食物,有利于预防缺铁性贫血,锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑,铁和稀硫酸Fe+H2SO4=FeSO4+H2↑;镁和稀硫酸Mg+H2SO4=MgSO4+H2↑,铝和稀硫酸2A1+3H2SO4=Al2(SO4)3+3H2↑,若四种金属分别产生 0. 2g气体,需要铁5. 6g、锌6. 5g、铝1. 8g、镁2. 4g由于混合物由两种金属组成,则所需金属质量一个得大于2. 4g,一个得小于2. 4g大于2. 4g的铁、锌小于2. 4g的只有铝,故合物中一定含有铝;
(2)细铁丝在空气中放置足够长的时间之后会与空气中的氧气反应(也就是生锈),氧气被消耗完之后,外界大气压与内部产生压强差,所以水面会上升;
(3)锌能和硝酸铜反应生成硝酸锌和铜,X为锌,溶液甲为硝酸锌,溶液乙为氯化锌,硝酸银和氯化锌反应生成硝酸锌和氯化银沉淀,Y为硝酸银。
①根据分析可知,Y为硝酸银,硝酸银和稀盐酸反应生成氯化银和硝酸,反应的化学方程式为:HCl+AgNO3=AgCl↓+HNO3;
②操作I和操作II分别是过滤操作和蒸发操作,其中都要用到的玻璃仪器是玻璃棒,玻璃棒在蒸发操作中的作用是搅拌以防止液体局部温度过高造成液滴飞溅;
(4)见答案。
23.26 24 化合物 c 红棕色固体变黑 澄清石灰水变浑浊 c E 防止倒吸,安全瓶 42% 96.6% BD
【详解】
(1)铁的原子序数为26;在原子中原子序数=质子数=核外电子数,故铁原子有26个电子,形成亚铁离子时失去了2个电子,故亚铁离子还有24个电子;(2)元素在人体内主要是以化合物的形式存在的,缺铁易患贫血;(3)一氧化碳还原氧化铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为;(4)由化学反应的化学方程式可知,红棕色的氧化铁被还原成黑色的铁,同时生成能使澄清石灰水变浑浊的二氧化碳气体,实验一段时间后,观察到A处B处现象分别是红棕色固体变黑;澄清石灰水变浑浊;铁能与稀硫酸反应生成硫酸亚铁和氢气,此现象说明黑色固体中含有铁,但不一定全部是铁。故化学方程式为:;(5)氢氧化钠溶液具有强烈的腐蚀性,且会从C中溢出,从安全与规范的角度考虑,装置C后面应连接E,B装置是安全瓶,防止溶液倒吸;(6)设四氧化三铁的质量为,由四氧化三铁和一氧化碳反应的化学方程式可知固体减少的质量就是四氧化三铁中氧元素的质量可知:
固体减少的质量
232 232-168=64
10g-8.4g=1.6g
=5.8g
则混合物中铁的质量分数为:
答:10g黑色粉末中单质铁的质量分数为42%。
(7)生成氢气的质量为(0.3L 0.076L)×0.09g/L=0.02g
设铁的质量为。
56 2
0.02g
=0.56g
生铁中铁的质量分数为;
(8)A、没等装置冷却就读数,气体膨胀,气体的体积较大,测得的铁的质量分数偏大;B、相同质量锌和铁与足量的酸反应,铁生成的氢气的质量大,生铁中含有少量锌,生成氢气的质量偏小,测得的铁的质量分数偏小;C、试管中有气体没有排出,排入集气瓶中,正好等于产生氢气的体积,对结果没影响。D、将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹,少量气体从注射器中逸出,导致压过去的水的体积减小,使测量到的氢气体积减小,测得的铁的质量分数会偏小。故选BD。
24.-4 CH4+2O2 CO2+2H2O C 2H2O2H2↑+O2↑ 吸附 肥皂水 BC < CO2 CO2+3H2 CH3OH+H2O 6.6
【解析】
(1) ①根据根据化合物中各元素正负化合价代数和为0及甲烷燃烧生成二氧化碳和水解答;②根据肉类主要富含蛋白质解答;③根据水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气解答;④根据活性炭有吸附性及用肥皂水检验软水和硬水解答;(2)①根据能源的分类及其对环境的影响来分析;②根据酸雨的形成与质量守恒定律来分析;③根据反应物和生成物书写有关反应的化学方程式;④依据质量守恒定律的有关应用解答即可;依据已知的化学方程式利用水的质量可以求出生成的二氧化碳质量。(1) ①甲烷中氢元素显+1价,碳元素的化合价是[0-(+1×4)]=-4;甲烷和氧气在点燃条件下生成二氧化碳和水,的化学方程式是CH4+2O2 点燃 2H2O+CO2;②肉、蛋、奶、大豆类食品给人提供丰富的蛋白质,故选C;(3)水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气,反应的化学方程式是2H2O2H2↑+O2↑ ;(4)活性炭结构疏松多孔,有吸附性,常用活性炭除去水中的色素和异味;检验饮用水是软水还是硬水,可用肥皂水来检验;加肥皂水后,泡沫少、浮渣多的为硬水,反之,为软水;(2)①A、煤、石油和天然气都属于不可再生能源,错误;B、氢气燃烧的错误是水,是理想的“绿色能源”,正确;C、人类使用的能源绝大部分来自太阳能,正确;D、废弃电池填埋在土壤里会造成土壤污染,错误。故选BC。②我们把pH<5.6的雨水称为酸雨;由反应的化学方程式2CaCO3+2SO2+O2=2CaSO4+2x,可知反应前后各原子的个数为反应前Ca原子2个、C原子 2个、O原子12个、S原子2个;反应后Ca原子2个、C原子0个、O原子8个、S原子2个。根据化学变化前后原子的种类、数目不变,可判断生成物x的2个分子中含有2个C原子和4个O原子,则每个x分子由1个C原子和2个O原子构成,物质x的化学式为CO2;③氢气和二氧化碳在催化剂和一定温度下反应生成甲醇和水,反应的化学方程式为CO2+3H2 CH3OH+H2O;④依据化学反应前后各原子的个数不会变化对x、m进行计算;反应前碳原子的个数是8,故反应后碳原子个数也是8,则有m+n=8;由题意可知:
8CH3OH+xO2mCO2+nCO+16H2O
32x 288
8.8g 7.2g
x=11
该化学方程式为8CH3OH+11O26CO2+2CO+16H2O
设生成的二氧化碳质量是y
8CH3OH+11O26CO2+2CO+16H2O
264 288
y 7.2g
y=6.6g
