2021-2022学年人教版(2019)高中化学选择性必修二1.1 能层与能级 基态和激发态 课件(19张ppt)
文档属性
| 名称 | 2021-2022学年人教版(2019)高中化学选择性必修二1.1 能层与能级 基态和激发态 课件(19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-06 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第1课时 能层与能级
基态与激发态
第一章 原子结构与性质
第一节 原子结构
能层与能级
基态与激发态
教学目标
原子光谱
新知导学
原子论
道尔顿 1803
汤姆逊
质子-电子模型 1897
卢瑟福
有核模型 1911
能层与能级
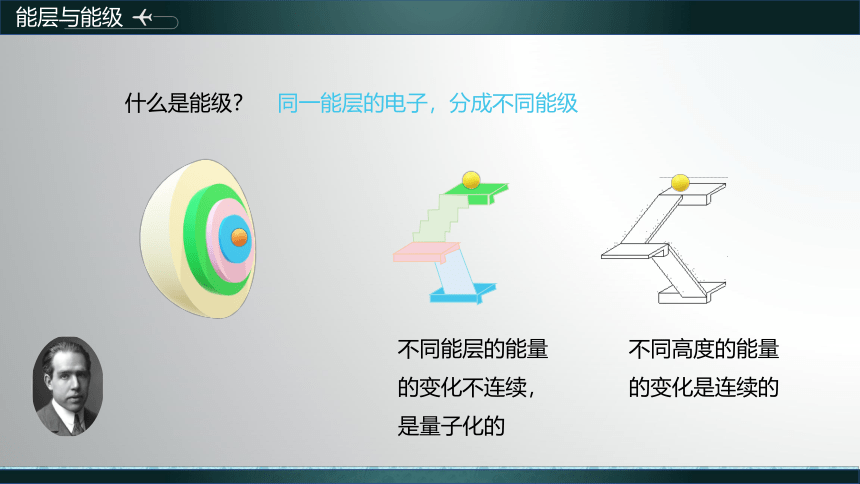
什么是能层?
能层与能级
按能量不同划分——能层(电子层)
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
n 越大,离核距离越远
电子能量越高
每能层最多容纳电子数为:
2n2
2
8
18
32
50
72
98
能层与能级
不同能层的能量的变化不连续,是量子化的
不同高度的能量的变化是连续的
同一能层的电子,分成不同能级
什么是能级?
能层与能级
能级数与能层序数有什么关系?
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
s、p、d
s
s、p
s、p、d、f
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级数等于该能层序数
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
1*2 3*2 5*2 7*2 9*2
容纳电子数
能层与能级
第五能层最多可容纳多少电子?
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
s、p、d
s
s、p
s、p、d、f
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
1*2 3*2 5*2 7*2 9*2
容纳电子数
1*2+3*2 +5*2+ 7*2 + 9*2
能层与能级
EnsE1sE2pE3dE(K)不同能层能级的能量大小关系
基态与激发态
原子核外的电子跃迁释放能量
基态原子:处于能量最低状态
激发态原子:基态原子吸收能量
光(辐射)是电子跃迁释放能量的重要方式
基态与激发态
基态与激发态
基态原子
激发态原子
(电子跃迁到 能级)
能量
吸收
较高
能量
释放
(电子跃迁到 能级)
较低
基态与激发态
原子光谱
锂、氦、汞的发射光谱
锂、氦、汞的吸收光谱
不同原子的电子发生跃迁时会吸收或者释放不同的光,用光谱仪可以摄取各种原子的吸收光谱或者发射光谱,总称原子光谱
He 氦
不同原子的电子发生跃迁时会吸收或者释放不同的光,用光谱仪可以摄取各种原子的吸收光谱或者发射光谱,总称原子光谱。
原子光谱的应用(1)—— 发现新元素
原子光谱
利用原则光谱上的特征谱线来鉴定元素,称为光谱分析。
不同元素的焰色试验—利用元素的发射光谱
原子光谱的应用(2)—— 检验元素
原子光谱
对点练习
1.若 n=3,以下能级符号错误的是 ( )
A. np B. nf C. nd D. ns
能级数等于该能层序数
B
2.下列现象和应用与电子跃迁无关的是( )
A. 激光 B. 焰色试验 C. 燃烧放热 D. 冕虹灯
电子跃迁是物理变化,燃烧放热是化学变化
C
对点练习
3.(1)已知短同期元章A、B,A元素原子的最外层电子数为m,次外层电子数为n;B元素原子的M层(有电子)电子数为刚m- n-1,L层电子数为用m+n+2,则A为 ,(填元素符号,下同),B为 。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子的多5。则X、Y分别为 。
A
B
…
m
n
m-n-1
m+n+2
L
K
M
m+n+2=8
m-n-1≤8
m = 4
n = 2
C
Mg
X
x
L
K
M
Y
L
K
M
x+3
2
x = 5
N
Mg
课堂小结
n(能层序数) =
1
2
3
4
5
6
7
…
s、p、d
s、p
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
K
L
M
N
O
P
Q
能层
s、p、d、f
s
基态原子
能量
激发态原子
能量
吸收
释放
吸收光谱
发射光谱
第1课时 能层与能级
基态与激发态
第一章 原子结构与性质
第一节 原子结构
能层与能级
基态与激发态
教学目标
原子光谱
新知导学
原子论
道尔顿 1803
汤姆逊
质子-电子模型 1897
卢瑟福
有核模型 1911
能层与能级
什么是能层?
能层与能级
按能量不同划分——能层(电子层)
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
n 越大,离核距离越远
电子能量越高
每能层最多容纳电子数为:
2n2
2
8
18
32
50
72
98
能层与能级
不同能层的能量的变化不连续,是量子化的
不同高度的能量的变化是连续的
同一能层的电子,分成不同能级
什么是能级?
能层与能级
能级数与能层序数有什么关系?
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
s、p、d
s
s、p
s、p、d、f
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级数等于该能层序数
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
1*2 3*2 5*2 7*2 9*2
容纳电子数
能层与能级
第五能层最多可容纳多少电子?
n(能层序数) =
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
……
s、p、d
s
s、p
s、p、d、f
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
1*2 3*2 5*2 7*2 9*2
容纳电子数
1*2+3*2 +5*2+ 7*2 + 9*2
能层与能级
Ens
基态与激发态
原子核外的电子跃迁释放能量
基态原子:处于能量最低状态
激发态原子:基态原子吸收能量
光(辐射)是电子跃迁释放能量的重要方式
基态与激发态
基态与激发态
基态原子
激发态原子
(电子跃迁到 能级)
能量
吸收
较高
能量
释放
(电子跃迁到 能级)
较低
基态与激发态
原子光谱
锂、氦、汞的发射光谱
锂、氦、汞的吸收光谱
不同原子的电子发生跃迁时会吸收或者释放不同的光,用光谱仪可以摄取各种原子的吸收光谱或者发射光谱,总称原子光谱
He 氦
不同原子的电子发生跃迁时会吸收或者释放不同的光,用光谱仪可以摄取各种原子的吸收光谱或者发射光谱,总称原子光谱。
原子光谱的应用(1)—— 发现新元素
原子光谱
利用原则光谱上的特征谱线来鉴定元素,称为光谱分析。
不同元素的焰色试验—利用元素的发射光谱
原子光谱的应用(2)—— 检验元素
原子光谱
对点练习
1.若 n=3,以下能级符号错误的是 ( )
A. np B. nf C. nd D. ns
能级数等于该能层序数
B
2.下列现象和应用与电子跃迁无关的是( )
A. 激光 B. 焰色试验 C. 燃烧放热 D. 冕虹灯
电子跃迁是物理变化,燃烧放热是化学变化
C
对点练习
3.(1)已知短同期元章A、B,A元素原子的最外层电子数为m,次外层电子数为n;B元素原子的M层(有电子)电子数为刚m- n-1,L层电子数为用m+n+2,则A为 ,(填元素符号,下同),B为 。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子的多5。则X、Y分别为 。
A
B
…
m
n
m-n-1
m+n+2
L
K
M
m+n+2=8
m-n-1≤8
m = 4
n = 2
C
Mg
X
x
L
K
M
Y
L
K
M
x+3
2
x = 5
N
Mg
课堂小结
n(能层序数) =
1
2
3
4
5
6
7
…
s、p、d
s、p
s、p、d、f 、g…
s、p、d、f 、g…
s、p、d、f 、g…
能级表示方法
3 3 3
1
2 2
4 4 4 4
5 5 5 5 5
6 6 6 6 6
7 7 7 7 7
K
L
M
N
O
P
Q
能层
s、p、d、f
s
基态原子
能量
激发态原子
能量
吸收
释放
吸收光谱
发射光谱
