1.6物质的分离 同步练习(含解析)
文档属性
| 名称 | 1.6物质的分离 同步练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 328.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-06 00:00:00 | ||
图片预览



文档简介
浙教版8年级科学上册第一章1.6物质的分离同步练习
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列实验操作中玻璃棒的作用与其他三组不同的是( )
A.配制蔗糖溶液 B.过滤泥水
C.获取氯化钠晶体 D.配制 10%的食盐水
2.粗盐提纯需经过称量、溶解、过滤、蒸发等操作,下列图示对应的操作规范的是( )
A. 称量 B.溶解 C.过滤 D.蒸发
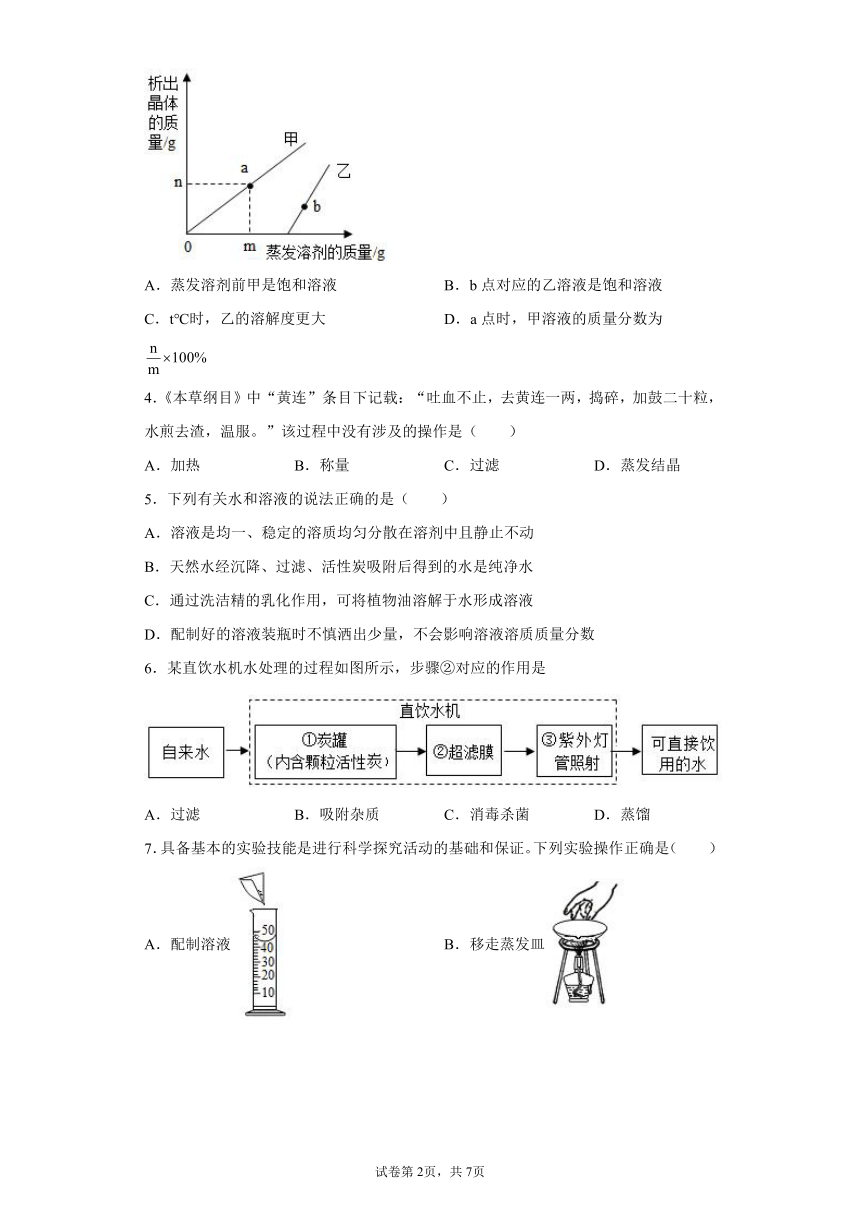
3.t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法错误的是( )
A.蒸发溶剂前甲是饱和溶液 B.b点对应的乙溶液是饱和溶液
C.t℃时,乙的溶解度更大 D.a点时,甲溶液的质量分数为
4.《本草纲目》中“黄连”条目下记载:“吐血不止,去黄连一两,捣碎,加鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是( )
A.加热 B.称量 C.过滤 D.蒸发结晶
5.下列有关水和溶液的说法正确的是( )
A.溶液是均一、稳定的溶质均匀分散在溶剂中且静止不动
B.天然水经沉降、过滤、活性炭吸附后得到的水是纯净水
C.通过洗洁精的乳化作用,可将植物油溶解于水形成溶液
D.配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数
6.某直饮水机水处理的过程如图所示,步骤②对应的作用是
A.过滤 B.吸附杂质 C.消毒杀菌 D.蒸馏
7.具备基本的实验技能是进行科学探究活动的基础和保证。下列实验操作正确是( )
A.配制溶液 B.移走蒸发皿
C.过滤液体 D.向试管中倾倒液体
8.石墨烯之父海姆带领的科研团队研制出氧化石墨烯薄膜制成“筛子”,能够很好地筛掉海水中的盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如下图)下列关于氧化石墨烯膜“筛掉”氯化钠的说法错误的是( )
A.“筛掉”氯化钠过程类似于过滤操作 B.该过程可应用于海水蒸馏
C.该过程属于物理变化 D.右侧海水的溶质的质量分数增大
9.河水净化制自来水的主要步骤如下图所示,有关说法错误的是( )
A.步骤Ⅰ可除去难溶性杂质 B.X试剂可以是活性炭
C.步骤Ⅲ可杀菌、消毒 D.净化的水为纯净水
二、填空题
10.小明同学得到了如下关于A、B的两种固体物质的溶解度表:
温度(℃) 0 10 20 30 40
溶解度(g) A 35 35.5 36 36.5 37
B 6 10 18 36.5 50
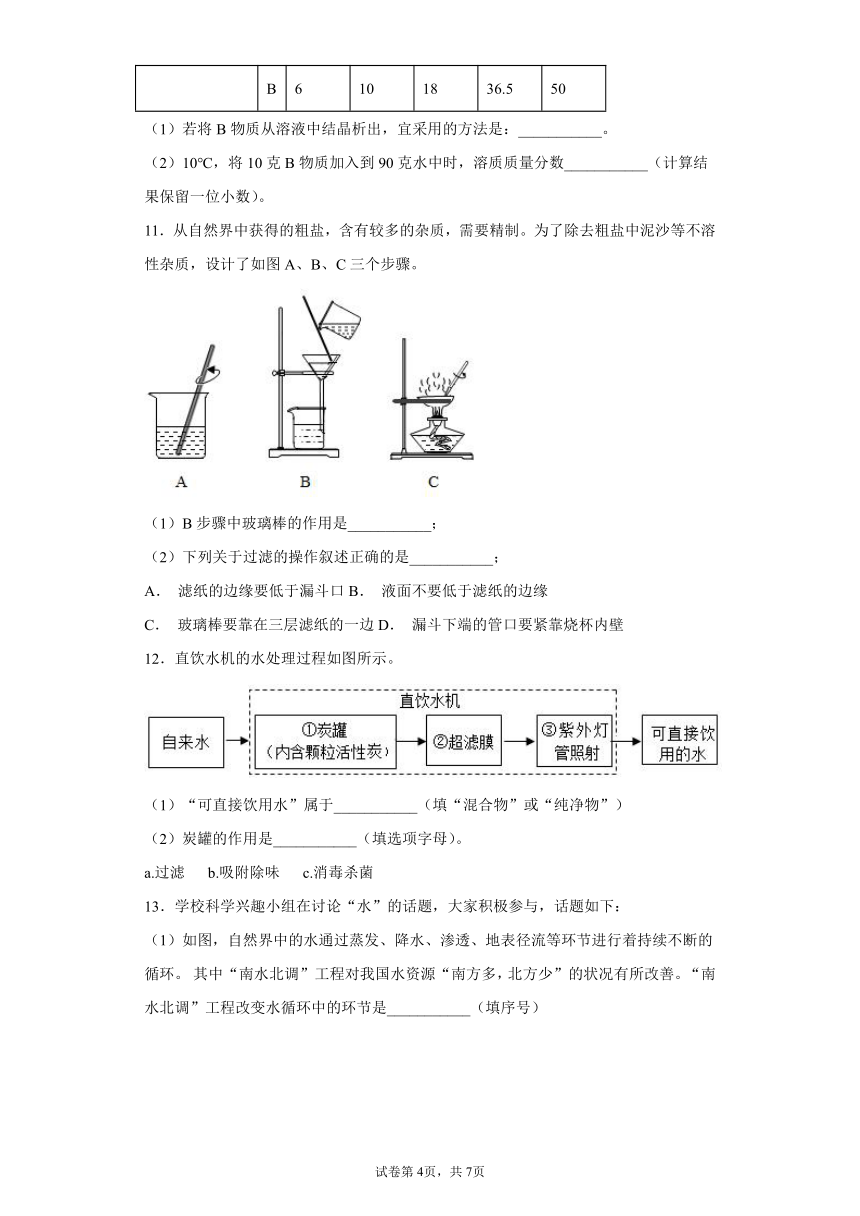
(1)若将B物质从溶液中结晶析出,宜采用的方法是:___________。
(2)10℃,将10克B物质加入到90克水中时,溶质质量分数___________(计算结果保留一位小数)。
11.从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质,设计了如图A、B、C三个步骤。
(1)B步骤中玻璃棒的作用是___________;
(2)下列关于过滤的操作叙述正确的是___________;
A. 滤纸的边缘要低于漏斗口B. 液面不要低于滤纸的边缘
C. 玻璃棒要靠在三层滤纸的一边D. 漏斗下端的管口要紧靠烧杯内壁
12.直饮水机的水处理过程如图所示。
(1)“可直接饮用水”属于___________(填“混合物”或“纯净物”)
(2)炭罐的作用是___________(填选项字母)。
a.过滤 b.吸附除味 c.消毒杀菌
13.学校科学兴趣小组在讨论“水”的话题,大家积极参与,话题如下:
(1)如图,自然界中的水通过蒸发、降水、渗透、地表径流等环节进行着持续不断的循环。 其中“南水北调”工程对我国水资源“南方多,北方少”的状况有所改善。“南水北调”工程改变水循环中的环节是___________(填序号)
(2)能确认水是由氢元素和氧元素组成的实验是___________;
A.水的蒸发
B.水的电解
C.水的净化
D.水的蒸馏
(3)某同学发现最近家里的自来水有点浑浊,就想着自制一个如图所示的简易净水器。该净化过程中,用到分离混合物的方法有___________等(填一个即可)。通过这个简易装置净化后的水还是不能直接饮用,原因是___________。
14.为保持云和湖的卫生洁净,环境卫生部门会定时组织人员对云和湖及上游沿途进入或即将进入的污染物进行处理。
(1)打捞漂浮在云和湖面的杂物,相当于混合物分离方法中的________(选填“过滤”、“结晶”或“蒸馏”);
(2)下列行为会污染云和湖的是_________;
A.排入普通雨水 B.排入工业废水 C.丢入各种垃圾
15.氯化钠是生活必得品,也是重要的化工原料。下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答问题。
温度/℃ 20 30 40 50 60
溶解度/g 氯化钠 36.0 36.3 36.6 37.0 37.3
硝酸钾 31.6 45.8 63.9 85.5 110
(1)要把硝酸钾从含有少量氯化钠的溶液中提出,最好采用的方法是___________。
(2)提纯含少量泥沙的粗盐,一般经过以下操作流程:
操作④的名称是___________ , 操作⑤中玻璃棒的作用是 ___________。
16.如图甲是自来水的生产过程。据图回答:
(1)由图甲可知,自来水生产过程中使用的净水方法有 ___________。
A. 沉淀B. 过滤 C. 蒸馏
(2)在物质分类上,杀菌后输送给用户的水属于___________;(选填 “混合物”或“纯净物”)
17.联合国确定2021年“世界水日”的主题为“Valuing Water”(珍惜水、爱护水)
(1)从组成的角度看:水是由______组成的。(填写选项编号)
A.氢元素和氧元素 B.氢原子和氧原子 C.氢气和氧气
(2)从能源的角度看:电解水产生理想的清洁高能燃料氢气。水电解的文字表达式为______。
(3)从净化的角度看:有关图1所示净化河水简易装置,说法错误的是______。
A.水本身是一种化学资源
B.此装置可以得到纯净水
C.利用此装置净化得到的水不宜直接饮用
(4)从变化的角度看:电解一定量的水(如图2),当阳极端产生 5mL 气体时, 理论上在阴极端产生气体的体积为______mL。
18.如下表是硝酸钾、氯化钠在不同温度下的溶解度。
温度/℃ 10 20 30 40 50
硝酸钾的溶解度g/100g 20.9 31.6 45.8 63.9 85.5
氯化钠的溶解度g/100g 35.8 36.0 36.3 36.6 37.0
(1)从表中数据分析,溶解度受温度影响较大的物质是______。
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾的方法为______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.B
【详解】
A、配制蔗糖溶液中玻璃棒的作用是搅拌,加速蔗糖溶解。
B、过滤时,玻璃棒的作用是引流。
C、蒸发结晶时,玻璃棒的作用是搅拌,防止受热不均匀导致液体飞溅。
D、配置10%的食盐水,玻璃棒的作用是搅拌。
故B选项玻璃棒的作用与其他三组不同。
故选B。
2.D
【详解】
A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误。
B、配制溶液时,溶解操作应在烧杯中进行,用玻璃棒不断搅拌,图中所示操作错误。
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中所示操作错误。
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作正确。
故选D。
3.D
【详解】
A、甲溶液在初始蒸发阶段就有晶体析岀,说明甲为饱和溶液,而乙镕液初始无固体析出,为不饱和溶液,故选项正确。
B、b点时乙溶液已经析出了固体,因此是饱和溶液,故选项正确。
C、t℃时,乙的溶解度更大,因为蒸发相同的溶剂,乙析出的溶质多,故选项正确。
D、a点时,甲溶液的质量分数应为溶质质量与溶液质量的比值,故选项错误。
故选D。
【点睛】
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
4.D
【详解】
“取黄连一两,捣碎,加鼓二十粒”,涉及到称量;“捣碎,水煎去渣”,涉及到加热和过滤操作,没有涉及的操作是蒸发结晶。
故选D。
5.D
【详解】
A、溶液是均一、稳定的混合物,溶质均匀分散在溶剂中,但是在不断的运动,不符合题意。
B、沉降只能使悬浮的杂质沉降,过滤只能除去难溶性杂质,活性炭只能吸附水中的色素和异味,天然水经沉降、过滤、活性炭吸附后得到的水中还含有可溶性杂质,不是纯净物,不符合题意。
C、洗洁精中含有乳化剂,具有乳化作用,能将油污乳化为细小油滴,形成乳浊液,不符合题意。
D、溶液具有均一性,配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数,符合题意。
故选D。
6.A
【详解】
超滤膜可以除去不溶性的杂质,所以步骤②对应的操作是过滤。
故选A。
7.D
【详解】
A、不能在量筒中配置溶液,故A错误。
B、取下蒸发皿用坩埚钳夹取,不能用手拿,以防烫伤,故B错误。
C、过滤时需要用玻璃棒引流,故C错误。
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,故D正确。
故选D。
8.B
【详解】
A、“筛掉”氯化钠过程类似于过滤操作,正确。
B、海水蒸馏得到的是纯净水,氧化石墨烯薄膜制成“筛子”,能够很好地筛掉海水中的盐类物质,但是得到水中含有其他的杂质,所以不能应用于海水蒸馏,错误。
C、该过程没有新物质生成,属于物理变化,正确。
D、右侧海水因溶剂质量减小,溶质的质量分数增大,正确。
故选B。
9.D
【详解】
A、步骤Ⅰ可除去难溶性杂质,不符合题意。
B、活性炭具有吸附性,可除去水中的色素和异味, X 试剂可以是活性炭,不符合题意。
C、步骤Ⅲ中液氯可杀菌、消毒,不符合题意。
D、净化的水中仍含有可溶性杂质,不是纯净水,符合题意。
故选D。
10.降温结晶 9.1%
【详解】
(1)由A、B的两种固体物质的溶解度表,B的溶解度随着温度的升高而增大,溶解度受温度的影响变化较大,一般采用降温结晶的方法,降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出。
(2)10℃时,B物质的溶解度为10g,则在该温度下,100g水中最多能溶解10gB物质。将10克B物质加入到90克水中时,B物质无法完全溶解,所形成的溶液为该温度下的饱和溶液,其溶液的溶质质量分数=。
11.引流 ACD
【详解】
(1)B步骤是过滤操作,玻璃棒的作用是引流。
(2)过滤液体时,注意“一贴、二低、三靠”的原则,滤纸的边缘要低于漏斗口,液面要低于滤纸的边缘,玻璃棒要靠在三层滤纸的一边, 漏斗下端的管口要紧靠烧杯内壁。故选ACD。
12.混合物 b
【详解】
(1)直饮水机不能除去水中的可溶性物质,“可直接饮用水”含有可溶性物质,属于混合物。
(2)活性炭具有吸附性,能吸附颜色和异味。炭罐含有活性炭,作用是 b。
13.⑤ B 过滤 水中还含有微生物和可溶性杂质
【详解】
(1) “南水北调”工程改变水循环中的环节是地表径流环节,即图中的⑤ 。
(2)水的电解实验产生氢气和氧气,说明水是由氢元素和氧元素组成,其它选项是物理变化,不能证明水的组成,故选B。
(3)小卵石、细沙、活性炭、棉花等物质是具有吸附作用的固体,用它们来过滤,不仅可以滤去液体中的不溶性物质,还可以吸附掉一些溶解的杂质,除去异味。但对于液体中含有的微生物以及一部分可溶性杂质是无法去除的,所以通过这个简易装置净化后的水还是不能直接饮用。
14.过滤 BC
【详解】
(1)过滤可以将不溶性固体和液体分离,打捞漂浮在河道的杂物,相当于混合物分离方法中的过滤。
(2)A.排入普通雨水,不会造成水体污染;
B.排入工业废水,会造成水体污染;
C.丢入废旧电池,会造成水体污染。
故选BC。
15.冷却热饱和溶液(降温结晶) 过滤 搅拌使滤液受热均匀,防止液体飞溅
【详解】
(1)根据表格可知,硝酸钾的溶解度随温度的升高而迅速增大,而氯化钠的溶解度几乎不受温度的影响,因此要把硝酸钾从含有少量氯化钠的溶液中提出,最好采用的方法是冷却热饱和溶液(降温结晶)。
(2)根据图片可知,操作④用于分离泥沙和滤液,应该是过滤。操作⑤从滤液中得到晶体,应该为结晶,在结晶操作中玻璃棒的作用:搅拌使滤液受热均匀,防止液体飞溅。
16.AB 混合物
【详解】
(1)自来水净化过程包括沉淀、过滤、吸附和消毒,故选AB。
(2)杀菌后的自来水看似无色透明,其中仍然含有大量的可溶性的钙镁化合物,因此属于混合物。
17.A 水氢气+氧气 B 10
【详解】
(1)物质是由元素组成的,所以从组成的角度看:水是由氢元素和氧元素组成的,故选:A。
(2)电解水产生氢气和氧气,文字表达式为:水氢气+氧气。
(3)A、水是一种重要的化学资源,故正确;
B、利用此装置不能得到纯净水,得到的水中还含有部分可溶性杂质,故错误;
C、利用此装置净化得到的水还含有可溶性杂质和细菌、病毒,所以还不能作为饮用水,故正确。
故选B。
(4)水通电分解,正极生成氧气,负极产生氢气,二者的体积比为1:2,所以正极(阳极)产生的气体是氧气,当正极产生的气体为5mL时,负极产生的气体体积为10mL。
18.硝酸钾 冷却热饱和溶液(降温结晶)
【详解】
(1) 从表中数据分析,溶解度受温度影响较大的物质是硝酸钾,氯化钠溶解度受温度影响不大。
(2)硝酸钾溶解度受温度影响大,氯化钠溶解度受温度影响小,所以当硝酸钾中混有少量氯化钠时,提纯硝酸钾的方法为冷却热饱和溶液(降温结晶)。答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列实验操作中玻璃棒的作用与其他三组不同的是( )
A.配制蔗糖溶液 B.过滤泥水
C.获取氯化钠晶体 D.配制 10%的食盐水
2.粗盐提纯需经过称量、溶解、过滤、蒸发等操作,下列图示对应的操作规范的是( )
A. 称量 B.溶解 C.过滤 D.蒸发
3.t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法错误的是( )
A.蒸发溶剂前甲是饱和溶液 B.b点对应的乙溶液是饱和溶液
C.t℃时,乙的溶解度更大 D.a点时,甲溶液的质量分数为
4.《本草纲目》中“黄连”条目下记载:“吐血不止,去黄连一两,捣碎,加鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是( )
A.加热 B.称量 C.过滤 D.蒸发结晶
5.下列有关水和溶液的说法正确的是( )
A.溶液是均一、稳定的溶质均匀分散在溶剂中且静止不动
B.天然水经沉降、过滤、活性炭吸附后得到的水是纯净水
C.通过洗洁精的乳化作用,可将植物油溶解于水形成溶液
D.配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数
6.某直饮水机水处理的过程如图所示,步骤②对应的作用是
A.过滤 B.吸附杂质 C.消毒杀菌 D.蒸馏
7.具备基本的实验技能是进行科学探究活动的基础和保证。下列实验操作正确是( )
A.配制溶液 B.移走蒸发皿
C.过滤液体 D.向试管中倾倒液体
8.石墨烯之父海姆带领的科研团队研制出氧化石墨烯薄膜制成“筛子”,能够很好地筛掉海水中的盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如下图)下列关于氧化石墨烯膜“筛掉”氯化钠的说法错误的是( )
A.“筛掉”氯化钠过程类似于过滤操作 B.该过程可应用于海水蒸馏
C.该过程属于物理变化 D.右侧海水的溶质的质量分数增大
9.河水净化制自来水的主要步骤如下图所示,有关说法错误的是( )
A.步骤Ⅰ可除去难溶性杂质 B.X试剂可以是活性炭
C.步骤Ⅲ可杀菌、消毒 D.净化的水为纯净水
二、填空题
10.小明同学得到了如下关于A、B的两种固体物质的溶解度表:
温度(℃) 0 10 20 30 40
溶解度(g) A 35 35.5 36 36.5 37
B 6 10 18 36.5 50
(1)若将B物质从溶液中结晶析出,宜采用的方法是:___________。
(2)10℃,将10克B物质加入到90克水中时,溶质质量分数___________(计算结果保留一位小数)。
11.从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质,设计了如图A、B、C三个步骤。
(1)B步骤中玻璃棒的作用是___________;
(2)下列关于过滤的操作叙述正确的是___________;
A. 滤纸的边缘要低于漏斗口B. 液面不要低于滤纸的边缘
C. 玻璃棒要靠在三层滤纸的一边D. 漏斗下端的管口要紧靠烧杯内壁
12.直饮水机的水处理过程如图所示。
(1)“可直接饮用水”属于___________(填“混合物”或“纯净物”)
(2)炭罐的作用是___________(填选项字母)。
a.过滤 b.吸附除味 c.消毒杀菌
13.学校科学兴趣小组在讨论“水”的话题,大家积极参与,话题如下:
(1)如图,自然界中的水通过蒸发、降水、渗透、地表径流等环节进行着持续不断的循环。 其中“南水北调”工程对我国水资源“南方多,北方少”的状况有所改善。“南水北调”工程改变水循环中的环节是___________(填序号)
(2)能确认水是由氢元素和氧元素组成的实验是___________;
A.水的蒸发
B.水的电解
C.水的净化
D.水的蒸馏
(3)某同学发现最近家里的自来水有点浑浊,就想着自制一个如图所示的简易净水器。该净化过程中,用到分离混合物的方法有___________等(填一个即可)。通过这个简易装置净化后的水还是不能直接饮用,原因是___________。
14.为保持云和湖的卫生洁净,环境卫生部门会定时组织人员对云和湖及上游沿途进入或即将进入的污染物进行处理。
(1)打捞漂浮在云和湖面的杂物,相当于混合物分离方法中的________(选填“过滤”、“结晶”或“蒸馏”);
(2)下列行为会污染云和湖的是_________;
A.排入普通雨水 B.排入工业废水 C.丢入各种垃圾
15.氯化钠是生活必得品,也是重要的化工原料。下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答问题。
温度/℃ 20 30 40 50 60
溶解度/g 氯化钠 36.0 36.3 36.6 37.0 37.3
硝酸钾 31.6 45.8 63.9 85.5 110
(1)要把硝酸钾从含有少量氯化钠的溶液中提出,最好采用的方法是___________。
(2)提纯含少量泥沙的粗盐,一般经过以下操作流程:
操作④的名称是___________ , 操作⑤中玻璃棒的作用是 ___________。
16.如图甲是自来水的生产过程。据图回答:
(1)由图甲可知,自来水生产过程中使用的净水方法有 ___________。
A. 沉淀B. 过滤 C. 蒸馏
(2)在物质分类上,杀菌后输送给用户的水属于___________;(选填 “混合物”或“纯净物”)
17.联合国确定2021年“世界水日”的主题为“Valuing Water”(珍惜水、爱护水)
(1)从组成的角度看:水是由______组成的。(填写选项编号)
A.氢元素和氧元素 B.氢原子和氧原子 C.氢气和氧气
(2)从能源的角度看:电解水产生理想的清洁高能燃料氢气。水电解的文字表达式为______。
(3)从净化的角度看:有关图1所示净化河水简易装置,说法错误的是______。
A.水本身是一种化学资源
B.此装置可以得到纯净水
C.利用此装置净化得到的水不宜直接饮用
(4)从变化的角度看:电解一定量的水(如图2),当阳极端产生 5mL 气体时, 理论上在阴极端产生气体的体积为______mL。
18.如下表是硝酸钾、氯化钠在不同温度下的溶解度。
温度/℃ 10 20 30 40 50
硝酸钾的溶解度g/100g 20.9 31.6 45.8 63.9 85.5
氯化钠的溶解度g/100g 35.8 36.0 36.3 36.6 37.0
(1)从表中数据分析,溶解度受温度影响较大的物质是______。
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾的方法为______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.B
【详解】
A、配制蔗糖溶液中玻璃棒的作用是搅拌,加速蔗糖溶解。
B、过滤时,玻璃棒的作用是引流。
C、蒸发结晶时,玻璃棒的作用是搅拌,防止受热不均匀导致液体飞溅。
D、配置10%的食盐水,玻璃棒的作用是搅拌。
故B选项玻璃棒的作用与其他三组不同。
故选B。
2.D
【详解】
A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误。
B、配制溶液时,溶解操作应在烧杯中进行,用玻璃棒不断搅拌,图中所示操作错误。
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中所示操作错误。
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作正确。
故选D。
3.D
【详解】
A、甲溶液在初始蒸发阶段就有晶体析岀,说明甲为饱和溶液,而乙镕液初始无固体析出,为不饱和溶液,故选项正确。
B、b点时乙溶液已经析出了固体,因此是饱和溶液,故选项正确。
C、t℃时,乙的溶解度更大,因为蒸发相同的溶剂,乙析出的溶质多,故选项正确。
D、a点时,甲溶液的质量分数应为溶质质量与溶液质量的比值,故选项错误。
故选D。
【点睛】
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
4.D
【详解】
“取黄连一两,捣碎,加鼓二十粒”,涉及到称量;“捣碎,水煎去渣”,涉及到加热和过滤操作,没有涉及的操作是蒸发结晶。
故选D。
5.D
【详解】
A、溶液是均一、稳定的混合物,溶质均匀分散在溶剂中,但是在不断的运动,不符合题意。
B、沉降只能使悬浮的杂质沉降,过滤只能除去难溶性杂质,活性炭只能吸附水中的色素和异味,天然水经沉降、过滤、活性炭吸附后得到的水中还含有可溶性杂质,不是纯净物,不符合题意。
C、洗洁精中含有乳化剂,具有乳化作用,能将油污乳化为细小油滴,形成乳浊液,不符合题意。
D、溶液具有均一性,配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数,符合题意。
故选D。
6.A
【详解】
超滤膜可以除去不溶性的杂质,所以步骤②对应的操作是过滤。
故选A。
7.D
【详解】
A、不能在量筒中配置溶液,故A错误。
B、取下蒸发皿用坩埚钳夹取,不能用手拿,以防烫伤,故B错误。
C、过滤时需要用玻璃棒引流,故C错误。
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,故D正确。
故选D。
8.B
【详解】
A、“筛掉”氯化钠过程类似于过滤操作,正确。
B、海水蒸馏得到的是纯净水,氧化石墨烯薄膜制成“筛子”,能够很好地筛掉海水中的盐类物质,但是得到水中含有其他的杂质,所以不能应用于海水蒸馏,错误。
C、该过程没有新物质生成,属于物理变化,正确。
D、右侧海水因溶剂质量减小,溶质的质量分数增大,正确。
故选B。
9.D
【详解】
A、步骤Ⅰ可除去难溶性杂质,不符合题意。
B、活性炭具有吸附性,可除去水中的色素和异味, X 试剂可以是活性炭,不符合题意。
C、步骤Ⅲ中液氯可杀菌、消毒,不符合题意。
D、净化的水中仍含有可溶性杂质,不是纯净水,符合题意。
故选D。
10.降温结晶 9.1%
【详解】
(1)由A、B的两种固体物质的溶解度表,B的溶解度随着温度的升高而增大,溶解度受温度的影响变化较大,一般采用降温结晶的方法,降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出。
(2)10℃时,B物质的溶解度为10g,则在该温度下,100g水中最多能溶解10gB物质。将10克B物质加入到90克水中时,B物质无法完全溶解,所形成的溶液为该温度下的饱和溶液,其溶液的溶质质量分数=。
11.引流 ACD
【详解】
(1)B步骤是过滤操作,玻璃棒的作用是引流。
(2)过滤液体时,注意“一贴、二低、三靠”的原则,滤纸的边缘要低于漏斗口,液面要低于滤纸的边缘,玻璃棒要靠在三层滤纸的一边, 漏斗下端的管口要紧靠烧杯内壁。故选ACD。
12.混合物 b
【详解】
(1)直饮水机不能除去水中的可溶性物质,“可直接饮用水”含有可溶性物质,属于混合物。
(2)活性炭具有吸附性,能吸附颜色和异味。炭罐含有活性炭,作用是 b。
13.⑤ B 过滤 水中还含有微生物和可溶性杂质
【详解】
(1) “南水北调”工程改变水循环中的环节是地表径流环节,即图中的⑤ 。
(2)水的电解实验产生氢气和氧气,说明水是由氢元素和氧元素组成,其它选项是物理变化,不能证明水的组成,故选B。
(3)小卵石、细沙、活性炭、棉花等物质是具有吸附作用的固体,用它们来过滤,不仅可以滤去液体中的不溶性物质,还可以吸附掉一些溶解的杂质,除去异味。但对于液体中含有的微生物以及一部分可溶性杂质是无法去除的,所以通过这个简易装置净化后的水还是不能直接饮用。
14.过滤 BC
【详解】
(1)过滤可以将不溶性固体和液体分离,打捞漂浮在河道的杂物,相当于混合物分离方法中的过滤。
(2)A.排入普通雨水,不会造成水体污染;
B.排入工业废水,会造成水体污染;
C.丢入废旧电池,会造成水体污染。
故选BC。
15.冷却热饱和溶液(降温结晶) 过滤 搅拌使滤液受热均匀,防止液体飞溅
【详解】
(1)根据表格可知,硝酸钾的溶解度随温度的升高而迅速增大,而氯化钠的溶解度几乎不受温度的影响,因此要把硝酸钾从含有少量氯化钠的溶液中提出,最好采用的方法是冷却热饱和溶液(降温结晶)。
(2)根据图片可知,操作④用于分离泥沙和滤液,应该是过滤。操作⑤从滤液中得到晶体,应该为结晶,在结晶操作中玻璃棒的作用:搅拌使滤液受热均匀,防止液体飞溅。
16.AB 混合物
【详解】
(1)自来水净化过程包括沉淀、过滤、吸附和消毒,故选AB。
(2)杀菌后的自来水看似无色透明,其中仍然含有大量的可溶性的钙镁化合物,因此属于混合物。
17.A 水氢气+氧气 B 10
【详解】
(1)物质是由元素组成的,所以从组成的角度看:水是由氢元素和氧元素组成的,故选:A。
(2)电解水产生氢气和氧气,文字表达式为:水氢气+氧气。
(3)A、水是一种重要的化学资源,故正确;
B、利用此装置不能得到纯净水,得到的水中还含有部分可溶性杂质,故错误;
C、利用此装置净化得到的水还含有可溶性杂质和细菌、病毒,所以还不能作为饮用水,故正确。
故选B。
(4)水通电分解,正极生成氧气,负极产生氢气,二者的体积比为1:2,所以正极(阳极)产生的气体是氧气,当正极产生的气体为5mL时,负极产生的气体体积为10mL。
18.硝酸钾 冷却热饱和溶液(降温结晶)
【详解】
(1) 从表中数据分析,溶解度受温度影响较大的物质是硝酸钾,氯化钠溶解度受温度影响不大。
(2)硝酸钾溶解度受温度影响大,氯化钠溶解度受温度影响小,所以当硝酸钾中混有少量氯化钠时,提纯硝酸钾的方法为冷却热饱和溶液(降温结晶)。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
