2022年化学九年级下册第八单元 金属和金属材料复习课 同步精选课件(15页)
文档属性
| 名称 | 2022年化学九年级下册第八单元 金属和金属材料复习课 同步精选课件(15页) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-06 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
2021-2022学年九年级化学下册同步精品课堂(人教版)
第八单元 金属和金属材料 Metals and metal materials
第八单元 金属和金属材料 单元复习课
1.
考点一:金属材料
2.
考点二:金属的化学性质
3.
考点三:冶炼生铁
4.
考点四:铁锈蚀的条件及防护措施
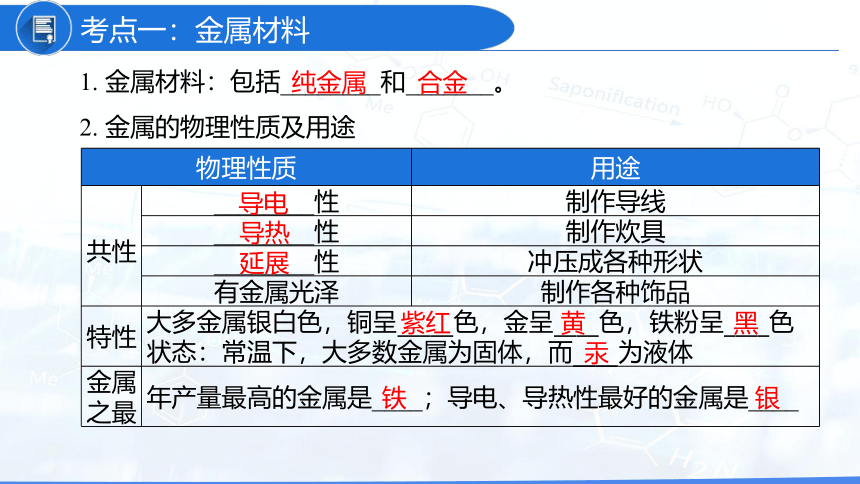
考点一:金属材料
1. 金属材料:包括________和_______。
2. 金属的物理性质及用途
纯金属
合金
物理性质 用途
共性 ________性 制作导线
________性 制作炊具
________性 冲压成各种形状
有金属光泽 制作各种饰品
特性 大多金属银白色,铜呈_____色,金呈____色,铁粉呈____色 状态:常温下,大多数金属为固体,而____为液体 金属之最 年产量最高的金属是____;导电、导热性最好的金属是____ 导电
导热
延展
紫红
黄
黑
汞
铁
银
考点一:金属材料
3. 合金及其特性
概念 在金属中加热熔合某些金属或非金属,制得具有______特征的物质。合金属于________(填物质类别)
性能 与其组分金属相比:合金的硬度和强度______;抗腐蚀性______;熔点______。
常见合金 铁合金:生铁(含碳量2%~4.3%)和钢(含碳量0.03%~2%)都属于铁合金,两者性能不同的原因是____________
黄铜: 合金
钛合金:熔点高、密度小、可塑性好。由于和人体具有良好的“相容性”,因此可用于制造人造骨
金属
更大
更强
更低
混合物
含碳量不同
铜锌
1.下列物品主要是由合金制成的是( )
A. 塑料水杯 B. 青铜铸像
C. 汽车轮胎 D. 羊毛大衣
B
2.下列有关金属材料的说法不正确的是( )
A. 生铁比纯铁的硬度大
B. 地壳中含量最高的金属元素是铁
C. 多数合金的抗腐蚀性能比组成它们的纯金属要好
D. 钢的含碳量比生铁的低
B
考点二:金属的化学性质
1.金属+氧气→金属氧化物
4Al + 3O2 = 2Al2O3
2Mg + O2 = 2MgO
2Cu+O2 2CuO
3Fe+2O2 Fe3O4
(铝制品耐腐蚀的原因)
2.金属+酸→盐+氢气
Mg + H2SO4 = MgSO4 + H2↑
Mg + 2HCl = MgCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
2Al + 6HCl = 2AlCl3 + 3H2↑
3.金属+盐溶液→新金属+新盐
考点二:金属的化学性质
2Al +3CuSO4 = 3Cu + Al2(SO4)3
Cu + 2AgNO3 = 2Ag + Cu(NO3)2
Fe + CuSO4 = Cu + FeSO4
Zn + Cu(NO3)2 = Cu + Zn(NO3)2
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性顺序
1.在金属活动性顺序里:金属的位置越 _____,它的活动性就越强。
2.在金属活动性顺序里:位于 ____ 前面的金属能置换出盐酸、稀硫酸中的____。
3.金属活动性顺序里:位于_____ 的金属能把位于_____ 的金属从它们的化合物的溶液里置换出来。
靠前
氢
后面
氢
前面
K
CaNa除外
氢元素,不是氢气
2.农业上不能用铁制容器配制和盛放波尔多液,请用化学方程式来表示 。
Fe + CuSO4 = Cu + FeSO4
1.下列物质不能由金属铁通过一步反应制得的是( )
A. Cu B. Fe3O4 C. H2 D. FeCl3
D
3.下列有关说法正确的是( )
A. 光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡
B. 将打磨好的铜丝在酒精灯上加热,铜丝表面由黑色变红色
C. 将铜片放入硝酸银溶液,溶液由无色变为蓝色
D. 将铁钉加入到稀硫酸中,溶液由无色变为黄色
C
考点三:冶炼生铁
【实验原理】
用赤铁矿炼铁________________________________
Fe2O3+3CO 2Fe + 3CO2
用磁铁矿炼铁________________________________
Fe3O4 + 4CO 3Fe + 4CO2
【实验现象】 化学方程式
红棕色粉末变成_______
澄清的石灰水_________
CO2+Ca(OH)2=CaCO3↓+H2O
黑色
变浑浊
Fe2O3+3CO 2Fe + 3CO2
考点三:冶炼生铁
防止石灰水倒吸,使玻璃管炸裂。
1.先通CO后加热:___________________________
防止CO和空气混合加热而爆炸
2.先停止加热,继续通CO至装置冷却:
4.应先点燃 (前面/后面)的酒精灯
3.尾气处理:方法____________
目的:________________
点燃或收集
防止CO污染空气
后面
5.用物理方法检验玻璃管中生成了铁?
用磁铁吸引
【注意事项】
1. 如图为CO还原氧化铁实验。下列说法中正确的是( )
A. 开始时应先预热玻璃管,后通入一氧化碳
B. 实验中玻璃管里粉末由黑色逐渐变成红棕色
C. 参加反应的氧化铁和一氧化碳质量比为40∶7
D. 将尾气点燃或收集,可防止一氧化碳污染空气
D
考点四、金属的锈蚀与防护
1.铁生锈的条件:铁与_________同时接触。
水和氧气
2.铁锈属于混合物,主要成分是 ,质地很 。
Fe2O3
疏松
3.防止金属腐蚀的措施(原理:隔绝_________。)
(1)保持铁制品表面干燥
(2)覆盖保护层(喷漆、涂油、电镀)
(3)改变金属结构(制成不锈钢)
氧气和水
(1)如图是某化学兴趣小组设计的铁钉锈蚀条件的探究实验,要达到实验目的还需补充什么实验?请简要叙述。
(2)写出用盐酸除铁锈的化学方程式。
1. 铁制品在潮湿的空气中容易生锈。
还需补充铁钉在干燥的空气中的实验。
Fe2O3+6HCl = 2FeCl3+3H2O
2021-2022学年九年级化学下册同步精品课堂(人教版)
第八单元 金属和金属材料 Metals and metal materials
第八单元 金属和金属材料 单元复习课
1.
考点一:金属材料
2.
考点二:金属的化学性质
3.
考点三:冶炼生铁
4.
考点四:铁锈蚀的条件及防护措施
考点一:金属材料
1. 金属材料:包括________和_______。
2. 金属的物理性质及用途
纯金属
合金
物理性质 用途
共性 ________性 制作导线
________性 制作炊具
________性 冲压成各种形状
有金属光泽 制作各种饰品
特性 大多金属银白色,铜呈_____色,金呈____色,铁粉呈____色 状态:常温下,大多数金属为固体,而____为液体 金属之最 年产量最高的金属是____;导电、导热性最好的金属是____ 导电
导热
延展
紫红
黄
黑
汞
铁
银
考点一:金属材料
3. 合金及其特性
概念 在金属中加热熔合某些金属或非金属,制得具有______特征的物质。合金属于________(填物质类别)
性能 与其组分金属相比:合金的硬度和强度______;抗腐蚀性______;熔点______。
常见合金 铁合金:生铁(含碳量2%~4.3%)和钢(含碳量0.03%~2%)都属于铁合金,两者性能不同的原因是____________
黄铜: 合金
钛合金:熔点高、密度小、可塑性好。由于和人体具有良好的“相容性”,因此可用于制造人造骨
金属
更大
更强
更低
混合物
含碳量不同
铜锌
1.下列物品主要是由合金制成的是( )
A. 塑料水杯 B. 青铜铸像
C. 汽车轮胎 D. 羊毛大衣
B
2.下列有关金属材料的说法不正确的是( )
A. 生铁比纯铁的硬度大
B. 地壳中含量最高的金属元素是铁
C. 多数合金的抗腐蚀性能比组成它们的纯金属要好
D. 钢的含碳量比生铁的低
B
考点二:金属的化学性质
1.金属+氧气→金属氧化物
4Al + 3O2 = 2Al2O3
2Mg + O2 = 2MgO
2Cu+O2 2CuO
3Fe+2O2 Fe3O4
(铝制品耐腐蚀的原因)
2.金属+酸→盐+氢气
Mg + H2SO4 = MgSO4 + H2↑
Mg + 2HCl = MgCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
2Al + 6HCl = 2AlCl3 + 3H2↑
3.金属+盐溶液→新金属+新盐
考点二:金属的化学性质
2Al +3CuSO4 = 3Cu + Al2(SO4)3
Cu + 2AgNO3 = 2Ag + Cu(NO3)2
Fe + CuSO4 = Cu + FeSO4
Zn + Cu(NO3)2 = Cu + Zn(NO3)2
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性顺序
1.在金属活动性顺序里:金属的位置越 _____,它的活动性就越强。
2.在金属活动性顺序里:位于 ____ 前面的金属能置换出盐酸、稀硫酸中的____。
3.金属活动性顺序里:位于_____ 的金属能把位于_____ 的金属从它们的化合物的溶液里置换出来。
靠前
氢
后面
氢
前面
K
CaNa除外
氢元素,不是氢气
2.农业上不能用铁制容器配制和盛放波尔多液,请用化学方程式来表示 。
Fe + CuSO4 = Cu + FeSO4
1.下列物质不能由金属铁通过一步反应制得的是( )
A. Cu B. Fe3O4 C. H2 D. FeCl3
D
3.下列有关说法正确的是( )
A. 光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡
B. 将打磨好的铜丝在酒精灯上加热,铜丝表面由黑色变红色
C. 将铜片放入硝酸银溶液,溶液由无色变为蓝色
D. 将铁钉加入到稀硫酸中,溶液由无色变为黄色
C
考点三:冶炼生铁
【实验原理】
用赤铁矿炼铁________________________________
Fe2O3+3CO 2Fe + 3CO2
用磁铁矿炼铁________________________________
Fe3O4 + 4CO 3Fe + 4CO2
【实验现象】 化学方程式
红棕色粉末变成_______
澄清的石灰水_________
CO2+Ca(OH)2=CaCO3↓+H2O
黑色
变浑浊
Fe2O3+3CO 2Fe + 3CO2
考点三:冶炼生铁
防止石灰水倒吸,使玻璃管炸裂。
1.先通CO后加热:___________________________
防止CO和空气混合加热而爆炸
2.先停止加热,继续通CO至装置冷却:
4.应先点燃 (前面/后面)的酒精灯
3.尾气处理:方法____________
目的:________________
点燃或收集
防止CO污染空气
后面
5.用物理方法检验玻璃管中生成了铁?
用磁铁吸引
【注意事项】
1. 如图为CO还原氧化铁实验。下列说法中正确的是( )
A. 开始时应先预热玻璃管,后通入一氧化碳
B. 实验中玻璃管里粉末由黑色逐渐变成红棕色
C. 参加反应的氧化铁和一氧化碳质量比为40∶7
D. 将尾气点燃或收集,可防止一氧化碳污染空气
D
考点四、金属的锈蚀与防护
1.铁生锈的条件:铁与_________同时接触。
水和氧气
2.铁锈属于混合物,主要成分是 ,质地很 。
Fe2O3
疏松
3.防止金属腐蚀的措施(原理:隔绝_________。)
(1)保持铁制品表面干燥
(2)覆盖保护层(喷漆、涂油、电镀)
(3)改变金属结构(制成不锈钢)
氧气和水
(1)如图是某化学兴趣小组设计的铁钉锈蚀条件的探究实验,要达到实验目的还需补充什么实验?请简要叙述。
(2)写出用盐酸除铁锈的化学方程式。
1. 铁制品在潮湿的空气中容易生锈。
还需补充铁钉在干燥的空气中的实验。
Fe2O3+6HCl = 2FeCl3+3H2O
同课章节目录
