第十单元酸和碱课题1常见的酸和碱第一课时基本概念—2021-2022学年九年级化学人教版下册(共16张PPT)
文档属性
| 名称 | 第十单元酸和碱课题1常见的酸和碱第一课时基本概念—2021-2022学年九年级化学人教版下册(共16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-09 00:00:00 | ||
图片预览






文档简介
(共16张PPT)
第一课时 酸碱盐的概念
第十单元 酸和碱
创设情境
生活中常见的酸
柠檬、山楂、食醋吃起来有酸味。生活中还有很多物质吃起来有酸味。生活中所说的酸和化学上所说的酸是同一个概念吗?
在学习金属的化学性质的时候,我们学习过很多活泼金属能与盐酸、稀硫酸发生化学反应。你还记得盐酸、硫酸的化学式吗?
盐酸
(HCl)
硫酸
(H2SO4)
除了盐酸和硫酸外,实验室中常见的酸还有硝酸和磷酸。
硝酸
( HNO3 )
磷酸
(H3PO4)
盐酸
(HCl)
硫酸
(H2SO4)
碳酸
(H2CO3)
硝酸
( HNO3 )
磷酸
(H3PO4)
从形式看:①名称: ;②化学式最左边的元素一般是 元素。
某酸
H
观察与思考:请观察下面这些酸的化学式,从组成上来看,它们都有哪些相同点?
酸:
电离时生成的阳离子全部是氢离子的化合物。
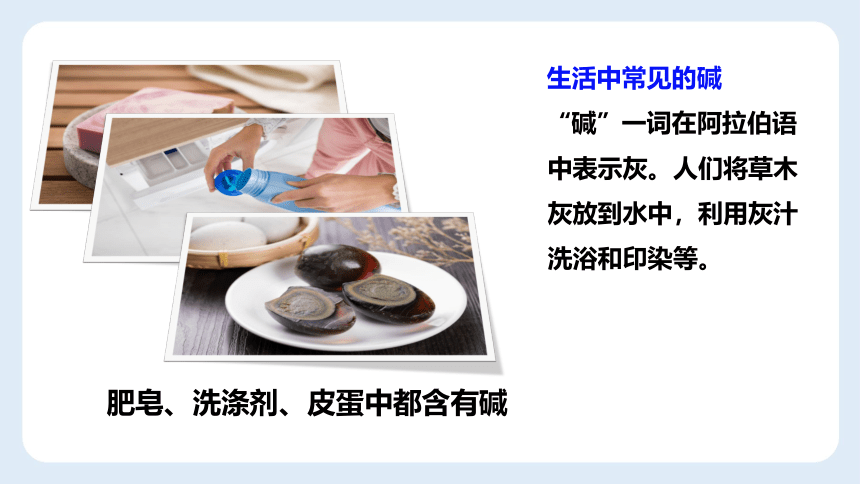
生活中常见的碱
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴和印染等。
肥皂、洗涤剂、皮蛋中都含有碱
氢氧化钠(NaOH)
氢氧化钙【 Ca(OH)2 】
观察与思考:请观察下面这些碱的化学式,从组成上来看,它们都有哪些相同点?
从形式看:①名称: ;②化学式最右边一般是 。
氢氧化某
氢氧根(OH )
碱:
电离时生成的阴离子全部是氢氧根离子的化合物。
氯化钠(NaCl)
硫酸铜(CuSO4)
碳酸钙(CaCO3)
观察与思考:请观察上面这些物质的化学式,从组成上来看,它们都有哪些相同点?它们是酸吗?它们是碱吗?
从形式看:由 和 构成。
金属离子
酸根离子
盐:
由金属离子(或NH4+)和酸根离子构成的一类化合物。
请你根据所学知识将下列物质分分类:
HCl
CaCO3
Na2CO3
Mg(OH)2
H2SO4
NaOH
CuSO4
Ba(OH)2
CaO
SO2
Fe
S
CuSO4
酸:
碱:
HCl
H2SO4
NaOH
Mg(OH)2
Ba(OH)2
CaCO3
Na2CO3
NH4Cl
单质:
盐:
S
Fe
氧化物:
CaO
SO2
化
合
物
单
质
碱
酸
金属
单质
非金
属单质
盐
氧
化
物
物质
混
合
物
纯
净
物
如盐酸(HCl)、硫酸( H2SO4 )、碳酸(H2CO3)
如氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)
如氯化钠(NaCl)、硫酸铜(CuSO4)
如MgO 、Fe3O4 、Al2O3 、SO2、 CO2 、P2O5、 H2O、 H2O2
如Mg、 Fe、 Cu 、Al、Hg、K、Mn
如S、 C、 P 、O2、 O3、H2、 N2
练习
下列物质中,属于单质的是 (填序号,下同) ;属于氧化物的是 ;属于酸的是 ;属于碱的是 ;属于盐的是 。
① H2SO4 ② MgCl2 ③ O3
④ H2CO3 ⑤ AgNO3 ⑥ Al(OH)3 ⑦ NH4NO3 ⑧ Ne ⑨ SO3
⑩ ZnO Fe Fe(OH)2
①
11
12
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
12
Na2CO3 、k2CO3、 MgCO3 、 FeCO3 、 CaCO3
Na2SO4 、K2SO4 、MgSO4 、 FeSO4 、 CaSO4
NaCl 、 KCl 、 MgCl2、 FeCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Fe (NO3)2 、Ca (NO3)2
碳酸盐
硫酸盐
盐酸盐
硝酸盐
钠盐
钾盐
镁盐
亚铁盐
钙盐
(NH4) 2CO3
(NH4) 2SO4
NH4 Cl
NH4 NO3
铵盐
从盐的组成上,我们怎样对盐进行分类?
盐
阳离子
阴离子
碳酸盐
钠盐
铵盐
镁盐
钾盐
硝酸盐
硫酸盐
盐酸盐
Na2CO3、Na2SO4 、NaCl、NaNO3
k2CO3、K2SO4、 KCl、 KNO3
(NH4) 2CO3 (NH4) 2SO4 NH4 Cl NH4 NO3
MgCO3、MgSO4 、MgCl2、Mg(NO3)2
Na2CO3 、k2CO3、 MgCO3 、CaCO3
Na2SO4 、K2SO4 、MgSO4 、CaSO4
NaCl 、 KCl 、 MgCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Ca (NO3)2
OH- NO3- Cl- SO42- CO32-
H+ 溶、挥 溶、挥 溶 溶、挥
NH4+ 溶、挥 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Ca2+ 微 溶 溶 微 不
Mg2+ 不 溶 溶 溶 微
Al3+ 不 溶 溶 溶 ——
Mn2+ 不 溶 溶 溶 不
Zn2+ 不 溶 溶 溶 不
Fe2+ 不 溶 溶 溶 不
Fe3+ 不 溶 溶 溶 ——
Cu2+ 不 溶 溶 溶 ——
Ag+ —— 溶 不 微 不
酸、碱、盐的溶解性(20℃)
说明:
“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“—”表示那种物质不存在或者遇到水就分解了。
物质溶解性口诀:
钾钠铵硝均可溶
盐酸盐不溶氯化银
硫酸盐不溶硫酸钡
碳磷酸盐多不溶
只溶钾钠铵
多数酸溶碱少溶
除了钾钠钙钡氨
初中化学常见的8个沉淀:AgCl、BaSO4、BaCO3、CaCO3、Cu(OH)2、Fe(OH)3、Mg(OH)2、Al(OH)3
根据盐的溶解性,我们怎样对盐进行分类?
盐
可溶性盐
可溶性盐
k2CO3、K2SO4、 KCl、 KNO3
Na2CO3、Na2SO4 、NaCl、NaNO3
(NH4) 2CO3 (NH4) 2SO4 NH4 Cl NH4 NO3
NaNO3 、 KNO3 、 Mg(NO3)2、Ca (NO3)2
AgCl、BaSO4、BaCO3、CaCO3、Ag2CO3
课堂小结
酸、碱、盐
酸
盐
概念
分类
溶解性
碱
第一课时 酸碱盐的概念
第十单元 酸和碱
创设情境
生活中常见的酸
柠檬、山楂、食醋吃起来有酸味。生活中还有很多物质吃起来有酸味。生活中所说的酸和化学上所说的酸是同一个概念吗?
在学习金属的化学性质的时候,我们学习过很多活泼金属能与盐酸、稀硫酸发生化学反应。你还记得盐酸、硫酸的化学式吗?
盐酸
(HCl)
硫酸
(H2SO4)
除了盐酸和硫酸外,实验室中常见的酸还有硝酸和磷酸。
硝酸
( HNO3 )
磷酸
(H3PO4)
盐酸
(HCl)
硫酸
(H2SO4)
碳酸
(H2CO3)
硝酸
( HNO3 )
磷酸
(H3PO4)
从形式看:①名称: ;②化学式最左边的元素一般是 元素。
某酸
H
观察与思考:请观察下面这些酸的化学式,从组成上来看,它们都有哪些相同点?
酸:
电离时生成的阳离子全部是氢离子的化合物。
生活中常见的碱
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴和印染等。
肥皂、洗涤剂、皮蛋中都含有碱
氢氧化钠(NaOH)
氢氧化钙【 Ca(OH)2 】
观察与思考:请观察下面这些碱的化学式,从组成上来看,它们都有哪些相同点?
从形式看:①名称: ;②化学式最右边一般是 。
氢氧化某
氢氧根(OH )
碱:
电离时生成的阴离子全部是氢氧根离子的化合物。
氯化钠(NaCl)
硫酸铜(CuSO4)
碳酸钙(CaCO3)
观察与思考:请观察上面这些物质的化学式,从组成上来看,它们都有哪些相同点?它们是酸吗?它们是碱吗?
从形式看:由 和 构成。
金属离子
酸根离子
盐:
由金属离子(或NH4+)和酸根离子构成的一类化合物。
请你根据所学知识将下列物质分分类:
HCl
CaCO3
Na2CO3
Mg(OH)2
H2SO4
NaOH
CuSO4
Ba(OH)2
CaO
SO2
Fe
S
CuSO4
酸:
碱:
HCl
H2SO4
NaOH
Mg(OH)2
Ba(OH)2
CaCO3
Na2CO3
NH4Cl
单质:
盐:
S
Fe
氧化物:
CaO
SO2
化
合
物
单
质
碱
酸
金属
单质
非金
属单质
盐
氧
化
物
物质
混
合
物
纯
净
物
如盐酸(HCl)、硫酸( H2SO4 )、碳酸(H2CO3)
如氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)
如氯化钠(NaCl)、硫酸铜(CuSO4)
如MgO 、Fe3O4 、Al2O3 、SO2、 CO2 、P2O5、 H2O、 H2O2
如Mg、 Fe、 Cu 、Al、Hg、K、Mn
如S、 C、 P 、O2、 O3、H2、 N2
练习
下列物质中,属于单质的是 (填序号,下同) ;属于氧化物的是 ;属于酸的是 ;属于碱的是 ;属于盐的是 。
① H2SO4 ② MgCl2 ③ O3
④ H2CO3 ⑤ AgNO3 ⑥ Al(OH)3 ⑦ NH4NO3 ⑧ Ne ⑨ SO3
⑩ ZnO Fe Fe(OH)2
①
11
12
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
12
Na2CO3 、k2CO3、 MgCO3 、 FeCO3 、 CaCO3
Na2SO4 、K2SO4 、MgSO4 、 FeSO4 、 CaSO4
NaCl 、 KCl 、 MgCl2、 FeCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Fe (NO3)2 、Ca (NO3)2
碳酸盐
硫酸盐
盐酸盐
硝酸盐
钠盐
钾盐
镁盐
亚铁盐
钙盐
(NH4) 2CO3
(NH4) 2SO4
NH4 Cl
NH4 NO3
铵盐
从盐的组成上,我们怎样对盐进行分类?
盐
阳离子
阴离子
碳酸盐
钠盐
铵盐
镁盐
钾盐
硝酸盐
硫酸盐
盐酸盐
Na2CO3、Na2SO4 、NaCl、NaNO3
k2CO3、K2SO4、 KCl、 KNO3
(NH4) 2CO3 (NH4) 2SO4 NH4 Cl NH4 NO3
MgCO3、MgSO4 、MgCl2、Mg(NO3)2
Na2CO3 、k2CO3、 MgCO3 、CaCO3
Na2SO4 、K2SO4 、MgSO4 、CaSO4
NaCl 、 KCl 、 MgCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Ca (NO3)2
OH- NO3- Cl- SO42- CO32-
H+ 溶、挥 溶、挥 溶 溶、挥
NH4+ 溶、挥 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Ca2+ 微 溶 溶 微 不
Mg2+ 不 溶 溶 溶 微
Al3+ 不 溶 溶 溶 ——
Mn2+ 不 溶 溶 溶 不
Zn2+ 不 溶 溶 溶 不
Fe2+ 不 溶 溶 溶 不
Fe3+ 不 溶 溶 溶 ——
Cu2+ 不 溶 溶 溶 ——
Ag+ —— 溶 不 微 不
酸、碱、盐的溶解性(20℃)
说明:
“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“—”表示那种物质不存在或者遇到水就分解了。
物质溶解性口诀:
钾钠铵硝均可溶
盐酸盐不溶氯化银
硫酸盐不溶硫酸钡
碳磷酸盐多不溶
只溶钾钠铵
多数酸溶碱少溶
除了钾钠钙钡氨
初中化学常见的8个沉淀:AgCl、BaSO4、BaCO3、CaCO3、Cu(OH)2、Fe(OH)3、Mg(OH)2、Al(OH)3
根据盐的溶解性,我们怎样对盐进行分类?
盐
可溶性盐
可溶性盐
k2CO3、K2SO4、 KCl、 KNO3
Na2CO3、Na2SO4 、NaCl、NaNO3
(NH4) 2CO3 (NH4) 2SO4 NH4 Cl NH4 NO3
NaNO3 、 KNO3 、 Mg(NO3)2、Ca (NO3)2
AgCl、BaSO4、BaCO3、CaCO3、Ag2CO3
课堂小结
酸、碱、盐
酸
盐
概念
分类
溶解性
碱
同课章节目录
