第十单元实验活动6:酸、碱的化学性质(课件18张PPT)
文档属性
| 名称 | 第十单元实验活动6:酸、碱的化学性质(课件18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 240.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-09 00:00:00 | ||
图片预览





文档简介
实验活动6 酸、碱的化学性质
夏天,被蚊虫叮咬以后,有人会用肥皂水来消痛止痒。你能利用学过的知识解释其中的化学原理吗?
实验目的
- Experimental purpose -
1.
加深对酸和碱的化学性质的认识
2.
通过实验解释生活中的一些现象
视频:酸、碱的化学性质
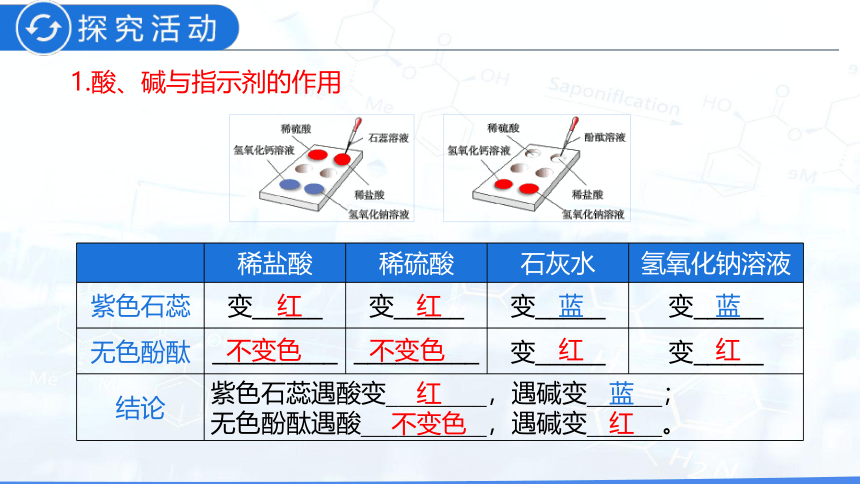
1.酸、碱与指示剂的作用
{5940675A-B579-460E-94D1-54222C63F5DA}
稀盐酸
稀硫酸
石灰水
氢氧化钠溶液
紫色石蕊
变_____
变_____
变_____
变_____
无色酚酞
_________
_________
变_____
变_____
结论
紫色石蕊遇酸变________,遇碱变______;
无色酚酞遇酸__________,遇碱变______。
红
红
蓝
蓝
不变色
不变色
红
红
红
蓝
不变色
红
1.使用点滴板与使用试管比较,使用点滴板的优点有哪些?
(1)节约药品;(2)操作简单;(3)便于观察
2.要一次鉴别出稀盐酸、澄清石灰水和食盐溶液,可以用 。
石蕊溶液
2.生锈铁钉与稀盐酸的反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①取两个生锈铁钉放于两支试管中,加入约2mL稀盐酸。
铁锈_____,铁钉变_____,溶液由___色变___色
化学方程式:______________________________
②将一只铁钉取出,洗净,继续观察另一支试管中现象。
铁钉表面有_______生成。
化学方程式:______________________________
结论:酸能与____________和____________反应。
①
②
消失
光亮
无
黄
6HCl+Fe2O3=2FeCl3+3H2O
气泡
2HCl+Fe=FeCl2+H2↑
金属氧化物
活泼金属
1.将铁钉放入试管时应如何操作?
2.生活中除去菜刀上的铁锈可以选择厨房中的 。
一横二放三慢竖,不能把铁钉直接投入试管中,防止打破试管。
食醋
3.用盐酸除铁锈时,能否将铁钉长时间浸没在稀盐酸中?
不能,因为稀盐酸能够与铁钉反应。
3.氢氧化钠与硫酸铜反应,氢氧化铜与稀盐酸反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①向试管加入2mL硫酸铜溶液,然后滴入氢氧化钠溶液。
生成____色沉淀,溶液由____色变为____色
化学方程式:___________________________
②向试管内的蓝色沉淀中加入稀盐酸,振荡,观察现象。
__________消失,溶液由____色变为____色
化学方程式:___________________________
结论:碱能与某些 反应;碱能与 反应。
蓝
蓝
无
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
蓝色沉淀
无
蓝
CuSO4+2HCl=CuCl2+2H2O
盐
酸
①
②
4.氢氧化钠溶液与稀盐酸反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液,观察。
溶液由____色变为____色
②向上述溶液中逐滴滴加稀盐酸,边滴边振荡。
溶液由____色变为____色
化学方程式:_______________________
③将少量反应后的溶液蒸干
蒸发皿中出现____色固体。
结论:酸能与_____发生中和反应。
③
无
红
红
无
HCl+NaOH=NaCl+H2O
白
碱
①
②
2.蒸干后,蒸发皿中剩余的白色固体可能是_________。
氯化钠
1.步骤中为什么要加入酚酞溶液,它在本实验中的作用是什么?
稀盐酸和氢氧化钠溶液反应无明显现象,加入酚酞起指示作用。
2.中和反应的实质是酸中 的和碱中的 结合生成水。
用离子方程式表示为 。
1.反应前后没有发生变化的离子有 。
氢氧化钠与盐酸反应微观示意图
Na+、Cl-
H++OH-=H2O
H+
OH-
1.农业上用熟石灰改良酸性土壤;
2.工业上处理工厂废水;
3.医疗上用碱性物质治疗胃酸过多。
酸碱中和反应在生活中有什么应用?
5.氢氧化钙的性质
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①向2支盛放Ca(OH)2粉末的试管中各加入1mL水,振荡。
形成____色浑浊液体
②各滴入1-2滴酚酞溶液
白色浑浊液体变为____色
③向其中一只试管中加入1mL水
红色液体仍然___________
④向另一只试管中加入约1mL稀盐酸,振荡。
浑浊液体变为___________
白
红
浑浊
无色澄清
①
②
③
④
1.通过本实验可以验证氢氧化钙的性质有:
氢氧化钙 溶于水;
氢氧化钙溶液显 性;
氢氧化钙能与 反应。
微
碱
酸
2.用澄清石灰水检验二氧化碳的反应为:CO2+Ca(OH)2=CaCO3↓+H2O,体现出碱能与 反应的化学性质。
非金属氧化物
指示剂
活泼金属
金属氧化物
H+ + OH- = H2O
中和反应
碱
酸
非金属氧化物
某些盐
酸、碱的化学性质
你的猜想:1. ;2. 。
{5940675A-B579-460E-94D1-54222C63F5DA}验证
方案
某学生做中和反应的实验,直接向氢氧化钠中加入稀盐酸,一段时间后发现忘了加酚酞,于是取反应后的溶液加入酚酞,发现酚酞不变色,就得出了恰好完全中和,所得溶液呈中性的结论。该同学的结论对吗?
②加锌粒,看是否有气泡;
①加紫色石蕊溶液,看是否变红;
③用pH试纸测定溶液的pH;
④加氧化铁,看是否溶解。
溶液呈中性
溶液呈酸性
https://www.21cnjy.com/help/help_extract.php
夏天,被蚊虫叮咬以后,有人会用肥皂水来消痛止痒。你能利用学过的知识解释其中的化学原理吗?
实验目的
- Experimental purpose -
1.
加深对酸和碱的化学性质的认识
2.
通过实验解释生活中的一些现象
视频:酸、碱的化学性质
1.酸、碱与指示剂的作用
{5940675A-B579-460E-94D1-54222C63F5DA}
稀盐酸
稀硫酸
石灰水
氢氧化钠溶液
紫色石蕊
变_____
变_____
变_____
变_____
无色酚酞
_________
_________
变_____
变_____
结论
紫色石蕊遇酸变________,遇碱变______;
无色酚酞遇酸__________,遇碱变______。
红
红
蓝
蓝
不变色
不变色
红
红
红
蓝
不变色
红
1.使用点滴板与使用试管比较,使用点滴板的优点有哪些?
(1)节约药品;(2)操作简单;(3)便于观察
2.要一次鉴别出稀盐酸、澄清石灰水和食盐溶液,可以用 。
石蕊溶液
2.生锈铁钉与稀盐酸的反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①取两个生锈铁钉放于两支试管中,加入约2mL稀盐酸。
铁锈_____,铁钉变_____,溶液由___色变___色
化学方程式:______________________________
②将一只铁钉取出,洗净,继续观察另一支试管中现象。
铁钉表面有_______生成。
化学方程式:______________________________
结论:酸能与____________和____________反应。
①
②
消失
光亮
无
黄
6HCl+Fe2O3=2FeCl3+3H2O
气泡
2HCl+Fe=FeCl2+H2↑
金属氧化物
活泼金属
1.将铁钉放入试管时应如何操作?
2.生活中除去菜刀上的铁锈可以选择厨房中的 。
一横二放三慢竖,不能把铁钉直接投入试管中,防止打破试管。
食醋
3.用盐酸除铁锈时,能否将铁钉长时间浸没在稀盐酸中?
不能,因为稀盐酸能够与铁钉反应。
3.氢氧化钠与硫酸铜反应,氢氧化铜与稀盐酸反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①向试管加入2mL硫酸铜溶液,然后滴入氢氧化钠溶液。
生成____色沉淀,溶液由____色变为____色
化学方程式:___________________________
②向试管内的蓝色沉淀中加入稀盐酸,振荡,观察现象。
__________消失,溶液由____色变为____色
化学方程式:___________________________
结论:碱能与某些 反应;碱能与 反应。
蓝
蓝
无
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
蓝色沉淀
无
蓝
CuSO4+2HCl=CuCl2+2H2O
盐
酸
①
②
4.氢氧化钠溶液与稀盐酸反应
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液,观察。
溶液由____色变为____色
②向上述溶液中逐滴滴加稀盐酸,边滴边振荡。
溶液由____色变为____色
化学方程式:_______________________
③将少量反应后的溶液蒸干
蒸发皿中出现____色固体。
结论:酸能与_____发生中和反应。
③
无
红
红
无
HCl+NaOH=NaCl+H2O
白
碱
①
②
2.蒸干后,蒸发皿中剩余的白色固体可能是_________。
氯化钠
1.步骤中为什么要加入酚酞溶液,它在本实验中的作用是什么?
稀盐酸和氢氧化钠溶液反应无明显现象,加入酚酞起指示作用。
2.中和反应的实质是酸中 的和碱中的 结合生成水。
用离子方程式表示为 。
1.反应前后没有发生变化的离子有 。
氢氧化钠与盐酸反应微观示意图
Na+、Cl-
H++OH-=H2O
H+
OH-
1.农业上用熟石灰改良酸性土壤;
2.工业上处理工厂废水;
3.医疗上用碱性物质治疗胃酸过多。
酸碱中和反应在生活中有什么应用?
5.氢氧化钙的性质
{5940675A-B579-460E-94D1-54222C63F5DA}步骤
现象
①向2支盛放Ca(OH)2粉末的试管中各加入1mL水,振荡。
形成____色浑浊液体
②各滴入1-2滴酚酞溶液
白色浑浊液体变为____色
③向其中一只试管中加入1mL水
红色液体仍然___________
④向另一只试管中加入约1mL稀盐酸,振荡。
浑浊液体变为___________
白
红
浑浊
无色澄清
①
②
③
④
1.通过本实验可以验证氢氧化钙的性质有:
氢氧化钙 溶于水;
氢氧化钙溶液显 性;
氢氧化钙能与 反应。
微
碱
酸
2.用澄清石灰水检验二氧化碳的反应为:CO2+Ca(OH)2=CaCO3↓+H2O,体现出碱能与 反应的化学性质。
非金属氧化物
指示剂
活泼金属
金属氧化物
H+ + OH- = H2O
中和反应
碱
酸
非金属氧化物
某些盐
酸、碱的化学性质
你的猜想:1. ;2. 。
{5940675A-B579-460E-94D1-54222C63F5DA}验证
方案
某学生做中和反应的实验,直接向氢氧化钠中加入稀盐酸,一段时间后发现忘了加酚酞,于是取反应后的溶液加入酚酞,发现酚酞不变色,就得出了恰好完全中和,所得溶液呈中性的结论。该同学的结论对吗?
②加锌粒,看是否有气泡;
①加紫色石蕊溶液,看是否变红;
③用pH试纸测定溶液的pH;
④加氧化铁,看是否溶解。
溶液呈中性
溶液呈酸性
https://www.21cnjy.com/help/help_extract.php
同课章节目录
