2022年浙江省中考科学一轮复习 第36课时 空气(课件 49张PPT)
文档属性
| 名称 | 2022年浙江省中考科学一轮复习 第36课时 空气(课件 49张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-11 00:00:00 | ||
图片预览








文档简介
(共49张PPT)
第36课时 空气
●知识体系梳理
●重难考点精讲
●当堂限时训练
知识体系
空气
空气的成分与利用
空气的污染与保护
大气环境问题
空气的污染与保护
空气污染
自净
废气
尾气
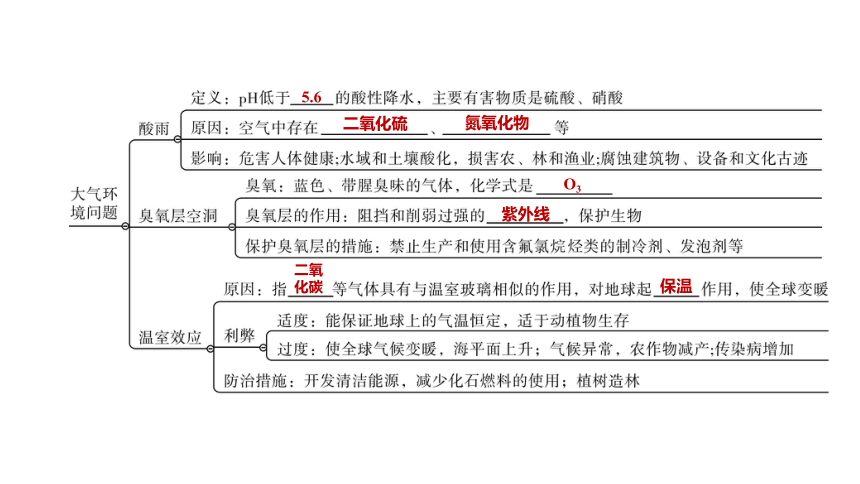
5.6
二氧化硫
氮氧化物
O3
紫外线
二氧
化碳
保温
重点梳理
1.空气(混合物)的主要成分及作用
成分 体积分数 主要作用
氧气(O2) ①供给 的重要物质
②用作 剂,用于钢铁冶炼、金属焊接等
氮气(N2) ①工业上生产硝酸和氮肥的重要原料
②氮气的化学性质 ,常用作 ,用于食品防腐保鲜、延长灯泡的使用寿命
21%
呼吸
助燃
78%
稳定
保护气
(续表)
成分 体积分数 主要作用
稀有气体( 、 、 、氡等) 0.94% ①化学性质稳定,常用作
②通电时能发出不同颜色的光,可作各种用途的
氦
氖
氩
保护气
电光源
(续表)
成分 体积分数 主要作用
二氧化碳 0.03% ①是 作用的原料
②固态CO2(俗称 )可作制冷剂,可用于
③工业上可用于制纯碱、尿素、汽水等
④可用于灭火
光合
干冰
人工降雨
2.测定空气中氧气的含量
(1)实验原理:在密闭容器内加热或燃烧某种可燃物(如点燃
),消耗容器内的 ,使密闭体系内的气压 ,在容器内外 的作用下,引起实验过程中的一些其他现象(如水倒吸),从而测出空气中氧气的含量。
(2)药品选择:常用药品为足量的 等,所选药品只能与空气中的 反应,不能和其他气体成分反应,且反应不能生成新的 。
红磷
氧气
减小
压强差
红磷
氧气
气体
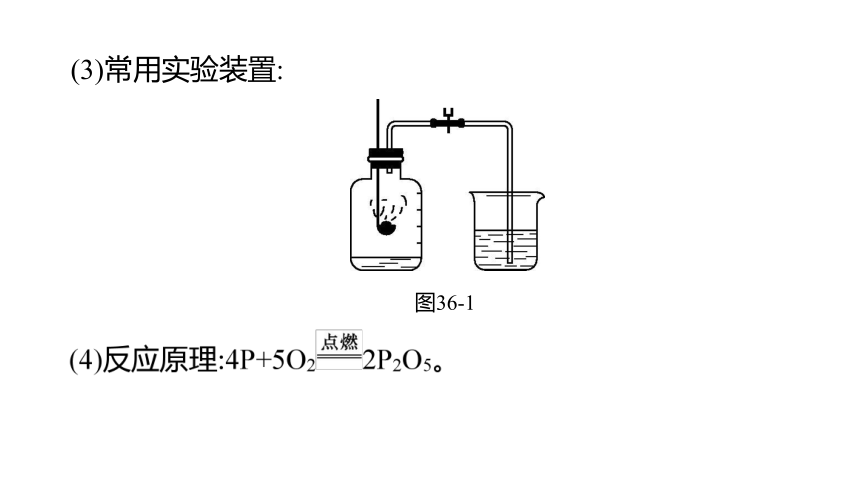
(3)常用实验装置:
图36-1
(5)实验步骤及误差分析
实验步骤 操作不当 对结果的影响 分析原因
①检查装置的气密性 装置气密性不好,反应结束后有部分空气进入集气瓶 ___________ ___________ ___________ ____________
外界空气进入
(续表)
实验步骤 操作不当 对结果的影响 分析原因
②集气瓶中加少量水,剩余容积分成5等份并标记;燃烧匙内放 的红磷 红磷的量不足 ___________ ___________ ___________ ___________
___________
用硫粉代替红磷 ___________ ____________
____________
____________
足量
瓶内氧气未
消耗完
无法测定
反应生成新的
气体,瓶内气
压变化不明显
(续表)
实验步骤 操作不当 对结果的影响 分析原因
③夹紧止水夹,点燃红磷,迅速伸入集气瓶,塞紧瓶塞 点燃红磷后燃烧匙伸入缓慢,导致瓶内部分空气逸出 ___________ ___________ ___________ ___________
___________
___________
测得氧气的
体积分数大
于
集气瓶内空
气因受热膨
胀而逸出
(续表)
实验步骤 操作不当 对结果的影响 分析原因
④火焰熄灭后,振荡集气瓶,装置______ 后打开止水夹并读数 未完全冷却即打开止水夹 ___________ ___________ ___________ ______________
______________
______________
______________
冷却
测得氧气的
体积分数小
于
集气瓶内温度偏高,气压偏大,倒吸进瓶中的水量偏少
(6)实验现象:红磷燃烧产生大量的白烟;进入集气瓶中水的体
积约占集气瓶内空气总体积的。
到室温
3.会看城市空气质量报告
(1)实时空气质量数据表:包括“空气质量指数”“空气质量等级”
“首要污染物”“对健康影响情况”“建议采取的措施”等。
(2)空气质量指数:是一种评价大气环境质量状况简单而直观的指标,指数范围为0~500,空气质量分为六个级别,指数越大,说明空气污染状况越严重。
考点1 空气的主要成分
1.[2021·台州路桥模拟]同学们正在参加适应性考试,让我们来做个深呼吸,缓和一下紧张的考试气氛。你呼出的气体中体积含量最高的是 ( )
A.氮气 B.氧气
C.二氧化碳 D.稀有气体
对点练习
A
2.用图36-2所示装置进行实验。下列现象能证明空气中O2含量的是 ( )
A.红磷燃烧,产生白烟
B.瓶中液面先下降,后上升
C.瓶中液面最终上升至1处
D.水槽中液面下降
图36-2
C
3.[2016·绍兴]下列利用空气某成分物理性质的是 ( )
A.氧气可以供给呼吸
B.氮气可以制造化肥
C.干冰用于人工降雨
D.稀有气体用作保护气
C
考点2 臭氧层、温室效应
4.下列属于温室气体的是 ( )
A.H2 B.N2
C.O2 D.CO2
D
5.[2017·舟山]臭氧是“地球卫士”,而近地面的臭氧会造成空气污染,下列说法错误的是 ( )
A.臭氧与氧气的化学性质不同
B.臭氧是空气质量指数的污染物之一
C.大量汽车尾气排放会导致臭氧污染
D.佩戴口罩能有效阻挡臭氧的吸入
D
6.[2016·湖州]最近中国科学技术大学的专家找到一种新型催化剂,可将二氧化碳转化为液体燃料甲酸,下列说法中,不正确的是( )
A.地球上二氧化碳含量上升的主要原因是植物的呼吸作用
B.二氧化碳能阻挡地面辐射,对地球有保温作用
C.二氧化碳转化为甲酸的过程属于化学变化
D.这种新型催化剂在反应前后质量不变
A
考点3 空气污染
7.下列不属于空气污染物的是 ( )
A.SO2 B.O3
C.CO2 D.PM2.5
C
8.[2020·郴州]“绿水青山就是金山银山”,保护环境就是保护我们自己。下列环境问题与其防治措施不合理的是 ( )
A.白色污染——焚烧或掩埋废弃塑料
B.温室效应——开发新能源,减少化石燃料的使用
C.酸雨——推广使用脱硫煤
D.臭氧空洞——研发新的制冷剂,减少氟利昂的使用
A
例1 [2015·杭州改编]如图36-3中甲所示为测定空气中氧气含量的装置及药品。
重点一
知道空气的主要成分和氧气、氮气在空气中的体积分数
图36-3
(1)实验原理及现象:红磷燃烧的化学方程式为____________
,主要现象是 。
图36-3
2P2O5
产生大量白烟,放出热量
(2)实验药品选择:判断下列药品能
否替代红磷,并说明理由(已知:镁条
能与空气中的氧气、二氧化碳和
氮气反应):
a.铁丝: ;
b.镁丝:__________________________________________________;
若要寻找红磷的替代物,该替代物应满足的条件是____________
(写两点)。
图36-3
不能,铁丝在空气中不能燃烧
不能,镁条与空气中的氮气、二氧化碳和氧气都能发生反应
只与空气中
的氧气发生反应,反应生成物为固体(合理即可)
(3)实验步骤:在集气瓶中加入少量水,并将水面上方空间分为5等份,接下来的实验步骤依次为 (填序号),最后打开弹簧夹。
①冷却至室温
②弹簧夹夹紧橡皮管
③点燃燃烧匙内的红磷后,
立即伸入瓶中并把塞子塞紧
图36-3
②③①
(4)实验分析:红磷熄灭后,集气瓶冷却至室温,
打开弹簧夹,水能倒吸入集气瓶中的原因是
______________________________________
,红磷必须足量的原因是_____________________________
。实验完毕,若进入集气瓶中水的体积小于瓶内空间的五分之一,可能的一种原因是__________________________________
;集气瓶内水面上升到一定高度后,不能继续上升,这种现象说明氮气具有 的性质。
红磷燃烧消耗氧气,并生成固体,使集气瓶内
压强减小
充分消耗装置内的氧气,使实验
结果更准确
未等装置冷却至室温就打开弹簧夹(合
理即可)
不燃烧也不支持燃烧,不易溶于水
(5)实验原理创新:方案①,小明用足量的木炭
代替红磷、氢氧化钠溶液代替水来做此实验。
小明操作正确,但是测得的数据小于用红磷测
得的数据,其原因是木炭燃烧除生成二氧化碳外,还可能生成 。方案②,市售“暖宝宝”中发热剂主要成分是铁粉、炭粉、水和食盐等,反应原理可简化为铁生锈。小明用配制的发热剂按图乙装置实验。他不是将足量的发热剂堆在瓶底,而是将其涂抹在广口瓶内壁的四周,目的是_____________
。在上述两个实验操作都正确的情况下,方案②实验的测量结果与空气中的氧气含量更接近,推测其更合理的主要原因是 。
CO
增大铁粉与
氧气的接触面积,加快反应
广口瓶内氧气消耗更充分
(6)实验装置创新:图36-4中的装置与图36-3装置相比,优势在哪儿
图36-4
图36-3
减少空气污染
减少空气污染
测量结果更准确
减少污染,测量结果更准确
例2 [2011·杭州]某学校科学兴趣小组想设计一个实验,来模拟研究CO2浓度增加是否增大地球“温室效应”。他们查阅了有关数据:
重点二
关注温室效应的成因、利弊和防止温室效应加剧的相关措施
CO2 空气
25 ℃,1标准大气压气体的比热 0.684 kJ/(kg·℃) 0.72 kJ/(kg·℃)
0 ℃,1标准大气压气体的密度 1.96 g/L 1.29 g/L
并设计了下面的实验和操作步骤:
Ⅰ.在两只同样的玻璃瓶里分别充满
CO2和空气,并编号为甲、乙,塞紧带
有同样温度计的橡皮塞。再把两只
玻璃瓶放在阳光下照射(如图36-5),
观察甲、乙瓶中的温度变化。
图36-5
Ⅱ.阳光持续照射,间隔一定时间测量两玻璃瓶温度值,并记录(见下表)。
时刻 9:23 9:28 9:33 9:38 9:43 9:48
甲瓶温度/℃ 13.0 19.8 23.5 26.0 26.4 27.0
乙瓶温度/℃ 13.0 19.0 22.8 25.0 26.0 26.5
时刻 9:53 9:58 10:06 10:11 10:25
甲瓶温度/℃ 27.5 27.8 28.0 28.0 28.1
乙瓶温度/℃ 27.0 27.4 27.9 28.0 28.1
(1)写出实验室制取CO2的化学方程式:
。
(2)往瓶中充CO2时,验证瓶中已充满了CO2的方法是________
。
图36-5
将燃着的
木条伸到瓶口,如果木条熄灭,则证明已充满了CO2
(3)该实验中,照射同样时间,根据上表的数据,比较甲、乙瓶温度变化的规律是______________________________________
。
时刻 9:23 9:28 9:33 9:38 9:43 9:48
甲瓶温度/℃ 13.0 19.8 23.5 26.0 26.4 27.0
乙瓶温度/℃ 13.0 19.0 22.8 25.0 26.0 26.5
时刻 9:53 9:58 10:06 10:11 10:25
甲瓶温度/℃ 27.5 27.8 28.0 28.0 28.1
乙瓶温度/℃ 27.0 27.4 27.9 28.0 28.1
开始一段时间内,甲瓶温度高于乙瓶(或甲瓶比乙瓶升温快),最后两瓶温度趋于一致
(4)该实验中,在阳光照射下,影响甲、乙
瓶温度不同的原因,除了CO2的温室效应
以外,还有的可能原因是_____________
(写出一点即可)。
(5)有同学认为根据该模拟实验的目的,实验设计存在问题,你认为是 (写出一点即可)。
图36-5
两种气体的
比热不同
该实验没有模拟地球的生态系统
【变式】[2016·杭州]大量排放以CO2为主的温室气体导致全球气候变暖已得到公认。控制大气中CO2含量刻不容缓。
(1)在自然界碳循环中,大气中CO2被消耗转化为有机物的主要途径是 。大气中部分CO2会溶解于水,导致海水酸化,其反应的化学方程式是 。
(2)科学家提出用某些溶液来吸收CO2,从而将CO2从工业尾气中“捕捉”出来。适合“捕捉”CO2的溶液有 (写出一种)。
光合作用
CO2+H2O === H2CO3
NaOH溶液
(3)一些城市在大型建筑的屋顶种植当地草类、花卉等植物,并配置相应的传感器与灌溉技术来降温,从而减少空调使用。这种“绿色屋顶”可以降温的主要原因是 。
(4)假定一台空调使用时的平均功率为2 kW,我们每天少使用空调1小时,据表计算,一个月(以30天计)可减少CO2排放 kg。
项目 使用量 CO2的排放量/kg
家庭用水/m3 1 0.93
家庭用电/(kW·h) 1 0.96
家用天然气/m3 1 2.77
植物的蒸腾作用
57.6
1.下列说法不正确的是 ( )
A.空气中N2的体积分数约为78%
B.O2的化学性质比较活泼,具有可燃性
C.二氧化碳是绿色植物进行光合作用的原料之一
D.稀有气体化学性质稳定,可用作保护气
B
2.臭氧(化学式为O3)可应用于游泳池、生活用水、污水的杀菌和消毒,大气中的臭氧层能有效阻挡紫外线。长期吸入大量臭氧会引起口干舌燥,咳嗽等不适症状。臭氧发生器是在高压电极的作用下将空气中的氧气转化为臭氧的装置。下列说法正确的是 ( )
A.氧气转化为臭氧是物理变化
B.臭氧分子的相对分子质量为36
C.一个臭氧分子中含有3个氧原子
D.臭氧对人的身体健康不利,应该拒绝使用臭氧
C
3.[2014·杭州]图36-6是北京本地PM2.5来源分布图。下列措施对减少PM2.5效果最不明显的是 ( )
A.减少汽车的保有量
B.植树造林
C.用风能与太阳能发电替代燃煤发电
D.减少工业生产中二氧化碳的排放
图36-6
D
4.[改编]利用传感器技术实时测定了
实验装置(图36-7甲)内的压强、温度
和氧气浓度的三条曲线变化趋势如
图乙所示。
(1)集气瓶中发生反应的化学方程式
为 。
图36-7
(2)该实验可以说明反应后集气瓶内
剩余的气体具有的化学性质是
。
(3)图乙中Y曲线表示的是_________
(填“温度”或“氧气的浓度”)。
(4)从图乙中哪里可以看出降至室温时
打开了弹簧夹 。
图36-7
不可燃也不支持燃烧,不与水反应
氧气的浓
度
D点之后压强突然增大
(5)从图乙中哪里可以看出集气瓶中
的氧气并没有消耗到0
____________________________
(6)图乙中AB段表示 ,
BC段气体压强变化的原因是_______
,集气瓶中的压强先增大后减小的原因是____________________________
。
Y曲线后部分纵坐标值增大
反应未开始
红磷燃
烧放热,使集气瓶内气体受热膨胀,瓶内气压增大
红磷燃烧时放热,压强增大,反应
结束冷却至室温,由于氧气被消耗,所以压强减小
图36-7
5.[2020·嘉兴]为提高测定空气中氧
气含量实验的精确度,科学兴趣小组
对课本实验进行了创新改进。
实验步骤 ①取一根玻璃管,用橡皮
塞将一端密封;
②将食品脱氧剂粉末迅速装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A。弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图36-8甲所示;
图36-8
③水平滚动玻璃管,使食品脱氧剂粉末
平铺在玻璃管中。静置至水滴不再移
动时,水滴的右端标为B,如图乙所示;
④用刻度尺测量出AO
段和AB段的长度,并计
算出AB与AO的比值,将
数据记录在表格中:
⑤洗涤、干燥实验装置,重复上述实验。
实验次数 AO/mm AB/mm AB/AO
1 523.5 109.5 0.209 2
2 525.5 110.0 0.209 3
3 527.0 110.5 0.209 7
得出结论 根据表格中的实验
数据,可知空气中氧气含量为
(用百分数表示)。
思考讨论
(1)实验步骤③中,将食品脱氧
剂粉末平铺在玻璃管中的目的
是________________________
。
20.94%
实验次数 AO/mm AB/mm AB/AO
1 523.5 109.5 0.209 2
2 525.5 110.0 0.209 3
3 527.0 110.5 0.209 7
增大与氧气的接触面积,使
氧气被脱氧剂粉末充分吸收
(2)实验步骤②中,如果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是____________________________
。
脱氧剂粉末不够紧密导致空气
柱测量值偏小
第36课时 空气
●知识体系梳理
●重难考点精讲
●当堂限时训练
知识体系
空气
空气的成分与利用
空气的污染与保护
大气环境问题
空气的污染与保护
空气污染
自净
废气
尾气
5.6
二氧化硫
氮氧化物
O3
紫外线
二氧
化碳
保温
重点梳理
1.空气(混合物)的主要成分及作用
成分 体积分数 主要作用
氧气(O2) ①供给 的重要物质
②用作 剂,用于钢铁冶炼、金属焊接等
氮气(N2) ①工业上生产硝酸和氮肥的重要原料
②氮气的化学性质 ,常用作 ,用于食品防腐保鲜、延长灯泡的使用寿命
21%
呼吸
助燃
78%
稳定
保护气
(续表)
成分 体积分数 主要作用
稀有气体( 、 、 、氡等) 0.94% ①化学性质稳定,常用作
②通电时能发出不同颜色的光,可作各种用途的
氦
氖
氩
保护气
电光源
(续表)
成分 体积分数 主要作用
二氧化碳 0.03% ①是 作用的原料
②固态CO2(俗称 )可作制冷剂,可用于
③工业上可用于制纯碱、尿素、汽水等
④可用于灭火
光合
干冰
人工降雨
2.测定空气中氧气的含量
(1)实验原理:在密闭容器内加热或燃烧某种可燃物(如点燃
),消耗容器内的 ,使密闭体系内的气压 ,在容器内外 的作用下,引起实验过程中的一些其他现象(如水倒吸),从而测出空气中氧气的含量。
(2)药品选择:常用药品为足量的 等,所选药品只能与空气中的 反应,不能和其他气体成分反应,且反应不能生成新的 。
红磷
氧气
减小
压强差
红磷
氧气
气体
(3)常用实验装置:
图36-1
(5)实验步骤及误差分析
实验步骤 操作不当 对结果的影响 分析原因
①检查装置的气密性 装置气密性不好,反应结束后有部分空气进入集气瓶 ___________ ___________ ___________ ____________
外界空气进入
(续表)
实验步骤 操作不当 对结果的影响 分析原因
②集气瓶中加少量水,剩余容积分成5等份并标记;燃烧匙内放 的红磷 红磷的量不足 ___________ ___________ ___________ ___________
___________
用硫粉代替红磷 ___________ ____________
____________
____________
足量
瓶内氧气未
消耗完
无法测定
反应生成新的
气体,瓶内气
压变化不明显
(续表)
实验步骤 操作不当 对结果的影响 分析原因
③夹紧止水夹,点燃红磷,迅速伸入集气瓶,塞紧瓶塞 点燃红磷后燃烧匙伸入缓慢,导致瓶内部分空气逸出 ___________ ___________ ___________ ___________
___________
___________
测得氧气的
体积分数大
于
集气瓶内空
气因受热膨
胀而逸出
(续表)
实验步骤 操作不当 对结果的影响 分析原因
④火焰熄灭后,振荡集气瓶,装置______ 后打开止水夹并读数 未完全冷却即打开止水夹 ___________ ___________ ___________ ______________
______________
______________
______________
冷却
测得氧气的
体积分数小
于
集气瓶内温度偏高,气压偏大,倒吸进瓶中的水量偏少
(6)实验现象:红磷燃烧产生大量的白烟;进入集气瓶中水的体
积约占集气瓶内空气总体积的。
到室温
3.会看城市空气质量报告
(1)实时空气质量数据表:包括“空气质量指数”“空气质量等级”
“首要污染物”“对健康影响情况”“建议采取的措施”等。
(2)空气质量指数:是一种评价大气环境质量状况简单而直观的指标,指数范围为0~500,空气质量分为六个级别,指数越大,说明空气污染状况越严重。
考点1 空气的主要成分
1.[2021·台州路桥模拟]同学们正在参加适应性考试,让我们来做个深呼吸,缓和一下紧张的考试气氛。你呼出的气体中体积含量最高的是 ( )
A.氮气 B.氧气
C.二氧化碳 D.稀有气体
对点练习
A
2.用图36-2所示装置进行实验。下列现象能证明空气中O2含量的是 ( )
A.红磷燃烧,产生白烟
B.瓶中液面先下降,后上升
C.瓶中液面最终上升至1处
D.水槽中液面下降
图36-2
C
3.[2016·绍兴]下列利用空气某成分物理性质的是 ( )
A.氧气可以供给呼吸
B.氮气可以制造化肥
C.干冰用于人工降雨
D.稀有气体用作保护气
C
考点2 臭氧层、温室效应
4.下列属于温室气体的是 ( )
A.H2 B.N2
C.O2 D.CO2
D
5.[2017·舟山]臭氧是“地球卫士”,而近地面的臭氧会造成空气污染,下列说法错误的是 ( )
A.臭氧与氧气的化学性质不同
B.臭氧是空气质量指数的污染物之一
C.大量汽车尾气排放会导致臭氧污染
D.佩戴口罩能有效阻挡臭氧的吸入
D
6.[2016·湖州]最近中国科学技术大学的专家找到一种新型催化剂,可将二氧化碳转化为液体燃料甲酸,下列说法中,不正确的是( )
A.地球上二氧化碳含量上升的主要原因是植物的呼吸作用
B.二氧化碳能阻挡地面辐射,对地球有保温作用
C.二氧化碳转化为甲酸的过程属于化学变化
D.这种新型催化剂在反应前后质量不变
A
考点3 空气污染
7.下列不属于空气污染物的是 ( )
A.SO2 B.O3
C.CO2 D.PM2.5
C
8.[2020·郴州]“绿水青山就是金山银山”,保护环境就是保护我们自己。下列环境问题与其防治措施不合理的是 ( )
A.白色污染——焚烧或掩埋废弃塑料
B.温室效应——开发新能源,减少化石燃料的使用
C.酸雨——推广使用脱硫煤
D.臭氧空洞——研发新的制冷剂,减少氟利昂的使用
A
例1 [2015·杭州改编]如图36-3中甲所示为测定空气中氧气含量的装置及药品。
重点一
知道空气的主要成分和氧气、氮气在空气中的体积分数
图36-3
(1)实验原理及现象:红磷燃烧的化学方程式为____________
,主要现象是 。
图36-3
2P2O5
产生大量白烟,放出热量
(2)实验药品选择:判断下列药品能
否替代红磷,并说明理由(已知:镁条
能与空气中的氧气、二氧化碳和
氮气反应):
a.铁丝: ;
b.镁丝:__________________________________________________;
若要寻找红磷的替代物,该替代物应满足的条件是____________
(写两点)。
图36-3
不能,铁丝在空气中不能燃烧
不能,镁条与空气中的氮气、二氧化碳和氧气都能发生反应
只与空气中
的氧气发生反应,反应生成物为固体(合理即可)
(3)实验步骤:在集气瓶中加入少量水,并将水面上方空间分为5等份,接下来的实验步骤依次为 (填序号),最后打开弹簧夹。
①冷却至室温
②弹簧夹夹紧橡皮管
③点燃燃烧匙内的红磷后,
立即伸入瓶中并把塞子塞紧
图36-3
②③①
(4)实验分析:红磷熄灭后,集气瓶冷却至室温,
打开弹簧夹,水能倒吸入集气瓶中的原因是
______________________________________
,红磷必须足量的原因是_____________________________
。实验完毕,若进入集气瓶中水的体积小于瓶内空间的五分之一,可能的一种原因是__________________________________
;集气瓶内水面上升到一定高度后,不能继续上升,这种现象说明氮气具有 的性质。
红磷燃烧消耗氧气,并生成固体,使集气瓶内
压强减小
充分消耗装置内的氧气,使实验
结果更准确
未等装置冷却至室温就打开弹簧夹(合
理即可)
不燃烧也不支持燃烧,不易溶于水
(5)实验原理创新:方案①,小明用足量的木炭
代替红磷、氢氧化钠溶液代替水来做此实验。
小明操作正确,但是测得的数据小于用红磷测
得的数据,其原因是木炭燃烧除生成二氧化碳外,还可能生成 。方案②,市售“暖宝宝”中发热剂主要成分是铁粉、炭粉、水和食盐等,反应原理可简化为铁生锈。小明用配制的发热剂按图乙装置实验。他不是将足量的发热剂堆在瓶底,而是将其涂抹在广口瓶内壁的四周,目的是_____________
。在上述两个实验操作都正确的情况下,方案②实验的测量结果与空气中的氧气含量更接近,推测其更合理的主要原因是 。
CO
增大铁粉与
氧气的接触面积,加快反应
广口瓶内氧气消耗更充分
(6)实验装置创新:图36-4中的装置与图36-3装置相比,优势在哪儿
图36-4
图36-3
减少空气污染
减少空气污染
测量结果更准确
减少污染,测量结果更准确
例2 [2011·杭州]某学校科学兴趣小组想设计一个实验,来模拟研究CO2浓度增加是否增大地球“温室效应”。他们查阅了有关数据:
重点二
关注温室效应的成因、利弊和防止温室效应加剧的相关措施
CO2 空气
25 ℃,1标准大气压气体的比热 0.684 kJ/(kg·℃) 0.72 kJ/(kg·℃)
0 ℃,1标准大气压气体的密度 1.96 g/L 1.29 g/L
并设计了下面的实验和操作步骤:
Ⅰ.在两只同样的玻璃瓶里分别充满
CO2和空气,并编号为甲、乙,塞紧带
有同样温度计的橡皮塞。再把两只
玻璃瓶放在阳光下照射(如图36-5),
观察甲、乙瓶中的温度变化。
图36-5
Ⅱ.阳光持续照射,间隔一定时间测量两玻璃瓶温度值,并记录(见下表)。
时刻 9:23 9:28 9:33 9:38 9:43 9:48
甲瓶温度/℃ 13.0 19.8 23.5 26.0 26.4 27.0
乙瓶温度/℃ 13.0 19.0 22.8 25.0 26.0 26.5
时刻 9:53 9:58 10:06 10:11 10:25
甲瓶温度/℃ 27.5 27.8 28.0 28.0 28.1
乙瓶温度/℃ 27.0 27.4 27.9 28.0 28.1
(1)写出实验室制取CO2的化学方程式:
。
(2)往瓶中充CO2时,验证瓶中已充满了CO2的方法是________
。
图36-5
将燃着的
木条伸到瓶口,如果木条熄灭,则证明已充满了CO2
(3)该实验中,照射同样时间,根据上表的数据,比较甲、乙瓶温度变化的规律是______________________________________
。
时刻 9:23 9:28 9:33 9:38 9:43 9:48
甲瓶温度/℃ 13.0 19.8 23.5 26.0 26.4 27.0
乙瓶温度/℃ 13.0 19.0 22.8 25.0 26.0 26.5
时刻 9:53 9:58 10:06 10:11 10:25
甲瓶温度/℃ 27.5 27.8 28.0 28.0 28.1
乙瓶温度/℃ 27.0 27.4 27.9 28.0 28.1
开始一段时间内,甲瓶温度高于乙瓶(或甲瓶比乙瓶升温快),最后两瓶温度趋于一致
(4)该实验中,在阳光照射下,影响甲、乙
瓶温度不同的原因,除了CO2的温室效应
以外,还有的可能原因是_____________
(写出一点即可)。
(5)有同学认为根据该模拟实验的目的,实验设计存在问题,你认为是 (写出一点即可)。
图36-5
两种气体的
比热不同
该实验没有模拟地球的生态系统
【变式】[2016·杭州]大量排放以CO2为主的温室气体导致全球气候变暖已得到公认。控制大气中CO2含量刻不容缓。
(1)在自然界碳循环中,大气中CO2被消耗转化为有机物的主要途径是 。大气中部分CO2会溶解于水,导致海水酸化,其反应的化学方程式是 。
(2)科学家提出用某些溶液来吸收CO2,从而将CO2从工业尾气中“捕捉”出来。适合“捕捉”CO2的溶液有 (写出一种)。
光合作用
CO2+H2O === H2CO3
NaOH溶液
(3)一些城市在大型建筑的屋顶种植当地草类、花卉等植物,并配置相应的传感器与灌溉技术来降温,从而减少空调使用。这种“绿色屋顶”可以降温的主要原因是 。
(4)假定一台空调使用时的平均功率为2 kW,我们每天少使用空调1小时,据表计算,一个月(以30天计)可减少CO2排放 kg。
项目 使用量 CO2的排放量/kg
家庭用水/m3 1 0.93
家庭用电/(kW·h) 1 0.96
家用天然气/m3 1 2.77
植物的蒸腾作用
57.6
1.下列说法不正确的是 ( )
A.空气中N2的体积分数约为78%
B.O2的化学性质比较活泼,具有可燃性
C.二氧化碳是绿色植物进行光合作用的原料之一
D.稀有气体化学性质稳定,可用作保护气
B
2.臭氧(化学式为O3)可应用于游泳池、生活用水、污水的杀菌和消毒,大气中的臭氧层能有效阻挡紫外线。长期吸入大量臭氧会引起口干舌燥,咳嗽等不适症状。臭氧发生器是在高压电极的作用下将空气中的氧气转化为臭氧的装置。下列说法正确的是 ( )
A.氧气转化为臭氧是物理变化
B.臭氧分子的相对分子质量为36
C.一个臭氧分子中含有3个氧原子
D.臭氧对人的身体健康不利,应该拒绝使用臭氧
C
3.[2014·杭州]图36-6是北京本地PM2.5来源分布图。下列措施对减少PM2.5效果最不明显的是 ( )
A.减少汽车的保有量
B.植树造林
C.用风能与太阳能发电替代燃煤发电
D.减少工业生产中二氧化碳的排放
图36-6
D
4.[改编]利用传感器技术实时测定了
实验装置(图36-7甲)内的压强、温度
和氧气浓度的三条曲线变化趋势如
图乙所示。
(1)集气瓶中发生反应的化学方程式
为 。
图36-7
(2)该实验可以说明反应后集气瓶内
剩余的气体具有的化学性质是
。
(3)图乙中Y曲线表示的是_________
(填“温度”或“氧气的浓度”)。
(4)从图乙中哪里可以看出降至室温时
打开了弹簧夹 。
图36-7
不可燃也不支持燃烧,不与水反应
氧气的浓
度
D点之后压强突然增大
(5)从图乙中哪里可以看出集气瓶中
的氧气并没有消耗到0
____________________________
(6)图乙中AB段表示 ,
BC段气体压强变化的原因是_______
,集气瓶中的压强先增大后减小的原因是____________________________
。
Y曲线后部分纵坐标值增大
反应未开始
红磷燃
烧放热,使集气瓶内气体受热膨胀,瓶内气压增大
红磷燃烧时放热,压强增大,反应
结束冷却至室温,由于氧气被消耗,所以压强减小
图36-7
5.[2020·嘉兴]为提高测定空气中氧
气含量实验的精确度,科学兴趣小组
对课本实验进行了创新改进。
实验步骤 ①取一根玻璃管,用橡皮
塞将一端密封;
②将食品脱氧剂粉末迅速装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A。弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图36-8甲所示;
图36-8
③水平滚动玻璃管,使食品脱氧剂粉末
平铺在玻璃管中。静置至水滴不再移
动时,水滴的右端标为B,如图乙所示;
④用刻度尺测量出AO
段和AB段的长度,并计
算出AB与AO的比值,将
数据记录在表格中:
⑤洗涤、干燥实验装置,重复上述实验。
实验次数 AO/mm AB/mm AB/AO
1 523.5 109.5 0.209 2
2 525.5 110.0 0.209 3
3 527.0 110.5 0.209 7
得出结论 根据表格中的实验
数据,可知空气中氧气含量为
(用百分数表示)。
思考讨论
(1)实验步骤③中,将食品脱氧
剂粉末平铺在玻璃管中的目的
是________________________
。
20.94%
实验次数 AO/mm AB/mm AB/AO
1 523.5 109.5 0.209 2
2 525.5 110.0 0.209 3
3 527.0 110.5 0.209 7
增大与氧气的接触面积,使
氧气被脱氧剂粉末充分吸收
(2)实验步骤②中,如果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是____________________________
。
脱氧剂粉末不够紧密导致空气
柱测量值偏小
同课章节目录
