2022年浙江省中考科学一轮复习 第42课时 物质的变化和性质(课件 44张PPT)
文档属性
| 名称 | 2022年浙江省中考科学一轮复习 第42课时 物质的变化和性质(课件 44张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 699.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-11 00:00:00 | ||
图片预览







文档简介
(共44张PPT)
第42课时 物质的变化和性质
●知识体系梳理
●重难考点精讲
●当堂限时训练
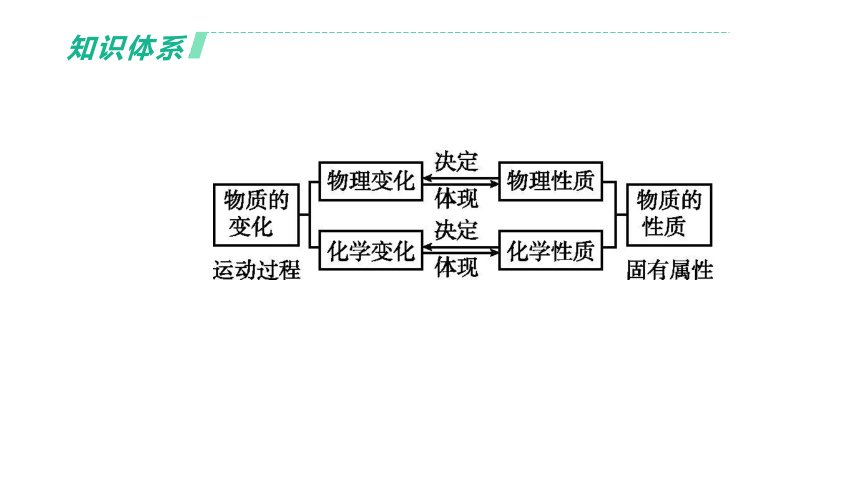
知识体系
重点梳理
1.物质的物理变化和化学变化
物理变化 化学变化
概念 的变化 ____________生成的变化
现象 通常在外形、状态等方面发生改变 常伴随发光、放热、颜色变化、生成气体、产生沉淀等现象
没有生成新物质
有新物质
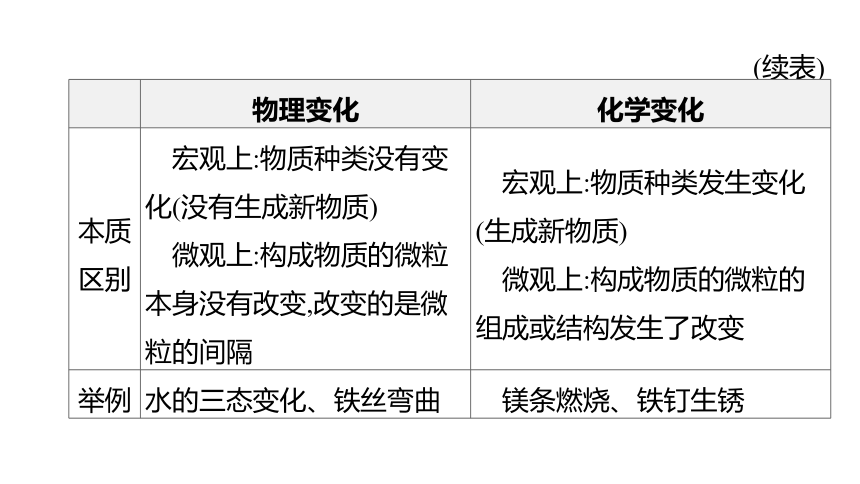
(续表)
物理变化 化学变化
本质 区别 宏观上:物质种类没有变化(没有生成新物质) 微观上:构成物质的微粒本身没有改变,改变的是微粒的间隔 宏观上:物质种类发生变化
(生成新物质)
微观上:构成物质的微粒的组成或结构发生了改变
举例 水的三态变化、铁丝弯曲 镁条燃烧、铁钉生锈
(续表)
物理变化 化学变化
联系 化学变化和物理变化往往同时发生。化学变化过程中 (填“一定”或“不一定”)同时发生物理变化;物理变化过程中不一定同时发生化学变化
一定
2.物质主要的物理性质和化学性质
物理性质 化学性质
定义 物质 发生化学变化就表现出来的性质 物质在 中表现出来的性质
举例 如颜色、状态、气味、密度、熔点、沸点、比热容、硬度、溶解性、挥发性、延展性、吸附性、导电性、导热性、磁性等 如助燃性、可燃性、稳定性、氧化性、还原性、酸碱性、毒性等
不需要
化学变化
(续表)
物理性质 化学性质
根本 区别 物质的性质是否需要通过 表现出来
影响 因素 外界条件能影响物质的性质,如温度影响物质的溶解度,压强影响物质的沸点
化学变化
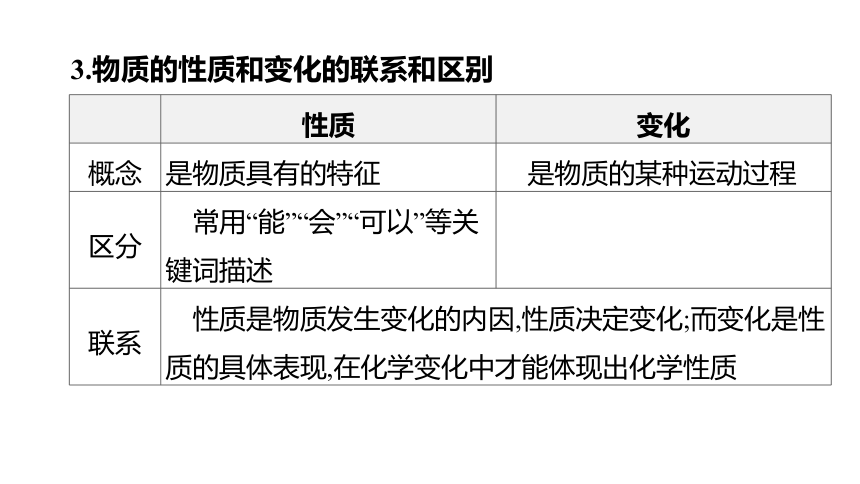
3.物质的性质和变化的联系和区别
性质 变化
概念 是物质具有的特征 是物质的某种运动过程
区分 常用“能”“会”“可以”等关键词描述
联系 性质是物质发生变化的内因,性质决定变化;而变化是性质的具体表现,在化学变化中才能体现出化学性质
4.氧化反应及氧气的氧化性
(1)物质与氧(包括氧气和含氧化合物)发生的反应,属于
反应。
(2)在氧化反应中,氧气是氧化剂,具有 性。
氧化
氧化
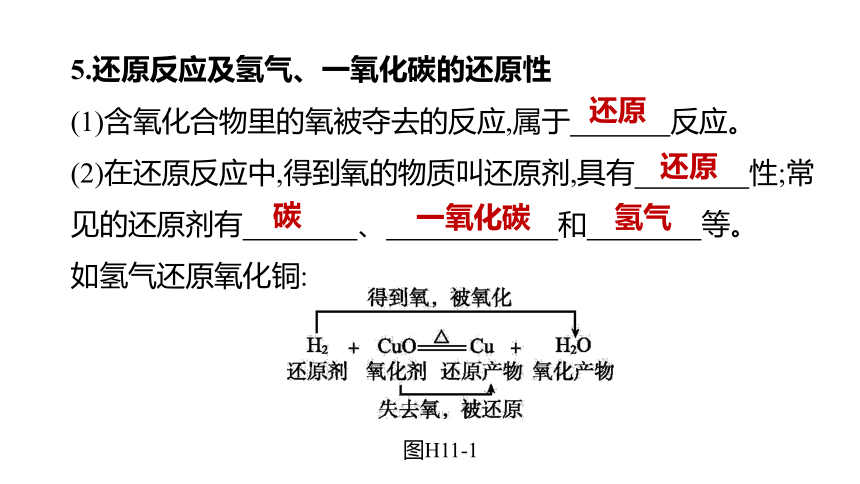
5.还原反应及氢气、一氧化碳的还原性
(1)含氧化合物里的氧被夺去的反应,属于 反应。
(2)在还原反应中,得到氧的物质叫还原剂,具有 性;常见的还原剂有 、 和 等。
如氢气还原氧化铜:
图H11-1
还原
还原
碳
一氧化碳
氢气
如炼铁的原理:Fe2O3+3CO 2Fe+3CO2。其中Fe2O3是
剂,具有 性;CO是 剂,具有 性。
氧化
氧化
还原
还原
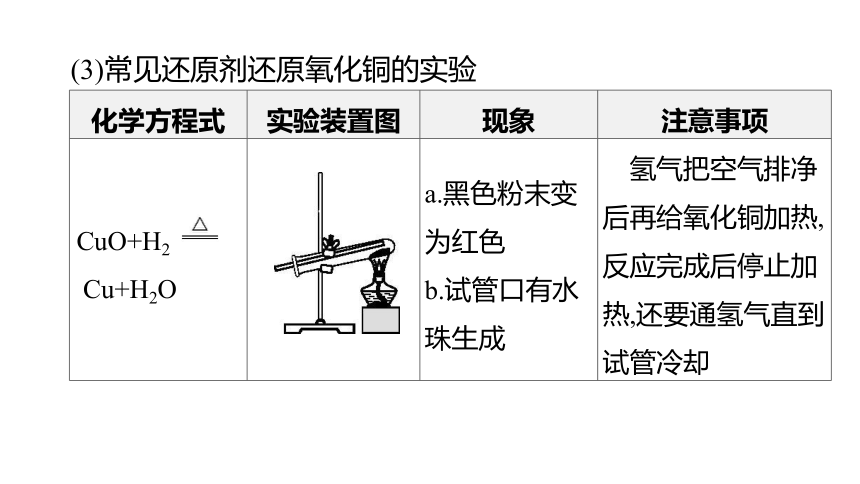
(3)常见还原剂还原氧化铜的实验
化学方程式 实验装置图 现象 注意事项
CuO+H2 Cu+H2O a.黑色粉末变为红色 b.试管口有水珠生成 氢气把空气排净后再给氧化铜加热,反应完成后停止加热,还要通氢气直到试管冷却
(续表)
化学方程式 实验装置图 现象 注意事项
CuO+CO Cu+CO2 a.黑色粉末变为红色 b.生成的气体使澄清石灰水变浑浊 CO有毒,因此尾气不能大量排向大气中,可点燃处理
(续表)
化学方程式 实验装置图 现象 注意事项
2CuO+C 2Cu+CO2↑ a.黑色粉末变为红色 b.生成的气体使澄清石灰水变浑浊
6.氢气和一氧化碳的可燃性及鉴别
(1)氢气和一氧化碳具有可燃性,点燃它们之前,需要进行
。
(2)根据燃烧产物来鉴别氢气和一氧化碳
物质 操作 现象
氢气 干冷的烧杯内壁出现水珠,倒置烧杯,注入澄清石灰水振荡后,石灰水不变浑浊
一氧 化碳 烧杯内壁无水珠出现,倒置烧杯,注入澄清石灰水振荡后,石灰水变浑浊
验纯
(3)可以利用氢气和一氧化碳还原金属氧化物,然后通过鉴别产物对它们进行区分。
考点1 物质的物理变化和化学变化
1.人们通过化学变化改造物质世界,并实现物质与能量的相互转化。化学变化中生成的新物质是指 ( )
A.分子分成原子,生成新的元素
B.原子重新组合,生成新的原子
C.生成了组成或结构与原物质不同的物质
D.生成了组成和结构与原物质相同的物质
对点练习
C
2.[2021·金华]金华酒传统酿造技艺、浦江剪纸、永康锡雕、东阳竹编等,是金华拥有的众多国家级非物质文化遗产的典型代表。下列非物质文化遗产制作过程,主要利用化学变化的是 ( )
图42-2
A
考点2 物质主要的物理性质和化学性质
3.[2021·杭州滨江期末]物质的性质在很大程度上决定了物质的用途,物质的用途体现了物质的性质。下列物质的用途主要体现了物质化学性质的是 ( )
A.氧气用于新冠病人急救
B.干冰用于人工降雨
C.钢水用于工件的铸造
D.钨丝用于制作灯泡灯丝
A
考点3 氧气的氧化性以及氢气、一氧化碳的还原性和可燃性
4.[2021·湖州]工业炼铁的部分
反应如图42-3所示,则下列说
法正确的是( )
A.X可以是木炭 B.X与CO都具有氧化性
C.③反应后的尾气可直接排放 D.Y中铁元素以游离态存在
A
图42-3
5. [2021·杭州]小金为了探究氧化铜与氢气的
反应和反应产物,用如图42-4所示装置进行
实验。注射器内装满氢气,并将注射器针头扎
入橡皮塞中。将少许氧化铜粉末送入长柄U形
石英玻璃管内并平铺于管底。将少量白色的
无水硫酸铜粉末送入长柄U形石英玻璃管中并平铺于直管中部。然后将一个气球套在长柄U形石英玻璃管的直管出口处,连接好整个实验装置(装置气密性良好)……
图42-4
(1)为确保实验安全,在点燃酒精灯加热前的
操作是_______________________________
。
(2)装置末端连接的气球的作用是
。
(3)实验过程中,当观察到 现象时可判断一定有水生成。
图42-4
向下推动注射器活塞,直至刻度从
200 mL变成170 mL
收集氢气,防止空气中的水和氧气进入
无水硫酸铜由白色变为蓝色
(4)实验开始时加入a g纯氧化铜粉末,实验结
束后取出长柄U形石英玻璃管底的固体称量
为b g,当b为 (用含有a式子表示)时,
可判断氧化铜已完全转化为铜。
图42-4
0.8a
6.某化学兴趣小组利用如图
42-5所示装置进行实验,探
究工业炼铁的化学原理,试按
要求回答下列问题。
(1)硬质玻璃管中观察到的现象是 ,写出一氧化碳和氧化铁反应的化学方程式:
。
图42-5
红色固体变为黑色
(2)实验时首先通入一氧化碳的目的是____________________
。
(3)装置中导管末端放置点燃的酒精灯的目的是____________
。
图42-5
排尽玻璃管内的空气,
防止加热时发生爆炸
除去多余的
CO,防止污染空气
例1 充有钠蒸气的高压钠灯发出的黄光射程远,
透雾能力强,常用于道路和广场的照明。钠的化
学性质活泼,常温下可以与氧气、水反应,在实验
室里,金属钠保存在煤油中,用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入盛有水(滴有酚酞试液)的烧杯中,发现钠块浮在水面上,很快熔化成银白色小球,四处游动,发出嘶嘶的响声,偶有火星出现,溶液变成红色。依据提供的信息,回答下列问题。
重点一
区别和辨认物理变化和化学变化、物理性质和化学性质
图42-6
(1)“钠保存在煤油中”说明钠具有的化学性质是 。
(2)“钠块浮在水面上”说明钠具有的物理性质是 。
(3)“溶液变成红色”说明钠与水反应的生成物中含有 性的物质。
(4)根据所学知识解释钠“熔化成银白色小球”的原因是
。
图42-6
常温下可以与氧气、水反应
钠的密度比水的密度小
碱
钠的熔点低
例2 [2017·杭州]小金利用图42-7所示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略)。
重点二
能说明氧气的氧化性和氢气、一氧化碳具有还原性
图42-7
步骤 操作 甲组现象 乙组现象
1 称量黑色粉末质量/g m1 m2
2 取黑色粉末,用磁铁 吸引 能被吸引 能被吸引
3 取黑色粉末,加入 稀盐酸 全部溶解, 有大量气泡 无明显现象
4 取黑色粉末,加入 足量CuSO4溶液 有红色物质生成 无明显现象
(1)从实验安全角度考虑,图示装置还应采取的改进措施是
。
图H11-7
在装置末端尖嘴导管处,放置一盏燃着的酒精灯
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
①甲组的黑色粉末与稀盐酸反应的化学方程式是__________________
。
步骤 操作 甲组现象 乙组现象
1 称量黑色粉末质量/g m1 m2
2 取黑色粉末,用磁铁吸引 能被吸引 能被吸引
3 取黑色粉末,加入稀盐酸 全部溶解, 有大量气泡 无明显现象
4 取黑色粉末,加入足量CuSO4溶液 有红色物质生成 无明显现象
Fe+2HCl === FeCl2
+H2↑
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。他又发现m2恰好为
g,这可成为支持上述猜想的新证据。
(3)甲、乙两组实验说明温度对CO和Fe2O3反应有影响,且均体现出CO的 (填写化学性质)。
4.64
还原性和可燃性
例3 某混合气体可能含有CO、H2、CO2、H2O(气)中的一种或几种。为验证其组成,同学们进行实验的装置和现象如图42-8所示(夹持仪器已省略,假设气体均吸收完全)。
重点三
氢气、一氧化碳等气体的鉴别
图42-8
结论 甲 乙 丙
含有CO、H2、H2O(气) 含有CO、H2、CO2 含有CO、H2、H2O(气)、CO2
(1)仪器a的名称是 。
锥形瓶
(2)装置D中溶液变浑浊的化学方程式是__________________
。点燃尾气,火焰呈 色。
CO2+Ca(OH)2 ===
CaCO3↓+H2O
蓝
(3)丁认为,由于他们对装置
(填序号)中的实验现象
分析不同而导致结论有差异。
根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的。请写出丁的实验操作过程与现象:_____________________________________________
。
结论 甲 乙 丙
含有CO、H2、H2O(气) 含有CO、H2、CO2 含有CO、H2、H2O
(气)、CO2
A
将A中固体取出,加入烧杯(或试管)中,加入过量稀盐
酸,无明显现象
1.镓是银白色金属,放在掌心会迅速变成液态,密度略大于铝,在空气中表面易氧化形成氧化膜。其中属于镓的化学性质的是 ( )
A.能被氧化 B.银白色
C.熔点低 D.密度较小
A
2.下列质量增加的变化有一种与其他三种存在本质的区别,这种变化是 ( )
A.长期放置在空气中的氢氧化钠质量增加
B.长期敞口放置的浓硫酸质量增加
C.久置的生石灰质量增加
D.久置的铁钉生锈质量增加
B
3.关于木炭、一氧化碳、氢气分别与氧化铜的反应,下列说法错误的是 ( )
A.都有红色物质生成
B.都有还原剂参加反应
C.都是置换反应
D.反应都需要加热或高温
C
4.[2018·杭州]图42-9为氢气还原氧化铜的实验
装置图。下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于
通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
图42-9
B
5.图42-10中甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验。
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是
性。
图42-10
还原
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先 ,后 ,否则生成的红色的铜会变成黑色。
图H11-10
移走酒精灯
停止通氢气
(3)某同学按正确操作做完乙实
验后,发现澄清石灰水变浑浊,
试管中粉末全部变为黑色,取少
量黑色粉末,加入足量稀硫酸充
分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
图H11-10
铁(或Fe)
(4)查阅资料,得到关于铁的氧化物的如下信息:
铁的氧化物化学式 Fe2O3 Fe3O4 FeO
颜色 红 黑 黑
化学性质 可溶于酸 常温下不溶于稀酸 可溶于酸
根据以上信息,试写出乙实验试管中反应的化学方程式:
。
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。
第42课时 物质的变化和性质
●知识体系梳理
●重难考点精讲
●当堂限时训练
知识体系
重点梳理
1.物质的物理变化和化学变化
物理变化 化学变化
概念 的变化 ____________生成的变化
现象 通常在外形、状态等方面发生改变 常伴随发光、放热、颜色变化、生成气体、产生沉淀等现象
没有生成新物质
有新物质
(续表)
物理变化 化学变化
本质 区别 宏观上:物质种类没有变化(没有生成新物质) 微观上:构成物质的微粒本身没有改变,改变的是微粒的间隔 宏观上:物质种类发生变化
(生成新物质)
微观上:构成物质的微粒的组成或结构发生了改变
举例 水的三态变化、铁丝弯曲 镁条燃烧、铁钉生锈
(续表)
物理变化 化学变化
联系 化学变化和物理变化往往同时发生。化学变化过程中 (填“一定”或“不一定”)同时发生物理变化;物理变化过程中不一定同时发生化学变化
一定
2.物质主要的物理性质和化学性质
物理性质 化学性质
定义 物质 发生化学变化就表现出来的性质 物质在 中表现出来的性质
举例 如颜色、状态、气味、密度、熔点、沸点、比热容、硬度、溶解性、挥发性、延展性、吸附性、导电性、导热性、磁性等 如助燃性、可燃性、稳定性、氧化性、还原性、酸碱性、毒性等
不需要
化学变化
(续表)
物理性质 化学性质
根本 区别 物质的性质是否需要通过 表现出来
影响 因素 外界条件能影响物质的性质,如温度影响物质的溶解度,压强影响物质的沸点
化学变化
3.物质的性质和变化的联系和区别
性质 变化
概念 是物质具有的特征 是物质的某种运动过程
区分 常用“能”“会”“可以”等关键词描述
联系 性质是物质发生变化的内因,性质决定变化;而变化是性质的具体表现,在化学变化中才能体现出化学性质
4.氧化反应及氧气的氧化性
(1)物质与氧(包括氧气和含氧化合物)发生的反应,属于
反应。
(2)在氧化反应中,氧气是氧化剂,具有 性。
氧化
氧化
5.还原反应及氢气、一氧化碳的还原性
(1)含氧化合物里的氧被夺去的反应,属于 反应。
(2)在还原反应中,得到氧的物质叫还原剂,具有 性;常见的还原剂有 、 和 等。
如氢气还原氧化铜:
图H11-1
还原
还原
碳
一氧化碳
氢气
如炼铁的原理:Fe2O3+3CO 2Fe+3CO2。其中Fe2O3是
剂,具有 性;CO是 剂,具有 性。
氧化
氧化
还原
还原
(3)常见还原剂还原氧化铜的实验
化学方程式 实验装置图 现象 注意事项
CuO+H2 Cu+H2O a.黑色粉末变为红色 b.试管口有水珠生成 氢气把空气排净后再给氧化铜加热,反应完成后停止加热,还要通氢气直到试管冷却
(续表)
化学方程式 实验装置图 现象 注意事项
CuO+CO Cu+CO2 a.黑色粉末变为红色 b.生成的气体使澄清石灰水变浑浊 CO有毒,因此尾气不能大量排向大气中,可点燃处理
(续表)
化学方程式 实验装置图 现象 注意事项
2CuO+C 2Cu+CO2↑ a.黑色粉末变为红色 b.生成的气体使澄清石灰水变浑浊
6.氢气和一氧化碳的可燃性及鉴别
(1)氢气和一氧化碳具有可燃性,点燃它们之前,需要进行
。
(2)根据燃烧产物来鉴别氢气和一氧化碳
物质 操作 现象
氢气 干冷的烧杯内壁出现水珠,倒置烧杯,注入澄清石灰水振荡后,石灰水不变浑浊
一氧 化碳 烧杯内壁无水珠出现,倒置烧杯,注入澄清石灰水振荡后,石灰水变浑浊
验纯
(3)可以利用氢气和一氧化碳还原金属氧化物,然后通过鉴别产物对它们进行区分。
考点1 物质的物理变化和化学变化
1.人们通过化学变化改造物质世界,并实现物质与能量的相互转化。化学变化中生成的新物质是指 ( )
A.分子分成原子,生成新的元素
B.原子重新组合,生成新的原子
C.生成了组成或结构与原物质不同的物质
D.生成了组成和结构与原物质相同的物质
对点练习
C
2.[2021·金华]金华酒传统酿造技艺、浦江剪纸、永康锡雕、东阳竹编等,是金华拥有的众多国家级非物质文化遗产的典型代表。下列非物质文化遗产制作过程,主要利用化学变化的是 ( )
图42-2
A
考点2 物质主要的物理性质和化学性质
3.[2021·杭州滨江期末]物质的性质在很大程度上决定了物质的用途,物质的用途体现了物质的性质。下列物质的用途主要体现了物质化学性质的是 ( )
A.氧气用于新冠病人急救
B.干冰用于人工降雨
C.钢水用于工件的铸造
D.钨丝用于制作灯泡灯丝
A
考点3 氧气的氧化性以及氢气、一氧化碳的还原性和可燃性
4.[2021·湖州]工业炼铁的部分
反应如图42-3所示,则下列说
法正确的是( )
A.X可以是木炭 B.X与CO都具有氧化性
C.③反应后的尾气可直接排放 D.Y中铁元素以游离态存在
A
图42-3
5. [2021·杭州]小金为了探究氧化铜与氢气的
反应和反应产物,用如图42-4所示装置进行
实验。注射器内装满氢气,并将注射器针头扎
入橡皮塞中。将少许氧化铜粉末送入长柄U形
石英玻璃管内并平铺于管底。将少量白色的
无水硫酸铜粉末送入长柄U形石英玻璃管中并平铺于直管中部。然后将一个气球套在长柄U形石英玻璃管的直管出口处,连接好整个实验装置(装置气密性良好)……
图42-4
(1)为确保实验安全,在点燃酒精灯加热前的
操作是_______________________________
。
(2)装置末端连接的气球的作用是
。
(3)实验过程中,当观察到 现象时可判断一定有水生成。
图42-4
向下推动注射器活塞,直至刻度从
200 mL变成170 mL
收集氢气,防止空气中的水和氧气进入
无水硫酸铜由白色变为蓝色
(4)实验开始时加入a g纯氧化铜粉末,实验结
束后取出长柄U形石英玻璃管底的固体称量
为b g,当b为 (用含有a式子表示)时,
可判断氧化铜已完全转化为铜。
图42-4
0.8a
6.某化学兴趣小组利用如图
42-5所示装置进行实验,探
究工业炼铁的化学原理,试按
要求回答下列问题。
(1)硬质玻璃管中观察到的现象是 ,写出一氧化碳和氧化铁反应的化学方程式:
。
图42-5
红色固体变为黑色
(2)实验时首先通入一氧化碳的目的是____________________
。
(3)装置中导管末端放置点燃的酒精灯的目的是____________
。
图42-5
排尽玻璃管内的空气,
防止加热时发生爆炸
除去多余的
CO,防止污染空气
例1 充有钠蒸气的高压钠灯发出的黄光射程远,
透雾能力强,常用于道路和广场的照明。钠的化
学性质活泼,常温下可以与氧气、水反应,在实验
室里,金属钠保存在煤油中,用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入盛有水(滴有酚酞试液)的烧杯中,发现钠块浮在水面上,很快熔化成银白色小球,四处游动,发出嘶嘶的响声,偶有火星出现,溶液变成红色。依据提供的信息,回答下列问题。
重点一
区别和辨认物理变化和化学变化、物理性质和化学性质
图42-6
(1)“钠保存在煤油中”说明钠具有的化学性质是 。
(2)“钠块浮在水面上”说明钠具有的物理性质是 。
(3)“溶液变成红色”说明钠与水反应的生成物中含有 性的物质。
(4)根据所学知识解释钠“熔化成银白色小球”的原因是
。
图42-6
常温下可以与氧气、水反应
钠的密度比水的密度小
碱
钠的熔点低
例2 [2017·杭州]小金利用图42-7所示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略)。
重点二
能说明氧气的氧化性和氢气、一氧化碳具有还原性
图42-7
步骤 操作 甲组现象 乙组现象
1 称量黑色粉末质量/g m1 m2
2 取黑色粉末,用磁铁 吸引 能被吸引 能被吸引
3 取黑色粉末,加入 稀盐酸 全部溶解, 有大量气泡 无明显现象
4 取黑色粉末,加入 足量CuSO4溶液 有红色物质生成 无明显现象
(1)从实验安全角度考虑,图示装置还应采取的改进措施是
。
图H11-7
在装置末端尖嘴导管处,放置一盏燃着的酒精灯
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
①甲组的黑色粉末与稀盐酸反应的化学方程式是__________________
。
步骤 操作 甲组现象 乙组现象
1 称量黑色粉末质量/g m1 m2
2 取黑色粉末,用磁铁吸引 能被吸引 能被吸引
3 取黑色粉末,加入稀盐酸 全部溶解, 有大量气泡 无明显现象
4 取黑色粉末,加入足量CuSO4溶液 有红色物质生成 无明显现象
Fe+2HCl === FeCl2
+H2↑
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。他又发现m2恰好为
g,这可成为支持上述猜想的新证据。
(3)甲、乙两组实验说明温度对CO和Fe2O3反应有影响,且均体现出CO的 (填写化学性质)。
4.64
还原性和可燃性
例3 某混合气体可能含有CO、H2、CO2、H2O(气)中的一种或几种。为验证其组成,同学们进行实验的装置和现象如图42-8所示(夹持仪器已省略,假设气体均吸收完全)。
重点三
氢气、一氧化碳等气体的鉴别
图42-8
结论 甲 乙 丙
含有CO、H2、H2O(气) 含有CO、H2、CO2 含有CO、H2、H2O(气)、CO2
(1)仪器a的名称是 。
锥形瓶
(2)装置D中溶液变浑浊的化学方程式是__________________
。点燃尾气,火焰呈 色。
CO2+Ca(OH)2 ===
CaCO3↓+H2O
蓝
(3)丁认为,由于他们对装置
(填序号)中的实验现象
分析不同而导致结论有差异。
根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的。请写出丁的实验操作过程与现象:_____________________________________________
。
结论 甲 乙 丙
含有CO、H2、H2O(气) 含有CO、H2、CO2 含有CO、H2、H2O
(气)、CO2
A
将A中固体取出,加入烧杯(或试管)中,加入过量稀盐
酸,无明显现象
1.镓是银白色金属,放在掌心会迅速变成液态,密度略大于铝,在空气中表面易氧化形成氧化膜。其中属于镓的化学性质的是 ( )
A.能被氧化 B.银白色
C.熔点低 D.密度较小
A
2.下列质量增加的变化有一种与其他三种存在本质的区别,这种变化是 ( )
A.长期放置在空气中的氢氧化钠质量增加
B.长期敞口放置的浓硫酸质量增加
C.久置的生石灰质量增加
D.久置的铁钉生锈质量增加
B
3.关于木炭、一氧化碳、氢气分别与氧化铜的反应,下列说法错误的是 ( )
A.都有红色物质生成
B.都有还原剂参加反应
C.都是置换反应
D.反应都需要加热或高温
C
4.[2018·杭州]图42-9为氢气还原氧化铜的实验
装置图。下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于
通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
图42-9
B
5.图42-10中甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验。
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是
性。
图42-10
还原
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先 ,后 ,否则生成的红色的铜会变成黑色。
图H11-10
移走酒精灯
停止通氢气
(3)某同学按正确操作做完乙实
验后,发现澄清石灰水变浑浊,
试管中粉末全部变为黑色,取少
量黑色粉末,加入足量稀硫酸充
分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
图H11-10
铁(或Fe)
(4)查阅资料,得到关于铁的氧化物的如下信息:
铁的氧化物化学式 Fe2O3 Fe3O4 FeO
颜色 红 黑 黑
化学性质 可溶于酸 常温下不溶于稀酸 可溶于酸
根据以上信息,试写出乙实验试管中反应的化学方程式:
。
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。
同课章节目录
