2022年浙江省中考科学一轮复习 第44课时 物质间的循环和转化(课件 38张PPT)
文档属性
| 名称 | 2022年浙江省中考科学一轮复习 第44课时 物质间的循环和转化(课件 38张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 870.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-11 20:54:03 | ||
图片预览





文档简介
(共38张PPT)
第44课时 物质间的循环和转化
●知识体系梳理
●重难考点精讲
●当堂限时训练
知识体系
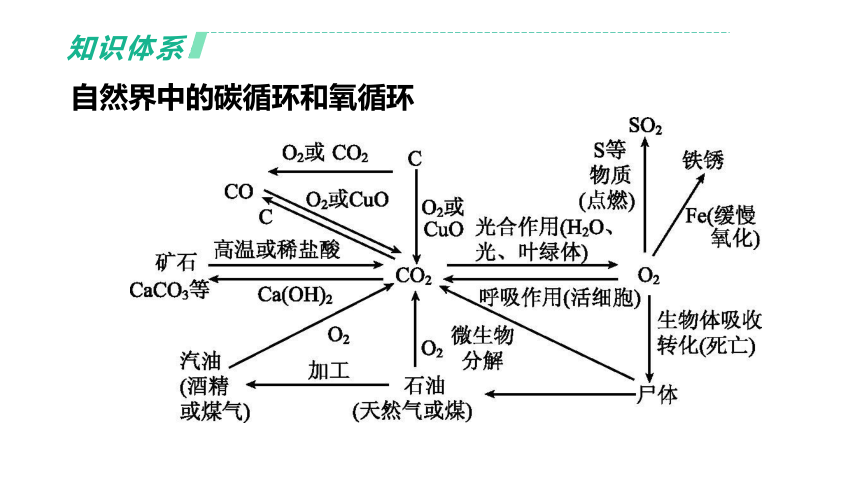
自然界中的碳循环和氧循环
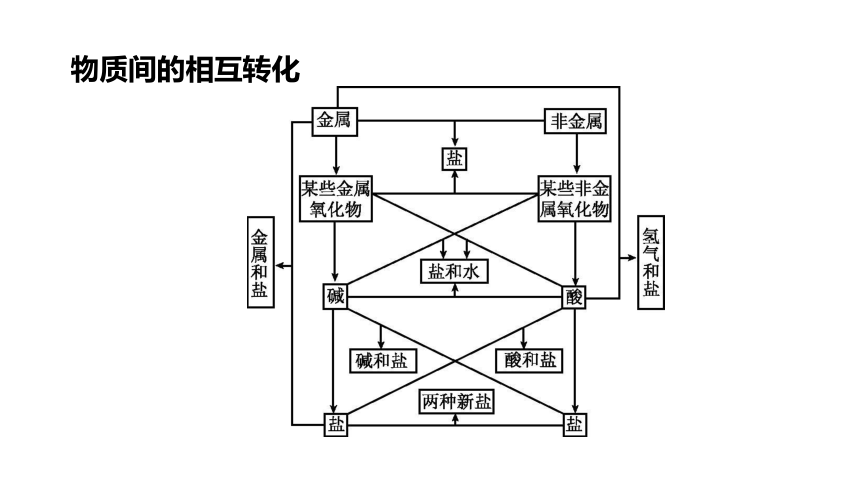
物质间的相互转化
重点梳理
1.自然界中的碳循环和氧循环
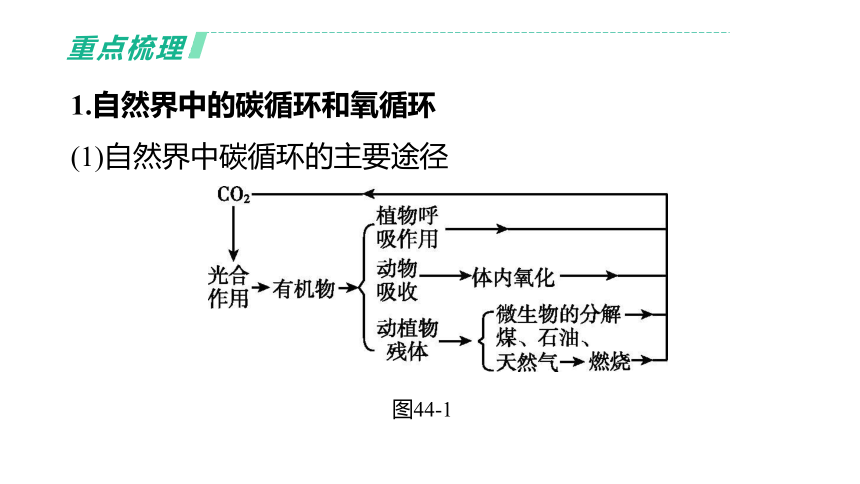
(1)自然界中碳循环的主要途径
图44-1
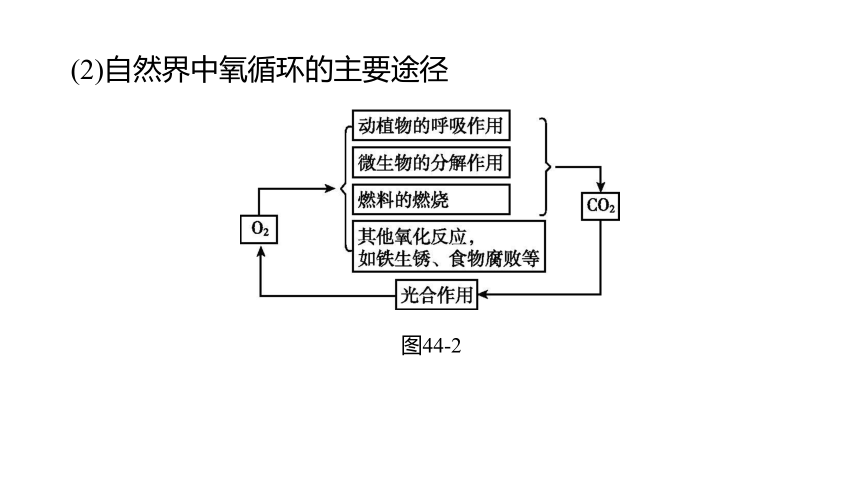
(2)自然界中氧循环的主要途径
图44-2
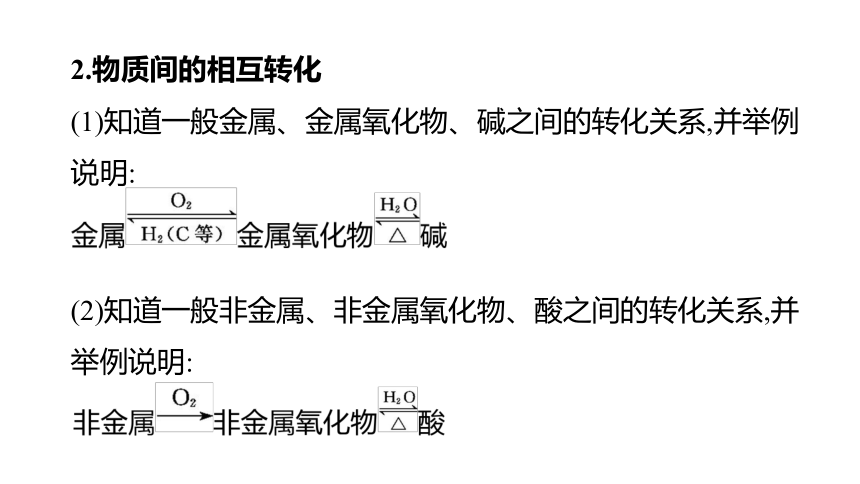
2.物质间的相互转化
(1)知道一般金属、金属氧化物、碱之间的转化关系,并举例说明:
(2)知道一般非金属、非金属氧化物、酸之间的转化关系,并举例说明:
考点1 自然界中的碳循环和氧循环
1.在初中化学学习中接触过几种循环,下列说法你认为正确的是 ( )
A.水的天然循环中水分子和水分子的能量都不变
B.二氧化碳的循环与大自然的森林绿化面积无关
C.自然界中的氧循环主要是通过化学变化实现的
D.自然界中的碳循环主要是通过物理变化实现的
对点练习
C
考点2 物质间的相互转化
2.[2021·嘉兴]如图44-3所示为小嘉构建的甲、乙、
丙、丁四种不同物质的关系图,“—”表示相邻的两
种物质能发生反应。若甲为铁,乙、丙、丁分别是
稀硫酸、CuCl2溶液、NaOH溶液中的任意一种,则
下列判断错误的是 ( )
A.乙可能是CuCl2溶液 B.丙一定是NaOH溶液
C.丁一定是稀硫酸 D.丙不可能是稀硫酸
图44-3
C
3.[2021·温州模拟]将下列物质同时加入水中,能大量共存且得到无色透明溶液的是 ( )
A. FeCl2、NaCl、KNO3
B. CaCl2、HCl、NaNO3
C. K2CO3、Mg(NO3)2、NaOH
D. KOH、NaCl、(NH4)2SO4
B
4.[2021·杭州余杭期末]为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
选项 物质 操作方法
A Fe(Fe2O3) 加入适量稀盐酸,充分反应后过滤
B CuSO4溶液(H2SO4) 加入过量CuO粉末,加热,充分反应后过滤
C NaNO3(Na2SO4) 加入过量的Ba(NO3)2溶液,充分反应后过滤
D NaOH溶液 (Na2CO3溶液) 加入适量的CaCl2溶液,充分反应后过滤
B
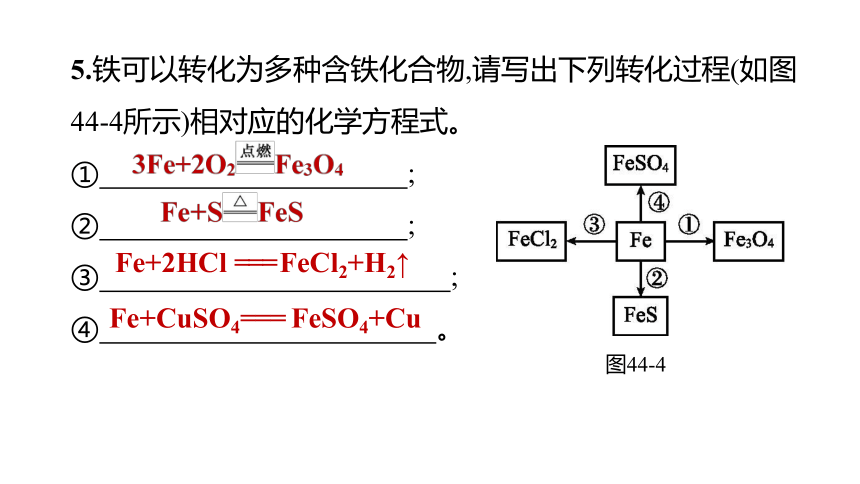
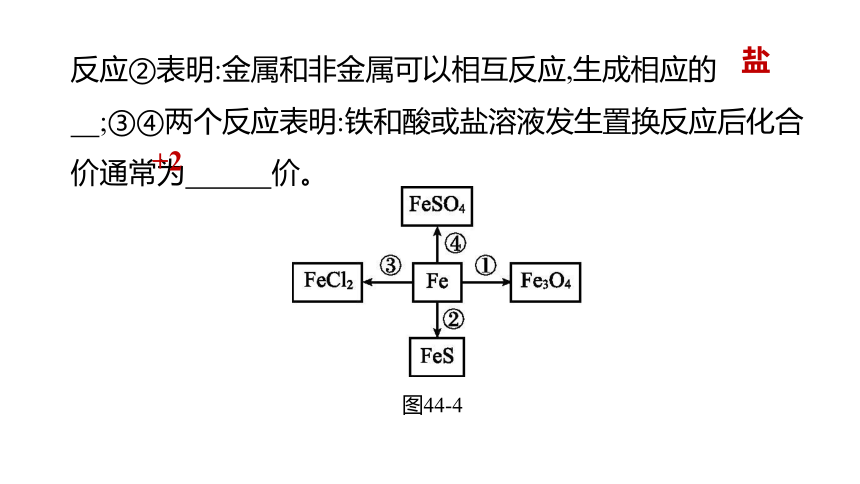
5.铁可以转化为多种含铁化合物,请写出下列转化过程(如图44-4所示)相对应的化学方程式。
① ;
② ;
③ ;
④ 。
图44-4
Fe+2HCl === FeCl2+H2↑
Fe+CuSO4=== FeSO4+Cu
反应②表明:金属和非金属可以相互反应,生成相应的 ;③④两个反应表明:铁和酸或盐溶液发生置换反应后化合价通常为 价。
图44-4
盐
+2
(1)写出图中“ ”处物质的化学式:
。
(2)要一步实现图中“Cu→Cu2+”的转化,可将铜加入适量的某种盐溶液中,则该溶液的溶质是_________________________
。
6.[2020·衢州]如图44-5是小科建
构的铜及其化合物之间相互转化
的关系图。
图44-5
CuO
硝酸银(或硝酸汞等,合理即
可)
(3)根据图中的转化关系,利用硝酸
铜溶液制备纯净的硫酸铜晶体。
请设计一个实验方案,要求写出主
要操作步骤及所需要的试剂:_____
____________________________________________________
。
在硝
铜溶液中加入氢氧化钠溶液,充分反应后过滤、洗涤沉淀,向沉淀中加入适量稀硫酸,充分反应后蒸发结晶(合理即可)
例1 关于碳循环和氧循环,下列说法错误的是( )
A.碳循环和氧循环分别是指二氧化碳和氧气的循环
B.碳循环和氧循环过程中均发生了化学变化
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
重点一
自然界中的碳循环和氧循环
A
例2 小梅同学学习了单质、氧化物、酸、碱和
盐的性质后,发现许多不同类别的物质反应时
均能生成盐,于是她构建了如图H13-6所示的
知识网络图。请根据网络图回答问题。
(1)请写出用酸和碱生产硫酸铜的化学方程式:
。
重点二
物质的制取
图4-6
H2SO4+Cu(OH)2===CuSO4+2H2O
(2)请你把图中①②处补充完整,要求不能与
图中已有信息重复。
① ;
② 。
图44-6
金属+盐
酸+盐
(3)根据网络图可制备
物质。例如,某回收含
铜电缆废料的工厂有
如图H13-7所示制铜
方案:
图44-7
①写出下列步骤的化学方程式。
步骤Ⅲ: ;
步骤Ⅴ: 。
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
②上述方案中可能造成空气污染的步骤是
(写化学方程式)。
【变式1】[2019·丽水]A、B、C为初中
科学常见的三种无机物,它们之间有如
图H13-8所示的转化关系(“→”表示某一
种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为
。
图44-8
(2)若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是 。
图44-8
酸(或碱或盐)
例3 [2021·杭州滨江期末]鉴别下列各组物质,所用试剂不正确的是 ( )
重点三
物质的鉴定和鉴别
选项 待鉴别的物质 鉴别试剂
A 稀盐酸和氯化钠溶液 无色酚酞试液
B 稀盐酸和稀硫酸 氢氧化钡溶液
C 稀硫酸和氢氧化钠溶液 石蕊试液
D 氢氧化钠溶液和氢氧化钙溶液 碳酸钠溶液
A
例4如何证明一瓶稀硫酸中含有盐酸杂质
____________________________________________________
____________________________________________________
__________________________________________________。
取1~2 mL样品,向其中加入过量Ba(NO3)2溶液,产生白色沉淀(为BaSO4),过滤后,向滤液中加入适量AgNO3溶液和稀硝酸,若产生白色沉淀(为AgCl),可证明稀硫酸中含有盐酸杂质
例5 一瓶不纯的K2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2CO3中的一种或几种。为确定其成分,进行如下实验:
①取少量该粉末于烧杯中,加入适量蒸馏水,充分搅拌,得无色澄清溶液;②取上述无色溶液少许于试管中,滴加AgNO3溶液有沉淀生成,再加入足量的稀硝酸,沉淀部分溶解;
重点四
物质的推断
③另称取1.38 g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的BaCl2溶液,充分反应后生成1.97 g 白色沉淀。
下列说法正确的是 ( )
A.杂质中可能含有KNO3、Na2CO3
B.杂质中肯定不含有Ca(NO3)2、CuCl2、Na2CO3
C.杂质中肯定含有KCl,可能含有Na2CO3
D.杂质中肯定含有KCl、Na2CO3,可能含有KNO3
D
例6 A~F是初中化学常见的六种物质,它们
之间的关系如图44-9所示(“→”表示物质
间的转化关系,“-”表示两种物质能相互反
应;部分反应物、生成物及反应条件未标出)。物质A可以与酸、碱、盐三类物质发生反应,D是厨房中常用的调味品,F的溶液呈黄色,反应①和②都有白色沉淀生成。
(1)写出A、C、D的化学式:A 、C 、D 。
图44-9
Na2CO3
NaOH
NaCl
(2)反应①的基本反应类型是 。
(3)反应②的化学方程式为 。
图44-9
复分解反应
HCl+AgNO3===AgCl↓+HNO3
例7 清洗、干燥后的黄铜渣中含有Zn 14%、ZnO 31%、Cu 50%、CuO 5%。处理黄铜渣可制得硫酸锌,其主要流程如图44-10所示。
已知:ZnO+H2SO4===ZnSO4+H2O;CuO+H2SO4===CuSO4+H2O。
重点五
物质的除杂
图44-10
(1)Ⅱ中发生了两个化学反应,请写出其中任意一个化学方程式: 。
(2)Ⅰ、Ⅱ中的操作均含 (填操作名称)。
(3)操作Ⅰ所得固体物质的化学式是 。
图44-10
Zn+H2SO4===ZnSO4+H2↑(或Zn+CuSO4===ZnSO4+Cu)
过滤
Cu
【变式2】[2019·杭州]下列实验中,实验原理和主要操作方法都符合实验目的的是 ( )
选项 实验目的 实验原理 主要操作方法
A 除去粗盐中的泥沙 各成分的溶解性差异 蒸发
B 分离水与酒精的混合物 各成分的密度差异 蒸馏
C 鉴别稀盐酸和稀硫酸 酸根离子的化学性质差异 加碳酸钠溶液,观察产生气泡快慢
D 除去FeSO4、CuSO4混合溶液中的CuSO4 金属活动性差异 加过量铁粉,充分反应后过滤
D
1. 下列关于自然界中碳循环和氧循环的说法中正确的( )
A.植物的光合作用使空气中的氧气含量逐年提升
B.动植物的呼吸作用使空气中的二氧化碳含量逐年增大
C.积极倡导“低碳”行动的目的是消除大气温室效应
D.大气中的氧气含量在各种因素作用下能保持相对稳定
图44-11
D
2.[2021·嘉兴]北宋沈括在《梦溪笔谈》中记载了用“苦泉水”制取铜的方法,其主要生产流程如图44-11所示。下列解释合理的是 ( )
A.①通过蒸发溶剂
可获得晶体
B.②是通过复分解反应获得铜
C.③所得硫酸铜溶液一定是饱和的
D.④说明铁元素变成了铜元素
图44-11
A
3.[2020·湖州]如“价—类”二维图可以表示元素化合价与物质类别之间的关系。如图44-12中的a、b、c、d、e代表常见的含碳物质,下列说法错误的是 ( )
A.X、Y、Z可以是CuSO4、Ca(OH)2和H2SO4
B.X和Z可以是CuO和CaCl2
C.Y和Z可以是K2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
图44-12
D
4.[2021·杭州西湖期末]如图
44-13所示X、Y、Z三种物
质的类别不同,连线两端的物
质常温下均能反应。下列说法正确的是 ( )
A.X、Y、Z可以是CuSO4、Ca(OH)2和H2SO4
B.X和Z可以是CuO和CaCl2
C.Y和Z可以是K2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
图44-13
C
5.[2021·杭州萧山模拟]按如图44-14所示装置进行实验。先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成。符合以上实验现象的一组试剂是 ( )
A.甲:NaHCO3、稀盐酸 乙:NaOH溶液
B.甲:Mg、稀硫酸 乙:Ba(NO3)2溶液
C.甲:MgO、稀盐酸 乙:AgNO3溶液
D.甲:Cu、稀硫酸 乙:BaCl2
图44-14
B
6.[2021·杭州三区期末]工业上用电解饱和食盐水的方法制备烧碱,小乐对用此方法生产的外包装破损的烧碱样品进行了如下探究。
提出问题 烧碱样品中含有哪些杂质
建立猜想 猜想1:可能含有碳酸钠,依据是氢氧化钠能和二氧化碳反应生成碳酸钠。
猜想2:可能含有氯化钠,依据是在化工生产中,原料可能
。
混入产品中
实验探究
实验操作 实验现象 实验结论
取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液 _________________________________________________________ 烧碱样品中含碳酸钠和氯化钠
先无明显现象,后有气
泡产生,加入硝酸银后
有白色沉淀生成
反思评价
除去烧碱样品中含有的少量碳酸钠,可选用的药品是______
(填序号)。
A.CuCl2溶液 B.Ba(NO3)2溶液
C.Ba(OH)2溶液 D.KOH溶液
C
第44课时 物质间的循环和转化
●知识体系梳理
●重难考点精讲
●当堂限时训练
知识体系
自然界中的碳循环和氧循环
物质间的相互转化
重点梳理
1.自然界中的碳循环和氧循环
(1)自然界中碳循环的主要途径
图44-1
(2)自然界中氧循环的主要途径
图44-2
2.物质间的相互转化
(1)知道一般金属、金属氧化物、碱之间的转化关系,并举例说明:
(2)知道一般非金属、非金属氧化物、酸之间的转化关系,并举例说明:
考点1 自然界中的碳循环和氧循环
1.在初中化学学习中接触过几种循环,下列说法你认为正确的是 ( )
A.水的天然循环中水分子和水分子的能量都不变
B.二氧化碳的循环与大自然的森林绿化面积无关
C.自然界中的氧循环主要是通过化学变化实现的
D.自然界中的碳循环主要是通过物理变化实现的
对点练习
C
考点2 物质间的相互转化
2.[2021·嘉兴]如图44-3所示为小嘉构建的甲、乙、
丙、丁四种不同物质的关系图,“—”表示相邻的两
种物质能发生反应。若甲为铁,乙、丙、丁分别是
稀硫酸、CuCl2溶液、NaOH溶液中的任意一种,则
下列判断错误的是 ( )
A.乙可能是CuCl2溶液 B.丙一定是NaOH溶液
C.丁一定是稀硫酸 D.丙不可能是稀硫酸
图44-3
C
3.[2021·温州模拟]将下列物质同时加入水中,能大量共存且得到无色透明溶液的是 ( )
A. FeCl2、NaCl、KNO3
B. CaCl2、HCl、NaNO3
C. K2CO3、Mg(NO3)2、NaOH
D. KOH、NaCl、(NH4)2SO4
B
4.[2021·杭州余杭期末]为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
选项 物质 操作方法
A Fe(Fe2O3) 加入适量稀盐酸,充分反应后过滤
B CuSO4溶液(H2SO4) 加入过量CuO粉末,加热,充分反应后过滤
C NaNO3(Na2SO4) 加入过量的Ba(NO3)2溶液,充分反应后过滤
D NaOH溶液 (Na2CO3溶液) 加入适量的CaCl2溶液,充分反应后过滤
B
5.铁可以转化为多种含铁化合物,请写出下列转化过程(如图44-4所示)相对应的化学方程式。
① ;
② ;
③ ;
④ 。
图44-4
Fe+2HCl === FeCl2+H2↑
Fe+CuSO4=== FeSO4+Cu
反应②表明:金属和非金属可以相互反应,生成相应的 ;③④两个反应表明:铁和酸或盐溶液发生置换反应后化合价通常为 价。
图44-4
盐
+2
(1)写出图中“ ”处物质的化学式:
。
(2)要一步实现图中“Cu→Cu2+”的转化,可将铜加入适量的某种盐溶液中,则该溶液的溶质是_________________________
。
6.[2020·衢州]如图44-5是小科建
构的铜及其化合物之间相互转化
的关系图。
图44-5
CuO
硝酸银(或硝酸汞等,合理即
可)
(3)根据图中的转化关系,利用硝酸
铜溶液制备纯净的硫酸铜晶体。
请设计一个实验方案,要求写出主
要操作步骤及所需要的试剂:_____
____________________________________________________
。
在硝
铜溶液中加入氢氧化钠溶液,充分反应后过滤、洗涤沉淀,向沉淀中加入适量稀硫酸,充分反应后蒸发结晶(合理即可)
例1 关于碳循环和氧循环,下列说法错误的是( )
A.碳循环和氧循环分别是指二氧化碳和氧气的循环
B.碳循环和氧循环过程中均发生了化学变化
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
重点一
自然界中的碳循环和氧循环
A
例2 小梅同学学习了单质、氧化物、酸、碱和
盐的性质后,发现许多不同类别的物质反应时
均能生成盐,于是她构建了如图H13-6所示的
知识网络图。请根据网络图回答问题。
(1)请写出用酸和碱生产硫酸铜的化学方程式:
。
重点二
物质的制取
图4-6
H2SO4+Cu(OH)2===CuSO4+2H2O
(2)请你把图中①②处补充完整,要求不能与
图中已有信息重复。
① ;
② 。
图44-6
金属+盐
酸+盐
(3)根据网络图可制备
物质。例如,某回收含
铜电缆废料的工厂有
如图H13-7所示制铜
方案:
图44-7
①写出下列步骤的化学方程式。
步骤Ⅲ: ;
步骤Ⅴ: 。
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
②上述方案中可能造成空气污染的步骤是
(写化学方程式)。
【变式1】[2019·丽水]A、B、C为初中
科学常见的三种无机物,它们之间有如
图H13-8所示的转化关系(“→”表示某一
种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为
。
图44-8
(2)若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是 。
图44-8
酸(或碱或盐)
例3 [2021·杭州滨江期末]鉴别下列各组物质,所用试剂不正确的是 ( )
重点三
物质的鉴定和鉴别
选项 待鉴别的物质 鉴别试剂
A 稀盐酸和氯化钠溶液 无色酚酞试液
B 稀盐酸和稀硫酸 氢氧化钡溶液
C 稀硫酸和氢氧化钠溶液 石蕊试液
D 氢氧化钠溶液和氢氧化钙溶液 碳酸钠溶液
A
例4如何证明一瓶稀硫酸中含有盐酸杂质
____________________________________________________
____________________________________________________
__________________________________________________。
取1~2 mL样品,向其中加入过量Ba(NO3)2溶液,产生白色沉淀(为BaSO4),过滤后,向滤液中加入适量AgNO3溶液和稀硝酸,若产生白色沉淀(为AgCl),可证明稀硫酸中含有盐酸杂质
例5 一瓶不纯的K2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2CO3中的一种或几种。为确定其成分,进行如下实验:
①取少量该粉末于烧杯中,加入适量蒸馏水,充分搅拌,得无色澄清溶液;②取上述无色溶液少许于试管中,滴加AgNO3溶液有沉淀生成,再加入足量的稀硝酸,沉淀部分溶解;
重点四
物质的推断
③另称取1.38 g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的BaCl2溶液,充分反应后生成1.97 g 白色沉淀。
下列说法正确的是 ( )
A.杂质中可能含有KNO3、Na2CO3
B.杂质中肯定不含有Ca(NO3)2、CuCl2、Na2CO3
C.杂质中肯定含有KCl,可能含有Na2CO3
D.杂质中肯定含有KCl、Na2CO3,可能含有KNO3
D
例6 A~F是初中化学常见的六种物质,它们
之间的关系如图44-9所示(“→”表示物质
间的转化关系,“-”表示两种物质能相互反
应;部分反应物、生成物及反应条件未标出)。物质A可以与酸、碱、盐三类物质发生反应,D是厨房中常用的调味品,F的溶液呈黄色,反应①和②都有白色沉淀生成。
(1)写出A、C、D的化学式:A 、C 、D 。
图44-9
Na2CO3
NaOH
NaCl
(2)反应①的基本反应类型是 。
(3)反应②的化学方程式为 。
图44-9
复分解反应
HCl+AgNO3===AgCl↓+HNO3
例7 清洗、干燥后的黄铜渣中含有Zn 14%、ZnO 31%、Cu 50%、CuO 5%。处理黄铜渣可制得硫酸锌,其主要流程如图44-10所示。
已知:ZnO+H2SO4===ZnSO4+H2O;CuO+H2SO4===CuSO4+H2O。
重点五
物质的除杂
图44-10
(1)Ⅱ中发生了两个化学反应,请写出其中任意一个化学方程式: 。
(2)Ⅰ、Ⅱ中的操作均含 (填操作名称)。
(3)操作Ⅰ所得固体物质的化学式是 。
图44-10
Zn+H2SO4===ZnSO4+H2↑(或Zn+CuSO4===ZnSO4+Cu)
过滤
Cu
【变式2】[2019·杭州]下列实验中,实验原理和主要操作方法都符合实验目的的是 ( )
选项 实验目的 实验原理 主要操作方法
A 除去粗盐中的泥沙 各成分的溶解性差异 蒸发
B 分离水与酒精的混合物 各成分的密度差异 蒸馏
C 鉴别稀盐酸和稀硫酸 酸根离子的化学性质差异 加碳酸钠溶液,观察产生气泡快慢
D 除去FeSO4、CuSO4混合溶液中的CuSO4 金属活动性差异 加过量铁粉,充分反应后过滤
D
1. 下列关于自然界中碳循环和氧循环的说法中正确的( )
A.植物的光合作用使空气中的氧气含量逐年提升
B.动植物的呼吸作用使空气中的二氧化碳含量逐年增大
C.积极倡导“低碳”行动的目的是消除大气温室效应
D.大气中的氧气含量在各种因素作用下能保持相对稳定
图44-11
D
2.[2021·嘉兴]北宋沈括在《梦溪笔谈》中记载了用“苦泉水”制取铜的方法,其主要生产流程如图44-11所示。下列解释合理的是 ( )
A.①通过蒸发溶剂
可获得晶体
B.②是通过复分解反应获得铜
C.③所得硫酸铜溶液一定是饱和的
D.④说明铁元素变成了铜元素
图44-11
A
3.[2020·湖州]如“价—类”二维图可以表示元素化合价与物质类别之间的关系。如图44-12中的a、b、c、d、e代表常见的含碳物质,下列说法错误的是 ( )
A.X、Y、Z可以是CuSO4、Ca(OH)2和H2SO4
B.X和Z可以是CuO和CaCl2
C.Y和Z可以是K2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
图44-12
D
4.[2021·杭州西湖期末]如图
44-13所示X、Y、Z三种物
质的类别不同,连线两端的物
质常温下均能反应。下列说法正确的是 ( )
A.X、Y、Z可以是CuSO4、Ca(OH)2和H2SO4
B.X和Z可以是CuO和CaCl2
C.Y和Z可以是K2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
图44-13
C
5.[2021·杭州萧山模拟]按如图44-14所示装置进行实验。先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成。符合以上实验现象的一组试剂是 ( )
A.甲:NaHCO3、稀盐酸 乙:NaOH溶液
B.甲:Mg、稀硫酸 乙:Ba(NO3)2溶液
C.甲:MgO、稀盐酸 乙:AgNO3溶液
D.甲:Cu、稀硫酸 乙:BaCl2
图44-14
B
6.[2021·杭州三区期末]工业上用电解饱和食盐水的方法制备烧碱,小乐对用此方法生产的外包装破损的烧碱样品进行了如下探究。
提出问题 烧碱样品中含有哪些杂质
建立猜想 猜想1:可能含有碳酸钠,依据是氢氧化钠能和二氧化碳反应生成碳酸钠。
猜想2:可能含有氯化钠,依据是在化工生产中,原料可能
。
混入产品中
实验探究
实验操作 实验现象 实验结论
取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液 _________________________________________________________ 烧碱样品中含碳酸钠和氯化钠
先无明显现象,后有气
泡产生,加入硝酸银后
有白色沉淀生成
反思评价
除去烧碱样品中含有的少量碳酸钠,可选用的药品是______
(填序号)。
A.CuCl2溶液 B.Ba(NO3)2溶液
C.Ba(OH)2溶液 D.KOH溶液
C
同课章节目录
