鲁教版九年级化学上册 4-2 物质组成的定量表示 课件(24张PPT)
文档属性
| 名称 | 鲁教版九年级化学上册 4-2 物质组成的定量表示 课件(24张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 10.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-14 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
第四单元第二节
第二课时
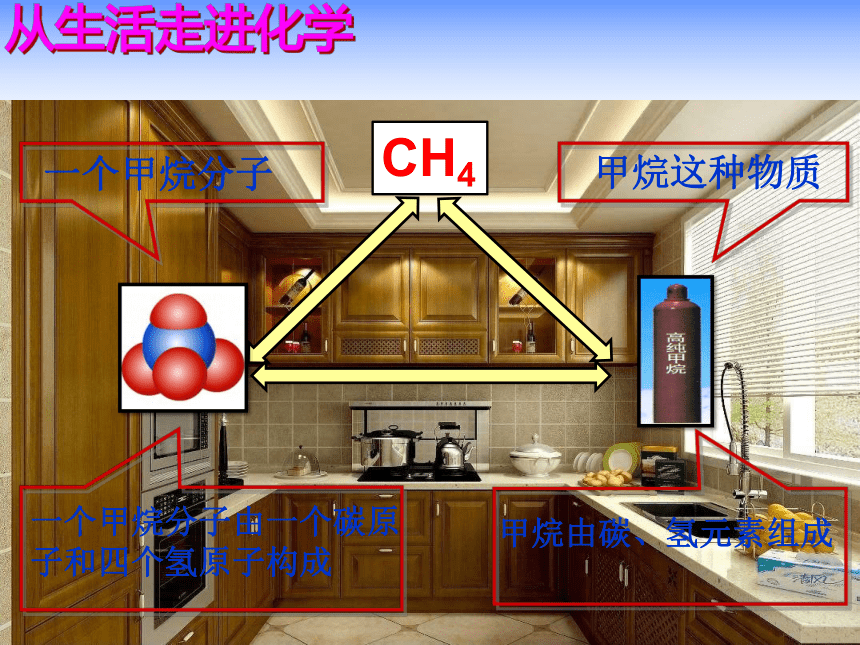
依据化学式你能获得哪些信息?
CH4
CH4
一个甲烷分子
一个甲烷分子由一个碳原子和四个氢原子构成
甲烷这种物质
甲烷由碳、氢元素组成
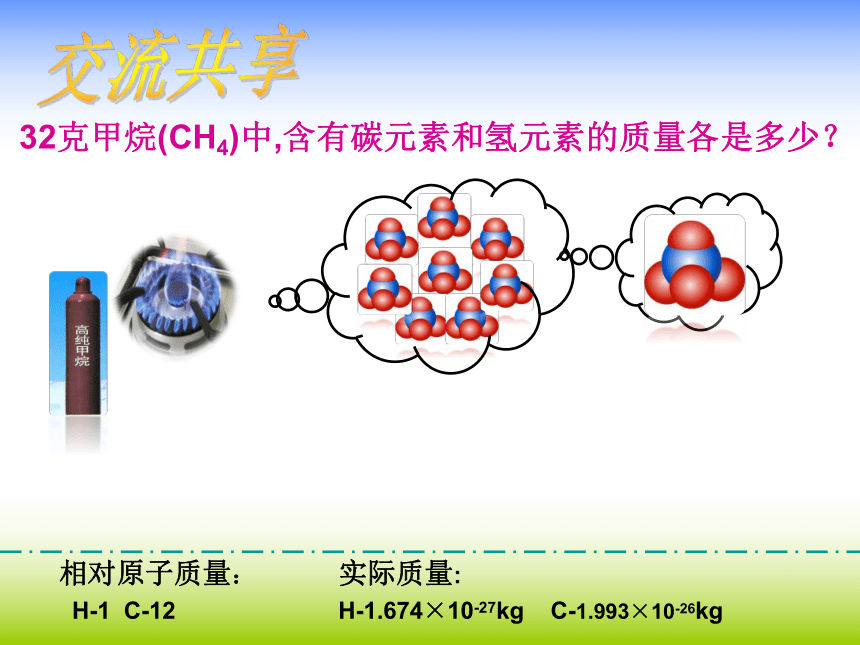
32克甲烷(CH4)中,含有碳元素和氢元素的质量各是多少?
实际质量:
H-1.674×10-27kg C-1.993×10-26kg
相对原子质量:
H-1 C-12
相对原子质量: H-1 C-12
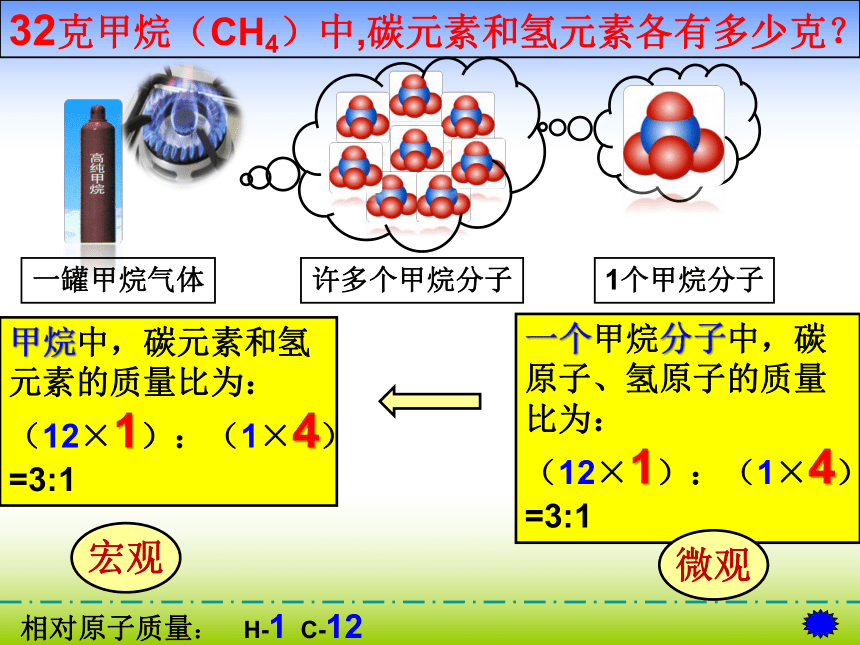
1个甲烷分子
许多个甲烷分子
一罐甲烷气体
一个甲烷分子中,碳原子、氢原子的质量比为: (12×1):(1×4)=3:1
甲烷中,碳元素和氢元素的质量比为:(12×1):(1×4)=3:1
微观
宏观
32克甲烷(CH4)中,碳元素和氢元素各有多少克?
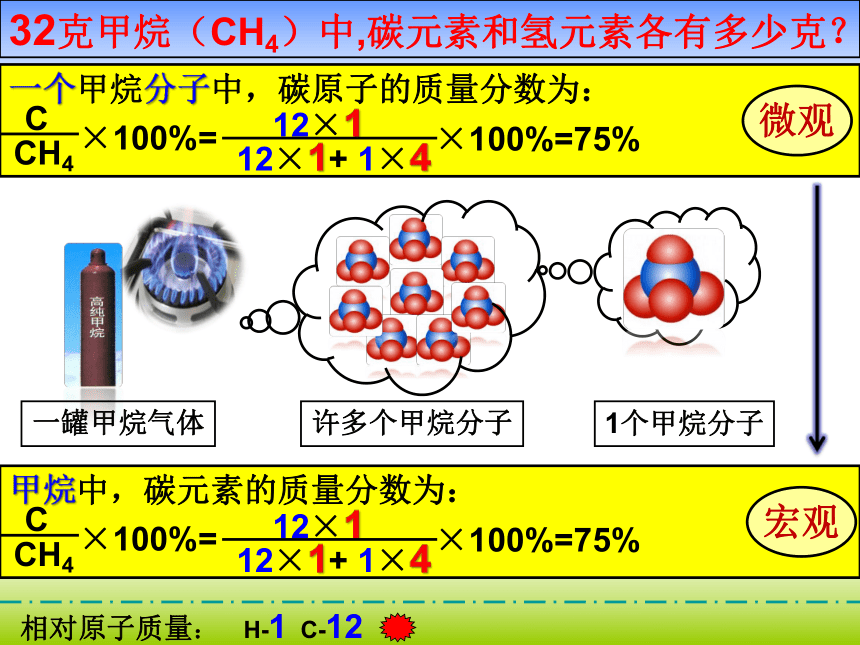
32克甲烷(CH4)中,碳元素和氢元素各有多少克?
相对原子质量: H-1 C-12
1个甲烷分子
许多个甲烷分子
一罐甲烷气体
一个甲烷分子中,碳原子的质量分数为:
12×1
12×1+ 1×4
×100%=75%
C
CH4
×100%=
甲烷中,碳元素的质量分数为:
12×1
12×1+ 1×4
×100%=75%
C
CH4
×100%=
微观
宏观
依据甲烷(CH4)能够进行的计算
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
2.化合物中各元素质量比
1.化学式量=化学式中各原子的
3.化合物中某元素质量分数
依据化学式能够进行的计算
相对原子质量的总和
=相对原子质量×原子个数之比
3.甲烷(CH4)中氢元素、碳元素质量分数:
C
×100%
C%=
CH4
=75%
12×1
16
×100%
=
4H
×100%
H%=
CH4
=
1× 4
×100%
16
=25%
相对原子质量: H-1 C-12
相对原子质量×原子个数
化学式量
×100%
=
依据甲烷(化学式为CH4)能够进行的计算:
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
3.甲烷(CH4)中氢元素、碳元素质量分数:
=75%
12×1
16
×100%
=
4H
×100%
H%=
CH4
=
1× 4
×100%
16
=25%
相对原子质量: H-1 C-12
C
×100%
C%=
CH4
32克甲烷(CH4)中,含有碳元素和氢元素的质量各是多少?
甲烷(CH4)中氢元素质量分数:
=
4H
×100%
H%=
CH4
1×4
×100%
16
=25%
相对原子质量: H-1 C-12
甲烷(CH4)中氢元素的质量:
H%=32g 25%=8g
×
×
32g
甲烷(CH4)中碳元素质量分数:
C
×100%
C%=
CH4
=75%
12×1
16
×100%
=
甲烷(CH4)中碳元素的质量:
C%=32g 75%=24g
×
×
32g
用铁锅炒菜能补充铁元素。工业上,铁用铁矿石来制取。铁矿石的主要成分是氧化铁, 化学式为Fe2O3。
铁矿石(Fe2O3)
请计算: Fe-56 O-16
(1) 氧化铁(化学式为Fe2O3)的化学式量=
(2)氧化铁(化学式为Fe2O3)中各元素的质量比:
(3)氧化铁(化学式为Fe2O3)中铁元素的质量分数:
(4)16g氧化铁(化学式为Fe2O3)中含铁元素多少克
=
依据甲烷(CH4)能够进行的计算
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
3.甲烷(CH4)中氢元素质量分数:
4H
×100%
H%=
CH4
1× 4
×100%
16
=25%
4.32g甲烷(CH4)中氢元素的质量:
32g H%=32g 25%=8g
×
×
请计算: Fe-56 O-16 (1) 氧化铁(化学式为Fe2O3)的化学式量=________________
(2)氧化铁(化学式为Fe2O3)中各元素的质量比:
______________________________________
(3)氧化铁(化学式为Fe2O3)中铁元素的质量分数:
(4)16g氧化铁(化学式为Fe2O3)中含铁元素多少克
Fe2O3
56×2+16×3=160
Fe:O=(56×2):(16×3)=7:3
Fe%=
2Fe
Fe2O3
×100%=
56×2
160
×100%=
70%
16g× Fe%=16g ×70%=11.2g
水果蔬菜中富含维生素C,又名抗坏血酸,化学式为 C6H8O6 ,由分子构成。易溶于水,易被氧化,受热时易被破坏。
请计算 :C-12 H-1 O-16
(1) Vc( C6H8O6 )的化学式量(相对分子质量)为
;(2) Vc (C6H8O6)中各元素的质量比为
请计算 :C-12 H-1 O-16
(1) Vc( 化学式为C6H8O6 )的化学式量(相对分子质量)为
_______________________;
(2) Vc (化学式为C6H8O6)中各元素的质量比为
_______________________。
12×6+1×8+16×6=176
C:H:O=(12×6):(1×8):(16×6)=9:1:12
NH4NO3
硝酸铵(化学式为NH4NO3)是农业上常用的氮肥,施用氮肥能提高农作物产量。
请计算: N-14 H-1 O-16
(1)硝酸铵(化学式为NH4NO3)的化学式量=
(2)硝酸铵(化学式为NH4NO3)中氮元素的质量分数
14×2+1×4+16×3=80
14×2
N%=
2N
NH4NO3
×100%=
80
×100%=
35%
净重:50Kg
含氮量:34.3%
世卫组织(WHO)将由 氯元素的某氧化物列为高效安全灭菌剂。实验测得氧化物中氯元素与氧元素的质量比为 71:64;该化合物中氯原子与氧原子个数比为 。
Cl- 35.5 O- 16
1:2
解:设该化合物的化学式为ClxOy
ClO2
35.5x
16y
=
:
71
:
64
X:
y
=
1:2
甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
二氧化氯
纯净物有固定的组成
测定
CH4
H2O
3:1 =(12×1):(1×4)= C :H
1:8 =(1×2):(16×1)= H :O
物质中元素质量比
分析计算
物质的构成
水中各元素的质量比:
甲烷中各元素的质量比:
纯净物有固定的组成
测定
物质中元素质量比
分析计算
物质的构成
黄花蒿
分离
提纯
合成
C15H22O5
C15H24O5
感悟与收获
谢谢惠听!
Ca-40 C-12 O-16
碳酸钙(CaCO3)是很多补钙产品的主要成分,请计算:
(1)碳酸钙中
Ca:C:O= ;
(2)碳酸钙的相对分子质量为 ;
(3)钙元素的质量分数为 。
10:3:12
100
40%
Ca%=
Ca
CaCO3
×100%=
40×1
100
×100%=40%
硫酸亚铁(FeSO4)可用于治疗缺铁性贫血。 请计算: (Fe 56 S 32 O 16)
(1)硫酸亚铁的相对分子质量是多少? (2)硫酸亚铁中各元素质量比是多少?
152
Fe:S:O=(56×1):(32×1):(16×4)=7:4:8
(3)某贫血患者每天需补充1.4g铁元素,服用药物中应含硫酸亚铁的质量为多少?
解:设硫酸亚铁的质量为X.
X=3.8g
方法1:
=1.4g
X ·
Fe
FeSO4
×100%
=1.4g
X ·
56
152
×100%
1.4g÷Fe%=1.4g÷(
Fe
FeSO4
×100%)
=3.8g
方法2:
(FeSO4相对分子质量为152)
第四单元第二节
第二课时
依据化学式你能获得哪些信息?
CH4
CH4
一个甲烷分子
一个甲烷分子由一个碳原子和四个氢原子构成
甲烷这种物质
甲烷由碳、氢元素组成
32克甲烷(CH4)中,含有碳元素和氢元素的质量各是多少?
实际质量:
H-1.674×10-27kg C-1.993×10-26kg
相对原子质量:
H-1 C-12
相对原子质量: H-1 C-12
1个甲烷分子
许多个甲烷分子
一罐甲烷气体
一个甲烷分子中,碳原子、氢原子的质量比为: (12×1):(1×4)=3:1
甲烷中,碳元素和氢元素的质量比为:(12×1):(1×4)=3:1
微观
宏观
32克甲烷(CH4)中,碳元素和氢元素各有多少克?
32克甲烷(CH4)中,碳元素和氢元素各有多少克?
相对原子质量: H-1 C-12
1个甲烷分子
许多个甲烷分子
一罐甲烷气体
一个甲烷分子中,碳原子的质量分数为:
12×1
12×1+ 1×4
×100%=75%
C
CH4
×100%=
甲烷中,碳元素的质量分数为:
12×1
12×1+ 1×4
×100%=75%
C
CH4
×100%=
微观
宏观
依据甲烷(CH4)能够进行的计算
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
2.化合物中各元素质量比
1.化学式量=化学式中各原子的
3.化合物中某元素质量分数
依据化学式能够进行的计算
相对原子质量的总和
=相对原子质量×原子个数之比
3.甲烷(CH4)中氢元素、碳元素质量分数:
C
×100%
C%=
CH4
=75%
12×1
16
×100%
=
4H
×100%
H%=
CH4
=
1× 4
×100%
16
=25%
相对原子质量: H-1 C-12
相对原子质量×原子个数
化学式量
×100%
=
依据甲烷(化学式为CH4)能够进行的计算:
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
3.甲烷(CH4)中氢元素、碳元素质量分数:
=75%
12×1
16
×100%
=
4H
×100%
H%=
CH4
=
1× 4
×100%
16
=25%
相对原子质量: H-1 C-12
C
×100%
C%=
CH4
32克甲烷(CH4)中,含有碳元素和氢元素的质量各是多少?
甲烷(CH4)中氢元素质量分数:
=
4H
×100%
H%=
CH4
1×4
×100%
16
=25%
相对原子质量: H-1 C-12
甲烷(CH4)中氢元素的质量:
H%=32g 25%=8g
×
×
32g
甲烷(CH4)中碳元素质量分数:
C
×100%
C%=
CH4
=75%
12×1
16
×100%
=
甲烷(CH4)中碳元素的质量:
C%=32g 75%=24g
×
×
32g
用铁锅炒菜能补充铁元素。工业上,铁用铁矿石来制取。铁矿石的主要成分是氧化铁, 化学式为Fe2O3。
铁矿石(Fe2O3)
请计算: Fe-56 O-16
(1) 氧化铁(化学式为Fe2O3)的化学式量=
(2)氧化铁(化学式为Fe2O3)中各元素的质量比:
(3)氧化铁(化学式为Fe2O3)中铁元素的质量分数:
(4)16g氧化铁(化学式为Fe2O3)中含铁元素多少克
=
依据甲烷(CH4)能够进行的计算
1.甲烷(CH4)化学式量(相对分子质量):
(12×1)+(1×4)=16
2.甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
3.甲烷(CH4)中氢元素质量分数:
4H
×100%
H%=
CH4
1× 4
×100%
16
=25%
4.32g甲烷(CH4)中氢元素的质量:
32g H%=32g 25%=8g
×
×
请计算: Fe-56 O-16 (1) 氧化铁(化学式为Fe2O3)的化学式量=________________
(2)氧化铁(化学式为Fe2O3)中各元素的质量比:
______________________________________
(3)氧化铁(化学式为Fe2O3)中铁元素的质量分数:
(4)16g氧化铁(化学式为Fe2O3)中含铁元素多少克
Fe2O3
56×2+16×3=160
Fe:O=(56×2):(16×3)=7:3
Fe%=
2Fe
Fe2O3
×100%=
56×2
160
×100%=
70%
16g× Fe%=16g ×70%=11.2g
水果蔬菜中富含维生素C,又名抗坏血酸,化学式为 C6H8O6 ,由分子构成。易溶于水,易被氧化,受热时易被破坏。
请计算 :C-12 H-1 O-16
(1) Vc( C6H8O6 )的化学式量(相对分子质量)为
;(2) Vc (C6H8O6)中各元素的质量比为
请计算 :C-12 H-1 O-16
(1) Vc( 化学式为C6H8O6 )的化学式量(相对分子质量)为
_______________________;
(2) Vc (化学式为C6H8O6)中各元素的质量比为
_______________________。
12×6+1×8+16×6=176
C:H:O=(12×6):(1×8):(16×6)=9:1:12
NH4NO3
硝酸铵(化学式为NH4NO3)是农业上常用的氮肥,施用氮肥能提高农作物产量。
请计算: N-14 H-1 O-16
(1)硝酸铵(化学式为NH4NO3)的化学式量=
(2)硝酸铵(化学式为NH4NO3)中氮元素的质量分数
14×2+1×4+16×3=80
14×2
N%=
2N
NH4NO3
×100%=
80
×100%=
35%
净重:50Kg
含氮量:34.3%
世卫组织(WHO)将由 氯元素的某氧化物列为高效安全灭菌剂。实验测得氧化物中氯元素与氧元素的质量比为 71:64;该化合物中氯原子与氧原子个数比为 。
Cl- 35.5 O- 16
1:2
解:设该化合物的化学式为ClxOy
ClO2
35.5x
16y
=
:
71
:
64
X:
y
=
1:2
甲烷(CH4)中碳、氢元素质量比:
C :H=(12×1):(1×4)=3:1
二氧化氯
纯净物有固定的组成
测定
CH4
H2O
3:1 =(12×1):(1×4)= C :H
1:8 =(1×2):(16×1)= H :O
物质中元素质量比
分析计算
物质的构成
水中各元素的质量比:
甲烷中各元素的质量比:
纯净物有固定的组成
测定
物质中元素质量比
分析计算
物质的构成
黄花蒿
分离
提纯
合成
C15H22O5
C15H24O5
感悟与收获
谢谢惠听!
Ca-40 C-12 O-16
碳酸钙(CaCO3)是很多补钙产品的主要成分,请计算:
(1)碳酸钙中
Ca:C:O= ;
(2)碳酸钙的相对分子质量为 ;
(3)钙元素的质量分数为 。
10:3:12
100
40%
Ca%=
Ca
CaCO3
×100%=
40×1
100
×100%=40%
硫酸亚铁(FeSO4)可用于治疗缺铁性贫血。 请计算: (Fe 56 S 32 O 16)
(1)硫酸亚铁的相对分子质量是多少? (2)硫酸亚铁中各元素质量比是多少?
152
Fe:S:O=(56×1):(32×1):(16×4)=7:4:8
(3)某贫血患者每天需补充1.4g铁元素,服用药物中应含硫酸亚铁的质量为多少?
解:设硫酸亚铁的质量为X.
X=3.8g
方法1:
=1.4g
X ·
Fe
FeSO4
×100%
=1.4g
X ·
56
152
×100%
1.4g÷Fe%=1.4g÷(
Fe
FeSO4
×100%)
=3.8g
方法2:
(FeSO4相对分子质量为152)
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
