江苏省三厂中学2012—2013学年度第一学期高二年级期中考试高二化学(必修)(有答案)
文档属性
| 名称 | 江苏省三厂中学2012—2013学年度第一学期高二年级期中考试高二化学(必修)(有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 153.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-11-14 07:40:37 | ||
图片预览



文档简介
三厂中学2012~2013学年度第一学期高二年级期中考试
高二化学(必修)
考试时间:90分钟 试卷总分:100分 命题人:陈 达
可能用到的相对的原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5 Ca:40 Mn:55 Fe:56 Cu:64 Ag:108 I:127 Ba:137
第I卷 选择题(共80分)
一、单项选择题(本题包括30小题,每题1分,共30分。每小题只有一个选项符合题意)
1.全球气候变暖。据报道,江苏在最近47年里平均气温升高1.38℃。下列哪种气体的增加是导致这种情况出现的主要原因
A.N2 B.O2 C.CO2 D.SO2
2.当光束通过豆浆时,可观察到丁达尔效应,表明豆浆是
A.胶体 B.溶液 C.悬浊液 D.乳浊液
3.下列元素中金属性最强的是
A.K B.Na C.Al D.Mg
4.下列物质属于离子化合物的是
A.O3 B.H2O C.K2SO4 D.C2H5OH
5.下列物质与水反应生成强酸的是
A.Na2O B.SO3 C.CO2 D.NH3
6.“西气东输”是西部大开发的重大工程,“西气”指的是
A.石油气 B.天然气 C.水煤气 D.煤气
7.用生石灰中和法阻止海水酸化是人们的一种设想,生石灰(CaO)属于
A.酸 B.碱 C.盐 D.氧化物
8.下列过程发生化学变化的是
A.花香四溢 B.海水晒盐 C.粮食酿酒 D.冰雪消融
9.下列不能由太阳能直接转化而成的能量形式是
A.核能 B.生物质能 C.电能 D.化学能
10.下列物质中,属于非电解质的是
A.蔗糖 B.金属镁 C.氧气 D.氧化钠
11.下列物质属于含有共价键的离子化合物的是
A.C60 B.NaOH C.KF D.C6H6
12.下列含氧酸酸性最强的是
A.HClO4 B.H3PO4 C.H2SO4 D.H2CO3
13.下列气体的排放可能会造成酸雨的是
A.CO B.CH4 C.SO2 D.N2
14.下列各组物质互为同分异构体的是
A.O2和O3 B.CH3CH2CH2CH3和CH(CH3)3 C.12C和13C D.CH3和CH3CH3
15.下列物质中含有自由移动Cl-的是
A.KClO3固体 B.Cl2 C.HCl气体 D.KCl溶液
16.2012年2月新华网报道,加拿大开发出生产医用放射性同位素99 43Tc的简单方法。下列关于99 43Tc的叙述正确的是
A.原子序数是99 B.质量数是43 C.中子数是99 D.电子数是43
17.下列物质不属于天然高分子化合物的是
A.淀粉 B.蚕丝 C.葡萄糖 D.纤维素
18.因具有放射性而被称为居室“隐形杀手”的是
A.甲醛 B.苯 C.氡 ???? D.一氧化碳
19.某主族元素的气态氢化物的化学式为RH3,此元素最高价氧化物对应水化物的化学式可能为
A.H3RO3 B.HRO3 C.H2RO4 D.HRO4
20.根据元素周期律判断,下列元素气态氢化物最稳定的是
A.Cl B.S C.P D.Si
21.下列物质不能使蛋白质变性的是
A.浓盐酸 ?B.食盐????? C.硫酸铜 D.氢氧化钠
22.食用下列物质与人体微量元素的摄入无关的是
A.铁强化酱油 B.加碘食盐 C.富锌面粉 D.高钙牛奶
23.某元素的一价阴离子,核外有10个电子,质量数为19,则中子数为
A.9 B.10 C.11 D.12
24.下列叙述正确的是
A.电能是一级能源 B.水力是二级能源 C.天然气是一级能源 D.水煤气是一级能源
25.为了使天空更蓝,空气更清新,目前江苏的各城市对没有申领到“绿色”通行证的高污染车实行限行。高污染车排出的尾气中所含的污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有
A.二氧化碳 B.氮氧化物 C.水蒸汽 D.氮气
26.Na和Na+两种粒子中,不相同的是
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数
A.①② B.②③ C.③④ D.②③④
27.我国三峡工程所提供的清洁、廉价、大功率可再生的水电,相当于每年燃烧3×107吨原煤的火力发电厂产生的电能。因此三峡工程有助于控制
A.温室效应 B.氮的氧化物的排放
C.白色污染 D.碳氢化合物的排放
28.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,?他外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
A.同系物 B.同分异构体 C.同位素 D.同素异形体
29.红葡萄酒密封储存时间越长,质量越好,香味越浓郁。其原因是久置的葡萄酒中,与原来相比含有更多的
A.(C6H10O5)n B.CH3CH2OH C.CH3COOC2H5 D.CH3COOH
30.下列说法正确的是
A.医疗上常用碳酸钡作X射线透视肠胃的内服药剂,即钡餐
B.人体补碘,所有的食品都应加碘
C.由于近几十年来温室效应加剧,加速了古建筑的风化
D.硅的提纯与应用,促进了半导体元件与集成芯片的发展
二、单项选择题(本题包括10小题,每题2分,共20分。每小题只有一个选项符合题意)
31.实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是
A.用锌粉代替锌粒 B.改用3mol/L硫酸溶液
C.改用热的确2mol/L硫酸溶液 D.向该硫酸溶液中加入等体积的水
32.关于元素周期表的说法正确的是
A.元素周期表有8个主族 B.ⅠA族的元素全部是金属元素
C.元素周期表有7个周期 D.短周期是指第一、二周期
33.人生病时要合理用药。下列药品与其作用相匹配的是
A.氢氧化铝:中和过多胃酸 B.阿司匹林:消炎抗菌
C.青霉素:解热镇痛 D.医用碘酒:人体补碘
34.下列有关日常生活中涉及到的化学知识使用错误的是
A.用铝锅长时间存放剩菜 B.用白醋清洗热水瓶中的水垢
C.用碘水检测土豆中含有淀粉 D.利用激光笔区别鸡蛋清和浓盐水
35.11H 、21H 、31H、H+、H2是
A.氢的五种同位素 B.五种氢元素
C.氢的五种同素异形体 D.氢元素的五种不同粒子
36.下列实验中,没有颜色变化的是
A.淀粉溶液中加入稀硫酸 B.鸡蛋清中加入浓硝酸
C.淀粉溶液中加入碘酒 D.葡萄糖溶液与新制氢氧化铜浊液混合加热
37.NO和CO都是汽车尾气里出有害物质,它们能缓慢起反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是
A.使用催化剂不改变反应速率 B.降低压强能加大反应速率
C.升高温度能加快反应速率 D.改变压强对反应速率无影响
38.下列有关化学反应与能量的说法中错误的是
A.中和反应是放热反应 B.油脂在人体中氧化是放热反应
C.镁与盐酸反应是吸热反应 D.氢分子(H-H)变成2个H需吸收能量
39.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍遇到它,都能水解而被除去,下列衣料中不能用加酶洗衣粉洗涤的是①棉织品? ②毛织品? ③腈纶制品? ④蚕丝制品? ⑤涤纶制品? ⑥锦纶制品
A.①②③??? B.②④??? C.③④⑤?? ? D.③⑤⑥
40.很多化学物质名称中含有“水”,“水”通常有三种含义:①表示水这种物质;②表示水溶液;③表示物质处于液态。下列物质名称中的“水”不属于以上三种含义的是
A.水晶 B.水银 C.溴水 D.重水
三、单项选择题(本题包括10小题,每题3分,共30分。每小题只有一个选项符合题意)
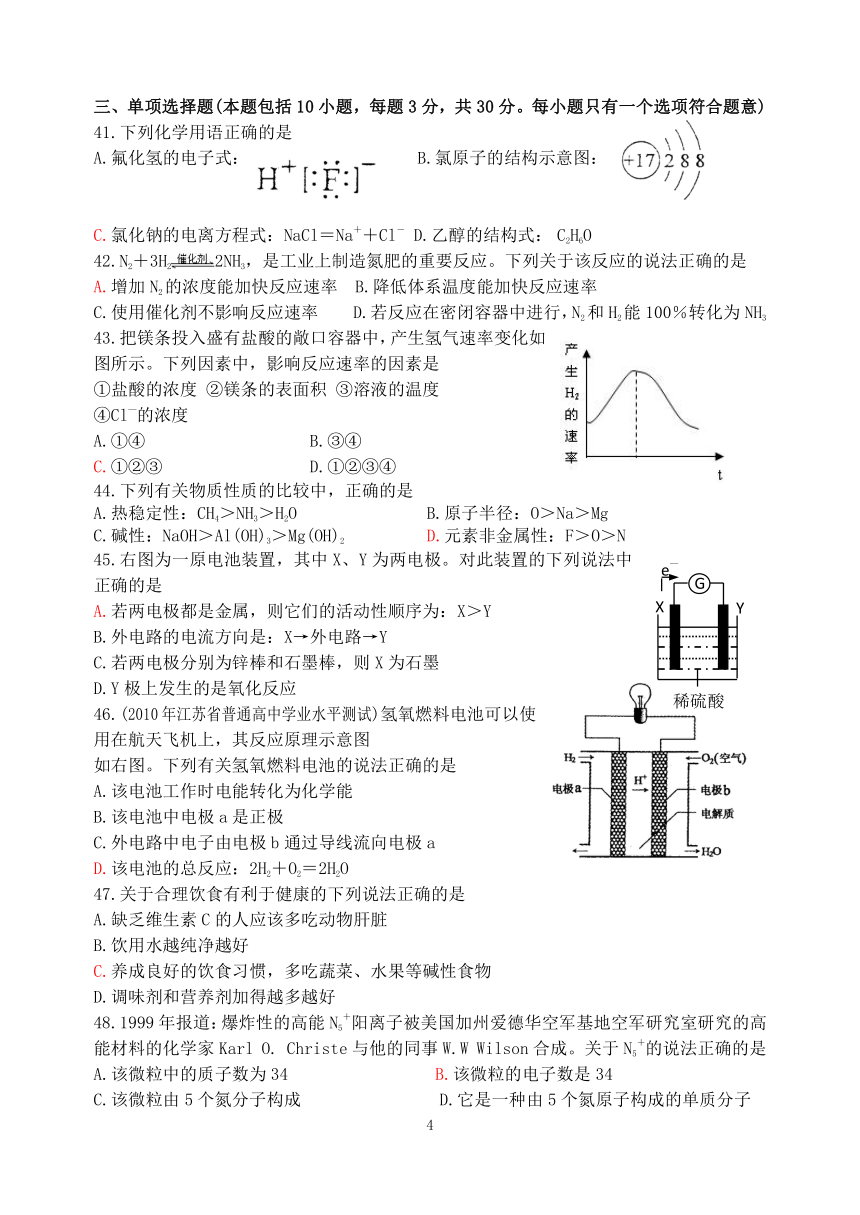
41.下列化学用语正确的是
A.氟化氢的电子式: B.氯原子的结构示意图:
C.氯化钠的电离方程式:NaCl=Na++Cl- D.乙醇的结构式: C2H6O
42.N2+3H22NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A.增加N2的浓度能加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率 D.若反应在密闭容器中进行,N2和H2能100%转化为NH3
43.把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示。下列因素中,影响反应速率的因素是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度
④Cl—的浓度
A.①④ B.③④
C.①②③ D.①②③④
44.下列有关物质性质的比较中,正确的是
A.热稳定性:CH4>NH3>H2O B.原子半径:O>Na>Mg
C.碱性:NaOH>Al(OH)3>Mg(OH)2 D.元素非金属性:F>O>N
45.右图为一原电池装置,其中X、Y为两电极。对此装置的下列说法中正确的是
A.若两电极都是金属,则它们的活动性顺序为:X>Y
B.外电路的电流方向是:X→外电路→Y
C.若两电极分别为锌棒和石墨棒,则X为石墨
D.Y极上发生的是氧化反应
46.(2010年江苏省普通高中学业水平测试)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图
如右图。下列有关氢氧燃料电池的说法正确的是
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H2+O2=2H2O
47.关于合理饮食有利于健康的下列说法正确的是
A.缺乏维生素C的人应该多吃动物肝脏
B.饮用水越纯净越好
C.养成良好的饮食习惯,多吃蔬菜、水果等碱性食物
D.调味剂和营养剂加得越多越好
48.1999年报道:爆炸性的高能N5+阳离子被美国加州爱德华空军基地空军研究室研究的高能材料的化学家Karl O. Christe与他的同事W.W Wilson合成。关于N5+的说法正确的是
A.该微粒中的质子数为34 B.该微粒的电子数是34
C.该微粒由5个氮分子构成 D.它是一种由5个氮原子构成的单质分子
49.(2011年江苏省普通高中学业水平测试)短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族.Y与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.原子半径:Y<Z<W B.Z在化合物中呈+1价
C.Y与W可形成离子化合物 D.Z的单质不能与X的氧化物反应
50.(2012年江苏省普通高中学业水平测试)X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增。已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大。Z和N可以形成ZN2型化合物。下列有关说法正确的是
A.X与Y只能形成一种化合物 B.最高价氧化物对应水化物的碱性:Y>Z
C.气态氢化物的热稳定性:M>N D.单质的氧化性:X<M
第Ⅱ卷 非选择题(共20分)
51.《化学与生活》(每空1分,共12分)
(1)现有下列物质:脂肪、甘油、多糖、蛋白质、维生素A、维生素C、碘元素、铁元素。请选择正确答案填在相应的空格里。
①人体缺乏某种维生素会引起坏血病,这种维生素是 。
②人体缺乏某种微量元素会发生贫血,这种微量元素是 。
③既能为人体提供热量,又能提供必需脂肪酸的物质是 。
④纤维素被称为“第七营养素”。食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质。从化学成分看,纤维素是一种 。
(2)了解一些用药常识,有利于自我保健。现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝。
①其中属于解热镇痛的药物是 。
②青霉素的作用是 。
③碳酸镁可治疗胃酸过多的原理是 (用离子方程表示)。
④药片常用淀粉作为黏合剂,淀粉水解的最终产物是 。
(3)人体摄入的蛋白质,在酶的催化作用下发生水解,最终生成氨基酸。这些氨基酸一部分重新合成人体所需的蛋白质、糖或脂类物质,以满足各种生命活动的需要;另一部分则发生氧化反应,释放能量。
①蛋白质分子中主要含有 四种元素。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
(写结构简式或名称)。
③蛋白质溶液遇到浓的硫酸铵等无机盐溶液,会析出沉淀;再加适量水后,蛋白质重新溶解,仍然具有原来的活性。这个过程称为 。
④人体中共有二十多种氨基酸,其中有几种是人体自身不能合成的,必须由食物获得,称为 氨基酸。
52.(每空1分,共4分)下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
请回答下列问题:
(1)物质A的化学式为 。
(2)化合物E的电子式为 。
(3)反应①的离子方程式为 ;
反应②的化学方程式为 。
53.(每空1分,共4分)下表为元素周期表的一部分,请针对给出的5种元素回答下列问题:
(1)元素①的原子结构示意图为: 。
(2)第二周期标出的元素中最高价氧化物对应的水化物酸性较强的是 (填元素符号);④⑤两种元素的离子氧化性较强的是 (填离子符号)。
(3)请写出元素⑤的氢氧化物和稀盐酸反应的离子方程式 。
三厂中学2012~2013学年度第一学期高二年级期中考试
高二化学(必修)第Ⅱ卷 非选择题答题纸
51.《化学与生活》(每空1分,共12分)
(1)① 。
② 。
③ 。
④ 。
(2)① 。
② 。
③ 。
④ 。
(3)① 。 ② 。
③ 。 ④ 。
52.(每空1分,共4分)
(1) 。
(2) 。
(3) ;
。
53.(每空1分,共4分)
(1) 。
(2) ; 。
(3) 。
三厂中学2012~2013学年度第一学期高二年级期中考试
高二化学(必修)参考答案及评分标准
第I卷 选择题(共80分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
A
C
B
B
D
C
A
A
题号
11
12
13
14
15
16
17
18
19
20
答案
B
A
C
B
D
D
C
C
B
A
题号
21
22
23
24
25
26
27
28
29
30
答案
B
D
B
C
B
D
A
D
C
D
题号
31
32
33
34
35
36
37
38
39
40
答案
D
C
A
A
D
A
C
C
B
A
题号
41
42
43
44
45
46
47
48
49
50
答案
C
A
C
D
A
D
C
B
B
B
第Ⅱ卷 非选择题(共20分)
51.(1) ①维生素C。②铁元素。③脂肪。④多糖。
(2)①阿司匹林。②消炎。③MgCO3+H+===Mg2++H2O+CO2↑。④葡萄糖。
(3)①C、H、O、N。②羧基或-COOH。③盐析。④必需。
52.(1)Na2O2 (2)
(3)2Na+2H2O===2Na++OH-+H2↑; 2NaHCO3Na2CO3+H2O+CO2↑。
53.(1) (2)N;Al3+ (3)Al(OH)3+3H+===Al3++3H2O。
高二化学(必修)
考试时间:90分钟 试卷总分:100分 命题人:陈 达
可能用到的相对的原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5 Ca:40 Mn:55 Fe:56 Cu:64 Ag:108 I:127 Ba:137
第I卷 选择题(共80分)
一、单项选择题(本题包括30小题,每题1分,共30分。每小题只有一个选项符合题意)
1.全球气候变暖。据报道,江苏在最近47年里平均气温升高1.38℃。下列哪种气体的增加是导致这种情况出现的主要原因
A.N2 B.O2 C.CO2 D.SO2
2.当光束通过豆浆时,可观察到丁达尔效应,表明豆浆是
A.胶体 B.溶液 C.悬浊液 D.乳浊液
3.下列元素中金属性最强的是
A.K B.Na C.Al D.Mg
4.下列物质属于离子化合物的是
A.O3 B.H2O C.K2SO4 D.C2H5OH
5.下列物质与水反应生成强酸的是
A.Na2O B.SO3 C.CO2 D.NH3
6.“西气东输”是西部大开发的重大工程,“西气”指的是
A.石油气 B.天然气 C.水煤气 D.煤气
7.用生石灰中和法阻止海水酸化是人们的一种设想,生石灰(CaO)属于
A.酸 B.碱 C.盐 D.氧化物
8.下列过程发生化学变化的是
A.花香四溢 B.海水晒盐 C.粮食酿酒 D.冰雪消融
9.下列不能由太阳能直接转化而成的能量形式是
A.核能 B.生物质能 C.电能 D.化学能
10.下列物质中,属于非电解质的是
A.蔗糖 B.金属镁 C.氧气 D.氧化钠
11.下列物质属于含有共价键的离子化合物的是
A.C60 B.NaOH C.KF D.C6H6
12.下列含氧酸酸性最强的是
A.HClO4 B.H3PO4 C.H2SO4 D.H2CO3
13.下列气体的排放可能会造成酸雨的是
A.CO B.CH4 C.SO2 D.N2
14.下列各组物质互为同分异构体的是
A.O2和O3 B.CH3CH2CH2CH3和CH(CH3)3 C.12C和13C D.CH3和CH3CH3
15.下列物质中含有自由移动Cl-的是
A.KClO3固体 B.Cl2 C.HCl气体 D.KCl溶液
16.2012年2月新华网报道,加拿大开发出生产医用放射性同位素99 43Tc的简单方法。下列关于99 43Tc的叙述正确的是
A.原子序数是99 B.质量数是43 C.中子数是99 D.电子数是43
17.下列物质不属于天然高分子化合物的是
A.淀粉 B.蚕丝 C.葡萄糖 D.纤维素
18.因具有放射性而被称为居室“隐形杀手”的是
A.甲醛 B.苯 C.氡 ???? D.一氧化碳
19.某主族元素的气态氢化物的化学式为RH3,此元素最高价氧化物对应水化物的化学式可能为
A.H3RO3 B.HRO3 C.H2RO4 D.HRO4
20.根据元素周期律判断,下列元素气态氢化物最稳定的是
A.Cl B.S C.P D.Si
21.下列物质不能使蛋白质变性的是
A.浓盐酸 ?B.食盐????? C.硫酸铜 D.氢氧化钠
22.食用下列物质与人体微量元素的摄入无关的是
A.铁强化酱油 B.加碘食盐 C.富锌面粉 D.高钙牛奶
23.某元素的一价阴离子,核外有10个电子,质量数为19,则中子数为
A.9 B.10 C.11 D.12
24.下列叙述正确的是
A.电能是一级能源 B.水力是二级能源 C.天然气是一级能源 D.水煤气是一级能源
25.为了使天空更蓝,空气更清新,目前江苏的各城市对没有申领到“绿色”通行证的高污染车实行限行。高污染车排出的尾气中所含的污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有
A.二氧化碳 B.氮氧化物 C.水蒸汽 D.氮气
26.Na和Na+两种粒子中,不相同的是
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数
A.①② B.②③ C.③④ D.②③④
27.我国三峡工程所提供的清洁、廉价、大功率可再生的水电,相当于每年燃烧3×107吨原煤的火力发电厂产生的电能。因此三峡工程有助于控制
A.温室效应 B.氮的氧化物的排放
C.白色污染 D.碳氢化合物的排放
28.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,?他外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
A.同系物 B.同分异构体 C.同位素 D.同素异形体
29.红葡萄酒密封储存时间越长,质量越好,香味越浓郁。其原因是久置的葡萄酒中,与原来相比含有更多的
A.(C6H10O5)n B.CH3CH2OH C.CH3COOC2H5 D.CH3COOH
30.下列说法正确的是
A.医疗上常用碳酸钡作X射线透视肠胃的内服药剂,即钡餐
B.人体补碘,所有的食品都应加碘
C.由于近几十年来温室效应加剧,加速了古建筑的风化
D.硅的提纯与应用,促进了半导体元件与集成芯片的发展
二、单项选择题(本题包括10小题,每题2分,共20分。每小题只有一个选项符合题意)
31.实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是
A.用锌粉代替锌粒 B.改用3mol/L硫酸溶液
C.改用热的确2mol/L硫酸溶液 D.向该硫酸溶液中加入等体积的水
32.关于元素周期表的说法正确的是
A.元素周期表有8个主族 B.ⅠA族的元素全部是金属元素
C.元素周期表有7个周期 D.短周期是指第一、二周期
33.人生病时要合理用药。下列药品与其作用相匹配的是
A.氢氧化铝:中和过多胃酸 B.阿司匹林:消炎抗菌
C.青霉素:解热镇痛 D.医用碘酒:人体补碘
34.下列有关日常生活中涉及到的化学知识使用错误的是
A.用铝锅长时间存放剩菜 B.用白醋清洗热水瓶中的水垢
C.用碘水检测土豆中含有淀粉 D.利用激光笔区别鸡蛋清和浓盐水
35.11H 、21H 、31H、H+、H2是
A.氢的五种同位素 B.五种氢元素
C.氢的五种同素异形体 D.氢元素的五种不同粒子
36.下列实验中,没有颜色变化的是
A.淀粉溶液中加入稀硫酸 B.鸡蛋清中加入浓硝酸
C.淀粉溶液中加入碘酒 D.葡萄糖溶液与新制氢氧化铜浊液混合加热
37.NO和CO都是汽车尾气里出有害物质,它们能缓慢起反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是
A.使用催化剂不改变反应速率 B.降低压强能加大反应速率
C.升高温度能加快反应速率 D.改变压强对反应速率无影响
38.下列有关化学反应与能量的说法中错误的是
A.中和反应是放热反应 B.油脂在人体中氧化是放热反应
C.镁与盐酸反应是吸热反应 D.氢分子(H-H)变成2个H需吸收能量
39.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍遇到它,都能水解而被除去,下列衣料中不能用加酶洗衣粉洗涤的是①棉织品? ②毛织品? ③腈纶制品? ④蚕丝制品? ⑤涤纶制品? ⑥锦纶制品
A.①②③??? B.②④??? C.③④⑤?? ? D.③⑤⑥
40.很多化学物质名称中含有“水”,“水”通常有三种含义:①表示水这种物质;②表示水溶液;③表示物质处于液态。下列物质名称中的“水”不属于以上三种含义的是
A.水晶 B.水银 C.溴水 D.重水
三、单项选择题(本题包括10小题,每题3分,共30分。每小题只有一个选项符合题意)
41.下列化学用语正确的是
A.氟化氢的电子式: B.氯原子的结构示意图:
C.氯化钠的电离方程式:NaCl=Na++Cl- D.乙醇的结构式: C2H6O
42.N2+3H22NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A.增加N2的浓度能加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率 D.若反应在密闭容器中进行,N2和H2能100%转化为NH3
43.把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示。下列因素中,影响反应速率的因素是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度
④Cl—的浓度
A.①④ B.③④
C.①②③ D.①②③④
44.下列有关物质性质的比较中,正确的是
A.热稳定性:CH4>NH3>H2O B.原子半径:O>Na>Mg
C.碱性:NaOH>Al(OH)3>Mg(OH)2 D.元素非金属性:F>O>N
45.右图为一原电池装置,其中X、Y为两电极。对此装置的下列说法中正确的是
A.若两电极都是金属,则它们的活动性顺序为:X>Y
B.外电路的电流方向是:X→外电路→Y
C.若两电极分别为锌棒和石墨棒,则X为石墨
D.Y极上发生的是氧化反应
46.(2010年江苏省普通高中学业水平测试)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图
如右图。下列有关氢氧燃料电池的说法正确的是
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H2+O2=2H2O
47.关于合理饮食有利于健康的下列说法正确的是
A.缺乏维生素C的人应该多吃动物肝脏
B.饮用水越纯净越好
C.养成良好的饮食习惯,多吃蔬菜、水果等碱性食物
D.调味剂和营养剂加得越多越好
48.1999年报道:爆炸性的高能N5+阳离子被美国加州爱德华空军基地空军研究室研究的高能材料的化学家Karl O. Christe与他的同事W.W Wilson合成。关于N5+的说法正确的是
A.该微粒中的质子数为34 B.该微粒的电子数是34
C.该微粒由5个氮分子构成 D.它是一种由5个氮原子构成的单质分子
49.(2011年江苏省普通高中学业水平测试)短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族.Y与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.原子半径:Y<Z<W B.Z在化合物中呈+1价
C.Y与W可形成离子化合物 D.Z的单质不能与X的氧化物反应
50.(2012年江苏省普通高中学业水平测试)X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增。已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大。Z和N可以形成ZN2型化合物。下列有关说法正确的是
A.X与Y只能形成一种化合物 B.最高价氧化物对应水化物的碱性:Y>Z
C.气态氢化物的热稳定性:M>N D.单质的氧化性:X<M
第Ⅱ卷 非选择题(共20分)
51.《化学与生活》(每空1分,共12分)
(1)现有下列物质:脂肪、甘油、多糖、蛋白质、维生素A、维生素C、碘元素、铁元素。请选择正确答案填在相应的空格里。
①人体缺乏某种维生素会引起坏血病,这种维生素是 。
②人体缺乏某种微量元素会发生贫血,这种微量元素是 。
③既能为人体提供热量,又能提供必需脂肪酸的物质是 。
④纤维素被称为“第七营养素”。食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质。从化学成分看,纤维素是一种 。
(2)了解一些用药常识,有利于自我保健。现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝。
①其中属于解热镇痛的药物是 。
②青霉素的作用是 。
③碳酸镁可治疗胃酸过多的原理是 (用离子方程表示)。
④药片常用淀粉作为黏合剂,淀粉水解的最终产物是 。
(3)人体摄入的蛋白质,在酶的催化作用下发生水解,最终生成氨基酸。这些氨基酸一部分重新合成人体所需的蛋白质、糖或脂类物质,以满足各种生命活动的需要;另一部分则发生氧化反应,释放能量。
①蛋白质分子中主要含有 四种元素。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
(写结构简式或名称)。
③蛋白质溶液遇到浓的硫酸铵等无机盐溶液,会析出沉淀;再加适量水后,蛋白质重新溶解,仍然具有原来的活性。这个过程称为 。
④人体中共有二十多种氨基酸,其中有几种是人体自身不能合成的,必须由食物获得,称为 氨基酸。
52.(每空1分,共4分)下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
请回答下列问题:
(1)物质A的化学式为 。
(2)化合物E的电子式为 。
(3)反应①的离子方程式为 ;
反应②的化学方程式为 。
53.(每空1分,共4分)下表为元素周期表的一部分,请针对给出的5种元素回答下列问题:
(1)元素①的原子结构示意图为: 。
(2)第二周期标出的元素中最高价氧化物对应的水化物酸性较强的是 (填元素符号);④⑤两种元素的离子氧化性较强的是 (填离子符号)。
(3)请写出元素⑤的氢氧化物和稀盐酸反应的离子方程式 。
三厂中学2012~2013学年度第一学期高二年级期中考试
高二化学(必修)第Ⅱ卷 非选择题答题纸
51.《化学与生活》(每空1分,共12分)
(1)① 。
② 。
③ 。
④ 。
(2)① 。
② 。
③ 。
④ 。
(3)① 。 ② 。
③ 。 ④ 。
52.(每空1分,共4分)
(1) 。
(2) 。
(3) ;
。
53.(每空1分,共4分)
(1) 。
(2) ; 。
(3) 。
三厂中学2012~2013学年度第一学期高二年级期中考试
高二化学(必修)参考答案及评分标准
第I卷 选择题(共80分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
A
C
B
B
D
C
A
A
题号
11
12
13
14
15
16
17
18
19
20
答案
B
A
C
B
D
D
C
C
B
A
题号
21
22
23
24
25
26
27
28
29
30
答案
B
D
B
C
B
D
A
D
C
D
题号
31
32
33
34
35
36
37
38
39
40
答案
D
C
A
A
D
A
C
C
B
A
题号
41
42
43
44
45
46
47
48
49
50
答案
C
A
C
D
A
D
C
B
B
B
第Ⅱ卷 非选择题(共20分)
51.(1) ①维生素C。②铁元素。③脂肪。④多糖。
(2)①阿司匹林。②消炎。③MgCO3+H+===Mg2++H2O+CO2↑。④葡萄糖。
(3)①C、H、O、N。②羧基或-COOH。③盐析。④必需。
52.(1)Na2O2 (2)
(3)2Na+2H2O===2Na++OH-+H2↑; 2NaHCO3Na2CO3+H2O+CO2↑。
53.(1) (2)N;Al3+ (3)Al(OH)3+3H+===Al3++3H2O。
同课章节目录
