8.1金属材料课后练习-2021_2022学年九年级化学人教版下册(含解析)
文档属性
| 名称 | 8.1金属材料课后练习-2021_2022学年九年级化学人教版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 273.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-15 00:00:00 | ||
图片预览




文档简介
8.1金属材料
一、选择题(共16题)
1.下列有关物质的性质与用途具有对应关系的是( )
A.钛合金与人体有很好的相容性,可制成人造骨 B.石墨很软,可用于制作石墨电极
C.氮气难溶于水,可用作保护气 D.稀有气体化学性质不活泼,可用作电光源
2.合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较中,不正确的是( )
A.含碳量:生铁>钢 B.抗腐蚀能力:不锈钢>纯铁
C.硬度:纯铜>黄铜 D.熔点:纯锡>武德合金
3.家用不锈钢(铁合金)汤勺,常在手柄上端加一木柄或塑料柄,说明铁具有的物理性质是
A.延展性
B.导电性好
C.导热性好
D.铁易生锈
4.生活中金属材料得到越来越广泛的应用,下列属于金属共性的是( )
A.熔点高 B.良好的导电性
C.硬度大 D.银白色的光泽
5.国产飞机C919机壳采用了先进的铝锂合金材料。下列有关说法错误的是
A.铝锂合金密度小
B.铝锂合金的硬度比纯铝大
C.铝锂合金抗腐蚀性强
D.铝锂合金是合成材料
6.不锈钢、黄铜(铜、镁元素组成)和碳化钨等是制作圆珠笔“笔头”的主要材料。下列 关于这些材料的说法错误的是
A.铁是不锈钢的主要组成元素之一 B.黄铜的硬度比纯铜大
C.不锈钢与黄铜都具有耐腐蚀的性能 D.碳化钨是一种混合物
7.下列有关钢铁的说法正确的是
A.钢是纯净物,生铁是混合物
B.生铁和不锈钢都是金属材料
C.生铁的熔点比纯铁高
D.生锈的钢铁制品没有回收价值
8.中国石墨烯制造处于世界领先地位。石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,因此,石墨烯的性质类似于石墨。用石墨烯与铝合金可制出一种具备特殊性能的烯合金。下列对石墨烯和烯合金的说法错误的是,
A.石墨烯在一定条件下能与氧气反应 B.石墨烯在常温下化学性质活泼
C.烯合金具有优良的导电性 D.烯合金是一种新型材料
9.下列有关资源、能源方面叙述正确的是
A.空气是一种宝贵的资源,其中氮气的约占空气质量的78%
B.地球上的水资源是丰富的,淡水资源却很少只约占全球水储量的5.23%
C.稀土金属有“工业的维生素”的美誉,是不可再生的重要战略资源
D.石油分馏能得到汽油、煤油、柴油和煤焦油等燃料
10.物质的性质决定用途。下列物质的用途主要由其物理性质决定的是
A.二氧化碳作气体肥料 B.碳素墨水书写档案 C.氮气用于食品防腐 D.武德合金作保险丝
11.下列物质中,属于合金的是
A.生铁 B.水银 C.磁铁矿 D.金刚石
12.下列物质中不属于合金的是
A.不锈钢 B.黄铜 C.生铁 D.赤铁矿
13.物质的组成和结构决定性质,性质决定用途,下列叙述正确的是( )
A.石墨的质地较软,所以可用作干电池的电极
B.生铁坚硬,所以可用作医疗手术器械
C.一氧化碳和氧化碳的分子构成不同,所以二者的性质存在差异
D.金刚石和石墨组成元素相同,所以二者的物理性质相同
14.下列对事实的解释中,不合理的是
A.水变为水蒸气体积变大——水分子间间隔变大
B.金刚石和石墨物理性质差异较大——碳原子的结构不同
C.生铁和钢的性能不同——含碳量不同
D.硫在空气和氧气中燃烧的火焰颜色不同——氧气浓度不同
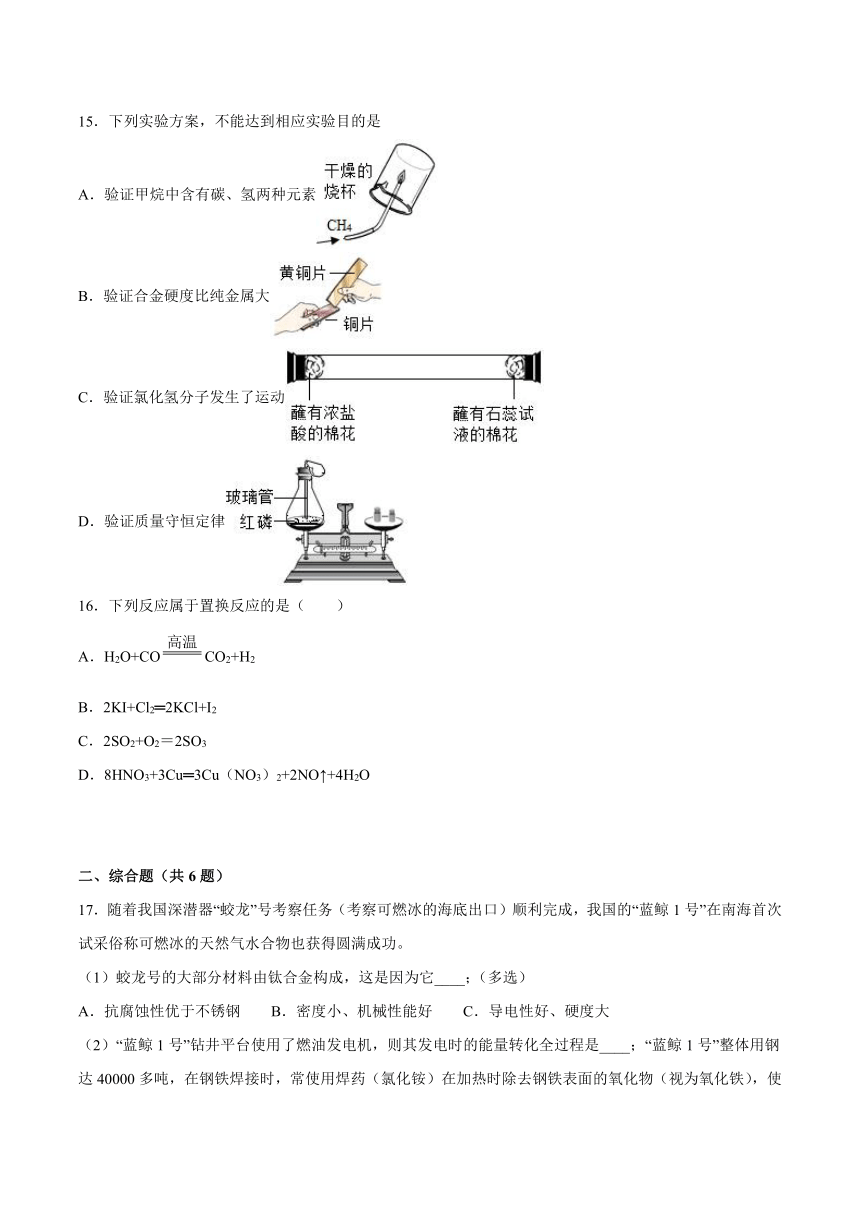
15.下列实验方案,不能达到相应实验目的是
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.下列反应属于置换反应的是( )
A.H2O+COCO2+H2
B.2KI+Cl2═2KCl+I2
C.2SO2+O2=2SO3
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O
二、综合题(共6题)
17.随着我国深潜器“蛟龙”号考察任务(考察可燃冰的海底出口)顺利完成,我国的“蓝鲸1号”在南海首次试采俗称可燃冰的天然气水合物也获得圆满成功。
(1)蛟龙号的大部分材料由钛合金构成,这是因为它____;(多选)
A.抗腐蚀性优于不锈钢 B.密度小、机械性能好 C.导电性好、硬度大
(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是____;“蓝鲸1号”整体用钢达40000多吨,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,该反应的化学方程式为____,反应前后氮元素的化合价变化为____。
(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少______(至少填两种物质的化学式)等有害气体的排放,可极大限度地减少空气污染。
18.依据所学知识回答问题
(1)网购、高铁、共享单车和打码支付被称为中国“新四大发明”。
①网购离不开光纤宽带。光纤的主要成分是SiO2,其中Si的化合价是_______。
②高铁车体的外壳由铝合金制成,用铝合金制作外壳的优点是_______(答一条)。
③共享单车的轮胎为实体轮胎,而普通自行车的轮胎在夏天易爆胎请用分子观点解释“夏天易爆胎”的原因_______。
④许多商品的二维码印在PVC不干胶贴纸上,PVC(化学式(C2H3C1)n)中碳、氢元素的质量比是_。
(2)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如下:
(其中,表示钠原子,表示氯原子, 表示氧原子)请回答题:
①A物质中氯元素的化合价为_______。
②D物质的名称是_______。
③该反应的化学方程式是_______。
19.我们的生活离不开化学。请回答下列问题。
(1)进入新装修的房间会闻到异味,这体现了粒子______的性质。人们常用活性炭来去除异味,这利用了活性炭的_____性。
(2)行外出旅游乘坐的飞机使用的航空煤油是由______炼制的产品。飞机的外壳主要是合金,这利用了镁铝合金的______性质。
A 密度小,材质轻 B 导电性 C 抗腐蚀性能好
20.2017年5月,国产大飞机C919成功进行首次试飞.请回答下列问题:
(1)图1中标示的材料中,属于有机合成材料的是 _____ ;
(2)飞机机身大量使用了铝合金材料.铝合金具有硬度大、密度小和 _____ 等优点;
(3)以金红石(主要成分是TiO2)为原料生产钛的流程如图2:其中“反应I”需要在高温条件下进行,反应的化学方程式为 _____ ;“反应II”中使用氩气的目的是 _____ ,该反应的基本反应类型属于 _____ 反应;
(4)现代民用飞机上使用的氧气发生器以氯酸钠为产氧剂,氯酸钠(NaClO3)中氯元素的化合价为 _____ ;
(5)C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能使燃油消耗减少16%.使用高密度空气的原因是 _____ .
21.开发利用氢能源是实现可持续发展的需要。根据图示分析,回答问题:
①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是_____(填序号)。
a.涤纶靠垫 b.橡胶轮胎 c.铜质导线 d.铝合金轮毂
②氢燃料电池的工作原理是:将氢气、氧气送到燃料电池中,经过催化剂的作用,发生反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式_____。
③氢气作燃料的优点是_____。
(2)工业上可通过下列工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
主反应器中反应的化学方程式是_____。膜反应器中的基本反应类型是_____。该工艺流程中,能被循环利用的物质是_____。
(3)采用电解水的方式制备10Kg氢气,理论上需要水的质量是多少千克?____
22.2019年12月16日,在我国西昌卫星发射中心,以“一箭双星”方式成功将第52、53颗北斗导航卫星送上了太空。随着这两颗卫星的升空,我国北斗三号全球系统核心星座部署完成。
(1)“长征三号乙”火箭发动机在焊接时需要使用氩弧焊。氩弧焊(如图)是在氩气保护下,通过在钨电极与焊件间产生的高压电弧放热,熔化焊丝或焊件的一种焊接技术。
①金属钨作电极是利用了金属钨的导电性和______;用氩气作保护气,是因为氩气的化学性质______。
②如果在没有保护气的情况下焊接金属,可能导致焊接不牢,原因是______。
(2)“长征三号乙”的第一、二级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)做推进剂,该反应的化学方程式为,则X的化学式是______。
(3)“长征三号乙”的第三级火箭采用液氢、液氧做推进剂。实验室可通过电解水得到氢气和氧气,氢气在与直流电源______极相连的电极上产生。氢能是未来最理想的能源,但目前应用并不广泛的原因是______(答一条即可)。
(4)北斗卫星的光伏发电板的主要构成材料是硅,单质硅由石英固体(SiO2)和碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是______。
参考答案
1.A
【详解】
A、钛合金与人体有很好的相容性,且性质稳定,抗腐蚀性强,所以可用来制造人造骨骼,故正确;
B、石墨具有良好的导电性,可用于制作石墨电极,故错误;
C、氮气的化学性质不活泼,可用作保护气,故错误;
D、稀有气体通电后发出不同颜色光,可用作不同用途的电光源,故错误。
故选A。
2.C
【详解】
A、生铁和钢都是铁的合金,生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,则生铁的含碳量高于钢的含碳量,故选项说法正确;B、不锈钢具有良好的抗腐蚀性能,抗腐蚀能力:不锈钢>纯铁,故选项说法正确;C、合金的硬度比组成它的纯金属的硬度大,硬度:纯铜<黄铜,故选项说法错误;D、合金的熔点比组成它的纯金属的熔点低,熔点:纯锡>武德合金,故选项说法正确。故选C。
3.C
【详解】
金属具有良好的导热性,不锈钢是良好的导热体,装木柄或塑料柄能起到很好的隔热作用,说明铁有良好的导热性。故选C。
4.B
【详解】
A.不是所有的金属熔点都很高,有一些金属熔点较低,例如:汞,故A错误;
B.金属具有良好的导电性,故B正确;
C.不是所有的金属硬度都很大,有一些金属的硬度很小,例如:铅硬度很小,故C错误;
D.金属不同,金属的颜色可能不同,如铁是银白色,但铜是紫红色,故D错误。
故选:B。
5.D
【详解】
A、铝锂合金密度小,故选项说法正确;
B、合金比组分金属硬度大,铝锂合金的硬度比纯铝大,故选项说法正确;
C、铝锂合金抗腐蚀性强,故选项说法正确;
D、铝锂合金属于金属材料,故选项说法错误。
故选D。
6.D
【详解】
A、不锈钢是指含铬13%以上的铁合金,铁是不锈钢的主要组成元素之一,故A正确;
B、合金的强度和硬度一般比组成它的纯金属更高,黄铜的硬度比纯铜大,故B正确
C、合金的抗腐蚀性能等比组成它的纯金属更好,不锈钢与黄铜都具有耐腐蚀的性能,故C正确;
D、碳化钨中含有一种物质,是一种纯净物,故D错误。故选D。
7.B
【分析】
【详解】
A、钢和生铁都是铁和碳的合金,是混合物,说法错误,故A不符合题意;
B、生铁和不锈钢都是金属材料,说法正确,故B符合题意;
C、合金的熔点比金属低,说法错误,故C不符合题意;
D、生锈的钢铁制品经过除锈之后,可以循环使用,说法错误,故D不符合题意;
故选B。
8.B
【详解】
A、石墨在一定条件下能与氧气反应,石墨烯的性质类似于石墨,故石墨烯在一定条件下能与氧气反应,正确;
B、石墨在常温下化学性质稳定,故石墨烯在常温下化学性质也稳定,错误;
C、烯合金具有优良的导电性 ,正确;
D、烯合金是一种新型材料,正确。故选B。
9.C
【详解】
试题分析:
A.氮气约占空气体积的78%,而不是质量的78%,所以A项错;
B.地球上水资源总量很大,但淡水资源却很少,在全球总储水量中只占2.53%,不是5.23%,所以B项错;
C.稀土金属是储量较少的一类金属的总称,它有“工业的维生素”的美誉,是不可再生的重要战略资源,所以C项正确;
D.煤焦油是煤经过干馏得到的,不是石油炼制得到的,所以D项错;
10.D
【详解】
A、二氧化碳使光合作用的原料,作气体肥料属于二氧化碳的化学性质,故选项错误;
B、碳素墨水书写档案是利用碳的稳定性,属于化学性质;故选项错误;
C、氮气用于食品防腐是利用氮气的化学性质不活泼,属于化学性质;故选项错误;
D、武德合金作保险丝是利用合金的熔点低,属于物理性质;故选项正确;
故选:D。
11.A
【详解】
A.生铁铁和碳的合金,属于合金;
B.水银是汞单质,不属于合金;
C.磁铁矿是指含有四氧化三铁的矿石,不属于合金;
D.金刚石是碳单质,不属于合金;
故选:A。
12.D
【详解】
A. 不锈钢是铁的合金,故错误;
B. 黄铜是铜的合金,故错误;
C. 生铁是含碳量较高的铁合金,故错误;
D. 赤铁矿是铁矿石,主要成分是氧化铁,故是混合物,不是合金,故正确。故选D。
13.C
【分析】
A、石墨具有导电性,所以可用作干电池的电极;
B、生铁接触到空气和水易发生锈蚀;
C、一氧化碳和二氧化碳的分子构成不同,所以二者的性质存在差异;
D、金刚石和石墨中碳原子排列方式不同,所以物理性质差异较大。
【详解】
A、石墨具有导电性,所以可用作干电池的电极,叙述错误,不符合题意;
B、生铁接触到空气和水易发生锈蚀,制造医疗手术器械应该用不锈钢,叙述错误,不符合题意;
C、一氧化碳和二氧化碳的分子构成不同,所以二者的性质存在差异,叙述正确,符合题意;
D、金刚石和石墨组成元素相同,所以二者的化学性质相同,二者中碳原子排列方式不同,所以物理性质差异较大,叙述错误,不符合题意。
故选C。
【详解】
A、分子间有间隔,水变为水蒸气体积变大是因为水分子间间隔变大,解释合理;
B、决定物质性质的是物质的组成和结构,金刚石和石墨物理性质差异较大,因为碳原子的排列方式不同,解释不合理;
C、生铁和钢的性能不同因为含碳量不同,生铁的含碳量比钢的高,解释合理;
D、硫在空气和氧气中燃烧的火焰颜色不同,因为氧气浓度不同,在纯氧中比在空气中燃烧更充分,解释合理。
故选B。
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.B
【详解】
A.H2O+COCO2+H2,反应物是两种化合物,不属于置换反应。
B.2KI+Cl2═2KCl+I2,是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应属于置换反应;
C.2SO2+O2=2SO3,反应物是两种,生成物是一种,属于“多变一”的化合反应;
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O,生成物是三种化合物,不属于置换反应。
故选:B。
【解析】
(1)蛟龙号的大部分材料由钛合金构成,这是因为它抗腐蚀性优于不锈钢,密度小、机械性能好;(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是化学能转化为内能转化为机械能再转化为电能,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,根据质量守恒定律可知:氯化铵和氧化铁在加热的条件下反应生成铁、氮气、水和氯化铁,该反应的化学方程式为6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3,反应前后氮元素的化合价变化-3价变为0价;(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少SO2、CO、NO2等有害气体的排放,可极大限度地减少空气污染。
18.
(1) +4 密度小 温度升高,分子间的间隔变大,体积膨胀 8:1
(2) +3 二氧化氯
【分析】
(1)
根据各元素的化合价的代数和为零,SiO2中氧元素的化合价为-2价,所以Si的化合价是+4价;
铝合金具有密度小,机械强度大 、抗腐蚀性强等优点;
夏天易爆胎”的原因是温度升高,分子运动剧烈,分子间的间隙增大,气体的体积膨胀;
PVC【化学式(C2H3C1)n】中碳、氢元素的质量比是
故填:+4;密度小;温度升高,分子间的间隔变大,体积膨胀;8:1
(2)
由微观示意图可知该反应方程式为:,所以A为NaClO2中钠元素的化合价为+1价,氧元素的化合价为-2价,根据元素的化合价的代数和为零,所以物质中氯元素的化合价为+3价;
D为ClO2,名称为二氧化氯;
该反应的化学方程式是:
故填:+3;二氧化氯;
19.不断运动 吸附 石油 AC
【详解】
(1)新装修的房间里污染气体主要是甲醛,由于甲醛分子的不断运动,使得整个房间充满异味,活性炭可以吸附气体,因此可以吸收有毒的甲醛气体,故答案为不断运动,吸附;
(2)航空煤油是由石油炼制的,由于石油为不可再生资源,因此煤油也是不可再生资源,飞机的外壳是铝镁合金,具有密度小,材质轻,抗腐蚀性能好的优点,故答案为石油,AC.
20.合成橡胶 抗腐蚀性好 TiO2+2C+2Cl2TiCl4+2CO 作保护气防止金属氧化 置换反应 +5 提供足够的氧气,使燃油燃烧更充分
【分析】
(1)(2)(3)根据已有的材料的类别、合金的性质以及化学方程式的书写的知识进行分析解答即可;
(4)化合价的代数和为零;
(5)从微观角度对现象进行解释,节约了能源,也就是保护了环境;
【详解】
(1)图中标示的材料中,合成橡胶属于有机合成材料;故填:合成橡胶;
(2)合金与组成它的成分相比较,一般情况下是密度小、硬度大、抗腐蚀性好,故答案为抗腐蚀性好;
(3)在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体是一氧化碳,反应的化学方程式为:TiO2+2C+2Cl2TiCl4+2CO; Mg容易被氧气氧化,使用氩气防止镁被氧化;在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,属于置换反应;故答案为TiO2+2C+2Cl2TiCl4+2CO;作保护气防止金属氧化;置换反应;
(4)设NaClO3中氯元素的化合价为x,由于钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合价的代数和为零可得(+1)+x+(-2×3)=0,解得x=+5,故答案为+5;
(5)高密度空气能使航空煤油更充分燃烧的微观原因是高密度空气中的氧分子与煤油分子接触更充分,使燃油燃烧更充分;故答案为供足够的氧气,使燃油燃烧更充分。
21.CD 2H2+O22H2O 燃烧产物是水,对环境无污染 2H2O+SO2+I2=H2SO4+2HI 分解反应 I2 90kg
【详解】
(1)①涤纶和合成橡胶属于合成材料;铜和铝合金属于金属材料;故填:CD;
②氢气与氧气在催化剂的作用下生成水;故填:2H2+O22H2O;
③氢气的热值高,氢气燃烧生成水,对环境无污染;故填:燃烧产物是水,对环境无污染;
(2)主反应器中反应是水和二氧化硫以及碘反应生成硫酸和碘化氢,对应的化学方程式是 2H2O+SO2+I2=H2SO4+2HI.膜反应器中是碘化氢分解为氢气和碘,为一变多,符合分解反应特征,属于分解反应。该工艺流程中,开始碘作为反应物,后来是生成物,所以能被循环利用的物质是 I2.故填:2H2O+SO2+I2=H2SO4+2HI;分解反应; I2;
(3)解:设需要水的质量为x,则:
x=90kg
答:理论上需要水90kg。
22.熔点高 不活泼 生成金属氧化物 CO2 负 制取成本高(贮存与运输困难等,合理答案答出一条即可)
【详解】
(1)金属钨作电极是利用了金属钨的导电性和熔点高;氩气是惰性气体,用氩气作保护气,是因为氩气的化学性质很不活泼;如果在没有保护气的情况下焊接金属,金属和空气中的氧气反应生成氧化物,可能导致焊接不牢;故①②③分别填:熔点高;不活泼;生成金属氧化物。
(2)在化学方程式中,反应物中C的个数为2,H的个数为8,N 的个数为6,O的个数为8;在生成物中N的个数为6个,H 的个数为8,所以,一个 X 中含有C的个数为1,含有O的个数为2,故X的化学式为CO2,故④填:CO2。
(3)根据“正氧负氢、氢二氧一”进行分析可知,氢气在与直流电源负极相连的电极上产生,因制取氢气是利用水分解得到,但水的分解一般需要电解,则制取成本高,因此目前应用并不广泛,故⑤⑥分别填:负;制取成本高(答案合理即可)。
(4)二氧化硅和碳在高温的条件下生成硅和一氧化碳,其化学方程式为:。
一、选择题(共16题)
1.下列有关物质的性质与用途具有对应关系的是( )
A.钛合金与人体有很好的相容性,可制成人造骨 B.石墨很软,可用于制作石墨电极
C.氮气难溶于水,可用作保护气 D.稀有气体化学性质不活泼,可用作电光源
2.合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较中,不正确的是( )
A.含碳量:生铁>钢 B.抗腐蚀能力:不锈钢>纯铁
C.硬度:纯铜>黄铜 D.熔点:纯锡>武德合金
3.家用不锈钢(铁合金)汤勺,常在手柄上端加一木柄或塑料柄,说明铁具有的物理性质是
A.延展性
B.导电性好
C.导热性好
D.铁易生锈
4.生活中金属材料得到越来越广泛的应用,下列属于金属共性的是( )
A.熔点高 B.良好的导电性
C.硬度大 D.银白色的光泽
5.国产飞机C919机壳采用了先进的铝锂合金材料。下列有关说法错误的是
A.铝锂合金密度小
B.铝锂合金的硬度比纯铝大
C.铝锂合金抗腐蚀性强
D.铝锂合金是合成材料
6.不锈钢、黄铜(铜、镁元素组成)和碳化钨等是制作圆珠笔“笔头”的主要材料。下列 关于这些材料的说法错误的是
A.铁是不锈钢的主要组成元素之一 B.黄铜的硬度比纯铜大
C.不锈钢与黄铜都具有耐腐蚀的性能 D.碳化钨是一种混合物
7.下列有关钢铁的说法正确的是
A.钢是纯净物,生铁是混合物
B.生铁和不锈钢都是金属材料
C.生铁的熔点比纯铁高
D.生锈的钢铁制品没有回收价值
8.中国石墨烯制造处于世界领先地位。石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,因此,石墨烯的性质类似于石墨。用石墨烯与铝合金可制出一种具备特殊性能的烯合金。下列对石墨烯和烯合金的说法错误的是,
A.石墨烯在一定条件下能与氧气反应 B.石墨烯在常温下化学性质活泼
C.烯合金具有优良的导电性 D.烯合金是一种新型材料
9.下列有关资源、能源方面叙述正确的是
A.空气是一种宝贵的资源,其中氮气的约占空气质量的78%
B.地球上的水资源是丰富的,淡水资源却很少只约占全球水储量的5.23%
C.稀土金属有“工业的维生素”的美誉,是不可再生的重要战略资源
D.石油分馏能得到汽油、煤油、柴油和煤焦油等燃料
10.物质的性质决定用途。下列物质的用途主要由其物理性质决定的是
A.二氧化碳作气体肥料 B.碳素墨水书写档案 C.氮气用于食品防腐 D.武德合金作保险丝
11.下列物质中,属于合金的是
A.生铁 B.水银 C.磁铁矿 D.金刚石
12.下列物质中不属于合金的是
A.不锈钢 B.黄铜 C.生铁 D.赤铁矿
13.物质的组成和结构决定性质,性质决定用途,下列叙述正确的是( )
A.石墨的质地较软,所以可用作干电池的电极
B.生铁坚硬,所以可用作医疗手术器械
C.一氧化碳和氧化碳的分子构成不同,所以二者的性质存在差异
D.金刚石和石墨组成元素相同,所以二者的物理性质相同
14.下列对事实的解释中,不合理的是
A.水变为水蒸气体积变大——水分子间间隔变大
B.金刚石和石墨物理性质差异较大——碳原子的结构不同
C.生铁和钢的性能不同——含碳量不同
D.硫在空气和氧气中燃烧的火焰颜色不同——氧气浓度不同
15.下列实验方案,不能达到相应实验目的是
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.下列反应属于置换反应的是( )
A.H2O+COCO2+H2
B.2KI+Cl2═2KCl+I2
C.2SO2+O2=2SO3
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O
二、综合题(共6题)
17.随着我国深潜器“蛟龙”号考察任务(考察可燃冰的海底出口)顺利完成,我国的“蓝鲸1号”在南海首次试采俗称可燃冰的天然气水合物也获得圆满成功。
(1)蛟龙号的大部分材料由钛合金构成,这是因为它____;(多选)
A.抗腐蚀性优于不锈钢 B.密度小、机械性能好 C.导电性好、硬度大
(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是____;“蓝鲸1号”整体用钢达40000多吨,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,该反应的化学方程式为____,反应前后氮元素的化合价变化为____。
(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少______(至少填两种物质的化学式)等有害气体的排放,可极大限度地减少空气污染。
18.依据所学知识回答问题
(1)网购、高铁、共享单车和打码支付被称为中国“新四大发明”。
①网购离不开光纤宽带。光纤的主要成分是SiO2,其中Si的化合价是_______。
②高铁车体的外壳由铝合金制成,用铝合金制作外壳的优点是_______(答一条)。
③共享单车的轮胎为实体轮胎,而普通自行车的轮胎在夏天易爆胎请用分子观点解释“夏天易爆胎”的原因_______。
④许多商品的二维码印在PVC不干胶贴纸上,PVC(化学式(C2H3C1)n)中碳、氢元素的质量比是_。
(2)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如下:
(其中,表示钠原子,表示氯原子, 表示氧原子)请回答题:
①A物质中氯元素的化合价为_______。
②D物质的名称是_______。
③该反应的化学方程式是_______。
19.我们的生活离不开化学。请回答下列问题。
(1)进入新装修的房间会闻到异味,这体现了粒子______的性质。人们常用活性炭来去除异味,这利用了活性炭的_____性。
(2)行外出旅游乘坐的飞机使用的航空煤油是由______炼制的产品。飞机的外壳主要是合金,这利用了镁铝合金的______性质。
A 密度小,材质轻 B 导电性 C 抗腐蚀性能好
20.2017年5月,国产大飞机C919成功进行首次试飞.请回答下列问题:
(1)图1中标示的材料中,属于有机合成材料的是 _____ ;
(2)飞机机身大量使用了铝合金材料.铝合金具有硬度大、密度小和 _____ 等优点;
(3)以金红石(主要成分是TiO2)为原料生产钛的流程如图2:其中“反应I”需要在高温条件下进行,反应的化学方程式为 _____ ;“反应II”中使用氩气的目的是 _____ ,该反应的基本反应类型属于 _____ 反应;
(4)现代民用飞机上使用的氧气发生器以氯酸钠为产氧剂,氯酸钠(NaClO3)中氯元素的化合价为 _____ ;
(5)C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能使燃油消耗减少16%.使用高密度空气的原因是 _____ .
21.开发利用氢能源是实现可持续发展的需要。根据图示分析,回答问题:
①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是_____(填序号)。
a.涤纶靠垫 b.橡胶轮胎 c.铜质导线 d.铝合金轮毂
②氢燃料电池的工作原理是:将氢气、氧气送到燃料电池中,经过催化剂的作用,发生反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式_____。
③氢气作燃料的优点是_____。
(2)工业上可通过下列工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
主反应器中反应的化学方程式是_____。膜反应器中的基本反应类型是_____。该工艺流程中,能被循环利用的物质是_____。
(3)采用电解水的方式制备10Kg氢气,理论上需要水的质量是多少千克?____
22.2019年12月16日,在我国西昌卫星发射中心,以“一箭双星”方式成功将第52、53颗北斗导航卫星送上了太空。随着这两颗卫星的升空,我国北斗三号全球系统核心星座部署完成。
(1)“长征三号乙”火箭发动机在焊接时需要使用氩弧焊。氩弧焊(如图)是在氩气保护下,通过在钨电极与焊件间产生的高压电弧放热,熔化焊丝或焊件的一种焊接技术。
①金属钨作电极是利用了金属钨的导电性和______;用氩气作保护气,是因为氩气的化学性质______。
②如果在没有保护气的情况下焊接金属,可能导致焊接不牢,原因是______。
(2)“长征三号乙”的第一、二级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)做推进剂,该反应的化学方程式为,则X的化学式是______。
(3)“长征三号乙”的第三级火箭采用液氢、液氧做推进剂。实验室可通过电解水得到氢气和氧气,氢气在与直流电源______极相连的电极上产生。氢能是未来最理想的能源,但目前应用并不广泛的原因是______(答一条即可)。
(4)北斗卫星的光伏发电板的主要构成材料是硅,单质硅由石英固体(SiO2)和碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是______。
参考答案
1.A
【详解】
A、钛合金与人体有很好的相容性,且性质稳定,抗腐蚀性强,所以可用来制造人造骨骼,故正确;
B、石墨具有良好的导电性,可用于制作石墨电极,故错误;
C、氮气的化学性质不活泼,可用作保护气,故错误;
D、稀有气体通电后发出不同颜色光,可用作不同用途的电光源,故错误。
故选A。
2.C
【详解】
A、生铁和钢都是铁的合金,生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,则生铁的含碳量高于钢的含碳量,故选项说法正确;B、不锈钢具有良好的抗腐蚀性能,抗腐蚀能力:不锈钢>纯铁,故选项说法正确;C、合金的硬度比组成它的纯金属的硬度大,硬度:纯铜<黄铜,故选项说法错误;D、合金的熔点比组成它的纯金属的熔点低,熔点:纯锡>武德合金,故选项说法正确。故选C。
3.C
【详解】
金属具有良好的导热性,不锈钢是良好的导热体,装木柄或塑料柄能起到很好的隔热作用,说明铁有良好的导热性。故选C。
4.B
【详解】
A.不是所有的金属熔点都很高,有一些金属熔点较低,例如:汞,故A错误;
B.金属具有良好的导电性,故B正确;
C.不是所有的金属硬度都很大,有一些金属的硬度很小,例如:铅硬度很小,故C错误;
D.金属不同,金属的颜色可能不同,如铁是银白色,但铜是紫红色,故D错误。
故选:B。
5.D
【详解】
A、铝锂合金密度小,故选项说法正确;
B、合金比组分金属硬度大,铝锂合金的硬度比纯铝大,故选项说法正确;
C、铝锂合金抗腐蚀性强,故选项说法正确;
D、铝锂合金属于金属材料,故选项说法错误。
故选D。
6.D
【详解】
A、不锈钢是指含铬13%以上的铁合金,铁是不锈钢的主要组成元素之一,故A正确;
B、合金的强度和硬度一般比组成它的纯金属更高,黄铜的硬度比纯铜大,故B正确
C、合金的抗腐蚀性能等比组成它的纯金属更好,不锈钢与黄铜都具有耐腐蚀的性能,故C正确;
D、碳化钨中含有一种物质,是一种纯净物,故D错误。故选D。
7.B
【分析】
【详解】
A、钢和生铁都是铁和碳的合金,是混合物,说法错误,故A不符合题意;
B、生铁和不锈钢都是金属材料,说法正确,故B符合题意;
C、合金的熔点比金属低,说法错误,故C不符合题意;
D、生锈的钢铁制品经过除锈之后,可以循环使用,说法错误,故D不符合题意;
故选B。
8.B
【详解】
A、石墨在一定条件下能与氧气反应,石墨烯的性质类似于石墨,故石墨烯在一定条件下能与氧气反应,正确;
B、石墨在常温下化学性质稳定,故石墨烯在常温下化学性质也稳定,错误;
C、烯合金具有优良的导电性 ,正确;
D、烯合金是一种新型材料,正确。故选B。
9.C
【详解】
试题分析:
A.氮气约占空气体积的78%,而不是质量的78%,所以A项错;
B.地球上水资源总量很大,但淡水资源却很少,在全球总储水量中只占2.53%,不是5.23%,所以B项错;
C.稀土金属是储量较少的一类金属的总称,它有“工业的维生素”的美誉,是不可再生的重要战略资源,所以C项正确;
D.煤焦油是煤经过干馏得到的,不是石油炼制得到的,所以D项错;
10.D
【详解】
A、二氧化碳使光合作用的原料,作气体肥料属于二氧化碳的化学性质,故选项错误;
B、碳素墨水书写档案是利用碳的稳定性,属于化学性质;故选项错误;
C、氮气用于食品防腐是利用氮气的化学性质不活泼,属于化学性质;故选项错误;
D、武德合金作保险丝是利用合金的熔点低,属于物理性质;故选项正确;
故选:D。
11.A
【详解】
A.生铁铁和碳的合金,属于合金;
B.水银是汞单质,不属于合金;
C.磁铁矿是指含有四氧化三铁的矿石,不属于合金;
D.金刚石是碳单质,不属于合金;
故选:A。
12.D
【详解】
A. 不锈钢是铁的合金,故错误;
B. 黄铜是铜的合金,故错误;
C. 生铁是含碳量较高的铁合金,故错误;
D. 赤铁矿是铁矿石,主要成分是氧化铁,故是混合物,不是合金,故正确。故选D。
13.C
【分析】
A、石墨具有导电性,所以可用作干电池的电极;
B、生铁接触到空气和水易发生锈蚀;
C、一氧化碳和二氧化碳的分子构成不同,所以二者的性质存在差异;
D、金刚石和石墨中碳原子排列方式不同,所以物理性质差异较大。
【详解】
A、石墨具有导电性,所以可用作干电池的电极,叙述错误,不符合题意;
B、生铁接触到空气和水易发生锈蚀,制造医疗手术器械应该用不锈钢,叙述错误,不符合题意;
C、一氧化碳和二氧化碳的分子构成不同,所以二者的性质存在差异,叙述正确,符合题意;
D、金刚石和石墨组成元素相同,所以二者的化学性质相同,二者中碳原子排列方式不同,所以物理性质差异较大,叙述错误,不符合题意。
故选C。
【详解】
A、分子间有间隔,水变为水蒸气体积变大是因为水分子间间隔变大,解释合理;
B、决定物质性质的是物质的组成和结构,金刚石和石墨物理性质差异较大,因为碳原子的排列方式不同,解释不合理;
C、生铁和钢的性能不同因为含碳量不同,生铁的含碳量比钢的高,解释合理;
D、硫在空气和氧气中燃烧的火焰颜色不同,因为氧气浓度不同,在纯氧中比在空气中燃烧更充分,解释合理。
故选B。
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.B
【详解】
A.H2O+COCO2+H2,反应物是两种化合物,不属于置换反应。
B.2KI+Cl2═2KCl+I2,是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应属于置换反应;
C.2SO2+O2=2SO3,反应物是两种,生成物是一种,属于“多变一”的化合反应;
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O,生成物是三种化合物,不属于置换反应。
故选:B。
【解析】
(1)蛟龙号的大部分材料由钛合金构成,这是因为它抗腐蚀性优于不锈钢,密度小、机械性能好;(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是化学能转化为内能转化为机械能再转化为电能,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,根据质量守恒定律可知:氯化铵和氧化铁在加热的条件下反应生成铁、氮气、水和氯化铁,该反应的化学方程式为6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3,反应前后氮元素的化合价变化-3价变为0价;(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少SO2、CO、NO2等有害气体的排放,可极大限度地减少空气污染。
18.
(1) +4 密度小 温度升高,分子间的间隔变大,体积膨胀 8:1
(2) +3 二氧化氯
【分析】
(1)
根据各元素的化合价的代数和为零,SiO2中氧元素的化合价为-2价,所以Si的化合价是+4价;
铝合金具有密度小,机械强度大 、抗腐蚀性强等优点;
夏天易爆胎”的原因是温度升高,分子运动剧烈,分子间的间隙增大,气体的体积膨胀;
PVC【化学式(C2H3C1)n】中碳、氢元素的质量比是
故填:+4;密度小;温度升高,分子间的间隔变大,体积膨胀;8:1
(2)
由微观示意图可知该反应方程式为:,所以A为NaClO2中钠元素的化合价为+1价,氧元素的化合价为-2价,根据元素的化合价的代数和为零,所以物质中氯元素的化合价为+3价;
D为ClO2,名称为二氧化氯;
该反应的化学方程式是:
故填:+3;二氧化氯;
19.不断运动 吸附 石油 AC
【详解】
(1)新装修的房间里污染气体主要是甲醛,由于甲醛分子的不断运动,使得整个房间充满异味,活性炭可以吸附气体,因此可以吸收有毒的甲醛气体,故答案为不断运动,吸附;
(2)航空煤油是由石油炼制的,由于石油为不可再生资源,因此煤油也是不可再生资源,飞机的外壳是铝镁合金,具有密度小,材质轻,抗腐蚀性能好的优点,故答案为石油,AC.
20.合成橡胶 抗腐蚀性好 TiO2+2C+2Cl2TiCl4+2CO 作保护气防止金属氧化 置换反应 +5 提供足够的氧气,使燃油燃烧更充分
【分析】
(1)(2)(3)根据已有的材料的类别、合金的性质以及化学方程式的书写的知识进行分析解答即可;
(4)化合价的代数和为零;
(5)从微观角度对现象进行解释,节约了能源,也就是保护了环境;
【详解】
(1)图中标示的材料中,合成橡胶属于有机合成材料;故填:合成橡胶;
(2)合金与组成它的成分相比较,一般情况下是密度小、硬度大、抗腐蚀性好,故答案为抗腐蚀性好;
(3)在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体是一氧化碳,反应的化学方程式为:TiO2+2C+2Cl2TiCl4+2CO; Mg容易被氧气氧化,使用氩气防止镁被氧化;在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,属于置换反应;故答案为TiO2+2C+2Cl2TiCl4+2CO;作保护气防止金属氧化;置换反应;
(4)设NaClO3中氯元素的化合价为x,由于钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合价的代数和为零可得(+1)+x+(-2×3)=0,解得x=+5,故答案为+5;
(5)高密度空气能使航空煤油更充分燃烧的微观原因是高密度空气中的氧分子与煤油分子接触更充分,使燃油燃烧更充分;故答案为供足够的氧气,使燃油燃烧更充分。
21.CD 2H2+O22H2O 燃烧产物是水,对环境无污染 2H2O+SO2+I2=H2SO4+2HI 分解反应 I2 90kg
【详解】
(1)①涤纶和合成橡胶属于合成材料;铜和铝合金属于金属材料;故填:CD;
②氢气与氧气在催化剂的作用下生成水;故填:2H2+O22H2O;
③氢气的热值高,氢气燃烧生成水,对环境无污染;故填:燃烧产物是水,对环境无污染;
(2)主反应器中反应是水和二氧化硫以及碘反应生成硫酸和碘化氢,对应的化学方程式是 2H2O+SO2+I2=H2SO4+2HI.膜反应器中是碘化氢分解为氢气和碘,为一变多,符合分解反应特征,属于分解反应。该工艺流程中,开始碘作为反应物,后来是生成物,所以能被循环利用的物质是 I2.故填:2H2O+SO2+I2=H2SO4+2HI;分解反应; I2;
(3)解:设需要水的质量为x,则:
x=90kg
答:理论上需要水90kg。
22.熔点高 不活泼 生成金属氧化物 CO2 负 制取成本高(贮存与运输困难等,合理答案答出一条即可)
【详解】
(1)金属钨作电极是利用了金属钨的导电性和熔点高;氩气是惰性气体,用氩气作保护气,是因为氩气的化学性质很不活泼;如果在没有保护气的情况下焊接金属,金属和空气中的氧气反应生成氧化物,可能导致焊接不牢;故①②③分别填:熔点高;不活泼;生成金属氧化物。
(2)在化学方程式中,反应物中C的个数为2,H的个数为8,N 的个数为6,O的个数为8;在生成物中N的个数为6个,H 的个数为8,所以,一个 X 中含有C的个数为1,含有O的个数为2,故X的化学式为CO2,故④填:CO2。
(3)根据“正氧负氢、氢二氧一”进行分析可知,氢气在与直流电源负极相连的电极上产生,因制取氢气是利用水分解得到,但水的分解一般需要电解,则制取成本高,因此目前应用并不广泛,故⑤⑥分别填:负;制取成本高(答案合理即可)。
(4)二氧化硅和碳在高温的条件下生成硅和一氧化碳,其化学方程式为:。
同课章节目录
