第十单元酸和碱 课题1 常见的酸和碱 同步练习—2021—2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第十单元酸和碱 课题1 常见的酸和碱 同步练习—2021—2022学年九年级化学人教版下册(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 147.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-16 00:00:00 | ||
图片预览



文档简介
2021——2022学年度人教版九年级化学下册 第十单元酸和碱 课题1 常见的酸和碱 同步练习
一、选择题
1.下列气体能使紫色石蕊溶液变红的是
A.CO2 B.O2 C.H2 D.N2
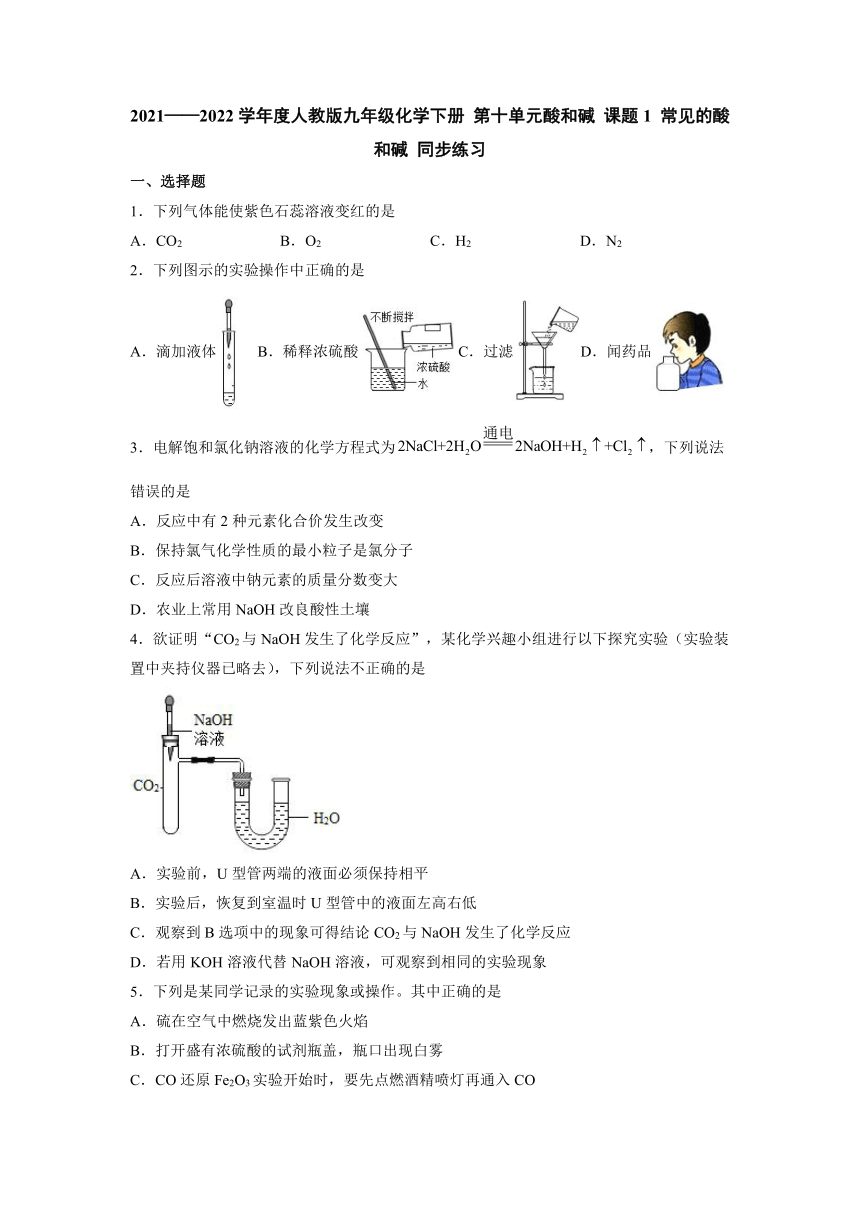
2.下列图示的实验操作中正确的是
A.滴加液体B.稀释浓硫酸C.过滤D.闻药品
3.电解饱和氯化钠溶液的化学方程式为,下列说法错误的是
A.反应中有2种元素化合价发生改变
B.保持氯气化学性质的最小粒子是氯分子
C.反应后溶液中钠元素的质量分数变大
D.农业上常用NaOH改良酸性土壤
4.欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去),下列说法不正确的是
A.实验前,U型管两端的液面必须保持相平
B.实验后,恢复到室温时U型管中的液面左高右低
C.观察到B选项中的现象可得结论CO2与NaOH发生了化学反应
D.若用KOH溶液代替NaOH溶液,可观察到相同的实验现象
5.下列是某同学记录的实验现象或操作。其中正确的是
A.硫在空气中燃烧发出蓝紫色火焰
B.打开盛有浓硫酸的试剂瓶盖,瓶口出现白雾
C.CO还原Fe2O3实验开始时,要先点燃酒精喷灯再通入CO
D.在滴有石蕊试液的氢氧化钠溶液中逐滴加入稀盐酸至过量,溶液颜色变化为蓝色、紫色、红色
6.下列有关说法正确的是
A.少量浓硫酸沾到手上,先用大量水冲洗,后涂上硼酸溶液
B.过滤时,玻璃棒下端应轻靠三层滤纸处
C.为了防止因潮解而变质,烧碱必须密封保存
D.配制氯化钠溶液时,液体飞溅一定会导致浓度减小
7.氢化钙(CaH2)常作供氢剂,遇水剧烈反应放出氢气。某学习小组设计如图实验制备氢化钙。下列说法正确的是
A.仪器不变,也可将装置Ⅰ中的粗锌粒换成锌粉
B.装置Ⅱ、Ⅲ盛装试剂依次为浓硫酸、NaOH溶液
C.去除装置V对制备氢化钙没有任何影响
D.氢化钙遇水反应的化学方程式为:
8.向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得到不溶物和滤液。在滤液中插入锌片,有气泡产生。则下列判断不正确的是( )
A.不溶物中一定含有铜 B.滤液中一定含有硫酸
C.不溶物中一定含有铁 D.滤液中一定含有硫酸亚铁
9.X、Y、Z有如图所示的转化(“→”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z依次为
A. B.
C. D.
10.为从废铜屑中得到较纯的单质铜设计了如下方案。有关说法正确的是 ( )
A.若X是铁,第③步反应还会生成氯化铁
B.X还可以是Zn,但不能是Ag
C.不需要第②步操作,直接进行第③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
11.只用一种试剂来鉴别NaOH溶液、澄清石灰水、稀H2SO4三种无色溶液,可以选用下列物质中的
A.无色酚酞试液 B.二氧化碳 C.铁粉 D.纯碱溶液
12.向铁粉和CuO的混合物中加入一定量的稀硫酸,微热,充分反应后冷却、过滤,向所得滤液中放入一枚洁净的铁钉,发现铁钉表面无任何变化,据此判断,下列结论正确的是( )
A.滤液中一定含有FeSO4,可能含有H2SO4 B.滤液中可能有CuSO4
C.滤渣里一定有Cu,可能有Fe和CuO D.滤渣里一定有Cu和Fe
13.将一定质量的某液体盛于烧杯中,敞口放置在实验室安全之处。绘制溶液质量与放置天数的图像如下图(不考虑水分的蒸发),有关描述不正确的是
A.甲可能是浓硫酸 B.乙可能是氯化钠溶液
C.丙可能是稀盐酸 D.丁可能是氢氧化钠溶液
14.已知,无水在时可发生如下反应:。取无水,在时充分加热,使之完全分解。将产生的气体产物通入足量浓硫酸(已知气体不能被浓硫酸吸收),浓硫酸质量增加,再通过溶液,溶液质量增加。则下列说法正确的是( )
A.化学式可能是 B.剩余固体的质量为
C.生成和气体的总质量为 D.方程式中
二、填空题
15.结合NaOH、Ca(OH)2的相关知识,回答下列问题
(1)能用来鉴别NaOH、Ca(OH)2的物质是__________;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是_________;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是______。
16.一辆载有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄漏,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡。泄漏出来的硝酸不断流进路边的排水沟,气味十分刺鼻。
(1)由题给信息可知,硝酸的物理性质是 ___________________________ (任写一条)。
(2)硝酸见光后,除分解生成二氧化氮气体外,还生成水及占空气体积分数约21%的气体。实验室保存硝酸应密封、避光保存在棕色瓶内,放在低温阴凉处。请写出硝酸见光分解的化学方程式。 ___________
(3)为消除硝酸对环境的污染,对泄漏的酸必须处理,请指出一种经济上合理、对环境污染小的化学处理方法。 ___________
17.下图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,B、C常温下是无色气体,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态氧化物,试回答下列问题:
(1)已知A含有三种元素,则A的俗名是 _______ ;F的化学式为: ______ 。
(2)上述物质转化过程中:B + X → C属于 _____________ 反应类型。
(3)指出C的一种用途 __ ,写出C + Y → D的化学方程式 ____________________________ 。
(4)若反应E→F为中和反应,应则E的化学式为 ___ 。
18.A、B、C、D是初中化学中的常见物质,它们之间有如图所示的转化关系,请根据有关信息写出相关反应的化学方程式:
①若该反应属复分解反应,其中B是钠盐,C是BaSO4:___________________________________
②若C为一种最轻的气体,且D溶液呈浅绿色:_____________________________
19.① 小明同学将一根生锈的铁丝放入过量的稀盐酸里,他观察到的现象是铁锈逐渐溶解,______________,请写出盐酸与铁锈反应的化学方程式_________________________。
② 小红在AgNO3和Cu(NO3)2的混合液中,加入一定量的锌粉,根据下述实验现象分析:
a.溶液呈蓝色,此时溶液中的溶质成分:__________________________,
b.溶液呈无色,此时析出金属的成分:____________________________。
20.某同学设计用如下图所示的装置将二氧化碳和一氧化碳进行分离和干燥。a、b均为活塞,供选择的试剂:足量的NaOH溶液、浓H2SO4、稀盐酸。(NaOH溶液能吸收CO2,其原理和澄清石灰水与CO2反应相似;浓浓H2SO4具有吸水性,能做干燥剂)。试回答:
(1)左瓶中应装的是_________溶液,右瓶中应装的是_______溶液,分液漏斗中应装的是_______溶液。
(2)当CO与CO2的混合气体通过该装置时,先分离得到的是_______,活塞操作是_______________________,此时发生反应的化学方程式为___________________________;
然后得到的是__________。活塞操作是___________________________。
三、简答题
21.生活中用洗涤剂 汽油 氢氧化钠处理油污,请说明它们的原理有何不同
22.现有生活中的两瓶无色溶液,分别是氢氧化钙溶液和稀醋酸溶液。试用三种不同的方法鉴别(不要求写出具体的操作过程和实验现象)。
(1)___________________________________________________ ;
(2)____________________________________________________;
(3)____________________________________________________。
23.金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,溶液变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
(1)溶液红色褪去说明溶液的碱性____________________________________________
(填“增强”或“减弱”)。
(2)据你推测,导致溶液碱性变化的原因可能是________________________。
(3)设计一个实验来验证你的一种推测,简要说明操作、现象及结论:______________________________________________________________。
24.设计实验和数据分析是学习化学重要的能力。
①利用酚酞溶液和氢氧化钠溶液,合理设计一个实验证明同浓度的浓盐酸敞口放置比密封的浓度变小了。_____。
②乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,将变质后溶液加热蒸干,称量所得固体质量为a,求a的取值范围_____。
四、综合应用题
25.实验是科学探究的重要途径。
(1)结合下列化学实验装置,回答有关问题。
①写出一个用A装置制取O2的化学方程式_____。
②若用B装置制取能使澄清的石灰水变浑浊的气体,则实验室制取该气体的化学方程式是__。与B相比较,C的主要优点是什么______。
③用试管采用排空气法收集氢气,请在D方框中画出装置图(只画试管和导气管)______。
(2)用实验室存放的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是红红判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因______。
为探究氢氧化钠是否完全变质,红红设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶红色。于是明明认为样品中还会有氢氧化钠,没有完全变质。
①康康认为红红的两个实验方案都不能达到目的,他的理由是____。
②请你设计一个方案来验证氢氧化钠是否完全变质。______。
工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。请计算废水中氯化氢的质量分数__。
【参考答案】
1.A 2.B 3.D 4.C 5.D 6.B 7.D 8.C 9.D 10.B 11.D 12.C 13.D 14.B
15.二氧化碳(或Na2CO3等) 都含有氢氧根离子 碳酸钠
16.有挥发性或有刺激性气味 4HNO34NO2↑+2H2O+O2↑ 洒熟石灰
17.纯碱 H2O 化合 燃料(或冶金) CuO + CO ==Cu + CO2 NaOH
18.Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3 Fe+2HCl═FeCl2+H2↑
19.溶液由无色变为黄色,产生气泡,溶液由黄色变成浅绿色 Fe2O3+6HCl=2FeCl3+3H2O 一定含有Cu(NO3)2、Zn(NO3)2,可能含有AgNO3 一定含有Ag、Cu,可能含有Zn
20.NaOH 浓 H2SO4 稀盐酸 CO 关a开b CO2 + 2NaOH=Na2CO3 + H2O CO2 关b开a
21.洗涤剂:乳化;汽油:溶解;氢氧化钠:与油污发生化学反应
22.滴加紫色石蕊试液 加入锌粒 滴加碳酸钠溶液(合理答案均可)
23.减弱 溶液吸收了空气中的CO2 做对比实验,让上述红色溶液分别在与空气接触、隔绝空气的条件下冷却,若前者褪色后者不褪色,则证明空气中的CO2使溶液碱性减弱,导致红色褪去
24.取两支试管,分别加入同一氢氧化钠溶液等量,分别加入相同滴数的酚酞试液,然后分别滴入敞口放置的浓盐酸和密封放置的浓盐酸,直到溶液恰好红色消失,记录所加盐酸的滴数,滴数越多证明浓度越低。 4.00~5.30。
25. 可以控制反应速度 方案1中,碳酸钠溶液也能使酚酞溶液变红,方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 1.46%
一、选择题
1.下列气体能使紫色石蕊溶液变红的是
A.CO2 B.O2 C.H2 D.N2
2.下列图示的实验操作中正确的是
A.滴加液体B.稀释浓硫酸C.过滤D.闻药品
3.电解饱和氯化钠溶液的化学方程式为,下列说法错误的是
A.反应中有2种元素化合价发生改变
B.保持氯气化学性质的最小粒子是氯分子
C.反应后溶液中钠元素的质量分数变大
D.农业上常用NaOH改良酸性土壤
4.欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去),下列说法不正确的是
A.实验前,U型管两端的液面必须保持相平
B.实验后,恢复到室温时U型管中的液面左高右低
C.观察到B选项中的现象可得结论CO2与NaOH发生了化学反应
D.若用KOH溶液代替NaOH溶液,可观察到相同的实验现象
5.下列是某同学记录的实验现象或操作。其中正确的是
A.硫在空气中燃烧发出蓝紫色火焰
B.打开盛有浓硫酸的试剂瓶盖,瓶口出现白雾
C.CO还原Fe2O3实验开始时,要先点燃酒精喷灯再通入CO
D.在滴有石蕊试液的氢氧化钠溶液中逐滴加入稀盐酸至过量,溶液颜色变化为蓝色、紫色、红色
6.下列有关说法正确的是
A.少量浓硫酸沾到手上,先用大量水冲洗,后涂上硼酸溶液
B.过滤时,玻璃棒下端应轻靠三层滤纸处
C.为了防止因潮解而变质,烧碱必须密封保存
D.配制氯化钠溶液时,液体飞溅一定会导致浓度减小
7.氢化钙(CaH2)常作供氢剂,遇水剧烈反应放出氢气。某学习小组设计如图实验制备氢化钙。下列说法正确的是
A.仪器不变,也可将装置Ⅰ中的粗锌粒换成锌粉
B.装置Ⅱ、Ⅲ盛装试剂依次为浓硫酸、NaOH溶液
C.去除装置V对制备氢化钙没有任何影响
D.氢化钙遇水反应的化学方程式为:
8.向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得到不溶物和滤液。在滤液中插入锌片,有气泡产生。则下列判断不正确的是( )
A.不溶物中一定含有铜 B.滤液中一定含有硫酸
C.不溶物中一定含有铁 D.滤液中一定含有硫酸亚铁
9.X、Y、Z有如图所示的转化(“→”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z依次为
A. B.
C. D.
10.为从废铜屑中得到较纯的单质铜设计了如下方案。有关说法正确的是 ( )
A.若X是铁,第③步反应还会生成氯化铁
B.X还可以是Zn,但不能是Ag
C.不需要第②步操作,直接进行第③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
11.只用一种试剂来鉴别NaOH溶液、澄清石灰水、稀H2SO4三种无色溶液,可以选用下列物质中的
A.无色酚酞试液 B.二氧化碳 C.铁粉 D.纯碱溶液
12.向铁粉和CuO的混合物中加入一定量的稀硫酸,微热,充分反应后冷却、过滤,向所得滤液中放入一枚洁净的铁钉,发现铁钉表面无任何变化,据此判断,下列结论正确的是( )
A.滤液中一定含有FeSO4,可能含有H2SO4 B.滤液中可能有CuSO4
C.滤渣里一定有Cu,可能有Fe和CuO D.滤渣里一定有Cu和Fe
13.将一定质量的某液体盛于烧杯中,敞口放置在实验室安全之处。绘制溶液质量与放置天数的图像如下图(不考虑水分的蒸发),有关描述不正确的是
A.甲可能是浓硫酸 B.乙可能是氯化钠溶液
C.丙可能是稀盐酸 D.丁可能是氢氧化钠溶液
14.已知,无水在时可发生如下反应:。取无水,在时充分加热,使之完全分解。将产生的气体产物通入足量浓硫酸(已知气体不能被浓硫酸吸收),浓硫酸质量增加,再通过溶液,溶液质量增加。则下列说法正确的是( )
A.化学式可能是 B.剩余固体的质量为
C.生成和气体的总质量为 D.方程式中
二、填空题
15.结合NaOH、Ca(OH)2的相关知识,回答下列问题
(1)能用来鉴别NaOH、Ca(OH)2的物质是__________;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是_________;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是______。
16.一辆载有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄漏,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡。泄漏出来的硝酸不断流进路边的排水沟,气味十分刺鼻。
(1)由题给信息可知,硝酸的物理性质是 ___________________________ (任写一条)。
(2)硝酸见光后,除分解生成二氧化氮气体外,还生成水及占空气体积分数约21%的气体。实验室保存硝酸应密封、避光保存在棕色瓶内,放在低温阴凉处。请写出硝酸见光分解的化学方程式。 ___________
(3)为消除硝酸对环境的污染,对泄漏的酸必须处理,请指出一种经济上合理、对环境污染小的化学处理方法。 ___________
17.下图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,B、C常温下是无色气体,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态氧化物,试回答下列问题:
(1)已知A含有三种元素,则A的俗名是 _______ ;F的化学式为: ______ 。
(2)上述物质转化过程中:B + X → C属于 _____________ 反应类型。
(3)指出C的一种用途 __ ,写出C + Y → D的化学方程式 ____________________________ 。
(4)若反应E→F为中和反应,应则E的化学式为 ___ 。
18.A、B、C、D是初中化学中的常见物质,它们之间有如图所示的转化关系,请根据有关信息写出相关反应的化学方程式:
①若该反应属复分解反应,其中B是钠盐,C是BaSO4:___________________________________
②若C为一种最轻的气体,且D溶液呈浅绿色:_____________________________
19.① 小明同学将一根生锈的铁丝放入过量的稀盐酸里,他观察到的现象是铁锈逐渐溶解,______________,请写出盐酸与铁锈反应的化学方程式_________________________。
② 小红在AgNO3和Cu(NO3)2的混合液中,加入一定量的锌粉,根据下述实验现象分析:
a.溶液呈蓝色,此时溶液中的溶质成分:__________________________,
b.溶液呈无色,此时析出金属的成分:____________________________。
20.某同学设计用如下图所示的装置将二氧化碳和一氧化碳进行分离和干燥。a、b均为活塞,供选择的试剂:足量的NaOH溶液、浓H2SO4、稀盐酸。(NaOH溶液能吸收CO2,其原理和澄清石灰水与CO2反应相似;浓浓H2SO4具有吸水性,能做干燥剂)。试回答:
(1)左瓶中应装的是_________溶液,右瓶中应装的是_______溶液,分液漏斗中应装的是_______溶液。
(2)当CO与CO2的混合气体通过该装置时,先分离得到的是_______,活塞操作是_______________________,此时发生反应的化学方程式为___________________________;
然后得到的是__________。活塞操作是___________________________。
三、简答题
21.生活中用洗涤剂 汽油 氢氧化钠处理油污,请说明它们的原理有何不同
22.现有生活中的两瓶无色溶液,分别是氢氧化钙溶液和稀醋酸溶液。试用三种不同的方法鉴别(不要求写出具体的操作过程和实验现象)。
(1)___________________________________________________ ;
(2)____________________________________________________;
(3)____________________________________________________。
23.金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,溶液变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
(1)溶液红色褪去说明溶液的碱性____________________________________________
(填“增强”或“减弱”)。
(2)据你推测,导致溶液碱性变化的原因可能是________________________。
(3)设计一个实验来验证你的一种推测,简要说明操作、现象及结论:______________________________________________________________。
24.设计实验和数据分析是学习化学重要的能力。
①利用酚酞溶液和氢氧化钠溶液,合理设计一个实验证明同浓度的浓盐酸敞口放置比密封的浓度变小了。_____。
②乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,将变质后溶液加热蒸干,称量所得固体质量为a,求a的取值范围_____。
四、综合应用题
25.实验是科学探究的重要途径。
(1)结合下列化学实验装置,回答有关问题。
①写出一个用A装置制取O2的化学方程式_____。
②若用B装置制取能使澄清的石灰水变浑浊的气体,则实验室制取该气体的化学方程式是__。与B相比较,C的主要优点是什么______。
③用试管采用排空气法收集氢气,请在D方框中画出装置图(只画试管和导气管)______。
(2)用实验室存放的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是红红判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因______。
为探究氢氧化钠是否完全变质,红红设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶红色。于是明明认为样品中还会有氢氧化钠,没有完全变质。
①康康认为红红的两个实验方案都不能达到目的,他的理由是____。
②请你设计一个方案来验证氢氧化钠是否完全变质。______。
工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。请计算废水中氯化氢的质量分数__。
【参考答案】
1.A 2.B 3.D 4.C 5.D 6.B 7.D 8.C 9.D 10.B 11.D 12.C 13.D 14.B
15.二氧化碳(或Na2CO3等) 都含有氢氧根离子 碳酸钠
16.有挥发性或有刺激性气味 4HNO34NO2↑+2H2O+O2↑ 洒熟石灰
17.纯碱 H2O 化合 燃料(或冶金) CuO + CO ==Cu + CO2 NaOH
18.Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3 Fe+2HCl═FeCl2+H2↑
19.溶液由无色变为黄色,产生气泡,溶液由黄色变成浅绿色 Fe2O3+6HCl=2FeCl3+3H2O 一定含有Cu(NO3)2、Zn(NO3)2,可能含有AgNO3 一定含有Ag、Cu,可能含有Zn
20.NaOH 浓 H2SO4 稀盐酸 CO 关a开b CO2 + 2NaOH=Na2CO3 + H2O CO2 关b开a
21.洗涤剂:乳化;汽油:溶解;氢氧化钠:与油污发生化学反应
22.滴加紫色石蕊试液 加入锌粒 滴加碳酸钠溶液(合理答案均可)
23.减弱 溶液吸收了空气中的CO2 做对比实验,让上述红色溶液分别在与空气接触、隔绝空气的条件下冷却,若前者褪色后者不褪色,则证明空气中的CO2使溶液碱性减弱,导致红色褪去
24.取两支试管,分别加入同一氢氧化钠溶液等量,分别加入相同滴数的酚酞试液,然后分别滴入敞口放置的浓盐酸和密封放置的浓盐酸,直到溶液恰好红色消失,记录所加盐酸的滴数,滴数越多证明浓度越低。 4.00~5.30。
25. 可以控制反应速度 方案1中,碳酸钠溶液也能使酚酞溶液变红,方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 1.46%
同课章节目录
