第二章 物质转化与材料利用 -提升训练(含答案) --2021—2022学年浙教版科学九年级上学期
文档属性
| 名称 | 第二章 物质转化与材料利用 -提升训练(含答案) --2021—2022学年浙教版科学九年级上学期 |

|
|
| 格式 | docx | ||
| 文件大小 | 223.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-20 00:00:00 | ||
图片预览



文档简介
第二章 物质转化与材料利用
一、选择题
1.下列物质中,有一种与其它三种物质不属于同一类别的是( )
A.纯碱 B.氨水 C.熟石灰 D.苛性钠
2.天平两边各放质量相等的烧杯,分别盛有等质量、等质量分数的足量稀硫酸,此时天平平衡。然后在两边的烧杯中各加入下列物质,充分反应后天平仍保持平衡的是( )
①10克铁和10克氧化铁
②10克铜和10克氧化铜
③5.6克铁和6.5克锌
④6.5克锌和6.3克氧化锌
A.①②③ B.①②④ C.②④ D.③④
3.风寒感冒时,中医建议用生姜水泡脚。因为生姜中含有姜辣素(C17H26O4),能使血管扩张,促进血液循环。从物质的分类角度来看,姜辣素属于( )
A.混合物 B.氧化物 C.有机化合物 D.无机化合物
4.古代金属锡的治炼发生的反应主要是:SnO2+2CSn+2CO↑下列分析正确的是( )
A.生成的CO可以用氢氧化钠溶液吸收
B.反应类型属于复分解反应
C.反应过程中化合价没有发生改变
D.二氧化锡是氧化物
5.下列物质中属于有机物的是( )
A.CO2 B.CaCO3 C.H2CO3 D.C2H6O
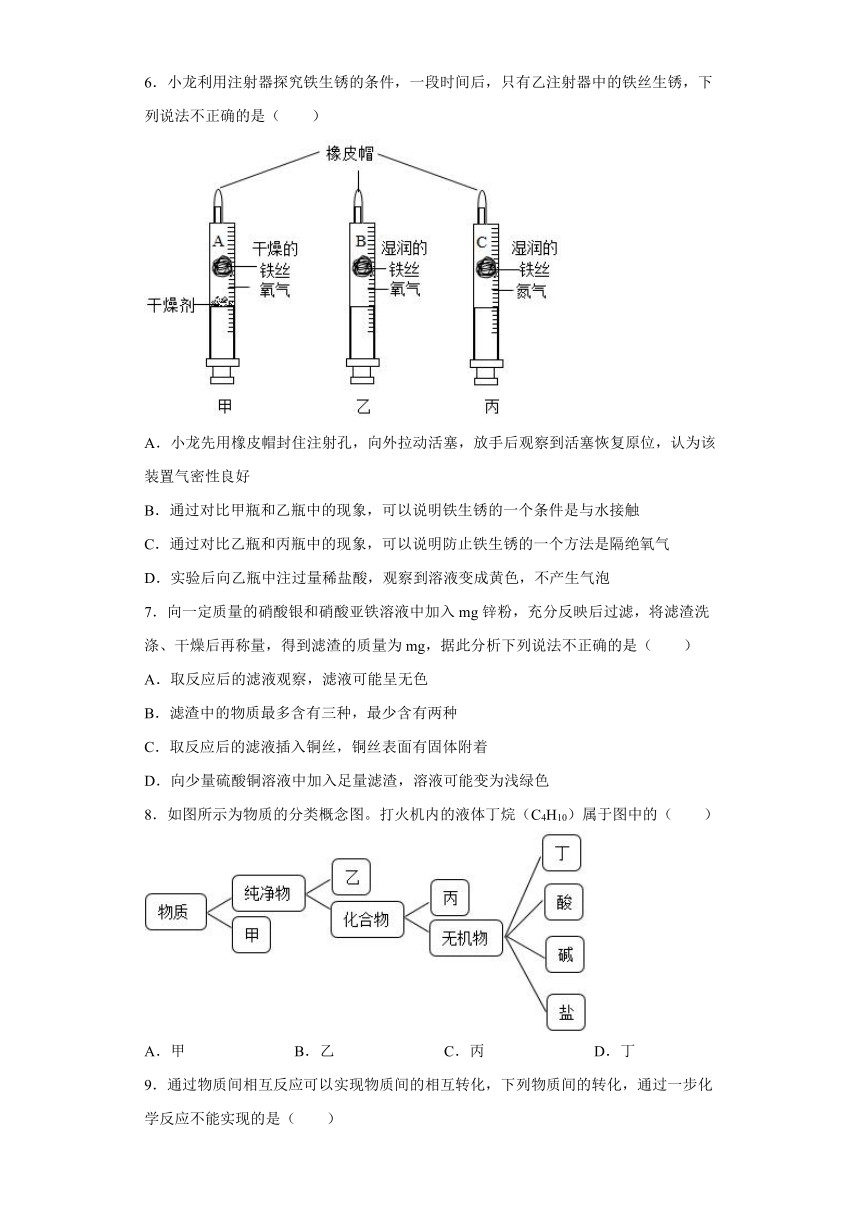
6.小龙利用注射器探究铁生锈的条件,一段时间后,只有乙注射器中的铁丝生锈,下列说法不正确的是( )
A.小龙先用橡皮帽封住注射孔,向外拉动活塞,放手后观察到活塞恢复原位,认为该装置气密性良好
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比乙瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向乙瓶中注过量稀盐酸,观察到溶液变成黄色,不产生气泡
7.向一定质量的硝酸银和硝酸亚铁溶液中加入mg锌粉,充分反映后过滤,将滤渣洗涤、干燥后再称量,得到滤渣的质量为mg,据此分析下列说法不正确的是( )
A.取反应后的滤液观察,滤液可能呈无色
B.滤渣中的物质最多含有三种,最少含有两种
C.取反应后的滤液插入铜丝,铜丝表面有固体附着
D.向少量硫酸铜溶液中加入足量滤渣,溶液可能变为浅绿色
8.如图所示为物质的分类概念图。打火机内的液体丁烷(C4H10)属于图中的( )
A.甲 B.乙 C.丙 D.丁
9.通过物质间相互反应可以实现物质间的相互转化,下列物质间的转化,通过一步化学反应不能实现的是( )
A.CaO→Ca(OH)2→CaCO3 B.Mg→MgO→MgCl2
C.CuO→Cu(OH)2→CuCl2 D.NaOH→NaCl→NaNO3
10.将 Fe3O4、Fe2O3、CuO的固体混合粉末mg,在加热条件下用足量CO还原得到金属混合物2.32g,将生成的CO2气体用足量澄清石灰水吸收后,产生5.00g白色沉淀,则m的数值为( )
A.5.32 B.3.12 C.3.59 D.2.37
11.现有铁粉、二氧化锰、硫酸钡和铁矿石四种固体,为了区分它们,小盟参照二歧分类法,制作了如图的检索表。下列叙述错误的是( )
1a 只含一种物质………2 1b 含有多种物质………甲 2a 只含一种元素………乙 2b 含有多种元素………3 3a ___________……………丙 3b 白色固体……………丁
A.甲表示的是铁矿石
B.乙表示的是铁粉
C.表中“___________”应该表示为“黑色固体”
D.也可根据是否含有氧元素对丙、丁分类
12.飞机的制造材料主要是铝合金。一架普通的飞机,差不多要用50万个铝合金做的铆钉,飞机的外壳、机翼、机尾螺旋桨、引擎的许多部件也是用铝合金制成的。对此,下列叙述错误的是( )
A.铝合金的导电性极差,使飞机不容易被闪电击中
B.铝的密度比较小,大量使用铝材能减小飞机质量,有利于飞行
C.铝的表面容易形成致密的氧化物保护膜,不容易生锈
D.飞机材料采用铝合金而不用纯铝的主要原因,是纯铝比较软而铝合金比较硬
二、填空题
13.某城市有甲、乙两工厂排放污水,污水中各含有下列6种离子中的3种(两厂不含相同离子,其中甲厂的污水能使酚酞试液变红:H+、Ba2+、Na+、OH-、CO32-、NO3-,甲厂含有的离子是_______;两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清的只含一种溶质的溶液,此溶液的溶质是_______(填化学名称)。
14.人人行动,推进垃圾分类,推动绿色、健康、可持续发展。
(1)垃圾分类回收是我县创建文明城市的一项重要举措。如图所示是街道垃圾桶。
①使用铝合金做内筒的优点是_______(写出一点即可)。
②某品牌饮料的空易拉罐应收入_______(选填“可回收”或“不可回收”)筒中。
(2)在农村,人们把秸秆、杂草、人畜粪便等废弃物放在密闭的池中发酵可获得沼气(主要成分是甲烷),沼气是很好的燃料,可用于家庭烹调、取暖和照明。
①甲烷(CH4)属于_______(选填“无机”或“有机”)化合物。
②甲烷在空气中完全燃烧的化学方程式为:CH4+2O2CO2+2H2O。丁烷燃烧的化学方程式为:2C4H10+13O28CO2+10H2O,相同条件下,气体体积比等于分子数比。若小明家由石油液化气(主要成分是丁烷)改为沼气,需要进行灶具的调整。改为沼气后,同体积燃料燃烧消耗空气的体积将_______(选填“增大”或“减小”),灶具的调整方法是减_______(选填“燃料”或“空气”)的进气量。
③甲烷是一种无色、无味的气体,密度比空气小。为了安全,在小明家厨房安装沼气泄漏报警器。根据甲烷的性质可知,图中_______(选填“a”或“b”)位置的安装是正确的。
(3)垃圾焚烧发电厂的建成,能缓解城市垃圾过多带来的危害。
①垃圾焚烧发电是利用了储存在垃圾中的_______能。
②下列与垃圾有关的各种说法中不科学的有_______(选填字母)。
A.垃圾发电厂可以有效地处理所有垃圾,并且没有任何污染
B.垃圾也是一种重要的资源,应对垃圾分类处理,综合利用
C.生活中的垃圾可以随意丢弃,因为它们很快都能被自然界分解
D.垃圾中塑料制品不要随意丢弃,避免白色污染
15.从古代到现代,材料的种类越来越多,用途也越来越广泛。请回答:
(1)早在西汉时期,我国就有湿法炼铜的记载,将铁置于硫酸铜溶液中得到铜单质,该反应属于______(填基本反应类型)。
(2)现代社会,玻璃是一种常见的非金属材料,SiO2是生产玻璃的原料之一。SiO2属于______ (选填“酸”、“碱”、“盐”或“氧化物”)。
16.铜是人类最早利用的金属之一。
(1)下列铜制品中,利用金属导热性的是________(填字母序号)。
(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为__________。
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):
已知:2Cu+2H2SO4+O22CuSO4+2H2O
①过程Ⅱ中分离操作的名称是_________。
②过程Ⅲ中有气体产生,反应的化学方程式为_________。
③A~E中含铜、锌两种元素的物质有______(填字母序号)。
17.下列分别盛有不同物质的容器中,所盛物质属于单质的是_____,化合物的是_____,混合物的是________,(均填容器下的代号)
18.用序号填空,下列物质中属于氧化物的是______,属于盐的是______。
A.H2O B.HNO3 C.BaC12 D.Zn E.Fe(OH)3
三、简答题
19.将未经砂布打磨的铝条放入盛有足量稀硫酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示。
(1)由图象可知密闭容器内发生了_____反应(选填“吸热”或“放热”);
(2)请对曲线各部分变化情况作出解释_____。
20.钢铁工业是一个国家的支柱产业之一,某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如图所示装置进行分析。分别称得锥形瓶与棉花的质量为44.1g,生铁样品的质量为9.0g。在锥形瓶中加入足量稀硫酸后,立即开始记录电子天平的示数,记录数据如图所示。
请认真分析数据,回答下列问题:
(1)如何判断试验中生铁样品已经完全反应。___________
(2)根据电子天平的数据变化进行分析,如图丙图像中正确的是___________
(3)计算反应后所得溶液中硫酸亚铁的质量分数___________。
四、探究题
21.半水煤气是工业合成氨的原料气,其主要成分是 H2、CO、CO2、N2和水蒸气。某科学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。
查阅资料可知碱石灰是 CaO 和 NaOH 的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,其反应的化学方程式是______。
(2)D装置中“冰水”的作用是______。
(3)实验结果证明有H2、CO、CO2存在,根据实验装置回答,证明CO存在,只需观察到的现象是______。
(4)为了测定半水煤气中 H2、CO 质量的实验方案如下:
若步骤Ⅳ中浓硫酸质量增加a 克,步骤Ⅴ的KOH溶液质量增加b 克,则半水煤气中H2与CO的质量比为______(用含字母a、b的代数式表示)。
参考答案
1.A
2.C
3.C
4.D
5.D
6.D
7.C
8.C
9.C
10.B
11.D
12.A
13.Na+、OH-、CO32- 硝酸钠
14.抗腐蚀性强 可回收 有机 减小 空气 a 化学 AC
15.置换反应 氧化物
16.C Fe+CuSO4=FeSO4+Cu 过滤 Zn+H2SO4=ZnSO4+H2↑ A、C
17.A D BCE
18.A C
19.放热 AB段:氧化铝和稀硫酸反应无气体生成,气压变化不大;BC段:铝和稀硫酸反应生成了氢气,放热导致气体膨胀,气压增大;CD段:完全反应后温度下降,气压减小;DE段:反应停止,温度不变,气压不变
20.继续向反应后的滤渣中加入稀硫酸,如果没有气泡冒出,则说明生铁样品已经完全反应 B 设铁的质量为x,生成硫酸亚铁的质量为y,
x=8.4g
y=22.8g
稀硫酸的质量为:159.0g-44.1g-9.0g=105.9g,
形成溶液的质量为:8.4g+105.9g-0.3g=114g,
反应后所得溶液中硫酸亚铁的质量分数为:×100%=20%
21.CO2+Ca(OH)2=CaCO3↓+H2O 验证气体通过灼热的氧化铜后是否有水生成 E中的澄清石灰水变浑浊
一、选择题
1.下列物质中,有一种与其它三种物质不属于同一类别的是( )
A.纯碱 B.氨水 C.熟石灰 D.苛性钠
2.天平两边各放质量相等的烧杯,分别盛有等质量、等质量分数的足量稀硫酸,此时天平平衡。然后在两边的烧杯中各加入下列物质,充分反应后天平仍保持平衡的是( )
①10克铁和10克氧化铁
②10克铜和10克氧化铜
③5.6克铁和6.5克锌
④6.5克锌和6.3克氧化锌
A.①②③ B.①②④ C.②④ D.③④
3.风寒感冒时,中医建议用生姜水泡脚。因为生姜中含有姜辣素(C17H26O4),能使血管扩张,促进血液循环。从物质的分类角度来看,姜辣素属于( )
A.混合物 B.氧化物 C.有机化合物 D.无机化合物
4.古代金属锡的治炼发生的反应主要是:SnO2+2CSn+2CO↑下列分析正确的是( )
A.生成的CO可以用氢氧化钠溶液吸收
B.反应类型属于复分解反应
C.反应过程中化合价没有发生改变
D.二氧化锡是氧化物
5.下列物质中属于有机物的是( )
A.CO2 B.CaCO3 C.H2CO3 D.C2H6O
6.小龙利用注射器探究铁生锈的条件,一段时间后,只有乙注射器中的铁丝生锈,下列说法不正确的是( )
A.小龙先用橡皮帽封住注射孔,向外拉动活塞,放手后观察到活塞恢复原位,认为该装置气密性良好
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比乙瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向乙瓶中注过量稀盐酸,观察到溶液变成黄色,不产生气泡
7.向一定质量的硝酸银和硝酸亚铁溶液中加入mg锌粉,充分反映后过滤,将滤渣洗涤、干燥后再称量,得到滤渣的质量为mg,据此分析下列说法不正确的是( )
A.取反应后的滤液观察,滤液可能呈无色
B.滤渣中的物质最多含有三种,最少含有两种
C.取反应后的滤液插入铜丝,铜丝表面有固体附着
D.向少量硫酸铜溶液中加入足量滤渣,溶液可能变为浅绿色
8.如图所示为物质的分类概念图。打火机内的液体丁烷(C4H10)属于图中的( )
A.甲 B.乙 C.丙 D.丁
9.通过物质间相互反应可以实现物质间的相互转化,下列物质间的转化,通过一步化学反应不能实现的是( )
A.CaO→Ca(OH)2→CaCO3 B.Mg→MgO→MgCl2
C.CuO→Cu(OH)2→CuCl2 D.NaOH→NaCl→NaNO3
10.将 Fe3O4、Fe2O3、CuO的固体混合粉末mg,在加热条件下用足量CO还原得到金属混合物2.32g,将生成的CO2气体用足量澄清石灰水吸收后,产生5.00g白色沉淀,则m的数值为( )
A.5.32 B.3.12 C.3.59 D.2.37
11.现有铁粉、二氧化锰、硫酸钡和铁矿石四种固体,为了区分它们,小盟参照二歧分类法,制作了如图的检索表。下列叙述错误的是( )
1a 只含一种物质………2 1b 含有多种物质………甲 2a 只含一种元素………乙 2b 含有多种元素………3 3a ___________……………丙 3b 白色固体……………丁
A.甲表示的是铁矿石
B.乙表示的是铁粉
C.表中“___________”应该表示为“黑色固体”
D.也可根据是否含有氧元素对丙、丁分类
12.飞机的制造材料主要是铝合金。一架普通的飞机,差不多要用50万个铝合金做的铆钉,飞机的外壳、机翼、机尾螺旋桨、引擎的许多部件也是用铝合金制成的。对此,下列叙述错误的是( )
A.铝合金的导电性极差,使飞机不容易被闪电击中
B.铝的密度比较小,大量使用铝材能减小飞机质量,有利于飞行
C.铝的表面容易形成致密的氧化物保护膜,不容易生锈
D.飞机材料采用铝合金而不用纯铝的主要原因,是纯铝比较软而铝合金比较硬
二、填空题
13.某城市有甲、乙两工厂排放污水,污水中各含有下列6种离子中的3种(两厂不含相同离子,其中甲厂的污水能使酚酞试液变红:H+、Ba2+、Na+、OH-、CO32-、NO3-,甲厂含有的离子是_______;两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清的只含一种溶质的溶液,此溶液的溶质是_______(填化学名称)。
14.人人行动,推进垃圾分类,推动绿色、健康、可持续发展。
(1)垃圾分类回收是我县创建文明城市的一项重要举措。如图所示是街道垃圾桶。
①使用铝合金做内筒的优点是_______(写出一点即可)。
②某品牌饮料的空易拉罐应收入_______(选填“可回收”或“不可回收”)筒中。
(2)在农村,人们把秸秆、杂草、人畜粪便等废弃物放在密闭的池中发酵可获得沼气(主要成分是甲烷),沼气是很好的燃料,可用于家庭烹调、取暖和照明。
①甲烷(CH4)属于_______(选填“无机”或“有机”)化合物。
②甲烷在空气中完全燃烧的化学方程式为:CH4+2O2CO2+2H2O。丁烷燃烧的化学方程式为:2C4H10+13O28CO2+10H2O,相同条件下,气体体积比等于分子数比。若小明家由石油液化气(主要成分是丁烷)改为沼气,需要进行灶具的调整。改为沼气后,同体积燃料燃烧消耗空气的体积将_______(选填“增大”或“减小”),灶具的调整方法是减_______(选填“燃料”或“空气”)的进气量。
③甲烷是一种无色、无味的气体,密度比空气小。为了安全,在小明家厨房安装沼气泄漏报警器。根据甲烷的性质可知,图中_______(选填“a”或“b”)位置的安装是正确的。
(3)垃圾焚烧发电厂的建成,能缓解城市垃圾过多带来的危害。
①垃圾焚烧发电是利用了储存在垃圾中的_______能。
②下列与垃圾有关的各种说法中不科学的有_______(选填字母)。
A.垃圾发电厂可以有效地处理所有垃圾,并且没有任何污染
B.垃圾也是一种重要的资源,应对垃圾分类处理,综合利用
C.生活中的垃圾可以随意丢弃,因为它们很快都能被自然界分解
D.垃圾中塑料制品不要随意丢弃,避免白色污染
15.从古代到现代,材料的种类越来越多,用途也越来越广泛。请回答:
(1)早在西汉时期,我国就有湿法炼铜的记载,将铁置于硫酸铜溶液中得到铜单质,该反应属于______(填基本反应类型)。
(2)现代社会,玻璃是一种常见的非金属材料,SiO2是生产玻璃的原料之一。SiO2属于______ (选填“酸”、“碱”、“盐”或“氧化物”)。
16.铜是人类最早利用的金属之一。
(1)下列铜制品中,利用金属导热性的是________(填字母序号)。
(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为__________。
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):
已知:2Cu+2H2SO4+O22CuSO4+2H2O
①过程Ⅱ中分离操作的名称是_________。
②过程Ⅲ中有气体产生,反应的化学方程式为_________。
③A~E中含铜、锌两种元素的物质有______(填字母序号)。
17.下列分别盛有不同物质的容器中,所盛物质属于单质的是_____,化合物的是_____,混合物的是________,(均填容器下的代号)
18.用序号填空,下列物质中属于氧化物的是______,属于盐的是______。
A.H2O B.HNO3 C.BaC12 D.Zn E.Fe(OH)3
三、简答题
19.将未经砂布打磨的铝条放入盛有足量稀硫酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示。
(1)由图象可知密闭容器内发生了_____反应(选填“吸热”或“放热”);
(2)请对曲线各部分变化情况作出解释_____。
20.钢铁工业是一个国家的支柱产业之一,某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如图所示装置进行分析。分别称得锥形瓶与棉花的质量为44.1g,生铁样品的质量为9.0g。在锥形瓶中加入足量稀硫酸后,立即开始记录电子天平的示数,记录数据如图所示。
请认真分析数据,回答下列问题:
(1)如何判断试验中生铁样品已经完全反应。___________
(2)根据电子天平的数据变化进行分析,如图丙图像中正确的是___________
(3)计算反应后所得溶液中硫酸亚铁的质量分数___________。
四、探究题
21.半水煤气是工业合成氨的原料气,其主要成分是 H2、CO、CO2、N2和水蒸气。某科学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。
查阅资料可知碱石灰是 CaO 和 NaOH 的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,其反应的化学方程式是______。
(2)D装置中“冰水”的作用是______。
(3)实验结果证明有H2、CO、CO2存在,根据实验装置回答,证明CO存在,只需观察到的现象是______。
(4)为了测定半水煤气中 H2、CO 质量的实验方案如下:
若步骤Ⅳ中浓硫酸质量增加a 克,步骤Ⅴ的KOH溶液质量增加b 克,则半水煤气中H2与CO的质量比为______(用含字母a、b的代数式表示)。
参考答案
1.A
2.C
3.C
4.D
5.D
6.D
7.C
8.C
9.C
10.B
11.D
12.A
13.Na+、OH-、CO32- 硝酸钠
14.抗腐蚀性强 可回收 有机 减小 空气 a 化学 AC
15.置换反应 氧化物
16.C Fe+CuSO4=FeSO4+Cu 过滤 Zn+H2SO4=ZnSO4+H2↑ A、C
17.A D BCE
18.A C
19.放热 AB段:氧化铝和稀硫酸反应无气体生成,气压变化不大;BC段:铝和稀硫酸反应生成了氢气,放热导致气体膨胀,气压增大;CD段:完全反应后温度下降,气压减小;DE段:反应停止,温度不变,气压不变
20.继续向反应后的滤渣中加入稀硫酸,如果没有气泡冒出,则说明生铁样品已经完全反应 B 设铁的质量为x,生成硫酸亚铁的质量为y,
x=8.4g
y=22.8g
稀硫酸的质量为:159.0g-44.1g-9.0g=105.9g,
形成溶液的质量为:8.4g+105.9g-0.3g=114g,
反应后所得溶液中硫酸亚铁的质量分数为:×100%=20%
21.CO2+Ca(OH)2=CaCO3↓+H2O 验证气体通过灼热的氧化铜后是否有水生成 E中的澄清石灰水变浑浊
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
