第4章 认识化学变化测试题—2021-2022学年九年级化学沪教版(全国)上册 (1)(word版 含答案)
文档属性
| 名称 | 第4章 认识化学变化测试题—2021-2022学年九年级化学沪教版(全国)上册 (1)(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 160.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-18 00:00:00 | ||
图片预览




文档简介
第4章《认识化学变化》测试题
一、单选题
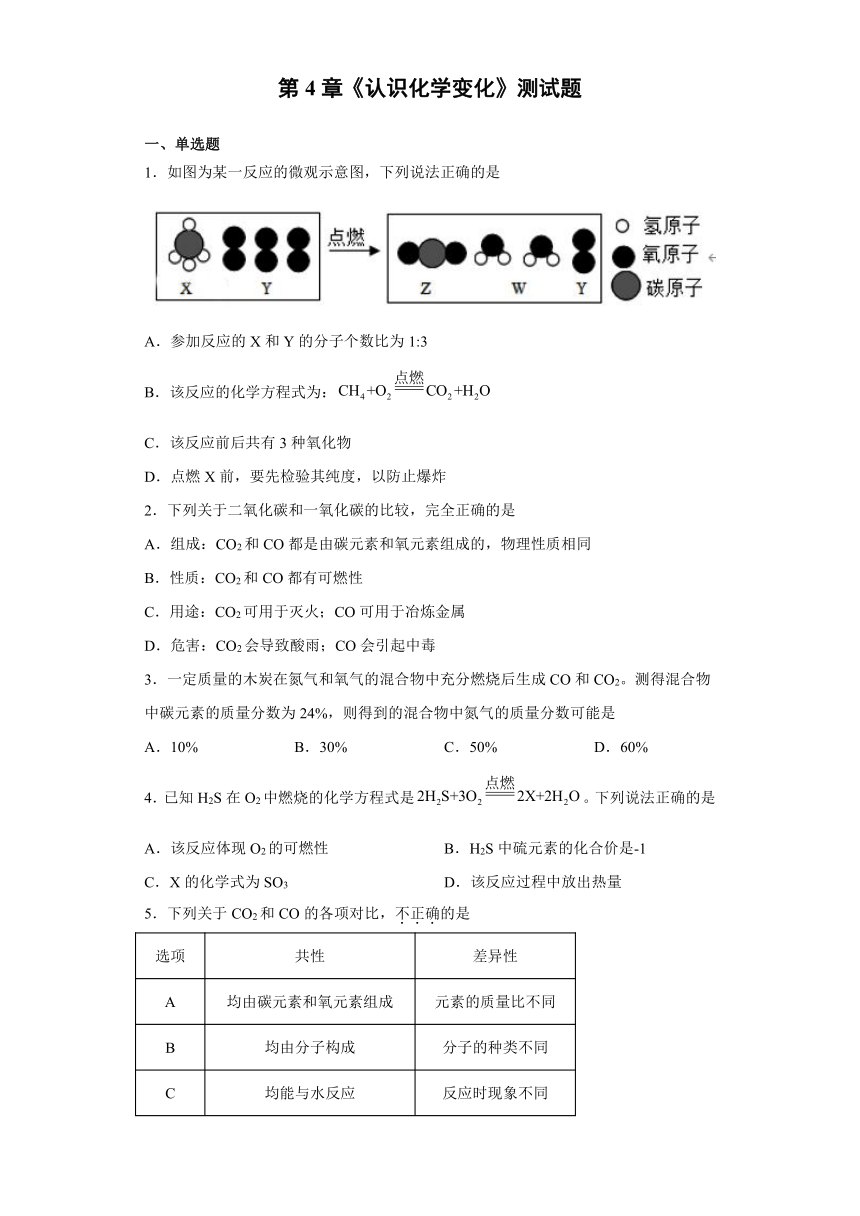
1.如图为某一反应的微观示意图,下列说法正确的是
A.参加反应的X和Y的分子个数比为1:3
B.该反应的化学方程式为:
C.该反应前后共有3种氧化物
D.点燃X前,要先检验其纯度,以防止爆炸
2.下列关于二氧化碳和一氧化碳的比较,完全正确的是
A.组成:CO2和CO都是由碳元素和氧元素组成的,物理性质相同
B.性质:CO2和CO都有可燃性
C.用途:CO2可用于灭火;CO可用于冶炼金属
D.危害:CO2会导致酸雨;CO会引起中毒
3.一定质量的木炭在氮气和氧气的混合物中充分燃烧后生成CO和CO2。测得混合物中碳元素的质量分数为24%,则得到的混合物中氮气的质量分数可能是
A.10% B.30% C.50% D.60%
4.已知H2S在O2中燃烧的化学方程式是。下列说法正确的是
A.该反应体现O2的可燃性 B.H2S中硫元素的化合价是-1
C.X的化学式为SO3 D.该反应过程中放出热量
5.下列关于CO2和CO的各项对比,不正确的是
选项 共性 差异性
A 均由碳元素和氧元素组成 元素的质量比不同
B 均由分子构成 分子的种类不同
C 均能与水反应 反应时现象不同
D 常温下均是无色气体 收集方法不同
A.A B.B C.C D.D
6.下列有关碳和碳的氧化物的说法,错误的是
A.C60是一种新型化合物
B.碳在空气中充分燃烧时生成CO2,不充分燃烧时生成CO
C.CO和CO2组成元素相同,但是它们的化学性质差异很大
D.清明上河图至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
7.关于燃烧和灭火的说法正确的是
A.电烤箱着火时,用水扑灭 B.室内起火应迅速开窗通风
C.燃烧一定伴随发光、放热现象,有发光、放热现象的变化一定是燃烧 D.图书资料着火,用二氧化碳灭火器灭火
8.方程式为;4X+5O24NO+6H2O,X的化学式为
A.NH3 B.NH2 C.NH4 D.N2H2
9.学习化学的目的是善于用化学知识去解决生产生活中的问题。下列有关燃烧与灭火的说法不正确的是
A.地铁的自动喷淋系统喷水灭火的原理是水蒸发吸热,降低可燃物的着火点
B.点燃野营篝火时,应该将木材架空,以增大木材与空气的接触面积
C.为了控制森林火灾的蔓延,可将大火蔓延路线前的一片树木砍掉,形成隔离带
D.图书、档案精密仪器等物的失火时,最好使用干冰灭火器扑救
10.下列化学方程式书写正确的是
A. B.
C. D.
11.设计实验方案,分析实验原理,解决实验问题,是化学独特的学科思维。认真分析以下实验,其中能达到实验目的的是
A. 测定空气中氧气的含量 B. 验证二氧化碳与水反应
C. 探究燃烧条件 D. 验证质量守恒定律
12.对下列事实的微观解释不正确的是
A.化学反应前后质量守恒的原因是原子的种类、数目、质量在反应前后不改变
B.水银温度计的工作原理是分子之间有间隔,能随温度改变
C.一滴水有1.67×1021个水分子,说明水分子的体积和质量都很小
D.冰的密度比水的密度小,说明水有反常膨胀现象
13.下列有关碳及化合物的说法正确的是
A.二氧化碳是导致酸雨的主要气体
B.室内放一盆水能防止一氧化碳中毒
C.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
D.金刚石、石墨、C60都是由碳原子构成的单质
14.相同质量的H2和CO完全燃烧需要氧气的质量
A.CO多 B.H2多 C.一样多 D.无法比较
15.下列图像能正确反映对应变化关系的是
A.等质量的甲烷(CH4)和酒精(C2H5OH)完全燃烧
B.加热一定质量的高锰酸钾
C.加热一定质量氯酸钾和二氧化锰的混合物
D.镁在氧气中燃烧
二、填空题
16.一氧化碳和二氧化碳只有一字之差。
(1)有人认为两者就像孪生兄弟,这是因为_______(填序号)。
A.他们的组成元素相同 B.他们的密度都大于空气
C.他们都有毒 D.他们都能溶于水
(2)也有人认为,两者化学性质相差甚远,请给出一条支持他的理由:(用化学方程式表示)________。
(3)为了防止CO中毒,冬天用煤火取暖时,一定要装烟囱,并且注意_______。
17.氢、氧两种元素组成的 A 物质可发生分解反应,其微观示意图如下:
上述物质中,A物质的名称是______;在上的“□”方框中画出 C 的微粒示意图______,写出该反应的化学方程式______。
18.科学家发现在高温下利用催化剂可以将二氧化碳转化成燃料甲醇(CH3OH),反应的微观示意图如下所示。
(1)此反应中的单质是___________(填化学式);
(2)该反应中没有发生改变的粒子是___________(填“分子”“原子”或“离子”);
(3)该反应的化学方程式为___________。
19.新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
(1)佩戴口罩预防感染的原理相当于化学实验中的______操作;
(2)活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有______性;
(3)医用酒精是75%酒精溶液,酒精和水化学性质不同的原因是______;酒精消毒液不适宜喷洒,由于其挥发形成的蒸气能与空气形成爆炸性混合物,乙醇燃烧化学方程式为______;
(4)温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释,其原因是______。
20.根据所学知识回答问题:
(1)如图1为某元素的原子结构示意图,请据此回答:
①该元素的元素符号为 ___________;
②该元素位于元素周期表中的第 ___________周期。
(2)从宏观知微观。气体X在氧气中燃烧生成二氧化硫和水,X分子中一定含有的原子是 ___________(填符号)。
(3)从微观知宏观。在点燃条件下,A和B反应生成C和D.反应前后分子变化的微观示意图如图2所示。关于该过程,下列说法正确的是 ___________(填字母)。
A.物质A由氨分子构成
B.物质B可作燃料
C.生成C和D的质量比为14:9
D.该反应是放热反应
三、推断题
21.如图是部分含碳物质的转化关系图,根据图示回答下列问题:
(1)用碳做燃料时,为防止反应①的发生,你的建议是___________。
(2)反应②的化学方程式___________。
22.下图中 A~E 是初中化学常见的物质,C 是能使澄清石灰水变浑浊的气体,D 是常见的一种液体。请分析回答:
(1)反应②的符号表达式为______。
(2)A 物质中一定含有的元素为_______。
(3)从微观的角度解释 B、E 化学性质有差异的原因是______。
四、实验题
23.根据下图回答有关问题:
(1)图一中仪器a的名称是______。
(2)实验室用A装置制二氧化碳的化学方程式为______。欲收集一瓶二氧化碳,可从图一中选择的收集装置是______(填字母)
(3)图二是探究燃烧条件的三组实验装置。
①通过甲装置中的铜片上红磷和白磷的变化现象对比,可得出燃烧发生的条件是______。
②甲和丙相比,丙更适合作为密闭教室的演示实验装置,原因是______。
③下列对三组实验进行的分析或总结中,正确的是______。(填字母)
A.三组实验中小烧杯里的热水都只起提高温度的作用
B.甲、丙两组实验都应用了“对比实验”的研究方法
C.若将乙组中的白磷换成红磷,也能观察到燃烧现象
五、计算题
24.某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表:
反应时间/min 1.0 1.5: 2.0 2.5- 3.0 3.5
剩余固体质量/g 5.1 4.5 4.2 4.08 4.08 4.08
分析表中数据,完成下列问题
(1)二氧化锰中锰元素和氧元素的质量比为________。
(2)生成氧气的质量为_______g。
(3)原混合物中氯酸钾的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
25.碳在高温时还原氧化铜的化学方程式为:C+2CuO2Cu+CO2↑。请计算:
(1)CO2分子中,C原子与O原子的原子个数比为___________;
(2)CuO中,Cu元素与O元素的质量比为___________;
(3)CuO中,Cu元素的质量分数为___________。
(4)要使320g氧化铜完全还原,需要碳的质量至少是多少?(计算结果保留一位小数)
参考答案
1.D 2.C 3.B 4.D 5.C 6.A 7.D 8.A 9.A 10.D 11.A 12.B 13.C 14.B 15.A
16.(1)A
(2)CO2+Ca(OH)2=CaCO3↓+H2O
(3)室内通风,防止CO中毒
17.过氧化氢
18.(1)H2
(2)原子
(3)
19.(1)过滤
(2)吸附
(3) 分子构成不同 C2H5OH+3O23H2O+2CO2
(4)温度越高,汞原子间隔越大
20.(1) P 三
(2)S和H
(3)AD
21.(1)增加通入空气的量(合理即可)
(2)(合理即可)
22.(1)
(2)碳元素和氢元素
(3)分子构成不同
23.(1)集气瓶
(2) B
(3) 温度达到可燃物的着火点
丙装置更环保 B
24.(1)
(2)1.92
(3)设:原混合物中氯酸钾的质量x
答:原混合物中氯酸钾的质量分数是81.7%
25.(1)1:2
(2)氧化铜中,铜元素与氧元素的质量比为:64:16=4:1
(3)氧化铜中,铜元素的质量分数为:
(4)解:设要使320g氧化铜完全还原,需要碳的质量至少是x
x=24.0g
答:使320g氧化铜完全还原,需要碳的质量至少是24.0g。
一、单选题
1.如图为某一反应的微观示意图,下列说法正确的是
A.参加反应的X和Y的分子个数比为1:3
B.该反应的化学方程式为:
C.该反应前后共有3种氧化物
D.点燃X前,要先检验其纯度,以防止爆炸
2.下列关于二氧化碳和一氧化碳的比较,完全正确的是
A.组成:CO2和CO都是由碳元素和氧元素组成的,物理性质相同
B.性质:CO2和CO都有可燃性
C.用途:CO2可用于灭火;CO可用于冶炼金属
D.危害:CO2会导致酸雨;CO会引起中毒
3.一定质量的木炭在氮气和氧气的混合物中充分燃烧后生成CO和CO2。测得混合物中碳元素的质量分数为24%,则得到的混合物中氮气的质量分数可能是
A.10% B.30% C.50% D.60%
4.已知H2S在O2中燃烧的化学方程式是。下列说法正确的是
A.该反应体现O2的可燃性 B.H2S中硫元素的化合价是-1
C.X的化学式为SO3 D.该反应过程中放出热量
5.下列关于CO2和CO的各项对比,不正确的是
选项 共性 差异性
A 均由碳元素和氧元素组成 元素的质量比不同
B 均由分子构成 分子的种类不同
C 均能与水反应 反应时现象不同
D 常温下均是无色气体 收集方法不同
A.A B.B C.C D.D
6.下列有关碳和碳的氧化物的说法,错误的是
A.C60是一种新型化合物
B.碳在空气中充分燃烧时生成CO2,不充分燃烧时生成CO
C.CO和CO2组成元素相同,但是它们的化学性质差异很大
D.清明上河图至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
7.关于燃烧和灭火的说法正确的是
A.电烤箱着火时,用水扑灭 B.室内起火应迅速开窗通风
C.燃烧一定伴随发光、放热现象,有发光、放热现象的变化一定是燃烧 D.图书资料着火,用二氧化碳灭火器灭火
8.方程式为;4X+5O24NO+6H2O,X的化学式为
A.NH3 B.NH2 C.NH4 D.N2H2
9.学习化学的目的是善于用化学知识去解决生产生活中的问题。下列有关燃烧与灭火的说法不正确的是
A.地铁的自动喷淋系统喷水灭火的原理是水蒸发吸热,降低可燃物的着火点
B.点燃野营篝火时,应该将木材架空,以增大木材与空气的接触面积
C.为了控制森林火灾的蔓延,可将大火蔓延路线前的一片树木砍掉,形成隔离带
D.图书、档案精密仪器等物的失火时,最好使用干冰灭火器扑救
10.下列化学方程式书写正确的是
A. B.
C. D.
11.设计实验方案,分析实验原理,解决实验问题,是化学独特的学科思维。认真分析以下实验,其中能达到实验目的的是
A. 测定空气中氧气的含量 B. 验证二氧化碳与水反应
C. 探究燃烧条件 D. 验证质量守恒定律
12.对下列事实的微观解释不正确的是
A.化学反应前后质量守恒的原因是原子的种类、数目、质量在反应前后不改变
B.水银温度计的工作原理是分子之间有间隔,能随温度改变
C.一滴水有1.67×1021个水分子,说明水分子的体积和质量都很小
D.冰的密度比水的密度小,说明水有反常膨胀现象
13.下列有关碳及化合物的说法正确的是
A.二氧化碳是导致酸雨的主要气体
B.室内放一盆水能防止一氧化碳中毒
C.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
D.金刚石、石墨、C60都是由碳原子构成的单质
14.相同质量的H2和CO完全燃烧需要氧气的质量
A.CO多 B.H2多 C.一样多 D.无法比较
15.下列图像能正确反映对应变化关系的是
A.等质量的甲烷(CH4)和酒精(C2H5OH)完全燃烧
B.加热一定质量的高锰酸钾
C.加热一定质量氯酸钾和二氧化锰的混合物
D.镁在氧气中燃烧
二、填空题
16.一氧化碳和二氧化碳只有一字之差。
(1)有人认为两者就像孪生兄弟,这是因为_______(填序号)。
A.他们的组成元素相同 B.他们的密度都大于空气
C.他们都有毒 D.他们都能溶于水
(2)也有人认为,两者化学性质相差甚远,请给出一条支持他的理由:(用化学方程式表示)________。
(3)为了防止CO中毒,冬天用煤火取暖时,一定要装烟囱,并且注意_______。
17.氢、氧两种元素组成的 A 物质可发生分解反应,其微观示意图如下:
上述物质中,A物质的名称是______;在上的“□”方框中画出 C 的微粒示意图______,写出该反应的化学方程式______。
18.科学家发现在高温下利用催化剂可以将二氧化碳转化成燃料甲醇(CH3OH),反应的微观示意图如下所示。
(1)此反应中的单质是___________(填化学式);
(2)该反应中没有发生改变的粒子是___________(填“分子”“原子”或“离子”);
(3)该反应的化学方程式为___________。
19.新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
(1)佩戴口罩预防感染的原理相当于化学实验中的______操作;
(2)活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有______性;
(3)医用酒精是75%酒精溶液,酒精和水化学性质不同的原因是______;酒精消毒液不适宜喷洒,由于其挥发形成的蒸气能与空气形成爆炸性混合物,乙醇燃烧化学方程式为______;
(4)温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释,其原因是______。
20.根据所学知识回答问题:
(1)如图1为某元素的原子结构示意图,请据此回答:
①该元素的元素符号为 ___________;
②该元素位于元素周期表中的第 ___________周期。
(2)从宏观知微观。气体X在氧气中燃烧生成二氧化硫和水,X分子中一定含有的原子是 ___________(填符号)。
(3)从微观知宏观。在点燃条件下,A和B反应生成C和D.反应前后分子变化的微观示意图如图2所示。关于该过程,下列说法正确的是 ___________(填字母)。
A.物质A由氨分子构成
B.物质B可作燃料
C.生成C和D的质量比为14:9
D.该反应是放热反应
三、推断题
21.如图是部分含碳物质的转化关系图,根据图示回答下列问题:
(1)用碳做燃料时,为防止反应①的发生,你的建议是___________。
(2)反应②的化学方程式___________。
22.下图中 A~E 是初中化学常见的物质,C 是能使澄清石灰水变浑浊的气体,D 是常见的一种液体。请分析回答:
(1)反应②的符号表达式为______。
(2)A 物质中一定含有的元素为_______。
(3)从微观的角度解释 B、E 化学性质有差异的原因是______。
四、实验题
23.根据下图回答有关问题:
(1)图一中仪器a的名称是______。
(2)实验室用A装置制二氧化碳的化学方程式为______。欲收集一瓶二氧化碳,可从图一中选择的收集装置是______(填字母)
(3)图二是探究燃烧条件的三组实验装置。
①通过甲装置中的铜片上红磷和白磷的变化现象对比,可得出燃烧发生的条件是______。
②甲和丙相比,丙更适合作为密闭教室的演示实验装置,原因是______。
③下列对三组实验进行的分析或总结中,正确的是______。(填字母)
A.三组实验中小烧杯里的热水都只起提高温度的作用
B.甲、丙两组实验都应用了“对比实验”的研究方法
C.若将乙组中的白磷换成红磷,也能观察到燃烧现象
五、计算题
24.某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表:
反应时间/min 1.0 1.5: 2.0 2.5- 3.0 3.5
剩余固体质量/g 5.1 4.5 4.2 4.08 4.08 4.08
分析表中数据,完成下列问题
(1)二氧化锰中锰元素和氧元素的质量比为________。
(2)生成氧气的质量为_______g。
(3)原混合物中氯酸钾的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
25.碳在高温时还原氧化铜的化学方程式为:C+2CuO2Cu+CO2↑。请计算:
(1)CO2分子中,C原子与O原子的原子个数比为___________;
(2)CuO中,Cu元素与O元素的质量比为___________;
(3)CuO中,Cu元素的质量分数为___________。
(4)要使320g氧化铜完全还原,需要碳的质量至少是多少?(计算结果保留一位小数)
参考答案
1.D 2.C 3.B 4.D 5.C 6.A 7.D 8.A 9.A 10.D 11.A 12.B 13.C 14.B 15.A
16.(1)A
(2)CO2+Ca(OH)2=CaCO3↓+H2O
(3)室内通风,防止CO中毒
17.过氧化氢
18.(1)H2
(2)原子
(3)
19.(1)过滤
(2)吸附
(3) 分子构成不同 C2H5OH+3O23H2O+2CO2
(4)温度越高,汞原子间隔越大
20.(1) P 三
(2)S和H
(3)AD
21.(1)增加通入空气的量(合理即可)
(2)(合理即可)
22.(1)
(2)碳元素和氢元素
(3)分子构成不同
23.(1)集气瓶
(2) B
(3) 温度达到可燃物的着火点
丙装置更环保 B
24.(1)
(2)1.92
(3)设:原混合物中氯酸钾的质量x
答:原混合物中氯酸钾的质量分数是81.7%
25.(1)1:2
(2)氧化铜中,铜元素与氧元素的质量比为:64:16=4:1
(3)氧化铜中,铜元素的质量分数为:
(4)解:设要使320g氧化铜完全还原,需要碳的质量至少是x
x=24.0g
答:使320g氧化铜完全还原,需要碳的质量至少是24.0g。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
