上海市金山区2021-2022学年高一上学期期末质量检测化学试题(Word版含答案)
文档属性
| 名称 | 上海市金山区2021-2022学年高一上学期期末质量检测化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 418.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-18 00:00:00 | ||
图片预览


文档简介
金山区2021-2022学年高一上学期期末质量检测
化学试卷
考生注意:
1.本试卷考试时间60分钟,满分100分。
2.答题必须涂或写在答题纸上,做在试卷上一律不得分。
3.答题前,务必用水笔或圆珠笔在答题纸正面清楚地填写学校、姓名、座位号,并将核对后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Mn-55
一、选择题(共40分,每小题2分,每小题只有一个正确答案。)
1.电影《长津湖》催人泪下,志愿军精神永存。观影时从放映室到银幕产生光柱,该现象与下列哪种分散系有关
A.溶液 B.胶体 C.悬浊液 D.乳浊液
2.制备物质时一般遵循的原则不包括
A.原料易得 B.原理绿色 C.装置复杂 D.分离方便
3.下列气体既有颜色又有毒性的是
A. B. C.HCl D.
4.氧化还原反应是一类重要的化学反应。下列过程不涉及氧化还原反应的是
A.生物呼吸 B.电池放电 C.海水晒盐 D.钢铁生锈
5.下列变化属于固氮的是
A. B. C. D.
6.分类思想在化学学习与研究中具有重要意义。下列关于物质的分类正确的是
A.酸性氧化物:、、CO B.碱:NaOH、、
C.混合物:食盐水、豆浆、液氯 D.弱电解质:醋酸、一水合氨、水
7.下列微粒的检验方法不合理的是
A.氯离子:沉淀法 B.钠离子:焰色反应 C.碘单质:显色法 D.硫酸根:气体法
8.从S元素的化合价判断,下列含硫物质只能做还原剂的是
A. B.S C. D.
9.下列物质中与氯气、盐酸都能发生反应,生成不同氯化物的是
A.Fe B.Al C.Cu D.Na
10.同温同压下,决定气体体积大小的主要因素是
A.微粒大小 B.微粒间距 C.微粒种类 D.微粒数目
11.氧化还原反应的本质是
A.电子得失 B.得氧失氧 C.化合价升降 D.电子转移
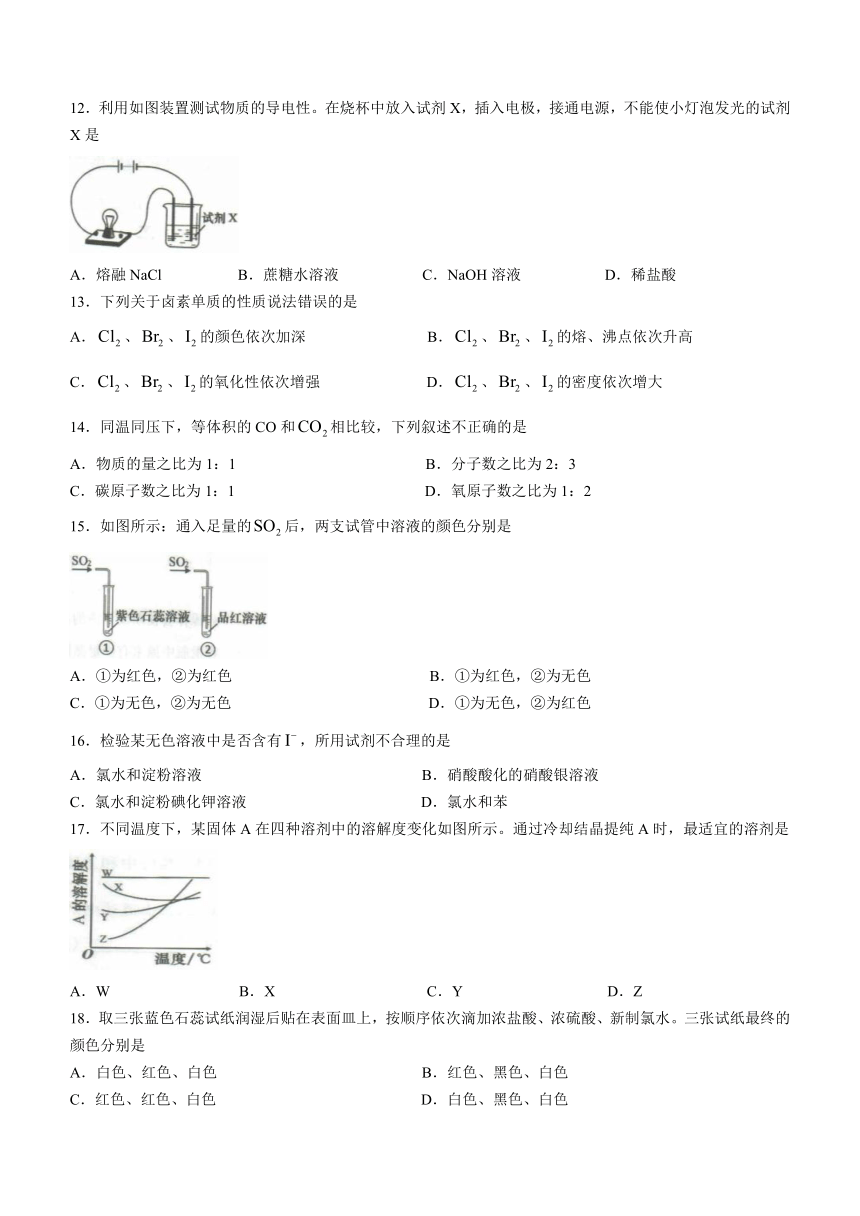
12.利用如图装置测试物质的导电性。在烧杯中放入试剂X,插入电极,接通电源,不能使小灯泡发光的试剂X是
A.熔融NaCl B.蔗糖水溶液 C.NaOH溶液 D.稀盐酸
13.下列关于卤素单质的性质说法错误的是
A.、、的颜色依次加深 B.、、的熔、沸点依次升高
C.、、的氧化性依次增强 D.、、的密度依次增大
14.同温同压下,等体积的CO和相比较,下列叙述不正确的是
A.物质的量之比为1:1 B.分子数之比为2:3
C.碳原子数之比为1:1 D.氧原子数之比为1:2
15.如图所示:通入足量的后,两支试管中溶液的颜色分别是
A.①为红色,②为红色 B.①为红色,②为无色
C.①为无色,②为无色 D.①为无色,②为红色
16.检验某无色溶液中是否含有,所用试剂不合理的是
A.氯水和淀粉溶液 B.硝酸酸化的硝酸银溶液
C.氯水和淀粉碘化钾溶液 D.氯水和苯
17.不同温度下,某固体A在四种溶剂中的溶解度变化如图所示。通过冷却结晶提纯A时,最适宜的溶剂是
A.W B.X C.Y D.Z
18.取三张蓝色石蕊试纸润湿后贴在表面皿上,按顺序依次滴加浓盐酸、浓硫酸、新制氯水。三张试纸最终的颜色分别是
A.白色、红色、白色 B.红色、黑色、白色
C.红色、红色、白色 D.白色、黑色、白色
19.下列反应中,能用离子方程式表示的是
A. B.
C. D.
20.标准状况下,22.4L 与的混合气体在一密闭容器中充分反应,冷却后气体体积不变;再用足量的NaOH溶液吸收反应后的气体,气体被完全吸收。则原混合气体中与的物质的量之比
A.等于1 B.大于1 C.小于或等于1 D.大于或等于1
二、综合题(共60分,其中选择题每小题有1~2个正确答案。)
(一)(本题共16分)
溴元素和碘元素在工农业生产和日常生活中有着广泛应用。根据信息,完成下列填空。
Ⅰ.下图是从海水中提取粗溴的主要流程
21.步骤①中,海水通过 (操作名称)、趁热过滤,得到苦卤;
步骤②选用作氧化剂,请写出发生反应的离子方程式。
22.可用热空气吹出溴是因为溴的 (选填编号)
a.熔点较低 b.熔点较高 c.沸点较低 d.沸点较高
23.下列关于含溴化合物的用途说法错误的是 (选填编号)
a.食盐添加剂 b.杀虫剂 c.镇静剂 d.感光材料
Ⅱ.实验小组从海带中提取碘
24.将干海带经过浸泡、 (操作名称),得到滤液。
25.用如图所示的仪器提取碘水中的碘。该仪器名称为 ,该步操作的名称为 ;图示的提取剂可以是 (选填编号)。
a.酒精 b.苯 c.四氯化碳 d.醋酸
碘在该溶剂中显 色
(二)(本题共16分)
硫是重要的非金属元素,也是人类较早认识的元素之一。下图为硫及其化合物在自然界中的部分转化关系。根据信息,完成下列填空。
26.硫元素在自然界中的存在形式 (选填编号)
a.只有游离态 b.只有化合态 c.既有游离态也有化合态
27.下列关于的说法正确的是 (选填编号)
a.是无色无味的有毒气体 b.与反应生成不稳定的
C.有毒,不能用作食品加工 d.气体通入溶液中产生白色沉淀
工业上常用漂白纸浆、毛、丝等,时间久了,漂白过的物质会发黄。简述原因。
28.请写出过程①发生反应的化学方程式,并标出电子转移的方向和数目。
29.浓硫酸是一种重要的无机酸
(1)浓硫酸在空气中放置一段时间后浓度变小,体现了浓硫酸的 (选填编号)。
a.吸水性 b.挥发性 c.脱水性 d.强酸性
(2)利用现象,工业上用铁或铝制容器盛装冷的浓硫酸。
(3)浓硫酸在使下列物质发生转化时,只表现出强氧化性的是 (选填编号)。
a. b. c.C→
30.金属离子可以与硫酸根结合形成硫酸盐,下列硫酸盐的化学式不正确的是 (选填编号)
a.明矾: b.重晶石: c.胆矾:
请书写溶于水的电离方程式。
(三)(本题共28分)
是一种重要的化工原料,可制备盐酸、含氯漂白剂和杀菌消毒剂等化工产品。根据信息,完成下列填空。
Ⅰ.实验室用以下反应制备:
31.可选择的发生装置为 (选填编号)
a. b. c.
32.实验室里将在空气中点燃后,伸入盛满的集气瓶中,可观察到产生 色的火焰,写出该反应的化学方程式。
33.实验室欲配制0.5的盐酸100mL
(1)所需10.0的浓盐酸 mL
(2)在配制溶液的过程中不需要使用的仪器有 (选填编号),还需要的仪器有 、 (仪器名称)。
a. b. c. d.
(3)下列操作会使所配溶液的浓度偏小的是 (选填编号)
a.容量瓶中原来有少量蒸馏水
b.转移溶液后未洗涤烧杯
c.摇匀后发现液面低于刻度线,再加水至刻度线
(4)恰好中和.上述配制的盐酸,需要氢氧化钠固体 g。
Ⅱ.工业上通过电解饱和食盐水制取氯气
34. (选填编号)是我国化工实业家,研发了通过电解食盐水生产盐酸等工艺。
a.傅鹰 b.吴蕴初 c.卢嘉锡
35.电解饱和食盐水时,阳极产生的气体是 (化学式)
写出电解饱和食盐水的化学方程式
该反应中被氧化的元素是 ;氧化剂与还原剂的物质的量之比为 。
36.含氯漂白剂和消毒剂在生活中被广泛使用
(1)与消石灰反应可制成漂白粉,漂白粉的有效成分是 (化学式)。
(2)可以直接用于自来水的杀菌、消毒,请写出与反应的化学方程式。
(3)“84消毒液”(主要成分为NaClO)不能与“洁厕灵”(含盐酸)混用,否则会发生反应:,产生有毒的氯气。该反应中 (选填编号)
a.NaClO作还原剂 b.既是氧化产物又是还原产物
c.HCl作氧化剂 d.是还原产物
金山区2021-2022学年高一上学期期末质量检测化学答案
一、选择题(共40分,每小题2分,每小题只有一个正确答案。)
1 2 3 4 5 6 7 8 9 10
B C A C B D D A A D
11 12 13 14 15 16 17 18 19 20
D B C B B C D B D C
二、综合题(共60分,其中选择题每小题有1~2个正确答案。)
(一)(本题共16分)
21.蒸发浓缩(或蒸发结晶);。
22.c。
23.a。
24.过滤。
25.分液漏斗,萃取;c。紫(或红、紫红)。
(二)(本题共16分)
26.c。
27.b。漂白漂白后的生成物不稳定,加热或经过一段时间后又会恢复原色。
28.。
29.(1)a;(2)钝化;(3)c。
30.b。。
(三)(本题共28分)
31.c。
32.苍白,。
33.(1)5。(2)d,玻璃棒、100mL容量瓶(各1分)。(3)bc。(4)2。
34.B
35.。。(或负一价的Cl元素)。1:2
36.(1)。(2)。(3)b。
化学试卷
考生注意:
1.本试卷考试时间60分钟,满分100分。
2.答题必须涂或写在答题纸上,做在试卷上一律不得分。
3.答题前,务必用水笔或圆珠笔在答题纸正面清楚地填写学校、姓名、座位号,并将核对后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Mn-55
一、选择题(共40分,每小题2分,每小题只有一个正确答案。)
1.电影《长津湖》催人泪下,志愿军精神永存。观影时从放映室到银幕产生光柱,该现象与下列哪种分散系有关
A.溶液 B.胶体 C.悬浊液 D.乳浊液
2.制备物质时一般遵循的原则不包括
A.原料易得 B.原理绿色 C.装置复杂 D.分离方便
3.下列气体既有颜色又有毒性的是
A. B. C.HCl D.
4.氧化还原反应是一类重要的化学反应。下列过程不涉及氧化还原反应的是
A.生物呼吸 B.电池放电 C.海水晒盐 D.钢铁生锈
5.下列变化属于固氮的是
A. B. C. D.
6.分类思想在化学学习与研究中具有重要意义。下列关于物质的分类正确的是
A.酸性氧化物:、、CO B.碱:NaOH、、
C.混合物:食盐水、豆浆、液氯 D.弱电解质:醋酸、一水合氨、水
7.下列微粒的检验方法不合理的是
A.氯离子:沉淀法 B.钠离子:焰色反应 C.碘单质:显色法 D.硫酸根:气体法
8.从S元素的化合价判断,下列含硫物质只能做还原剂的是
A. B.S C. D.
9.下列物质中与氯气、盐酸都能发生反应,生成不同氯化物的是
A.Fe B.Al C.Cu D.Na
10.同温同压下,决定气体体积大小的主要因素是
A.微粒大小 B.微粒间距 C.微粒种类 D.微粒数目
11.氧化还原反应的本质是
A.电子得失 B.得氧失氧 C.化合价升降 D.电子转移
12.利用如图装置测试物质的导电性。在烧杯中放入试剂X,插入电极,接通电源,不能使小灯泡发光的试剂X是
A.熔融NaCl B.蔗糖水溶液 C.NaOH溶液 D.稀盐酸
13.下列关于卤素单质的性质说法错误的是
A.、、的颜色依次加深 B.、、的熔、沸点依次升高
C.、、的氧化性依次增强 D.、、的密度依次增大
14.同温同压下,等体积的CO和相比较,下列叙述不正确的是
A.物质的量之比为1:1 B.分子数之比为2:3
C.碳原子数之比为1:1 D.氧原子数之比为1:2
15.如图所示:通入足量的后,两支试管中溶液的颜色分别是
A.①为红色,②为红色 B.①为红色,②为无色
C.①为无色,②为无色 D.①为无色,②为红色
16.检验某无色溶液中是否含有,所用试剂不合理的是
A.氯水和淀粉溶液 B.硝酸酸化的硝酸银溶液
C.氯水和淀粉碘化钾溶液 D.氯水和苯
17.不同温度下,某固体A在四种溶剂中的溶解度变化如图所示。通过冷却结晶提纯A时,最适宜的溶剂是
A.W B.X C.Y D.Z
18.取三张蓝色石蕊试纸润湿后贴在表面皿上,按顺序依次滴加浓盐酸、浓硫酸、新制氯水。三张试纸最终的颜色分别是
A.白色、红色、白色 B.红色、黑色、白色
C.红色、红色、白色 D.白色、黑色、白色
19.下列反应中,能用离子方程式表示的是
A. B.
C. D.
20.标准状况下,22.4L 与的混合气体在一密闭容器中充分反应,冷却后气体体积不变;再用足量的NaOH溶液吸收反应后的气体,气体被完全吸收。则原混合气体中与的物质的量之比
A.等于1 B.大于1 C.小于或等于1 D.大于或等于1
二、综合题(共60分,其中选择题每小题有1~2个正确答案。)
(一)(本题共16分)
溴元素和碘元素在工农业生产和日常生活中有着广泛应用。根据信息,完成下列填空。
Ⅰ.下图是从海水中提取粗溴的主要流程
21.步骤①中,海水通过 (操作名称)、趁热过滤,得到苦卤;
步骤②选用作氧化剂,请写出发生反应的离子方程式。
22.可用热空气吹出溴是因为溴的 (选填编号)
a.熔点较低 b.熔点较高 c.沸点较低 d.沸点较高
23.下列关于含溴化合物的用途说法错误的是 (选填编号)
a.食盐添加剂 b.杀虫剂 c.镇静剂 d.感光材料
Ⅱ.实验小组从海带中提取碘
24.将干海带经过浸泡、 (操作名称),得到滤液。
25.用如图所示的仪器提取碘水中的碘。该仪器名称为 ,该步操作的名称为 ;图示的提取剂可以是 (选填编号)。
a.酒精 b.苯 c.四氯化碳 d.醋酸
碘在该溶剂中显 色
(二)(本题共16分)
硫是重要的非金属元素,也是人类较早认识的元素之一。下图为硫及其化合物在自然界中的部分转化关系。根据信息,完成下列填空。
26.硫元素在自然界中的存在形式 (选填编号)
a.只有游离态 b.只有化合态 c.既有游离态也有化合态
27.下列关于的说法正确的是 (选填编号)
a.是无色无味的有毒气体 b.与反应生成不稳定的
C.有毒,不能用作食品加工 d.气体通入溶液中产生白色沉淀
工业上常用漂白纸浆、毛、丝等,时间久了,漂白过的物质会发黄。简述原因。
28.请写出过程①发生反应的化学方程式,并标出电子转移的方向和数目。
29.浓硫酸是一种重要的无机酸
(1)浓硫酸在空气中放置一段时间后浓度变小,体现了浓硫酸的 (选填编号)。
a.吸水性 b.挥发性 c.脱水性 d.强酸性
(2)利用现象,工业上用铁或铝制容器盛装冷的浓硫酸。
(3)浓硫酸在使下列物质发生转化时,只表现出强氧化性的是 (选填编号)。
a. b. c.C→
30.金属离子可以与硫酸根结合形成硫酸盐,下列硫酸盐的化学式不正确的是 (选填编号)
a.明矾: b.重晶石: c.胆矾:
请书写溶于水的电离方程式。
(三)(本题共28分)
是一种重要的化工原料,可制备盐酸、含氯漂白剂和杀菌消毒剂等化工产品。根据信息,完成下列填空。
Ⅰ.实验室用以下反应制备:
31.可选择的发生装置为 (选填编号)
a. b. c.
32.实验室里将在空气中点燃后,伸入盛满的集气瓶中,可观察到产生 色的火焰,写出该反应的化学方程式。
33.实验室欲配制0.5的盐酸100mL
(1)所需10.0的浓盐酸 mL
(2)在配制溶液的过程中不需要使用的仪器有 (选填编号),还需要的仪器有 、 (仪器名称)。
a. b. c. d.
(3)下列操作会使所配溶液的浓度偏小的是 (选填编号)
a.容量瓶中原来有少量蒸馏水
b.转移溶液后未洗涤烧杯
c.摇匀后发现液面低于刻度线,再加水至刻度线
(4)恰好中和.上述配制的盐酸,需要氢氧化钠固体 g。
Ⅱ.工业上通过电解饱和食盐水制取氯气
34. (选填编号)是我国化工实业家,研发了通过电解食盐水生产盐酸等工艺。
a.傅鹰 b.吴蕴初 c.卢嘉锡
35.电解饱和食盐水时,阳极产生的气体是 (化学式)
写出电解饱和食盐水的化学方程式
该反应中被氧化的元素是 ;氧化剂与还原剂的物质的量之比为 。
36.含氯漂白剂和消毒剂在生活中被广泛使用
(1)与消石灰反应可制成漂白粉,漂白粉的有效成分是 (化学式)。
(2)可以直接用于自来水的杀菌、消毒,请写出与反应的化学方程式。
(3)“84消毒液”(主要成分为NaClO)不能与“洁厕灵”(含盐酸)混用,否则会发生反应:,产生有毒的氯气。该反应中 (选填编号)
a.NaClO作还原剂 b.既是氧化产物又是还原产物
c.HCl作氧化剂 d.是还原产物
金山区2021-2022学年高一上学期期末质量检测化学答案
一、选择题(共40分,每小题2分,每小题只有一个正确答案。)
1 2 3 4 5 6 7 8 9 10
B C A C B D D A A D
11 12 13 14 15 16 17 18 19 20
D B C B B C D B D C
二、综合题(共60分,其中选择题每小题有1~2个正确答案。)
(一)(本题共16分)
21.蒸发浓缩(或蒸发结晶);。
22.c。
23.a。
24.过滤。
25.分液漏斗,萃取;c。紫(或红、紫红)。
(二)(本题共16分)
26.c。
27.b。漂白漂白后的生成物不稳定,加热或经过一段时间后又会恢复原色。
28.。
29.(1)a;(2)钝化;(3)c。
30.b。。
(三)(本题共28分)
31.c。
32.苍白,。
33.(1)5。(2)d,玻璃棒、100mL容量瓶(各1分)。(3)bc。(4)2。
34.B
35.。。(或负一价的Cl元素)。1:2
36.(1)。(2)。(3)b。
同课章节目录
