9.3 溶液的浓度课后练习-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 9.3 溶液的浓度课后练习-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 64.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-19 00:00:00 | ||
图片预览

文档简介
9.3 溶液的浓度
1.关于100g10%的氯化钠溶液,下列叙述正确的是( )
A.将10g氯化钠溶于90g水中,可制得该溶液
B.该溶液一定是饱和溶液
C.溶液中溶质与溶剂的质量比为1:10
D.100g水中溶有10g氯化钠
2.在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度。下列说法中正确的是( )
A.溶液浓度不变 B.溶质质量增加
C.溶剂质量不变 D.溶解度变大
3.往100 g 20%的食盐溶液中加入100 g水,则稀释前后( )
A.溶剂的质量不变 B.溶液的质量不变
C.溶质的质量不变 D.溶液中溶质的质量分数不变
4.蒸干20克NaCl溶液得到1.6克NaCl,计算原溶液中NaCl的质量分数为( )
A.8.7% B.8% C.7.4% D.无法确定
5.欲使100g5%氯化钠溶液中的溶质质量分数提高到10%,可采取的措施( )
A.蒸发50g水 B.取出50g溶液 C.蒸发45g水 D.加入5g氯化钠
6.将100g10%的氯化钠溶液质量分数增大一倍,可采取的方法是( )
A.加入10g氯化钠 B.蒸发掉45g水
C.加入12.5g氯化钠 D.加入100g10%的氯化钠溶液
7.A、B两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.A物质的溶解度大于B物质的溶解度
B.t1℃时,A、B两种物质的溶液中,溶质质量分数相等
C.t2℃时,A的溶解度大于B的溶解度
D.t2℃时,A的饱和溶液中溶质质量分数为30%
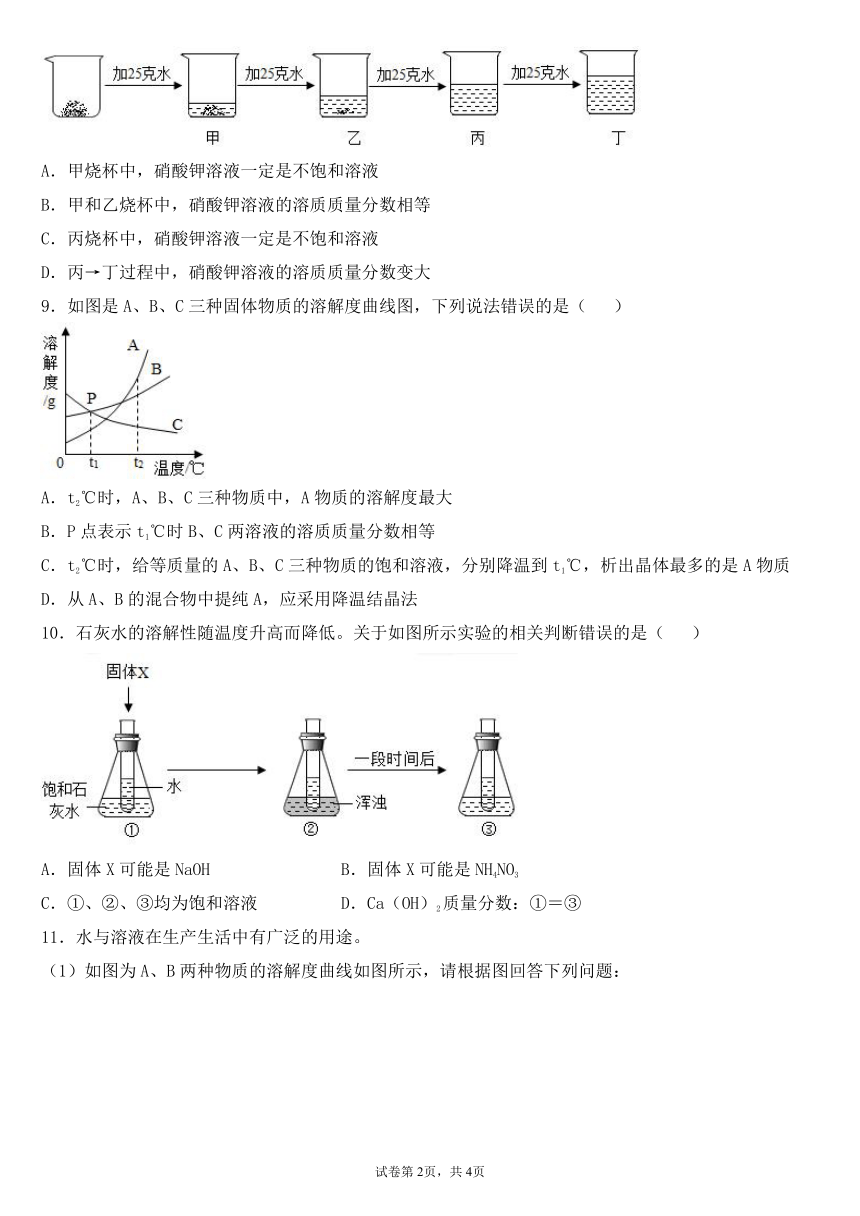
8.20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分溶解,实验过程如图所示。下列分析正确的是( )
A.甲烧杯中,硝酸钾溶液一定是不饱和溶液
B.甲和乙烧杯中,硝酸钾溶液的溶质质量分数相等
C.丙烧杯中,硝酸钾溶液一定是不饱和溶液
D.丙→丁过程中,硝酸钾溶液的溶质质量分数变大
9.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是( )
A.t2℃时,A、B、C三种物质中,A物质的溶解度最大
B.P点表示t1℃时B、C两溶液的溶质质量分数相等
C.t2℃时,给等质量的A、B、C三种物质的饱和溶液,分别降温到t1℃,析出晶体最多的是A物质
D.从A、B的混合物中提纯A,应采用降温结晶法
10.石灰水的溶解性随温度升高而降低。关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH B.固体X可能是NH4NO3
C.①、②、③均为饱和溶液 D.Ca(OH)2质量分数:①=③
11.水与溶液在生产生活中有广泛的用途。
(1)如图为A、B两种物质的溶解度曲线如图所示,请根据图回答下列问题:
①甲的溶解度受温度的影响比乙的溶解度受温度影响______(填“大”或“小”);若甲中含有少量的乙,提纯甲应采用的结晶方法是______。
②t2℃时,将60g的甲、乙分别加入到100g水中,充分溶解,能形成的饱和溶液是______物质。
③将t1oC时甲、乙的饱和溶液升温到t2oC,所得溶液的溶质质量分数的关系是甲______(填“﹥”“﹤”“=”)乙。
(2)欲配制50 g溶质质量分数为0.9%的氯化钠溶液,需溶质质量分数为11%的氯化钠溶液的质量为______(列式即可)。
12.水是最常见的溶剂,也是生命的源泉。
(1)自来水厂生产过程中常用到液氯,其作用是_________。
(2)铁丝在氧气中燃烧时,集气瓶内放少量水的目的是_________。
(3)气体在水中的溶解度与温度和压强有关。室温下,打开可乐瓶盖后有气泡冒出,说明气体的溶解度随压强的减小而_________。
(4)向20°C时100g水中加入20g硝酸钾进行下列实验(如图1),a-e表示所得溶液编号;其溶解度曲线如图2。
1. 20°C时硝酸钾的溶解度是_________,c是硝酸钾的_________(填“饱和"或“不饱和”)溶液,其所得溶液的质量为_________g。
II. 图1中的实验,溶液中溶质质量分数相等的有________(填溶液编号)。
III. 除去KNO3固体中混有的少量NaCl可采用降温结晶的方法,原因是_________。
13.如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)10℃,甲、乙、丙三种物质的溶解度由小到大的顺序______。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量是______。
(3)若乙中混有少量甲,最好采用______的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(4)30℃时,把等质量的甲、乙、丙三种物质配成各自的饱和溶液,需水最多的是______。
(5)30℃时,甲乙丙三种物质的饱和溶液将其温度降到10℃时所得溶液的溶质质量分数由大到小的是______。
三、计算题
14.徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 剩余固体的质量
第一次加入10g 3.0g
第二次加入10g 2.0g
第三次加入10g 1.0g
第四次加入10g 0.4g
(1)4.0g石灰石样品中碳酸钙的质量是__________g。
(2)求稀盐酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
试卷第2页,共2页
试卷第1页,共1页
答案
1.A 2.A 3.C 4.B 5.A 6.C 7.C 8.B 9.B 10.B
11.(1) 大 降温结晶(或冷却热饱和溶液) 乙 <
(2)
12.(1)杀菌消毒
(2)防止高温熔化物溅落,使集气瓶底炸裂
(3)减小
(4) 31.6g
不饱和 150 b和e 硝酸钾的溶解度随温度升高而增大且变化较大,氯化钠的溶解度受温度影响变化不大
13.(1)甲<丙<乙 (2)22.5g (3)蒸发结晶 (4)丙 (5)乙>甲>丙
14.
(1)3.6g
(2)设10g盐酸中HCl的质量为x
x=0.73g
稀盐酸的溶质质量分数为
答:稀盐酸的溶质质量分数为7.3%。答案第1页,共2页
答案第1页,共2页
1.关于100g10%的氯化钠溶液,下列叙述正确的是( )
A.将10g氯化钠溶于90g水中,可制得该溶液
B.该溶液一定是饱和溶液
C.溶液中溶质与溶剂的质量比为1:10
D.100g水中溶有10g氯化钠
2.在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度。下列说法中正确的是( )
A.溶液浓度不变 B.溶质质量增加
C.溶剂质量不变 D.溶解度变大
3.往100 g 20%的食盐溶液中加入100 g水,则稀释前后( )
A.溶剂的质量不变 B.溶液的质量不变
C.溶质的质量不变 D.溶液中溶质的质量分数不变
4.蒸干20克NaCl溶液得到1.6克NaCl,计算原溶液中NaCl的质量分数为( )
A.8.7% B.8% C.7.4% D.无法确定
5.欲使100g5%氯化钠溶液中的溶质质量分数提高到10%,可采取的措施( )
A.蒸发50g水 B.取出50g溶液 C.蒸发45g水 D.加入5g氯化钠
6.将100g10%的氯化钠溶液质量分数增大一倍,可采取的方法是( )
A.加入10g氯化钠 B.蒸发掉45g水
C.加入12.5g氯化钠 D.加入100g10%的氯化钠溶液
7.A、B两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.A物质的溶解度大于B物质的溶解度
B.t1℃时,A、B两种物质的溶液中,溶质质量分数相等
C.t2℃时,A的溶解度大于B的溶解度
D.t2℃时,A的饱和溶液中溶质质量分数为30%
8.20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分溶解,实验过程如图所示。下列分析正确的是( )
A.甲烧杯中,硝酸钾溶液一定是不饱和溶液
B.甲和乙烧杯中,硝酸钾溶液的溶质质量分数相等
C.丙烧杯中,硝酸钾溶液一定是不饱和溶液
D.丙→丁过程中,硝酸钾溶液的溶质质量分数变大
9.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是( )
A.t2℃时,A、B、C三种物质中,A物质的溶解度最大
B.P点表示t1℃时B、C两溶液的溶质质量分数相等
C.t2℃时,给等质量的A、B、C三种物质的饱和溶液,分别降温到t1℃,析出晶体最多的是A物质
D.从A、B的混合物中提纯A,应采用降温结晶法
10.石灰水的溶解性随温度升高而降低。关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH B.固体X可能是NH4NO3
C.①、②、③均为饱和溶液 D.Ca(OH)2质量分数:①=③
11.水与溶液在生产生活中有广泛的用途。
(1)如图为A、B两种物质的溶解度曲线如图所示,请根据图回答下列问题:
①甲的溶解度受温度的影响比乙的溶解度受温度影响______(填“大”或“小”);若甲中含有少量的乙,提纯甲应采用的结晶方法是______。
②t2℃时,将60g的甲、乙分别加入到100g水中,充分溶解,能形成的饱和溶液是______物质。
③将t1oC时甲、乙的饱和溶液升温到t2oC,所得溶液的溶质质量分数的关系是甲______(填“﹥”“﹤”“=”)乙。
(2)欲配制50 g溶质质量分数为0.9%的氯化钠溶液,需溶质质量分数为11%的氯化钠溶液的质量为______(列式即可)。
12.水是最常见的溶剂,也是生命的源泉。
(1)自来水厂生产过程中常用到液氯,其作用是_________。
(2)铁丝在氧气中燃烧时,集气瓶内放少量水的目的是_________。
(3)气体在水中的溶解度与温度和压强有关。室温下,打开可乐瓶盖后有气泡冒出,说明气体的溶解度随压强的减小而_________。
(4)向20°C时100g水中加入20g硝酸钾进行下列实验(如图1),a-e表示所得溶液编号;其溶解度曲线如图2。
1. 20°C时硝酸钾的溶解度是_________,c是硝酸钾的_________(填“饱和"或“不饱和”)溶液,其所得溶液的质量为_________g。
II. 图1中的实验,溶液中溶质质量分数相等的有________(填溶液编号)。
III. 除去KNO3固体中混有的少量NaCl可采用降温结晶的方法,原因是_________。
13.如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)10℃,甲、乙、丙三种物质的溶解度由小到大的顺序______。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量是______。
(3)若乙中混有少量甲,最好采用______的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(4)30℃时,把等质量的甲、乙、丙三种物质配成各自的饱和溶液,需水最多的是______。
(5)30℃时,甲乙丙三种物质的饱和溶液将其温度降到10℃时所得溶液的溶质质量分数由大到小的是______。
三、计算题
14.徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 剩余固体的质量
第一次加入10g 3.0g
第二次加入10g 2.0g
第三次加入10g 1.0g
第四次加入10g 0.4g
(1)4.0g石灰石样品中碳酸钙的质量是__________g。
(2)求稀盐酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
试卷第2页,共2页
试卷第1页,共1页
答案
1.A 2.A 3.C 4.B 5.A 6.C 7.C 8.B 9.B 10.B
11.(1) 大 降温结晶(或冷却热饱和溶液) 乙 <
(2)
12.(1)杀菌消毒
(2)防止高温熔化物溅落,使集气瓶底炸裂
(3)减小
(4) 31.6g
不饱和 150 b和e 硝酸钾的溶解度随温度升高而增大且变化较大,氯化钠的溶解度受温度影响变化不大
13.(1)甲<丙<乙 (2)22.5g (3)蒸发结晶 (4)丙 (5)乙>甲>丙
14.
(1)3.6g
(2)设10g盐酸中HCl的质量为x
x=0.73g
稀盐酸的溶质质量分数为
答:稀盐酸的溶质质量分数为7.3%。答案第1页,共2页
答案第1页,共2页
同课章节目录
