4.2物质组成的表示小节练习-2021-2022学年九年级化学鲁教版上册(word版 含解析)
文档属性
| 名称 | 4.2物质组成的表示小节练习-2021-2022学年九年级化学鲁教版上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 172.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-22 00:00:00 | ||
图片预览




文档简介
4.2物质组成的表示
一、选择题(共16题)
1.下列化学用语或对化学用语表示正确的是
A.二氧化硅:SiO2 B.水银:Ag C.锰酸钾:KMnO4 D.氯元素:Al
2.下列化学用语书写正确的是( )
A.2个氢原子:H2 B.氧化铝:AlO
C.氧离子:O﹣2 D.硅元素:Si
3.下列元素符号都表示金属的是
A.C、Cu、Ca B.S、Fe、P C.K、Mg、Ba D.H、Na、He
4.下列含有氯元素的物质中,氯元素的化合价最高的是
A. B.NaClO C. D.
5.下列化学用语关于数字“3”的意义,说法正确的是
①3Hg ②Fe3+ ③SO3 ④3H2O
A.表示分子个数的是③
B.表示离子所带电荷数的是②
C.表示原子个数的是④
D.表示一个分子中含有某种原子个数的是①
6.一个甲醛(CH2O)分子和一个水(H2O)分子都含有
A.一个水分子 B.氢元素和氧元素
C.两个氢原子和一个氧原子 D.氢气
7.葡萄糖化学式为是生物的主要供能物质。下列说法正确的是( )
A.一个葡萄糖分子中含有6个水分子
B.葡萄糖的相对分子质量为180g
C.葡萄糖中C、H 元素的质量比为6:1
D.葡萄糖中氢元素的质量分数最大
8.关于水的下列认识中错误的是( )
A.自来水厂净水的方法主要有沉淀、过滤、吸附和蒸馏
B.保持水的化学性质的最小粒子是水分子
C.生活中将硬水软化的方法通常是煮沸
D.水体污染的主要污染源是工业废水、农业污水和生活污水
9.能表示两个分子的是
A.2H B.2CO2 C.2SO4 D.SO2
10.下列归纳总结完全正确的一组是
A分子特征 B 数字含义
①水分子很小 ②固体物质的分子不运动 ③气体分子间的间隔很大 ①H2:2 个氢原子 ②:氧化汞中汞元素显+2 价 ③NO2:1 个二氧化氮分子中含有 2 个原子
C生活经验 D节约资源
①禁燃烟花爆竹——降低 PM2.5 ②食品包装中抽真空防腐 ③CO2 增多——酸雨 ①提倡使用太阳能 ②回收利用废旧金属 ③农业灌溉采用滴灌
A.A B.B C.C D.D
11.下列关于化学式“H2O2”的含义描述不正确的是
A.宏观上能表示过氧化氢这种物质
B.表示过氧化氢由氢气与氧气组成
C.表示过氧化氢由氢元素与氧元素组成
D.微观上表示1个过氧化氢分子由2个氢原子和2个氧原子构成
12.抗击新冠肺炎疫情中,化学合成的新药瑞德西韦(分子式:C27H35N6O8P)被寄予厚望。下列有关瑞德西韦说法正确的是
A.瑞德西韦属于有机化合物
B.瑞德西韦由77个原子构成
C.瑞德西韦中氢元素的质量分数最大
D.瑞德西韦的相对分子质量是602g
13.2021年,全民抗疫。在全国抗击新冠疫情中,常用戊二醛(化学式C5H8O2)对医疗器械等进行消毒。下列关于戊二醛说法正确的是
A.从宏观上看:戊二醛由碳、氢、氧三种元素组成
B.从微观上看:戊二醛中含有5个碳原子、8个氢原子和2个氧原子
C.从变化上看:戊二醛在氧气中完全燃烧生成二氧化硫和水
D.从质量上看:戊二醛中碳、氢元素的质量比为5:2
14.毒品带给人类的只会是毁灭,所以我们要珍爱生命,远离毒品.毒品K粉会对大脑造成永久损害,其主要成分是盐酸氯胺酮(化学式为C13H16ONCl).则有关盐酸氯胺酮的下列说法不正确的是
A.该物质是化合物
B.该物质由5种元素组成
C.该物质中C与H元素的质量比是13:16
D.该物质一个分子含有32个原子
15.某物质R是人类生命活动中不可缺少的物质。已知R的相对分子质量为150,其中含碳元素40%,含氢元素6.7%,其余为氧元素。则R的化学式为
A.C5H10O5 B.C5H10O2 C.C6H12O6 D.C6H6O
16.我国C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(),其中硅元素的化合价为价,则氮元素的化合价为
A.-3 B.+3 C.-4 D.+4
二、综合题(共6题)
17.硝酸铵是一种化肥。试计算:
(1)每个硝酸铵分子中共有________个原子;
(2)硝酸铵中氢、氧二种元素原子的个数比是________;
(3)硝酸铵的相对分子质量是________;
(4)硝酸铵中氮元素的质量分数是________(精确到)。
18.用化学用语填空
(1)可用作某些食品干燥剂的氧化物_______;(2)氯化铁溶液中的阳离子_____;
(3)氢硫酸(H2S)中硫元素的化合价为-2价_____; (4)3个氨分子_______。
19.为了消除碘缺病,我国政府规定某地区居民的食用盐必须加碘。下图为广东盐业总公司生产的加碘盐的部分标签,请根据标签图回答:
加碘盐 质量等级:二级 碘含量:20~50mg/kg 配料:食盐、碘酸钾、抗结剂 储存方法:防潮、防热、避光 食用方法:在汤、菜即将煮好时再加入碘盐、确保碘效 保质期:12个月
(1)食用盐必须加碘的“碘”是指________(填单质或元素或原子);该加碘盐属于________(填纯净物或混合物)
(2)碘酸钾(KIO3)中碘元素的化合价为___________;
(3)从标签的“食用方法”推测,碘酸钾的一种化学性质是______________________。
(4)请根据化学式计算:
①碘酸钾的相对分子质量:_________________;(列式计算);
②碘酸钾中各元素间的质量比K:I:O=_____________________;
③碘酸钾中碘元素的质量分数:_____________________(列式计算, 精确到0.1%);
(5)为确保碘盐中碘的最低含量,1Kg碘盐中至少应加入碘酸钾_______mg(精确到0.1 mg)
20.在化学的学习中化学用语非常重要,熟练掌握化学用语对于学习化学至关重要。
(1)下图是钠的原子结构示意图。下列说法不正确的是_______。
a. 钠属于金属元素 b. 钠原子的质子数为11
c. 钠离子的符号为Na+ d.钠在化学反应中易得到电子
(2)请用化学用语表示:
①2个氢原子:___________;②3个氧分子___________;③镁离子:___________;
(3)写出地壳中最多的金属元素的氧化物的化学式:________________ ;
(4)维生素C(C6H806)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。请回答以下问题:
①计算维生素C的相对分子质量______(只要写出结果即可);
②计算维生素C中C、O两种元素的质量比_________(要求写出计算过程);
③计算维生素C中氢元素的质量分数___________(要求写出计算过程,精确到0.1%)。
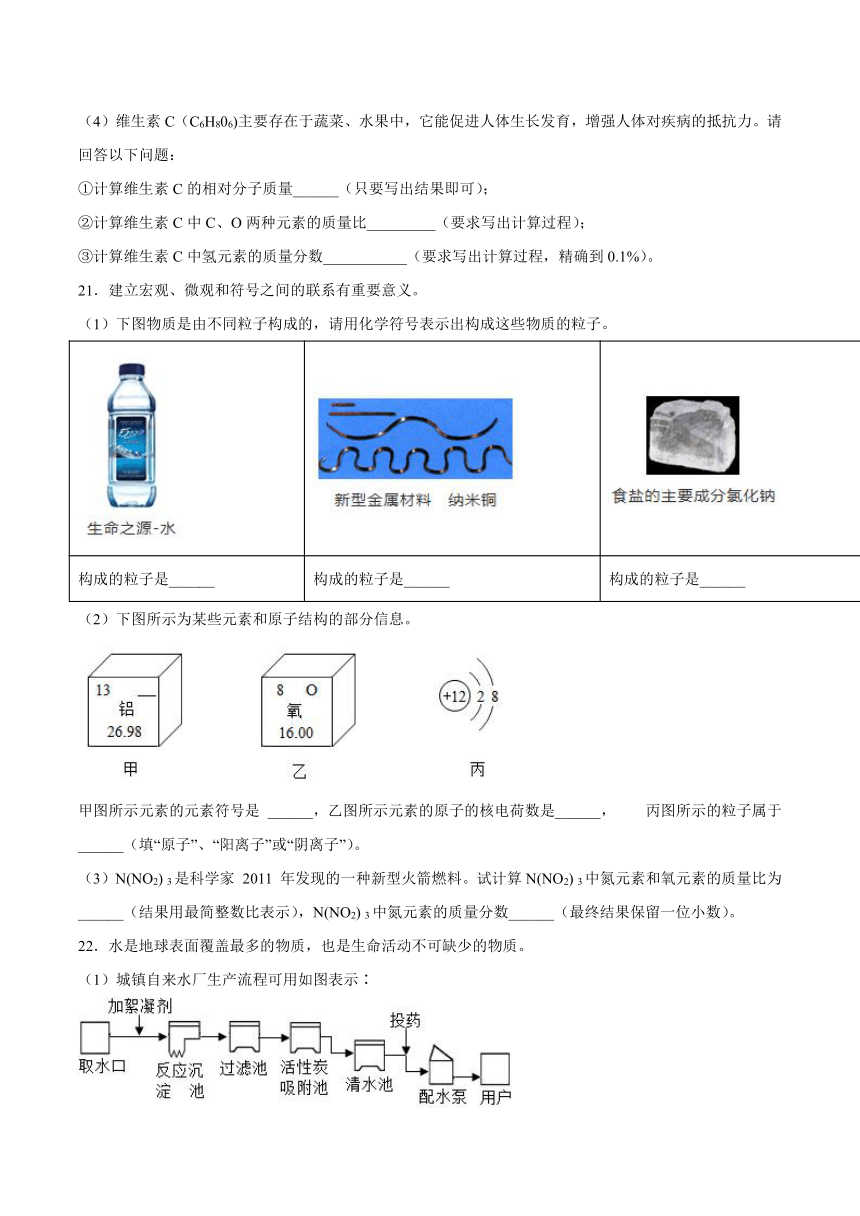
21.建立宏观、微观和符号之间的联系有重要意义。
(1)下图物质是由不同粒子构成的,请用化学符号表示出构成这些物质的粒子。
构成的粒子是______ 构成的粒子是______ 构成的粒子是______
(2)下图所示为某些元素和原子结构的部分信息。
甲图所示元素的元素符号是 ______,乙图所示元素的原子的核电荷数是______, 丙图所示的粒子属于 ______(填“原子”、“阳离子”或“阴离子”)。
(3)N(NO2) 3是科学家 2011 年发现的一种新型火箭燃料。试计算N(NO2) 3中氮元素和氧元素的质量比为 ______(结果用最简整数比表示),N(NO2) 3中氮元素的质量分数______(最终结果保留一位小数)。
22.水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。
(1)城镇自来水厂生产流程可用如图表示∶
①自来水厂净水过程中用到_____,其作用是吸附;
②自来水厂生产自来水时,使用的净水方法有_____。
A沉淀 B过滤 C煮沸 D蒸馏 E吸附
③世界卫生组织将某氧化物 RO2列为A级高效安全灭菌消毒剂,它在食品保鲜、水的消毒等方面有着广泛应用。实验测得该氧化物中R与O元素的质量比为71∶64,则RO2的化学式为______。
(2)生活中常讲的"烧开水"是指利用_______的方法,获得可以饮用的水,这样既可以降低水的硬度又可以杀灭水中的细菌。
(3)如图表示自来水消毒过程中发生的一个反应的微观过程∶
写出上述物质中单质的化学式∶_________。
参考答案
1.A
【详解】
A、二氧化硅的化学式可以根据其名称写出:SiO2,故A选项正确;
B、水银不银,是金属汞的俗称,化学式为:Hg,故B选项错误;
C、锰酸钾中钾元素为+1价,锰酸根的化合价为-2价,所以其化学式为:K2MnO4,题中符号为高锰酸钾的化学式,故C选项错误;
D、氯元素的符号为:Cl,题中符号为铝元素符号,故D选项错误;
故选A。
2.D
【解析】
试题分析:A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为:2H,故选项化学用语书写错误.
B、氧化铝中铝元素显+3价,氧元素显﹣2价,其化学式为,其化学式为:Al2O3,故选项化学用语书写错误.
C、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故氧根离子可表示为:O2﹣,故选项化学用语书写错误.
D、硅元素的元素符号可表示为:Si,故选项化学用语书写正确.
故选D.
3.C
【详解】
A、C表示的是碳,属于非金属元素,故A错误;
B、S表示的硫,属于非金属元素,P表示的是磷,属于非金属元素,故B错误;
C、K、Mg、Ba都表示的是金属元素,故C正确;
D、H表示的是氢、He表示的是氦,属于非金属元素,故D错误;
4.A
【详解】
A、根据氢元素为价,氧元素为价,设中氯元素的化合价为X。
则(+1)+X+(-2)×4=0,得X=+7,故氯元素的化合价为+7价;
B、根据钠元素为价,氧元素为价,设 NaClO中氯元素的化合价为X。
则(+1)+X+(-2) =0,得X=+1,故氯元素的化合价为+1价;
C、根据氧元素为价,设 中氯元素的化合价为X。
则X×2+(-2)×5=0,得X=+5,故氯元素的化合价为+5价;
D、根据钡元素为价,设 中氯元素的化合价为X。
则+2+X×2=0,得X=-1,故氯元素的化合价为-1价;
故中氯元素的化合价最高,故选A。
5.B
【详解】
①3Hg表示的是3个汞原子;②Fe3 + 表示的是3个铁离子;③S03表示的意义有四种:三氧化硫、三氧化硫是由硫元素和氧元素组成的、一个三氧化硫分子、一个三氧化硫分子是由一个硫元素和3个氧原子构成的;④3H2 O表示的是3个水分子。故选B。
6.C
【详解】
试题分析:一个甲醛(CH2O)分子和一个水(H2O)分子都含有两个氢原子和一个氧原子,不能再描述为表示宏观的意义,因为前面的说法中都强调了一个分子,属于微观的概念。故选C.
7.C
【详解】
A、分子是由原子构成的,葡萄糖分子中不含水分子,故A错误;
B、相对分子质量单位是“1”,不是“克”,常常省略不写,故B错误;
C、葡萄糖中C、H 元素的质量比为(12×6):(1×12)=6:1,故C正确;
D、葡萄糖中碳、氢、氧元素的质量比为(12×6):(1×12):(16×6)=6:1:8,葡萄糖中氧元素的质量分数最大,故D错误。故选C。
8.A
【详解】
A、自来水厂净水的方法中没有蒸馏,错误;
B、水由水分子构成;保持水的化学性质的最小粒子是水分子,正确;
C、硬水是含钙镁离子较多的水;可溶性钙、镁化合物在加热时,能形成沉淀,故生活中常煮沸的方法软化硬水,正确;
D、水体污染的主要污染源是工业废水、农业污水和生活污水,正确;
故选A。
9.B
【详解】
A、2H表示两个氢原子,故不符合题意;
B、2CO2表示两个二氧化碳分子,故符合题意;
C、2SO4缺少粒子所带电荷,错误,故不符合题意;
D、SO2表示一个二氧化硫分子,故不符合题意。
10.D
【详解】
A、固体物质的分子也运动,故不符合题意;
B、H2:一个氢分子由两个氢原子构成,故不符合题意;
C、SO2 增多——酸雨,故不符合题意;
D、提倡使用太阳能、回收利用废旧金属、农业灌溉采用滴灌都符合节约能源,故符合题意。
11.B
【详解】
A、宏观上能表示过氧化氢这种物质;故选项正确,但不符合题意;
B、表示一个过氧化氢分子的;故选项错误,但符合题意;
C、表示过氧化氢由氢元素与氧元素组成;故选项正确,但不符合题意;
D、微观上表示1个过氧化氢分子由2个氢原子和2个氧原子构成;故选项正确,但不符合题意;
故选:B。
12.A
【详解】
A、瑞德西韦是含碳元素的化合物,属于有机化合物,符合题意;
B、瑞德西韦是由瑞德西韦分子构成的,1个瑞德西韦分子是由77个原子构成的,不符合题意;
C、瑞德西韦中碳、氢、氮、氧、磷五种元素的质量比为(12×27):(1×35):(14×6):(16×8):(31×1)=324:35:84:128:31,则瑞德西韦中碳元素的质量分数最高,不符合题意;
D、相对分子质量单位是“1”,不是“克”,常常省略不写,瑞德西韦的相对分子质量为602,不符合题意。故选A。
13.A
【详解】
A、戊二醛是由碳、氢、氧三种元素组成的,故选项说法正确;
B、1个戊二醛分子中含有5个碳原子、8个氢原子和2个氧原子,故选项说法错误;
C、戊二醛在氧气中完全燃烧生成二氧化碳和水,故选项说法错误;
D、戊二醛中碳、氢元素的质量比为(12×5):(1×8)=15:2;故选项说法错误。
故选:A。
14.C
【解析】A、该物质由多种物质组成,故是化合物,正确;B、由化学式可知,该物质由碳元素、氢元素、氧元素、氮元素、氯元素估计5种元素组成,正确;C、该物质中C与H元素的质量比是(13):16=39:4,错误;D、该物质一个分子含有13个碳原子,16个氢原子,1个氧原子,1个氮原子,1个氯原子,估计32个原子,正确。故选C。
15.A
【解析】
设该化合物的化学式为CxHyOz,则相对分子质量=12x+y+16z=150(1)
40%(2) =6.7%(3),由(1)、(2)、(3)式解得:x=5 y=10 z=5,故选A。
16.A
【详解】
硅元素的化合价为+4价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+4)×3+4x=0,则x=-3。
故选:A。
17.9 80
【详解】
(1)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则每个硝酸铵分子中含有9个原子;故填:9;
(2)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则硝酸铵分子中氢、氧两种元素原子的个数比是4:3;故填:4:3;
(3)相对分子质量为构成分子的各原子的相对原子质量之和,所以硝酸铵的相对分子质量为14×2+1×4+16×3=80。故填:80;
(4)化合物中某元素的质量分数是化学式中某元素的相对原子质量与相应原子个数的乘积与相对分子质量之比,硝酸铵中氮元素的质量分数是;故填:35%。
18.CaO; Fe3+; ; 3NH3;
【解析】
(1)氧化钙能与空气中的水蒸气发生反应生成氢氧化钙,故可用作某些食品干燥剂的氧化物CaO;(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。氯化铁溶液中的阳离子可表示为:Fe3+;(3)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,氢硫酸(H2S)中,氢元素的化合价为+1价;氢硫酸(H2S)中硫元素化合价可表示为:;(4)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个氨分子可表示为:3NH3。
19.元素 混合物 +5 受热会分解 39+127+16×3=214 K:I:O= 39:127:48 59.3% 33.7mg
【解析】
(1)食盐中的“碘”不是单质,也不是原子,而是元素,加碘食盐属于混合物;(2)
根据在化合物中正负化合价代数和为零,设碘酸钾(KIO 3 )中碘元素的化合价为,则 (+1)++(-2)×3=0,=+5;(3)根据加碘盐图中标签信息,在汤、菜即将煮好时再加入碘盐、确保碘效,可得碘酸钾的一种化学性质是:受热易分解或受热不稳定;(4)①根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得碘酸钾的相对分子质量为:39+127+16×3=214;②碘酸钾中各元素间的质量比K:I:O=39:127:(16x3)=39:127:48;③碘酸钾中碘元素的质量分数:;(5)根据物质中某元素的质量=物质的质量×该元素的质量分数,依据1kg加碘盐中碘含量:20~50mg/kg,设1kg碘盐中至少应加入碘酸钾为 g,
解得 ≈33.7 mg。
20.d 2H 3O2 Mg2+ Al2O3 176 3:4 4.5%
【详解】
(1)a、由某元素的原子结构示意图,圆圈内数字表示核内质子数,其核内质子数为11,为钠元素,属于金属元素,故正确;
b、某元素的原子结构示意图,圆圈内数字表示核内质子数,其核内质子数为11,故正确;
c、由某元素的原子结构示意图,最外层电子数是1,在化学反应中失去1个电子而形成阳离子,钠离子的符号为Na+,故正确;
d、由某元素的原子结构示意图,最外层电子数是1,在化学反应中失去1个电子而形成阳离子,故错误;
(2)①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以2个氢原子,就可表示为:2H;
②由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则3个氧分子可表示为:3O2;
③离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故镁离子可表示为:Mg2+;
(3)先弄清地壳中含量最多的金属元素为铝元素,形成的氧化物为氧化铝,其中铝元素的化合价为+3价,氧元素的化合价为-2价,所以化学式为Al2O3;
(4)①维生素C的相对分子质量为12×6+1×8+16×6=176;
②维生素C中碳、氧元素的质量比=(12×6):(16×6)=3:4;
③维生素C中氢元素的质量分数为: =4.5%。
21.H2O Cu Na+、Cl- Al 8 阳离子 7:12 36.8%
【详解】
(1)水是由水分子构成的,H2O可表示水分子;铜是由铜原子构成的,单独的一个元素符号可表示一个该原子,Cu可表示铜原子;氯化钠是由钠离子(Na+)、氯离子(Cl-)构成的。
(2)铝的元素符号为Al;乙图所示是氧元素的元素周期表信息,原子序数在数值上等于原子的核电荷数,故该原子的核电荷数为8;丙图所示的粒子中有12个质子、10个电子,质子数>核外电子数,所以该粒子属于阳离子。
(3)N(NO2) 3中氮元素和氧元素的质量比为:(14×4):(16×6)≈7:12 ,N(NO2) 3中氮元素的质量分数为:=36.8%
22.活性炭 ABE ClO2 煮沸 Cl2
【详解】
(1)①自来水厂净水过程中用到活性炭,活性炭具有疏松多孔的结构,其作用是吸附;
②来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附、消毒。故选ABE;
③实验测得该氧化物中R与O元素的质量比为71∶64,设R的相对原子质量为x,则x:(16×2)=71:62,x=35.5,故R是Cl,RO2的化学式为ClO2;
(2)生活中常讲的"烧开水"是指利用煮沸的方法,获得可以饮用的水,这样既可以降低水的硬度又可以杀灭水中的细菌;
(3)由图可知,B是由同种元素组成的纯净物,属于单质,每个B分子由2个氯原子构成,化学式为Cl2。
一、选择题(共16题)
1.下列化学用语或对化学用语表示正确的是
A.二氧化硅:SiO2 B.水银:Ag C.锰酸钾:KMnO4 D.氯元素:Al
2.下列化学用语书写正确的是( )
A.2个氢原子:H2 B.氧化铝:AlO
C.氧离子:O﹣2 D.硅元素:Si
3.下列元素符号都表示金属的是
A.C、Cu、Ca B.S、Fe、P C.K、Mg、Ba D.H、Na、He
4.下列含有氯元素的物质中,氯元素的化合价最高的是
A. B.NaClO C. D.
5.下列化学用语关于数字“3”的意义,说法正确的是
①3Hg ②Fe3+ ③SO3 ④3H2O
A.表示分子个数的是③
B.表示离子所带电荷数的是②
C.表示原子个数的是④
D.表示一个分子中含有某种原子个数的是①
6.一个甲醛(CH2O)分子和一个水(H2O)分子都含有
A.一个水分子 B.氢元素和氧元素
C.两个氢原子和一个氧原子 D.氢气
7.葡萄糖化学式为是生物的主要供能物质。下列说法正确的是( )
A.一个葡萄糖分子中含有6个水分子
B.葡萄糖的相对分子质量为180g
C.葡萄糖中C、H 元素的质量比为6:1
D.葡萄糖中氢元素的质量分数最大
8.关于水的下列认识中错误的是( )
A.自来水厂净水的方法主要有沉淀、过滤、吸附和蒸馏
B.保持水的化学性质的最小粒子是水分子
C.生活中将硬水软化的方法通常是煮沸
D.水体污染的主要污染源是工业废水、农业污水和生活污水
9.能表示两个分子的是
A.2H B.2CO2 C.2SO4 D.SO2
10.下列归纳总结完全正确的一组是
A分子特征 B 数字含义
①水分子很小 ②固体物质的分子不运动 ③气体分子间的间隔很大 ①H2:2 个氢原子 ②:氧化汞中汞元素显+2 价 ③NO2:1 个二氧化氮分子中含有 2 个原子
C生活经验 D节约资源
①禁燃烟花爆竹——降低 PM2.5 ②食品包装中抽真空防腐 ③CO2 增多——酸雨 ①提倡使用太阳能 ②回收利用废旧金属 ③农业灌溉采用滴灌
A.A B.B C.C D.D
11.下列关于化学式“H2O2”的含义描述不正确的是
A.宏观上能表示过氧化氢这种物质
B.表示过氧化氢由氢气与氧气组成
C.表示过氧化氢由氢元素与氧元素组成
D.微观上表示1个过氧化氢分子由2个氢原子和2个氧原子构成
12.抗击新冠肺炎疫情中,化学合成的新药瑞德西韦(分子式:C27H35N6O8P)被寄予厚望。下列有关瑞德西韦说法正确的是
A.瑞德西韦属于有机化合物
B.瑞德西韦由77个原子构成
C.瑞德西韦中氢元素的质量分数最大
D.瑞德西韦的相对分子质量是602g
13.2021年,全民抗疫。在全国抗击新冠疫情中,常用戊二醛(化学式C5H8O2)对医疗器械等进行消毒。下列关于戊二醛说法正确的是
A.从宏观上看:戊二醛由碳、氢、氧三种元素组成
B.从微观上看:戊二醛中含有5个碳原子、8个氢原子和2个氧原子
C.从变化上看:戊二醛在氧气中完全燃烧生成二氧化硫和水
D.从质量上看:戊二醛中碳、氢元素的质量比为5:2
14.毒品带给人类的只会是毁灭,所以我们要珍爱生命,远离毒品.毒品K粉会对大脑造成永久损害,其主要成分是盐酸氯胺酮(化学式为C13H16ONCl).则有关盐酸氯胺酮的下列说法不正确的是
A.该物质是化合物
B.该物质由5种元素组成
C.该物质中C与H元素的质量比是13:16
D.该物质一个分子含有32个原子
15.某物质R是人类生命活动中不可缺少的物质。已知R的相对分子质量为150,其中含碳元素40%,含氢元素6.7%,其余为氧元素。则R的化学式为
A.C5H10O5 B.C5H10O2 C.C6H12O6 D.C6H6O
16.我国C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(),其中硅元素的化合价为价,则氮元素的化合价为
A.-3 B.+3 C.-4 D.+4
二、综合题(共6题)
17.硝酸铵是一种化肥。试计算:
(1)每个硝酸铵分子中共有________个原子;
(2)硝酸铵中氢、氧二种元素原子的个数比是________;
(3)硝酸铵的相对分子质量是________;
(4)硝酸铵中氮元素的质量分数是________(精确到)。
18.用化学用语填空
(1)可用作某些食品干燥剂的氧化物_______;(2)氯化铁溶液中的阳离子_____;
(3)氢硫酸(H2S)中硫元素的化合价为-2价_____; (4)3个氨分子_______。
19.为了消除碘缺病,我国政府规定某地区居民的食用盐必须加碘。下图为广东盐业总公司生产的加碘盐的部分标签,请根据标签图回答:
加碘盐 质量等级:二级 碘含量:20~50mg/kg 配料:食盐、碘酸钾、抗结剂 储存方法:防潮、防热、避光 食用方法:在汤、菜即将煮好时再加入碘盐、确保碘效 保质期:12个月
(1)食用盐必须加碘的“碘”是指________(填单质或元素或原子);该加碘盐属于________(填纯净物或混合物)
(2)碘酸钾(KIO3)中碘元素的化合价为___________;
(3)从标签的“食用方法”推测,碘酸钾的一种化学性质是______________________。
(4)请根据化学式计算:
①碘酸钾的相对分子质量:_________________;(列式计算);
②碘酸钾中各元素间的质量比K:I:O=_____________________;
③碘酸钾中碘元素的质量分数:_____________________(列式计算, 精确到0.1%);
(5)为确保碘盐中碘的最低含量,1Kg碘盐中至少应加入碘酸钾_______mg(精确到0.1 mg)
20.在化学的学习中化学用语非常重要,熟练掌握化学用语对于学习化学至关重要。
(1)下图是钠的原子结构示意图。下列说法不正确的是_______。
a. 钠属于金属元素 b. 钠原子的质子数为11
c. 钠离子的符号为Na+ d.钠在化学反应中易得到电子
(2)请用化学用语表示:
①2个氢原子:___________;②3个氧分子___________;③镁离子:___________;
(3)写出地壳中最多的金属元素的氧化物的化学式:________________ ;
(4)维生素C(C6H806)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。请回答以下问题:
①计算维生素C的相对分子质量______(只要写出结果即可);
②计算维生素C中C、O两种元素的质量比_________(要求写出计算过程);
③计算维生素C中氢元素的质量分数___________(要求写出计算过程,精确到0.1%)。
21.建立宏观、微观和符号之间的联系有重要意义。
(1)下图物质是由不同粒子构成的,请用化学符号表示出构成这些物质的粒子。
构成的粒子是______ 构成的粒子是______ 构成的粒子是______
(2)下图所示为某些元素和原子结构的部分信息。
甲图所示元素的元素符号是 ______,乙图所示元素的原子的核电荷数是______, 丙图所示的粒子属于 ______(填“原子”、“阳离子”或“阴离子”)。
(3)N(NO2) 3是科学家 2011 年发现的一种新型火箭燃料。试计算N(NO2) 3中氮元素和氧元素的质量比为 ______(结果用最简整数比表示),N(NO2) 3中氮元素的质量分数______(最终结果保留一位小数)。
22.水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。
(1)城镇自来水厂生产流程可用如图表示∶
①自来水厂净水过程中用到_____,其作用是吸附;
②自来水厂生产自来水时,使用的净水方法有_____。
A沉淀 B过滤 C煮沸 D蒸馏 E吸附
③世界卫生组织将某氧化物 RO2列为A级高效安全灭菌消毒剂,它在食品保鲜、水的消毒等方面有着广泛应用。实验测得该氧化物中R与O元素的质量比为71∶64,则RO2的化学式为______。
(2)生活中常讲的"烧开水"是指利用_______的方法,获得可以饮用的水,这样既可以降低水的硬度又可以杀灭水中的细菌。
(3)如图表示自来水消毒过程中发生的一个反应的微观过程∶
写出上述物质中单质的化学式∶_________。
参考答案
1.A
【详解】
A、二氧化硅的化学式可以根据其名称写出:SiO2,故A选项正确;
B、水银不银,是金属汞的俗称,化学式为:Hg,故B选项错误;
C、锰酸钾中钾元素为+1价,锰酸根的化合价为-2价,所以其化学式为:K2MnO4,题中符号为高锰酸钾的化学式,故C选项错误;
D、氯元素的符号为:Cl,题中符号为铝元素符号,故D选项错误;
故选A。
2.D
【解析】
试题分析:A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为:2H,故选项化学用语书写错误.
B、氧化铝中铝元素显+3价,氧元素显﹣2价,其化学式为,其化学式为:Al2O3,故选项化学用语书写错误.
C、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故氧根离子可表示为:O2﹣,故选项化学用语书写错误.
D、硅元素的元素符号可表示为:Si,故选项化学用语书写正确.
故选D.
3.C
【详解】
A、C表示的是碳,属于非金属元素,故A错误;
B、S表示的硫,属于非金属元素,P表示的是磷,属于非金属元素,故B错误;
C、K、Mg、Ba都表示的是金属元素,故C正确;
D、H表示的是氢、He表示的是氦,属于非金属元素,故D错误;
4.A
【详解】
A、根据氢元素为价,氧元素为价,设中氯元素的化合价为X。
则(+1)+X+(-2)×4=0,得X=+7,故氯元素的化合价为+7价;
B、根据钠元素为价,氧元素为价,设 NaClO中氯元素的化合价为X。
则(+1)+X+(-2) =0,得X=+1,故氯元素的化合价为+1价;
C、根据氧元素为价,设 中氯元素的化合价为X。
则X×2+(-2)×5=0,得X=+5,故氯元素的化合价为+5价;
D、根据钡元素为价,设 中氯元素的化合价为X。
则+2+X×2=0,得X=-1,故氯元素的化合价为-1价;
故中氯元素的化合价最高,故选A。
5.B
【详解】
①3Hg表示的是3个汞原子;②Fe3 + 表示的是3个铁离子;③S03表示的意义有四种:三氧化硫、三氧化硫是由硫元素和氧元素组成的、一个三氧化硫分子、一个三氧化硫分子是由一个硫元素和3个氧原子构成的;④3H2 O表示的是3个水分子。故选B。
6.C
【详解】
试题分析:一个甲醛(CH2O)分子和一个水(H2O)分子都含有两个氢原子和一个氧原子,不能再描述为表示宏观的意义,因为前面的说法中都强调了一个分子,属于微观的概念。故选C.
7.C
【详解】
A、分子是由原子构成的,葡萄糖分子中不含水分子,故A错误;
B、相对分子质量单位是“1”,不是“克”,常常省略不写,故B错误;
C、葡萄糖中C、H 元素的质量比为(12×6):(1×12)=6:1,故C正确;
D、葡萄糖中碳、氢、氧元素的质量比为(12×6):(1×12):(16×6)=6:1:8,葡萄糖中氧元素的质量分数最大,故D错误。故选C。
8.A
【详解】
A、自来水厂净水的方法中没有蒸馏,错误;
B、水由水分子构成;保持水的化学性质的最小粒子是水分子,正确;
C、硬水是含钙镁离子较多的水;可溶性钙、镁化合物在加热时,能形成沉淀,故生活中常煮沸的方法软化硬水,正确;
D、水体污染的主要污染源是工业废水、农业污水和生活污水,正确;
故选A。
9.B
【详解】
A、2H表示两个氢原子,故不符合题意;
B、2CO2表示两个二氧化碳分子,故符合题意;
C、2SO4缺少粒子所带电荷,错误,故不符合题意;
D、SO2表示一个二氧化硫分子,故不符合题意。
10.D
【详解】
A、固体物质的分子也运动,故不符合题意;
B、H2:一个氢分子由两个氢原子构成,故不符合题意;
C、SO2 增多——酸雨,故不符合题意;
D、提倡使用太阳能、回收利用废旧金属、农业灌溉采用滴灌都符合节约能源,故符合题意。
11.B
【详解】
A、宏观上能表示过氧化氢这种物质;故选项正确,但不符合题意;
B、表示一个过氧化氢分子的;故选项错误,但符合题意;
C、表示过氧化氢由氢元素与氧元素组成;故选项正确,但不符合题意;
D、微观上表示1个过氧化氢分子由2个氢原子和2个氧原子构成;故选项正确,但不符合题意;
故选:B。
12.A
【详解】
A、瑞德西韦是含碳元素的化合物,属于有机化合物,符合题意;
B、瑞德西韦是由瑞德西韦分子构成的,1个瑞德西韦分子是由77个原子构成的,不符合题意;
C、瑞德西韦中碳、氢、氮、氧、磷五种元素的质量比为(12×27):(1×35):(14×6):(16×8):(31×1)=324:35:84:128:31,则瑞德西韦中碳元素的质量分数最高,不符合题意;
D、相对分子质量单位是“1”,不是“克”,常常省略不写,瑞德西韦的相对分子质量为602,不符合题意。故选A。
13.A
【详解】
A、戊二醛是由碳、氢、氧三种元素组成的,故选项说法正确;
B、1个戊二醛分子中含有5个碳原子、8个氢原子和2个氧原子,故选项说法错误;
C、戊二醛在氧气中完全燃烧生成二氧化碳和水,故选项说法错误;
D、戊二醛中碳、氢元素的质量比为(12×5):(1×8)=15:2;故选项说法错误。
故选:A。
14.C
【解析】A、该物质由多种物质组成,故是化合物,正确;B、由化学式可知,该物质由碳元素、氢元素、氧元素、氮元素、氯元素估计5种元素组成,正确;C、该物质中C与H元素的质量比是(13):16=39:4,错误;D、该物质一个分子含有13个碳原子,16个氢原子,1个氧原子,1个氮原子,1个氯原子,估计32个原子,正确。故选C。
15.A
【解析】
设该化合物的化学式为CxHyOz,则相对分子质量=12x+y+16z=150(1)
40%(2) =6.7%(3),由(1)、(2)、(3)式解得:x=5 y=10 z=5,故选A。
16.A
【详解】
硅元素的化合价为+4价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+4)×3+4x=0,则x=-3。
故选:A。
17.9 80
【详解】
(1)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则每个硝酸铵分子中含有9个原子;故填:9;
(2)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则硝酸铵分子中氢、氧两种元素原子的个数比是4:3;故填:4:3;
(3)相对分子质量为构成分子的各原子的相对原子质量之和,所以硝酸铵的相对分子质量为14×2+1×4+16×3=80。故填:80;
(4)化合物中某元素的质量分数是化学式中某元素的相对原子质量与相应原子个数的乘积与相对分子质量之比,硝酸铵中氮元素的质量分数是;故填:35%。
18.CaO; Fe3+; ; 3NH3;
【解析】
(1)氧化钙能与空气中的水蒸气发生反应生成氢氧化钙,故可用作某些食品干燥剂的氧化物CaO;(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。氯化铁溶液中的阳离子可表示为:Fe3+;(3)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,氢硫酸(H2S)中,氢元素的化合价为+1价;氢硫酸(H2S)中硫元素化合价可表示为:;(4)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个氨分子可表示为:3NH3。
19.元素 混合物 +5 受热会分解 39+127+16×3=214 K:I:O= 39:127:48 59.3% 33.7mg
【解析】
(1)食盐中的“碘”不是单质,也不是原子,而是元素,加碘食盐属于混合物;(2)
根据在化合物中正负化合价代数和为零,设碘酸钾(KIO 3 )中碘元素的化合价为,则 (+1)++(-2)×3=0,=+5;(3)根据加碘盐图中标签信息,在汤、菜即将煮好时再加入碘盐、确保碘效,可得碘酸钾的一种化学性质是:受热易分解或受热不稳定;(4)①根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得碘酸钾的相对分子质量为:39+127+16×3=214;②碘酸钾中各元素间的质量比K:I:O=39:127:(16x3)=39:127:48;③碘酸钾中碘元素的质量分数:;(5)根据物质中某元素的质量=物质的质量×该元素的质量分数,依据1kg加碘盐中碘含量:20~50mg/kg,设1kg碘盐中至少应加入碘酸钾为 g,
解得 ≈33.7 mg。
20.d 2H 3O2 Mg2+ Al2O3 176 3:4 4.5%
【详解】
(1)a、由某元素的原子结构示意图,圆圈内数字表示核内质子数,其核内质子数为11,为钠元素,属于金属元素,故正确;
b、某元素的原子结构示意图,圆圈内数字表示核内质子数,其核内质子数为11,故正确;
c、由某元素的原子结构示意图,最外层电子数是1,在化学反应中失去1个电子而形成阳离子,钠离子的符号为Na+,故正确;
d、由某元素的原子结构示意图,最外层电子数是1,在化学反应中失去1个电子而形成阳离子,故错误;
(2)①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以2个氢原子,就可表示为:2H;
②由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则3个氧分子可表示为:3O2;
③离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故镁离子可表示为:Mg2+;
(3)先弄清地壳中含量最多的金属元素为铝元素,形成的氧化物为氧化铝,其中铝元素的化合价为+3价,氧元素的化合价为-2价,所以化学式为Al2O3;
(4)①维生素C的相对分子质量为12×6+1×8+16×6=176;
②维生素C中碳、氧元素的质量比=(12×6):(16×6)=3:4;
③维生素C中氢元素的质量分数为: =4.5%。
21.H2O Cu Na+、Cl- Al 8 阳离子 7:12 36.8%
【详解】
(1)水是由水分子构成的,H2O可表示水分子;铜是由铜原子构成的,单独的一个元素符号可表示一个该原子,Cu可表示铜原子;氯化钠是由钠离子(Na+)、氯离子(Cl-)构成的。
(2)铝的元素符号为Al;乙图所示是氧元素的元素周期表信息,原子序数在数值上等于原子的核电荷数,故该原子的核电荷数为8;丙图所示的粒子中有12个质子、10个电子,质子数>核外电子数,所以该粒子属于阳离子。
(3)N(NO2) 3中氮元素和氧元素的质量比为:(14×4):(16×6)≈7:12 ,N(NO2) 3中氮元素的质量分数为:=36.8%
22.活性炭 ABE ClO2 煮沸 Cl2
【详解】
(1)①自来水厂净水过程中用到活性炭,活性炭具有疏松多孔的结构,其作用是吸附;
②来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附、消毒。故选ABE;
③实验测得该氧化物中R与O元素的质量比为71∶64,设R的相对原子质量为x,则x:(16×2)=71:62,x=35.5,故R是Cl,RO2的化学式为ClO2;
(2)生活中常讲的"烧开水"是指利用煮沸的方法,获得可以饮用的水,这样既可以降低水的硬度又可以杀灭水中的细菌;
(3)由图可知,B是由同种元素组成的纯净物,属于单质,每个B分子由2个氯原子构成,化学式为Cl2。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
