高中化学人教版(2019)必修第一册1.3.2.氧化剂和还原剂(共14张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第一册1.3.2.氧化剂和还原剂(共14张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 236.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-26 09:45:48 | ||
图片预览






文档简介
(共14张PPT)
氧化剂和还原剂
课前准备你做好了吗?请集中精力学习吧!
学习目标:
1、了解氧化还原反应中氧化剂和还原剂的概念。
2、了解氧化剂和还原剂在氧化还原反应中的变化规律。
月饼盒中为什么要放一包脱氧剂呢?
脱氧剂
Fe粉
月饼变质主要存在两方面的原因:
一是月饼中微生物指标超标。食品包装容器内的大量氧气,会引起好氧性细菌和霉菌的快速生长,导致食品霉变和腐败。
二是油脂酸败。月饼中的植物油脂在空气中能被氧气氧化,从而导致月饼的酸败,产生异味,影响月饼的品质。
还原剂:所含的某种元素化合价升高的反应物。
4Fe+3O2+6H2O 4Fe(OH)3
原理:
脱氧剂 Fe粉的作用是什么?
氧化剂:所含的某种元素化合价降低的反应物。
具有氧化性。
具有还原性。
0
0
+3
-2
+1
-2
+1
4Fe+3O2+6H2O 4Fe(OH)3
0
0
+3
-2
Fe
Fe(OH)3
0
+3
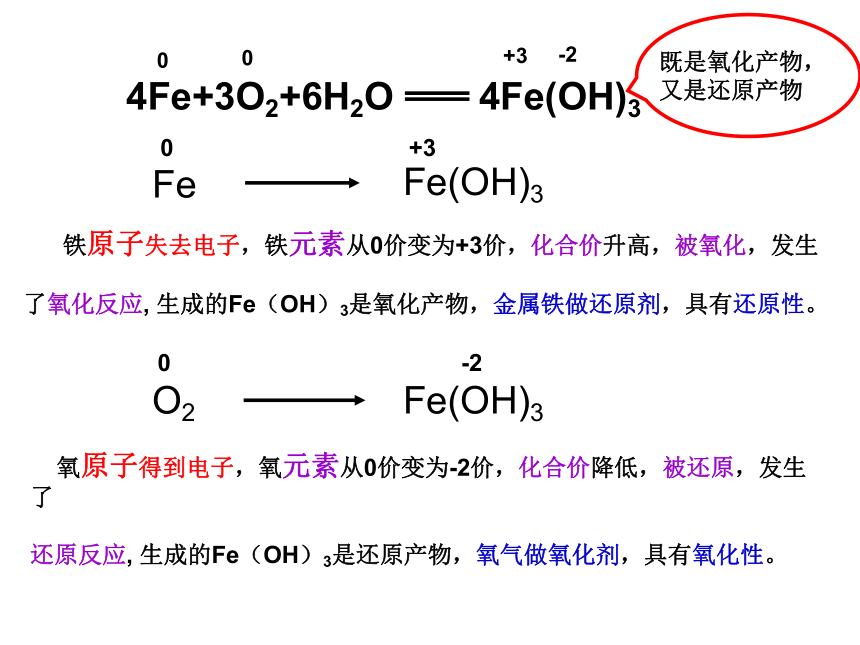
铁原子失去电子,铁元素从0价变为+3价,化合价升高,被氧化,发生
了氧化反应, 生成的Fe(OH)3是氧化产物,金属铁做还原剂,具有还原性。
O2
Fe(OH)3
0
-2
氧原子得到电子,氧元素从0价变为-2价,化合价降低,被还原,发生了
还原反应, 生成的Fe(OH)3是还原产物,氧气做氧化剂,具有氧化性。
既是氧化产物,
又是还原产物
升 失 氧,
降 得 还,
若 说 剂,
则 相 反。
【口诀】
化合价升高
化合价降低
失去电子
发生氧化反应
被氧化,
对应氧化产物
得到电子
若发生氧化反应,
则为还原剂
若发生还原反应,
则为氧化剂
发生还原反应
被还原,
对应还原产物
Fe2O3+3CO 2Fe+3CO2
高温
+3
+2
0
+4
得到2×3e- ,化合价降低
失去3×2e-,化合价升高
升、失、氧
降、得、还
若 说 剂
则 相 反
铁元素被( ),发生( )反应,生成的Fe是( )产物
Fe2O3作( )剂,具有( )性。
碳元素被( ),发生( )反应,生成的CO2是( )产物
CO作( )剂,具有( )性。
还原
还原
还原
还原
还原
氧化
氧化
氧化
氧化
氧化
S+2KNO3+3C K2S+3CO2+N2
点燃
0
0
0
+5
-2
+4
得到1×2e-,化合价降低
失去3×4e-,化合价升高
升、失、氧
降、得、还
若 说 剂
则 相 反
得到2×5e-,化合价降低
( )作氧化剂,具有氧化性;( )作还原剂,具有还原性。
( )是氧化产物,( )是还原产物 。
S、KNO3
C
CO2
K2S、N2
Cl2+2NaOH NaCl+NaClO+H2O
0
-1
+1
失去1×1e-电子,化合价升高
得到1×1e-电子,化合价降低
升、失、氧
降、得、还
若 说 剂
则 相 反
( )元素化合价升高,( )原子失去电子,( )元素被氧化,
发生了氧化反应,生成的氧化产物是( ),( )是还原剂。
( )元素化合价降低,( )原子得到电子,( )元素被还原,
发生了还原反应,生成的还原产物是( ),( )是氧化剂。
Cl
Cl
Cl
Cl
Cl
Cl
NaClO
Cl2
NaCl
Cl2
总结:
Fe2O3+3CO 2Fe+3CO2
高温
S+2KNO3+3C K2S+3CO2+N2
点燃
Cl2+2NaOH NaCl+NaClO+H2O
氧化剂
还原剂
氧化剂
还原剂
既是氧化剂又是还原剂
【课堂小结】
氧化剂和还原剂
概念
氧化剂:所含某种元素化合价降低的反应物。
还原剂:所含某种元素化合价升高的反应物。
规律
化合价升高 失去电子 发生氧化反应 被氧化 对应氧化产物 做还原剂 具有还原性
化合价降低 得到电子 发生还原反应 被还原
对应还原产物 做氧化剂 具有氧化性
口诀
谢谢大家!
再见!
氧化剂和还原剂
课前准备你做好了吗?请集中精力学习吧!
学习目标:
1、了解氧化还原反应中氧化剂和还原剂的概念。
2、了解氧化剂和还原剂在氧化还原反应中的变化规律。
月饼盒中为什么要放一包脱氧剂呢?
脱氧剂
Fe粉
月饼变质主要存在两方面的原因:
一是月饼中微生物指标超标。食品包装容器内的大量氧气,会引起好氧性细菌和霉菌的快速生长,导致食品霉变和腐败。
二是油脂酸败。月饼中的植物油脂在空气中能被氧气氧化,从而导致月饼的酸败,产生异味,影响月饼的品质。
还原剂:所含的某种元素化合价升高的反应物。
4Fe+3O2+6H2O 4Fe(OH)3
原理:
脱氧剂 Fe粉的作用是什么?
氧化剂:所含的某种元素化合价降低的反应物。
具有氧化性。
具有还原性。
0
0
+3
-2
+1
-2
+1
4Fe+3O2+6H2O 4Fe(OH)3
0
0
+3
-2
Fe
Fe(OH)3
0
+3
铁原子失去电子,铁元素从0价变为+3价,化合价升高,被氧化,发生
了氧化反应, 生成的Fe(OH)3是氧化产物,金属铁做还原剂,具有还原性。
O2
Fe(OH)3
0
-2
氧原子得到电子,氧元素从0价变为-2价,化合价降低,被还原,发生了
还原反应, 生成的Fe(OH)3是还原产物,氧气做氧化剂,具有氧化性。
既是氧化产物,
又是还原产物
升 失 氧,
降 得 还,
若 说 剂,
则 相 反。
【口诀】
化合价升高
化合价降低
失去电子
发生氧化反应
被氧化,
对应氧化产物
得到电子
若发生氧化反应,
则为还原剂
若发生还原反应,
则为氧化剂
发生还原反应
被还原,
对应还原产物
Fe2O3+3CO 2Fe+3CO2
高温
+3
+2
0
+4
得到2×3e- ,化合价降低
失去3×2e-,化合价升高
升、失、氧
降、得、还
若 说 剂
则 相 反
铁元素被( ),发生( )反应,生成的Fe是( )产物
Fe2O3作( )剂,具有( )性。
碳元素被( ),发生( )反应,生成的CO2是( )产物
CO作( )剂,具有( )性。
还原
还原
还原
还原
还原
氧化
氧化
氧化
氧化
氧化
S+2KNO3+3C K2S+3CO2+N2
点燃
0
0
0
+5
-2
+4
得到1×2e-,化合价降低
失去3×4e-,化合价升高
升、失、氧
降、得、还
若 说 剂
则 相 反
得到2×5e-,化合价降低
( )作氧化剂,具有氧化性;( )作还原剂,具有还原性。
( )是氧化产物,( )是还原产物 。
S、KNO3
C
CO2
K2S、N2
Cl2+2NaOH NaCl+NaClO+H2O
0
-1
+1
失去1×1e-电子,化合价升高
得到1×1e-电子,化合价降低
升、失、氧
降、得、还
若 说 剂
则 相 反
( )元素化合价升高,( )原子失去电子,( )元素被氧化,
发生了氧化反应,生成的氧化产物是( ),( )是还原剂。
( )元素化合价降低,( )原子得到电子,( )元素被还原,
发生了还原反应,生成的还原产物是( ),( )是氧化剂。
Cl
Cl
Cl
Cl
Cl
Cl
NaClO
Cl2
NaCl
Cl2
总结:
Fe2O3+3CO 2Fe+3CO2
高温
S+2KNO3+3C K2S+3CO2+N2
点燃
Cl2+2NaOH NaCl+NaClO+H2O
氧化剂
还原剂
氧化剂
还原剂
既是氧化剂又是还原剂
【课堂小结】
氧化剂和还原剂
概念
氧化剂:所含某种元素化合价降低的反应物。
还原剂:所含某种元素化合价升高的反应物。
规律
化合价升高 失去电子 发生氧化反应 被氧化 对应氧化产物 做还原剂 具有还原性
化合价降低 得到电子 发生还原反应 被还原
对应还原产物 做氧化剂 具有氧化性
口诀
谢谢大家!
再见!
