1.2有机化合物的结构与性质——2021-2022学年高二化学鲁科版(2019)选择性必修三同步课时作业
文档属性
| 名称 | 1.2有机化合物的结构与性质——2021-2022学年高二化学鲁科版(2019)选择性必修三同步课时作业 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-26 00:00:00 | ||
图片预览




文档简介
1.2有机化合物的结构与性质
1.下列关于有机化合物种类繁多的原因叙述不正确的是( )
A.碳原子性质活泼,容易形成化合物
B.碳原子之间能以共价键形成碳链或碳环
C.碳原子之间能形成单键,也能形成双键或三键
D.碳原子除了彼此间可以成键外,还可以与其他元素的原子成键
2.对于分子式为的有机化合物结构的说法中不正确的是( )
A.可能是分子中只有一个双键的链烃 B.分子中可能有两个双键
C.分子中可能只含有一个三键 D.分子中含有一个双键的环烃
3.下列各组物质中互为同分异构体的是( )
A.水与冰
B.
C. 与
D. 与
4.下列各组物质,属于官能团类型异构的是( )
A.和
B.和
C.和
D.和
5.下列说法正确的是( )
A.两种烃相对分子质量相同,但结构不同,性质也不同,一定互为同分异构体
B.有机化合物和无机物之间可能出现同分异构现象
C.两种有机化合物若互为同分异构体,则它们一定不互为同系物
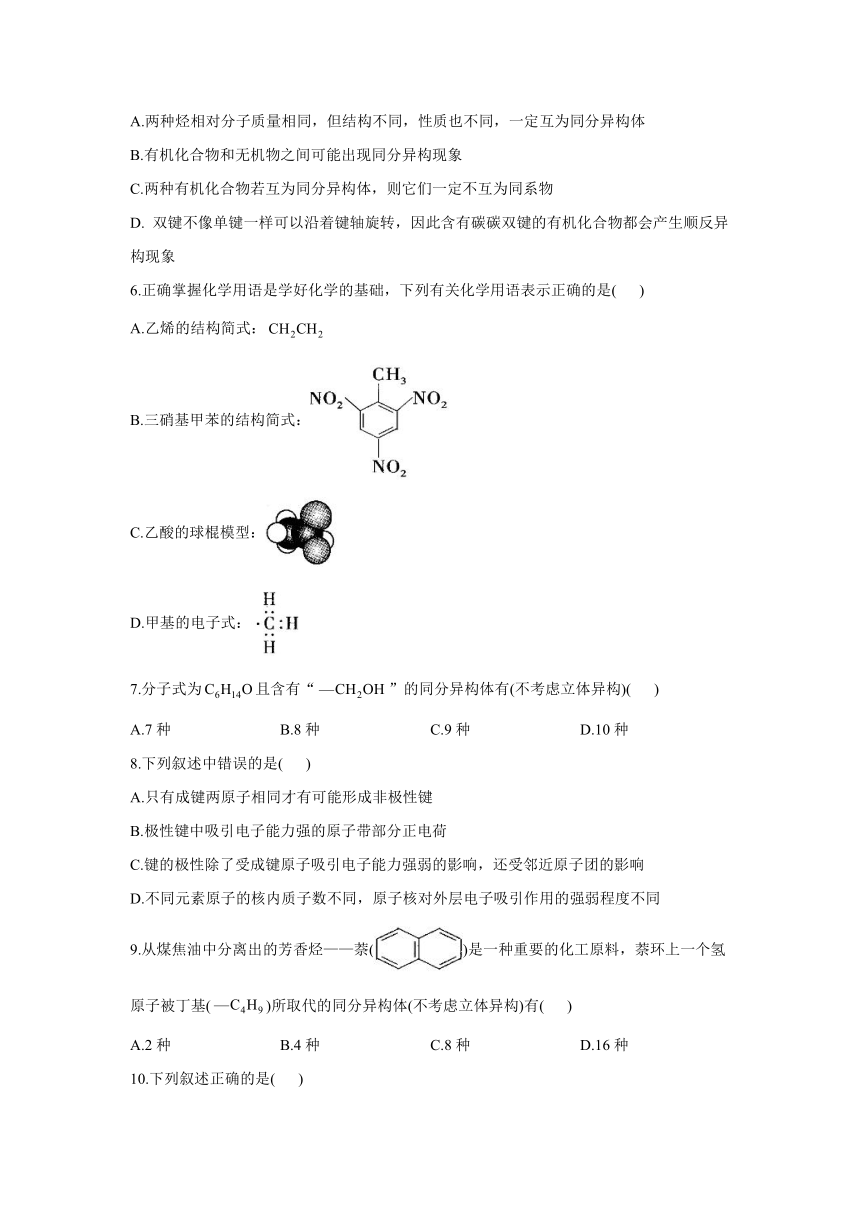
D. 双键不像单键一样可以沿着键轴旋转,因此含有碳碳双键的有机化合物都会产生顺反异构现象
6.正确掌握化学用语是学好化学的基础,下列有关化学用语表示正确的是( )
A.乙烯的结构简式:
B.三硝基甲苯的结构简式:
C.乙酸的球棍模型:
D.甲基的电子式:
7.分子式为且含有“”的同分异构体有(不考虑立体异构)( )
A.7种 B.8种 C.9种 D.10种
8.下列叙述中错误的是( )
A.只有成键两原子相同才有可能形成非极性键
B.极性键中吸引电子能力强的原子带部分正电荷
C.键的极性除了受成键原子吸引电子能力强弱的影响,还受邻近原子团的影响
D.不同元素原子的核内质子数不同,原子核对外层电子吸引作用的强弱程度不同
9.从煤焦油中分离出的芳香烃——萘()是一种重要的化工原料,萘环上一个氢原子被丁基()所取代的同分异构体(不考虑立体异构)有( )
A.2种 B.4种 C.8种 D.16种
10.下列叙述正确的是( )
A.苯分子是环状结构,其性质跟环状烷烃相似
B.表示苯分子的结构,其中含有碳碳单键、双键,因此苯的性质跟烯烃相同
C.苯的分子式为,分子中碳原子远远没有饱和,因此能和溴水中的溴发生加成反应
D.苯不能使酸性溶液褪色
11.下列对有机化合物的化学性质的叙述错误的是( )
A.1 mol该物质能与2 mol 发生加成反应
B.能与乙醇发生酯化反应
C.能发生加聚反应,生成高聚物
D.能与溶液反应放出气体
12.下列说法正确的是( )
A.甲醇与乙醇的官能团都是羟基,它们具有完全相同的性质
B.甲苯与苯互为同分异构体,它们具有相似的性质
C.烯烃的官能团是碳碳双键,任何烯烃在一定条件下都能发生加成反应
D.乙醛、丙酮、乙酸中都含有羰基,因此它们具有相似的化学性质
13.下列各组物质中,属于立体异构的是( )
A.和
B. 和
C. 和
D.和
14.现有下列各组物质:
①
②和
③和
④
⑤
⑥和质量数为238、中子数为146的原子
⑦
按要求用序号填空:
(1)互为同系物的是______________。
(2)互为同分异构体的是________________。
(3)互为同位素的是__________。
(4)互为同素异形体的是_____________。
(5)属于同种物质的是_________________。
15.回答下列问题:
(1)键线式表示的物质的分子式:_____________。
(2) 中含有的官能团的名称为___________________。
(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:____________________。
(4)某芳香烃的结构为,它的分子式为___________,一氯代物有__________________种。
(5)分子式为的某烃的所有碳原子都在同一平面上,则该烃的结构简式为__________________,若分子式为的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_________________。
答案以及解析
1.答案:A
解析:碳原子最外层有4个电子,很难得失电子,化学性质不活泼,故A错误;碳原子之间能相互成键,可以成碳链,也可以成碳环,是有机化合物种类繁多的原因之一,故B正确;碳原子能形成四个共价单键,碳原子之间可以形成单键、双键或三键,是有机化合物种类繁多的原因之一,故C正确;碳原子除了彼此间可以成键外,还可以与其他元素的原子成键,是有机化合物种类繁多的原因之一,故D正确。
2.答案:A
解析:含5个碳原子的饱和烃应含有12个氢原子,较饱和烃少了12-8=4个氢原子,每减少2个氢原子就增加一个不饱和度,所以该分子结构有四种可能:①两个双键,②一个三键,③一个双键和一个环,④两个环。故A项不合理。
3.答案:D
解析:水与冰均由分子构成,为同一种物质,故A错误;是O元素形成的两种不同的单质,两者互为同素异形体,故B错误;与分子式相同,结构也相同,为同一物质,都是丙烷,故C错误;与的分子式都是,但结构不同,前者为异戊烷,后者为新戊烷,两者互为同分异构体,故D正确。
4.答案:C
解析:的分子式相同,碳骨架不同,属于碳骨架异构,故A不符合题意;和的分子式相同,碳碳双键的位置不同,属于官能团位置异构,故B不符合题意;的分子式相同,官能团分别为羟基和醚键,属于官能团类型异构,故C符合题意;的分子式相同,官能团相同,碳骨架不同,属于碳骨架异构,故D不符合题意。
5.答案:BC
解析:两种烃相对分子质量相同,但结构不同,两者分子组成不一定相同,如,则不一定互为同分异构体,故A错误;有机化合物和无机物之间可能出现同分异构现象,如尿素和氰酸铵,故B错误;同分异构体要求分子组成相同,而同系物要求分子组成相差一个或若干个原子团,分子组成不相同,即互为同分异构体的两种有机化合物一定不互为同系物,故C正确;只有当碳碳双键的两个碳原子所连其他两个原子或原子团不同时,含有碳碳双键的有机化合物才会产生顺反异构现象,故D错误。
6.答案:D
解析:书写结构简式时,乙烯中的碳碳双键不可省略,结构简式应为,故A错误;硝基中的N原子直接与苯环相连,三硝基甲苯的结构简式应为,故B错误;为乙酸的空间填充模型,乙酸的球棍模型为,故C错误;甲基中含有一个单电子,电子式为,故D正确。
7.答案:B
解析:由题意知该醇的结构简式一定满足,因具有8种不同的结构,则的同分异构体有8种,故B正确。
8.答案:B
解析:要形成非极性键,必须保证成键原子相同,如果成键原子不同,则吸引电子能力强的原子带部分负电荷,并且键的极性受邻近基团影响,故B项错误。
9.答案:C
解析:丁基有四种结构:,萘环上有2种化学环境的氢原子:,则萘环上一个氢原子被丁基()所取代的同分异构体(不考虑立体异构)有8种,故C正确。
10.答案:D
解析:苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊共价键,因此具有与单键和双键不同的性质,与环烷烃、烯烃的性质均不相同,也不能与溴水中的溴发生加成反应,故A、B、C错误;苯不能使酸性溶液褪色,D项正确。
11.答案:A
解析:该物质中含和COOH两种官能团, COOH不能与发生加成反应,1 mol该物质能与1 mol 发生加成反应,故A错误。
12.答案:C
解析: 甲醇与乙醇都含有羟基,具有相似的性质,但是与羟基相连的基团不同,性质会有差异,不完全相同,A项错误;甲苯与苯互为同系物,而不是同分异构体,因都含有苯环而具有某些相似的性质,B项错误;烯烃中必定含有碳碳双键,因而能发生加成反应,C项正确;乙醛、丙酮、乙酸虽都含有结构,但结构所连基团不同,官能团不同,三者性质有很大差别,D项错误。
13.答案:C
解析:分子式为,分子式为,二者分子式不同,不互为同分异构体,A错误;属于芳香醇,属于醚,二者属于官能团类型异构,B错误;与属于立体异构,C正确;与为同一物质,D错误。
14.答案:(1)⑤
(2)⑦
(3)⑥
(4)①
(5)③④
解析: (1)的结构相似,分子组成上相差2个,二者互为同系物。
(2)的分子式相同,均是,结构不同,互为同分异构体。
(3)质量数为238、中子数为146的原子的质子数为238-146=92,与的质子数相同,中子数不同,二者互为同位素。
(4)是由氧元素形成的不同单质,二者互为同素异形体。
(5) 和均表示二氯甲烷,是同种物质,均表示水分子,属于同种物质。
15.答案:(1)
(2) 羟基、酯基
(3)
(4);4
(5) ;
解析: (1)由键线式可知,该物质属于饱和烃,分子中含有6个碳原子,分子式为。
(2) 中含有的官能团的名称为羟基、酯基。
(3)戊烷的某种同分异构体只有一种一氯代物,则该有机化合物分子中只含1种化学环境的氢原子,该烃的结构简式为。
(4)芳香烃的结构简式是,则其分子式是。该有机化合物的结构对称,分子中有4种化学环境的氢原子,所以其一氯代物有4种。
(5)根据乙烯是平面形分子,可看作乙烯中的四个氢原子被甲基取代,所以分子式为、所有碳原子都在同一平面上的烃的结构简式为;乙炔是直线形分子,可看作甲基取代乙炔分子中的氢原子,所以分子式为、所有的碳原子都在同一条直线上的烃的结构简式是。
1.下列关于有机化合物种类繁多的原因叙述不正确的是( )
A.碳原子性质活泼,容易形成化合物
B.碳原子之间能以共价键形成碳链或碳环
C.碳原子之间能形成单键,也能形成双键或三键
D.碳原子除了彼此间可以成键外,还可以与其他元素的原子成键
2.对于分子式为的有机化合物结构的说法中不正确的是( )
A.可能是分子中只有一个双键的链烃 B.分子中可能有两个双键
C.分子中可能只含有一个三键 D.分子中含有一个双键的环烃
3.下列各组物质中互为同分异构体的是( )
A.水与冰
B.
C. 与
D. 与
4.下列各组物质,属于官能团类型异构的是( )
A.和
B.和
C.和
D.和
5.下列说法正确的是( )
A.两种烃相对分子质量相同,但结构不同,性质也不同,一定互为同分异构体
B.有机化合物和无机物之间可能出现同分异构现象
C.两种有机化合物若互为同分异构体,则它们一定不互为同系物
D. 双键不像单键一样可以沿着键轴旋转,因此含有碳碳双键的有机化合物都会产生顺反异构现象
6.正确掌握化学用语是学好化学的基础,下列有关化学用语表示正确的是( )
A.乙烯的结构简式:
B.三硝基甲苯的结构简式:
C.乙酸的球棍模型:
D.甲基的电子式:
7.分子式为且含有“”的同分异构体有(不考虑立体异构)( )
A.7种 B.8种 C.9种 D.10种
8.下列叙述中错误的是( )
A.只有成键两原子相同才有可能形成非极性键
B.极性键中吸引电子能力强的原子带部分正电荷
C.键的极性除了受成键原子吸引电子能力强弱的影响,还受邻近原子团的影响
D.不同元素原子的核内质子数不同,原子核对外层电子吸引作用的强弱程度不同
9.从煤焦油中分离出的芳香烃——萘()是一种重要的化工原料,萘环上一个氢原子被丁基()所取代的同分异构体(不考虑立体异构)有( )
A.2种 B.4种 C.8种 D.16种
10.下列叙述正确的是( )
A.苯分子是环状结构,其性质跟环状烷烃相似
B.表示苯分子的结构,其中含有碳碳单键、双键,因此苯的性质跟烯烃相同
C.苯的分子式为,分子中碳原子远远没有饱和,因此能和溴水中的溴发生加成反应
D.苯不能使酸性溶液褪色
11.下列对有机化合物的化学性质的叙述错误的是( )
A.1 mol该物质能与2 mol 发生加成反应
B.能与乙醇发生酯化反应
C.能发生加聚反应,生成高聚物
D.能与溶液反应放出气体
12.下列说法正确的是( )
A.甲醇与乙醇的官能团都是羟基,它们具有完全相同的性质
B.甲苯与苯互为同分异构体,它们具有相似的性质
C.烯烃的官能团是碳碳双键,任何烯烃在一定条件下都能发生加成反应
D.乙醛、丙酮、乙酸中都含有羰基,因此它们具有相似的化学性质
13.下列各组物质中,属于立体异构的是( )
A.和
B. 和
C. 和
D.和
14.现有下列各组物质:
①
②和
③和
④
⑤
⑥和质量数为238、中子数为146的原子
⑦
按要求用序号填空:
(1)互为同系物的是______________。
(2)互为同分异构体的是________________。
(3)互为同位素的是__________。
(4)互为同素异形体的是_____________。
(5)属于同种物质的是_________________。
15.回答下列问题:
(1)键线式表示的物质的分子式:_____________。
(2) 中含有的官能团的名称为___________________。
(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:____________________。
(4)某芳香烃的结构为,它的分子式为___________,一氯代物有__________________种。
(5)分子式为的某烃的所有碳原子都在同一平面上,则该烃的结构简式为__________________,若分子式为的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_________________。
答案以及解析
1.答案:A
解析:碳原子最外层有4个电子,很难得失电子,化学性质不活泼,故A错误;碳原子之间能相互成键,可以成碳链,也可以成碳环,是有机化合物种类繁多的原因之一,故B正确;碳原子能形成四个共价单键,碳原子之间可以形成单键、双键或三键,是有机化合物种类繁多的原因之一,故C正确;碳原子除了彼此间可以成键外,还可以与其他元素的原子成键,是有机化合物种类繁多的原因之一,故D正确。
2.答案:A
解析:含5个碳原子的饱和烃应含有12个氢原子,较饱和烃少了12-8=4个氢原子,每减少2个氢原子就增加一个不饱和度,所以该分子结构有四种可能:①两个双键,②一个三键,③一个双键和一个环,④两个环。故A项不合理。
3.答案:D
解析:水与冰均由分子构成,为同一种物质,故A错误;是O元素形成的两种不同的单质,两者互为同素异形体,故B错误;与分子式相同,结构也相同,为同一物质,都是丙烷,故C错误;与的分子式都是,但结构不同,前者为异戊烷,后者为新戊烷,两者互为同分异构体,故D正确。
4.答案:C
解析:的分子式相同,碳骨架不同,属于碳骨架异构,故A不符合题意;和的分子式相同,碳碳双键的位置不同,属于官能团位置异构,故B不符合题意;的分子式相同,官能团分别为羟基和醚键,属于官能团类型异构,故C符合题意;的分子式相同,官能团相同,碳骨架不同,属于碳骨架异构,故D不符合题意。
5.答案:BC
解析:两种烃相对分子质量相同,但结构不同,两者分子组成不一定相同,如,则不一定互为同分异构体,故A错误;有机化合物和无机物之间可能出现同分异构现象,如尿素和氰酸铵,故B错误;同分异构体要求分子组成相同,而同系物要求分子组成相差一个或若干个原子团,分子组成不相同,即互为同分异构体的两种有机化合物一定不互为同系物,故C正确;只有当碳碳双键的两个碳原子所连其他两个原子或原子团不同时,含有碳碳双键的有机化合物才会产生顺反异构现象,故D错误。
6.答案:D
解析:书写结构简式时,乙烯中的碳碳双键不可省略,结构简式应为,故A错误;硝基中的N原子直接与苯环相连,三硝基甲苯的结构简式应为,故B错误;为乙酸的空间填充模型,乙酸的球棍模型为,故C错误;甲基中含有一个单电子,电子式为,故D正确。
7.答案:B
解析:由题意知该醇的结构简式一定满足,因具有8种不同的结构,则的同分异构体有8种,故B正确。
8.答案:B
解析:要形成非极性键,必须保证成键原子相同,如果成键原子不同,则吸引电子能力强的原子带部分负电荷,并且键的极性受邻近基团影响,故B项错误。
9.答案:C
解析:丁基有四种结构:,萘环上有2种化学环境的氢原子:,则萘环上一个氢原子被丁基()所取代的同分异构体(不考虑立体异构)有8种,故C正确。
10.答案:D
解析:苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊共价键,因此具有与单键和双键不同的性质,与环烷烃、烯烃的性质均不相同,也不能与溴水中的溴发生加成反应,故A、B、C错误;苯不能使酸性溶液褪色,D项正确。
11.答案:A
解析:该物质中含和COOH两种官能团, COOH不能与发生加成反应,1 mol该物质能与1 mol 发生加成反应,故A错误。
12.答案:C
解析: 甲醇与乙醇都含有羟基,具有相似的性质,但是与羟基相连的基团不同,性质会有差异,不完全相同,A项错误;甲苯与苯互为同系物,而不是同分异构体,因都含有苯环而具有某些相似的性质,B项错误;烯烃中必定含有碳碳双键,因而能发生加成反应,C项正确;乙醛、丙酮、乙酸虽都含有结构,但结构所连基团不同,官能团不同,三者性质有很大差别,D项错误。
13.答案:C
解析:分子式为,分子式为,二者分子式不同,不互为同分异构体,A错误;属于芳香醇,属于醚,二者属于官能团类型异构,B错误;与属于立体异构,C正确;与为同一物质,D错误。
14.答案:(1)⑤
(2)⑦
(3)⑥
(4)①
(5)③④
解析: (1)的结构相似,分子组成上相差2个,二者互为同系物。
(2)的分子式相同,均是,结构不同,互为同分异构体。
(3)质量数为238、中子数为146的原子的质子数为238-146=92,与的质子数相同,中子数不同,二者互为同位素。
(4)是由氧元素形成的不同单质,二者互为同素异形体。
(5) 和均表示二氯甲烷,是同种物质,均表示水分子,属于同种物质。
15.答案:(1)
(2) 羟基、酯基
(3)
(4);4
(5) ;
解析: (1)由键线式可知,该物质属于饱和烃,分子中含有6个碳原子,分子式为。
(2) 中含有的官能团的名称为羟基、酯基。
(3)戊烷的某种同分异构体只有一种一氯代物,则该有机化合物分子中只含1种化学环境的氢原子,该烃的结构简式为。
(4)芳香烃的结构简式是,则其分子式是。该有机化合物的结构对称,分子中有4种化学环境的氢原子,所以其一氯代物有4种。
(5)根据乙烯是平面形分子,可看作乙烯中的四个氢原子被甲基取代,所以分子式为、所有碳原子都在同一平面上的烃的结构简式为;乙炔是直线形分子,可看作甲基取代乙炔分子中的氢原子,所以分子式为、所有的碳原子都在同一条直线上的烃的结构简式是。
