第九单元 溶液 单元测试B卷-2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 第九单元 溶液 单元测试B卷-2021-2022学年九年级化学人教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 197.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-24 00:00:00 | ||
图片预览

文档简介
第九单元 溶液
B卷·名校好题提升卷
(满分100分,考试时间60分钟)
相对原子质量 H:1 C:12 O:16 Na:23 Mg:24 Al:27 Ca:40 Cu:64 Zn:65 Ag:108
可能用到的相对原子质量:H——1 C——12 O——16 S——32 Fe——56
一、选择题(每小题2分,共30分,每小题只有一个选项符合题意)
1.(2020·河北石家庄第二十八中学模拟)溶解适量的固体碘制成消毒液,应该使用( )
A.蒸馏水 B.酒精 C.汽油 D.生理盐水
2.(2021·广西钦州四中月考)溶液这种混合物,之所以具有均一性和稳定性,是因为( )
A.溶质是固体 B.溶剂是水
C.溶液是液体 D.溶质被解离成分子或离子状态
3.(2021·安徽蚌埠模拟)把20℃的100g硝酸钾饱和溶液升温至60℃,下列叙述错误的是( )
A.溶液仍然为饱和溶液 B.溶质的质量不变
C.溶剂的质量不变 D.溶液变为不饱和溶液
4.(2021·山东肥城期中)关于100g10%的硝酸钾溶液,下列叙述正确的是( )
A.100g水中溶有10g硝酸钾
B.溶液中硝酸钾与水的质量比为1:10
C.将硝酸钾和水按9:1的质量比配成的溶液
D.将10g硝酸钾溶于90g水中,可制得该溶液
5.下列现象,不能说明气体溶解度随温度升高而减小的是( )
A.天气闷热时,池塘里的鱼浮出水面
B.喝下汽水时,感到有气体冲击胃,易打嗝
C.揭开啤酒瓶瓶盖,有大量气泡逸出
D.烧开水时,沸腾前有气泡逸出
6.下列清洁方法中,利用了乳化原理的是( )
A.用自来水洗手 B.用生理盐水清洗伤口
C.用洗涤剂洗衣服上的油污 D.用酒精清洗医疗器械
7.(2021·山东东营模拟)实验室配制50g溶质质量分数为15%的氯化钠溶液。下列有关操作中不会造成误差的是( )
A.用量筒量取水时仰视读数
B.溶解过程中使用玻璃棒搅拌
C.用托盘天平称取食盐时,将食盐放在右盘,且称量时使用了游码
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
8.(2021·四川成都模拟)25℃时,取100mL氯化钠饱和溶液进行如图所示实验,下列分析错误的是( )
A.实验1后,甲、乙两溶液完全相同
B.实验2后,甲、乙两溶液的质量相等
C.实验2后,乙中溶液为氯化钠的饱和溶液
D.实验2后,甲、乙溶液所含溶质质量相等
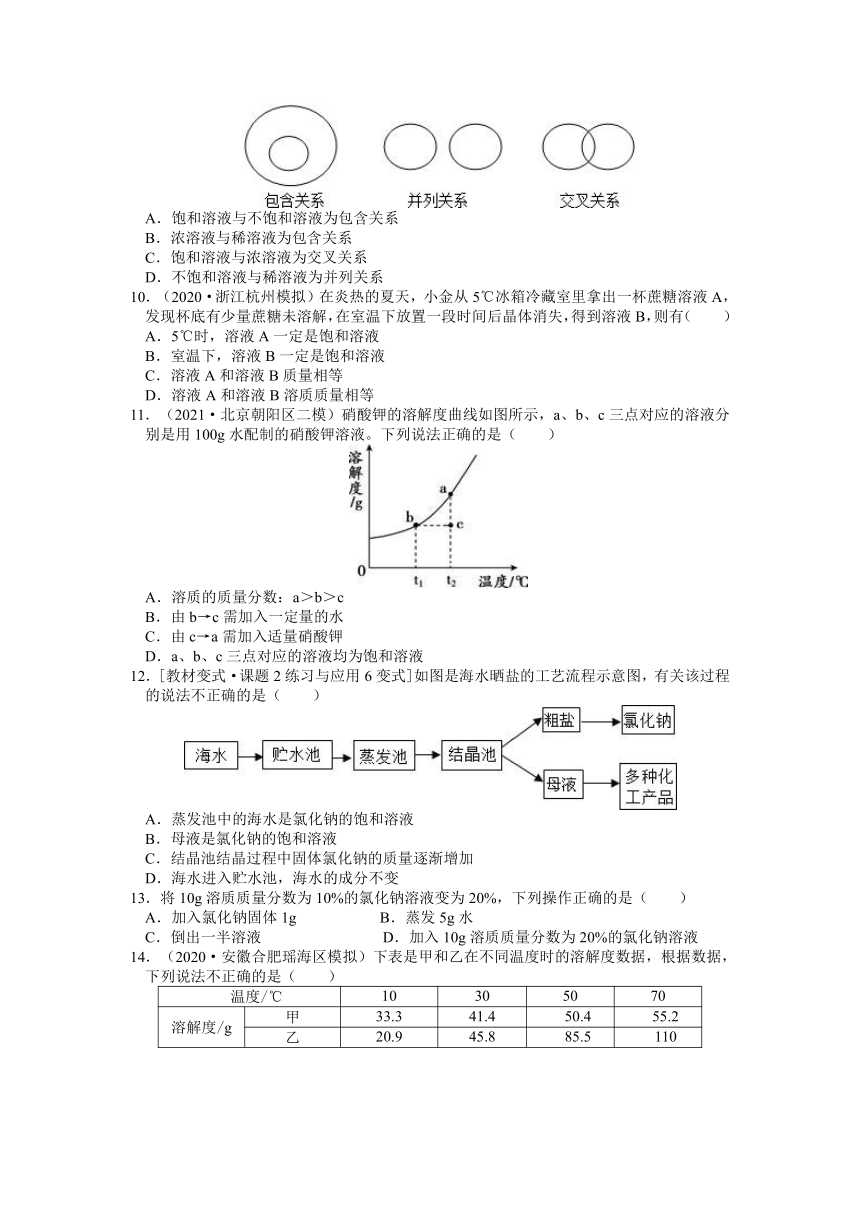
9.(2020·江苏镇江实验学校月考)化学概念在辑上存在如图所示关系。对下列概念的说法正确的是( )
A.饱和溶液与不饱和溶液为包含关系
B.浓溶液与稀溶液为包含关系
C.饱和溶液与浓溶液为交叉关系
D.不饱和溶液与稀溶液为并列关系
10.(2020·浙江杭州模拟)在炎热的夏天,小金从5℃冰箱冷藏室里拿出一杯蔗糖溶液A,发现杯底有少量蔗糖未溶解,在室温下放置一段时间后晶体消失,得到溶液B,则有( )
A.5℃时,溶液A一定是饱和溶液
B.室温下,溶液B一定是饱和溶液
C.溶液A和溶液B质量相等
D.溶液A和溶液B溶质质量相等
11.(2021·北京朝阳区二模)硝酸钾的溶解度曲线如图所示,a、b、c三点对应的溶液分别是用100g水配制的硝酸钾溶液。下列说法正确的是( )
A.溶质的质量分数:a>b>c
B.由b→c需加入一定量的水
C.由c→a需加入适量硝酸钾
D.a、b、c三点对应的溶液均为饱和溶液
12.[教材变式·课题2练习与应用6变式]如图是海水晒盐的工艺流程示意图,有关该过程的说法不正确的是( )
A.蒸发池中的海水是氯化钠的饱和溶液
B.母液是氯化钠的饱和溶液
C.结晶池结晶过程中固体氯化钠的质量逐渐增加
D.海水进入贮水池,海水的成分不变
13.将10g溶质质量分数为10%的氯化钠溶液变为20%,下列操作正确的是( )
A.加入氯化钠固体1g B.蒸发5g水
C.倒出一半溶液 D.加入10g溶质质量分数为20%的氯化钠溶液
14.(2020·安徽合肥瑶海区模拟)下表是甲和乙在不同温度时的溶解度数据,根据数据,下列说法不正确的是( )
温度/℃ 10 30 50 70
溶解度/g 甲 33.3 41.4 50.4 55.2
乙 20.9 45.8 85.5 110
A.由上表可知,50℃时,甲的溶解度为50.4g
B.甲、乙溶解度受温度变化影响较大的是乙
C.甲、乙的溶解度可能相等的温度范围为30~50℃
D.如图,若烧杯a中是60℃时含有100g水的甲的不饱和溶液,经过如图所示的变化过
程,c烧杯中溶液的质量为133.3g
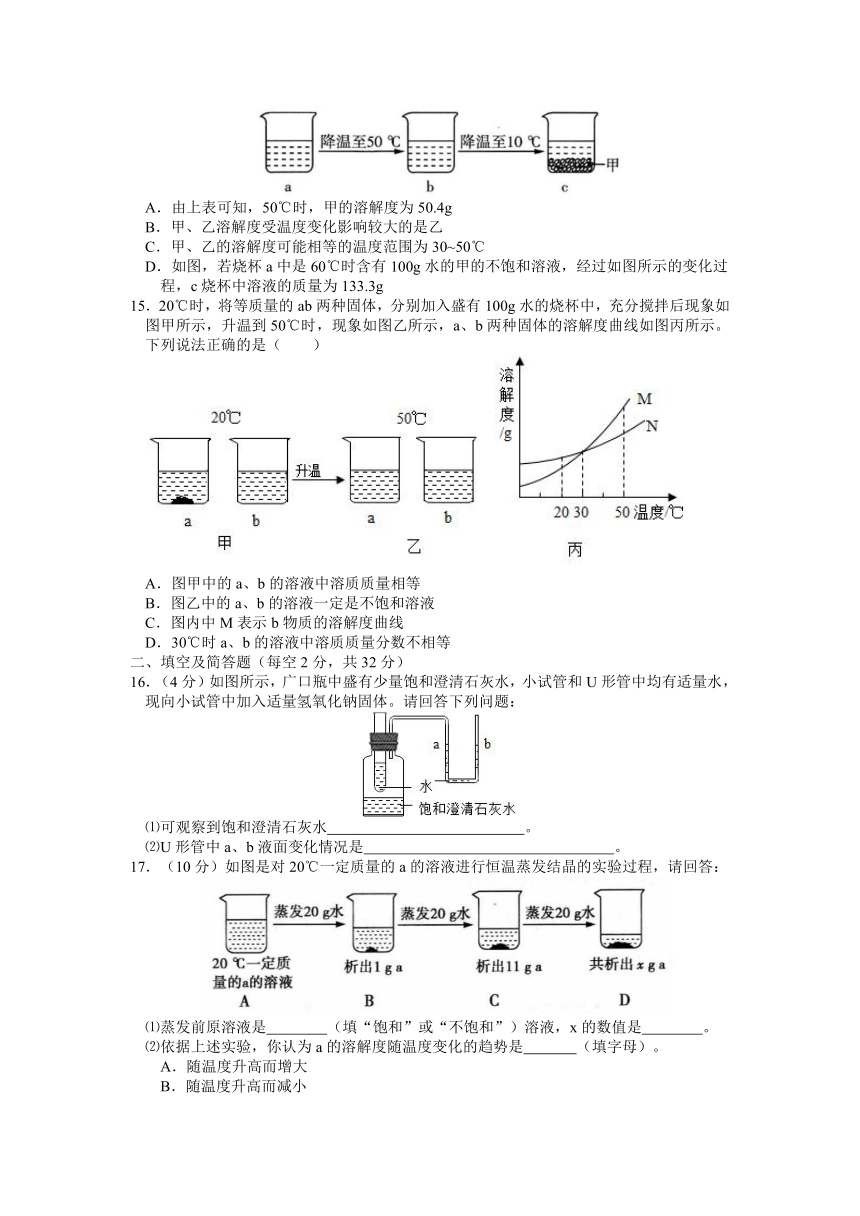
15.20℃时,将等质量的ab两种固体,分别加入盛有100g水的烧杯中,充分搅拌后现象如
图甲所示,升温到50℃时,现象如图乙所示,a、b两种固体的溶解度曲线如图丙所示。下列说法正确的是( )
A.图甲中的a、b的溶液中溶质质量相等
B.图乙中的a、b的溶液一定是不饱和溶液
C.图内中M表示b物质的溶解度曲线
D.30℃时a、b的溶液中溶质质量分数不相等
二、填空及简答题(每空2分,共32分)
16.(4分)如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中加入适量氢氧化钠固体。请回答下列问题:
⑴可观察到饱和澄清石灰水 。
⑵U形管中a、b液面变化情况是 。
17.(10分)如图是对20℃一定质量的a的溶液进行恒温蒸发结晶的实验过程,请回答:
⑴蒸发前原溶液是 (填“饱和”或“不饱和”)溶液,x的数值是 。
⑵依据上述实验,你认为a的溶解度随温度变化的趋势是 (填字母)。
A.随温度升高而增大
B.随温度升高而减小
C.无法判断
⑶20℃时,a的溶解度为 g,共析出11g a后溶液的溶质质量分数为 (精确到0.1%)。
(8分)下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ 20 40 60 80
溶解度/g 氯化钠 36.0 36.6 37.3 38.4
硝酸钾 31.6 63.9 110 169
⑴两种物质中,溶解度受温度变化影响较小的是 。
⑵20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为 。
⑶使接近饱和的硝酸钾溶液变为饱和溶液的种方法是 。
⑷60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是 。
19.(2021·上海奉贤区二模改编)(10分)KNO3与NH4Cl在水中的溶解度曲线如图1所示,请回答下列问题:
⑴t1℃时,KNO3的溶解度 (填“>”“=”或“<”)NH4Cl的溶解度,该温度下将25gKNO3加入50g水中,充分搅拌后所得溶液的质量为 g。
⑵t℃时,将一定质量的KNO3和NH4Cl溶液分别进行恒温蒸发,蒸发溶剂质量与析出
晶体质量间的关系如图2所示,原溶液中属于饱和溶液的是填 (填“甲”或“乙”),其溶质质量分数为 (用含字母的代数式表示);若甲是NH4Cl溶液,则t的取值范围是 。
三、实验与探究题(每空2分,共24分)
20.(2021·天津北辰区期末)(12分)配制50g溶质质量分数为6%的氯化钠溶液的过程如图1所示:
⑴所需氯化钠的质量为 g。
⑵称量氯化钠时,氯化钠应放在托盘天平的 (填“左”或“右”)盘。
⑶溶解过程中玻璃棒的作用是 。
⑷配制好的溶液要装在试剂瓶中,并贴好标签。请在如图2标签中填上相应的内容。
⑸对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有 (填序号)。
A.装瓶时,有少量溶液洒出
B.量取水的体积时,仰视读数
⑹把50g溶质质量分数为6%的氯化钠溶液稀释成溶质质量分数为2%的氯化钠溶
液,需要水的质量是 g。
21.(2021·陕西咸阳乾县期末)(12分)下面是某小组进行的“哪些因素影响固体物质在水中的溶解度”的实验探究,请你完成探究报告。
探究实验:哪些因素影响固体物质在水中的溶解度
⑴溶质种类的影响
在实验中要改变的因素是:溶质的种类。要保持不变的因素是: 。
实验步骤:30℃时,用量筒各取5mL蒸馏水分别加入①、②两支试管中,再分别加入
KNO3、Ca(OH)2各2g,振荡,观察各物质溶解情况。
实验现象:试管①中KNO3全部溶解,试管②中有较多Ca(OH)2未溶。
实验结论:在 保持不变的情况下,不同种类的物质在水中的溶解度 。
⑵温度的影响(以KNO3为例)
在实验中要改变的因素是 ;要保持不变的因素是 。
实验步骤:用量筒各取5mL蒸馏水,分别加入①、②两支试管中,再分别加入5g KNO3晶体,将试管①保持在常温下,将试管②加热并保持在60℃,振荡,观察各试管中KNO3的溶解情况。
实验现象:试管①中有较多KNO3未溶,试管②中KNO3全部溶解。
实验结论:在不同 下,同种固体物质在水中的溶解度不相等。
四、计算题(共14分)
22.(5分)消毒酒精、84消毒液、过氧乙酸(CH3COOOH)等都是杀灭新型冠状病毒的消毒剂。
⑴小明得知某过氧乙酸溶液中过氧乙酸和水中所含氢原子个数比为1:40,则此溶液的溶质质量分数约为 。
A.3% B.4% C.5% D.10%
⑵市售过氧乙酸溶液的浓度一般为20%,小华若用该溶液500g可以配制成多少千克的0.5%的过氧乙酸溶液
23.(2021·四川资阳模拟)(9分)为了分析生铁中铁的含量,某学习小组称取5.9g生铁样品,并粉碎,然后往粉末中逐滴加入质量分数为20%的硫酸,反应过程中产生气体的质量与加入硫酸的质量关系如图所示(假设生铁中杂质不与稀硫酸反应,也不溶于水)。
气体的质量g
⑴样品中的铁完全反应时,消耗20%硫酸的质量是 g。
⑵计算生铁样品中铁的质量分数。(精确到0.1%)
⑶恰好完全反应时,所得溶液中溶质的质量分数为多少 (精确到1%)
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B D A D C C B B C A C A B C B
⑴变浑浊 ⑵a液面下降,b液面上升
⑴不饱和 21 ⑵C ⑶50 33.3%
18.⑴氯化钠 ⑵20% ⑶加入硝酸钾(合理即可) ⑷降温结晶,再过滤
19.⑴= 70 ⑵甲 ⑶n/(n+m1)×100% t>t1
⑴3 ⑵左 ⑶搅拌,加快溶解
⑷ ⑸B ⑹100
⑴温度、溶剂的质量 温度 不同
⑵温度 溶质的质量和溶剂的质量 温度
⑴C(2分)
⑵解:设可以配制0.5%的过氧乙酸溶液的质量为y,则
500g×20%=y×0.5%
y=20000g=20kg
答:可以配制成20千克的0.5%的过氧乙酸溶液
⑴49(2分)
⑵解:设生铁样品中铁的质量为x,生成硫酸亚铁的质量为y,生成氢气的质量为z。
Fe+H2SO4===FeSO4+H2↑ (2分)
56 98 152 2
x 49g×20% y z
=== (1分)
解得:x=5.6g,y=15.2g,z=0.2g (1分)
生铁样品中铁的质量分数:
×100%≈94.9% (1分)
答:生铁样品中铁的质量分数约为94.9%。
⑶恰好完全反应时所得溶液的质量为:5.6g+49g-0.2g=54.4g (1分)
所得溶液中溶质的质量分数为:×100%≈28% (1分)
答:所得溶液中溶质的质量分数约为28%
B卷·名校好题提升卷
(满分100分,考试时间60分钟)
相对原子质量 H:1 C:12 O:16 Na:23 Mg:24 Al:27 Ca:40 Cu:64 Zn:65 Ag:108
可能用到的相对原子质量:H——1 C——12 O——16 S——32 Fe——56
一、选择题(每小题2分,共30分,每小题只有一个选项符合题意)
1.(2020·河北石家庄第二十八中学模拟)溶解适量的固体碘制成消毒液,应该使用( )
A.蒸馏水 B.酒精 C.汽油 D.生理盐水
2.(2021·广西钦州四中月考)溶液这种混合物,之所以具有均一性和稳定性,是因为( )
A.溶质是固体 B.溶剂是水
C.溶液是液体 D.溶质被解离成分子或离子状态
3.(2021·安徽蚌埠模拟)把20℃的100g硝酸钾饱和溶液升温至60℃,下列叙述错误的是( )
A.溶液仍然为饱和溶液 B.溶质的质量不变
C.溶剂的质量不变 D.溶液变为不饱和溶液
4.(2021·山东肥城期中)关于100g10%的硝酸钾溶液,下列叙述正确的是( )
A.100g水中溶有10g硝酸钾
B.溶液中硝酸钾与水的质量比为1:10
C.将硝酸钾和水按9:1的质量比配成的溶液
D.将10g硝酸钾溶于90g水中,可制得该溶液
5.下列现象,不能说明气体溶解度随温度升高而减小的是( )
A.天气闷热时,池塘里的鱼浮出水面
B.喝下汽水时,感到有气体冲击胃,易打嗝
C.揭开啤酒瓶瓶盖,有大量气泡逸出
D.烧开水时,沸腾前有气泡逸出
6.下列清洁方法中,利用了乳化原理的是( )
A.用自来水洗手 B.用生理盐水清洗伤口
C.用洗涤剂洗衣服上的油污 D.用酒精清洗医疗器械
7.(2021·山东东营模拟)实验室配制50g溶质质量分数为15%的氯化钠溶液。下列有关操作中不会造成误差的是( )
A.用量筒量取水时仰视读数
B.溶解过程中使用玻璃棒搅拌
C.用托盘天平称取食盐时,将食盐放在右盘,且称量时使用了游码
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
8.(2021·四川成都模拟)25℃时,取100mL氯化钠饱和溶液进行如图所示实验,下列分析错误的是( )
A.实验1后,甲、乙两溶液完全相同
B.实验2后,甲、乙两溶液的质量相等
C.实验2后,乙中溶液为氯化钠的饱和溶液
D.实验2后,甲、乙溶液所含溶质质量相等
9.(2020·江苏镇江实验学校月考)化学概念在辑上存在如图所示关系。对下列概念的说法正确的是( )
A.饱和溶液与不饱和溶液为包含关系
B.浓溶液与稀溶液为包含关系
C.饱和溶液与浓溶液为交叉关系
D.不饱和溶液与稀溶液为并列关系
10.(2020·浙江杭州模拟)在炎热的夏天,小金从5℃冰箱冷藏室里拿出一杯蔗糖溶液A,发现杯底有少量蔗糖未溶解,在室温下放置一段时间后晶体消失,得到溶液B,则有( )
A.5℃时,溶液A一定是饱和溶液
B.室温下,溶液B一定是饱和溶液
C.溶液A和溶液B质量相等
D.溶液A和溶液B溶质质量相等
11.(2021·北京朝阳区二模)硝酸钾的溶解度曲线如图所示,a、b、c三点对应的溶液分别是用100g水配制的硝酸钾溶液。下列说法正确的是( )
A.溶质的质量分数:a>b>c
B.由b→c需加入一定量的水
C.由c→a需加入适量硝酸钾
D.a、b、c三点对应的溶液均为饱和溶液
12.[教材变式·课题2练习与应用6变式]如图是海水晒盐的工艺流程示意图,有关该过程的说法不正确的是( )
A.蒸发池中的海水是氯化钠的饱和溶液
B.母液是氯化钠的饱和溶液
C.结晶池结晶过程中固体氯化钠的质量逐渐增加
D.海水进入贮水池,海水的成分不变
13.将10g溶质质量分数为10%的氯化钠溶液变为20%,下列操作正确的是( )
A.加入氯化钠固体1g B.蒸发5g水
C.倒出一半溶液 D.加入10g溶质质量分数为20%的氯化钠溶液
14.(2020·安徽合肥瑶海区模拟)下表是甲和乙在不同温度时的溶解度数据,根据数据,下列说法不正确的是( )
温度/℃ 10 30 50 70
溶解度/g 甲 33.3 41.4 50.4 55.2
乙 20.9 45.8 85.5 110
A.由上表可知,50℃时,甲的溶解度为50.4g
B.甲、乙溶解度受温度变化影响较大的是乙
C.甲、乙的溶解度可能相等的温度范围为30~50℃
D.如图,若烧杯a中是60℃时含有100g水的甲的不饱和溶液,经过如图所示的变化过
程,c烧杯中溶液的质量为133.3g
15.20℃时,将等质量的ab两种固体,分别加入盛有100g水的烧杯中,充分搅拌后现象如
图甲所示,升温到50℃时,现象如图乙所示,a、b两种固体的溶解度曲线如图丙所示。下列说法正确的是( )
A.图甲中的a、b的溶液中溶质质量相等
B.图乙中的a、b的溶液一定是不饱和溶液
C.图内中M表示b物质的溶解度曲线
D.30℃时a、b的溶液中溶质质量分数不相等
二、填空及简答题(每空2分,共32分)
16.(4分)如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中加入适量氢氧化钠固体。请回答下列问题:
⑴可观察到饱和澄清石灰水 。
⑵U形管中a、b液面变化情况是 。
17.(10分)如图是对20℃一定质量的a的溶液进行恒温蒸发结晶的实验过程,请回答:
⑴蒸发前原溶液是 (填“饱和”或“不饱和”)溶液,x的数值是 。
⑵依据上述实验,你认为a的溶解度随温度变化的趋势是 (填字母)。
A.随温度升高而增大
B.随温度升高而减小
C.无法判断
⑶20℃时,a的溶解度为 g,共析出11g a后溶液的溶质质量分数为 (精确到0.1%)。
(8分)下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ 20 40 60 80
溶解度/g 氯化钠 36.0 36.6 37.3 38.4
硝酸钾 31.6 63.9 110 169
⑴两种物质中,溶解度受温度变化影响较小的是 。
⑵20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为 。
⑶使接近饱和的硝酸钾溶液变为饱和溶液的种方法是 。
⑷60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是 。
19.(2021·上海奉贤区二模改编)(10分)KNO3与NH4Cl在水中的溶解度曲线如图1所示,请回答下列问题:
⑴t1℃时,KNO3的溶解度 (填“>”“=”或“<”)NH4Cl的溶解度,该温度下将25gKNO3加入50g水中,充分搅拌后所得溶液的质量为 g。
⑵t℃时,将一定质量的KNO3和NH4Cl溶液分别进行恒温蒸发,蒸发溶剂质量与析出
晶体质量间的关系如图2所示,原溶液中属于饱和溶液的是填 (填“甲”或“乙”),其溶质质量分数为 (用含字母的代数式表示);若甲是NH4Cl溶液,则t的取值范围是 。
三、实验与探究题(每空2分,共24分)
20.(2021·天津北辰区期末)(12分)配制50g溶质质量分数为6%的氯化钠溶液的过程如图1所示:
⑴所需氯化钠的质量为 g。
⑵称量氯化钠时,氯化钠应放在托盘天平的 (填“左”或“右”)盘。
⑶溶解过程中玻璃棒的作用是 。
⑷配制好的溶液要装在试剂瓶中,并贴好标签。请在如图2标签中填上相应的内容。
⑸对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有 (填序号)。
A.装瓶时,有少量溶液洒出
B.量取水的体积时,仰视读数
⑹把50g溶质质量分数为6%的氯化钠溶液稀释成溶质质量分数为2%的氯化钠溶
液,需要水的质量是 g。
21.(2021·陕西咸阳乾县期末)(12分)下面是某小组进行的“哪些因素影响固体物质在水中的溶解度”的实验探究,请你完成探究报告。
探究实验:哪些因素影响固体物质在水中的溶解度
⑴溶质种类的影响
在实验中要改变的因素是:溶质的种类。要保持不变的因素是: 。
实验步骤:30℃时,用量筒各取5mL蒸馏水分别加入①、②两支试管中,再分别加入
KNO3、Ca(OH)2各2g,振荡,观察各物质溶解情况。
实验现象:试管①中KNO3全部溶解,试管②中有较多Ca(OH)2未溶。
实验结论:在 保持不变的情况下,不同种类的物质在水中的溶解度 。
⑵温度的影响(以KNO3为例)
在实验中要改变的因素是 ;要保持不变的因素是 。
实验步骤:用量筒各取5mL蒸馏水,分别加入①、②两支试管中,再分别加入5g KNO3晶体,将试管①保持在常温下,将试管②加热并保持在60℃,振荡,观察各试管中KNO3的溶解情况。
实验现象:试管①中有较多KNO3未溶,试管②中KNO3全部溶解。
实验结论:在不同 下,同种固体物质在水中的溶解度不相等。
四、计算题(共14分)
22.(5分)消毒酒精、84消毒液、过氧乙酸(CH3COOOH)等都是杀灭新型冠状病毒的消毒剂。
⑴小明得知某过氧乙酸溶液中过氧乙酸和水中所含氢原子个数比为1:40,则此溶液的溶质质量分数约为 。
A.3% B.4% C.5% D.10%
⑵市售过氧乙酸溶液的浓度一般为20%,小华若用该溶液500g可以配制成多少千克的0.5%的过氧乙酸溶液
23.(2021·四川资阳模拟)(9分)为了分析生铁中铁的含量,某学习小组称取5.9g生铁样品,并粉碎,然后往粉末中逐滴加入质量分数为20%的硫酸,反应过程中产生气体的质量与加入硫酸的质量关系如图所示(假设生铁中杂质不与稀硫酸反应,也不溶于水)。
气体的质量g
⑴样品中的铁完全反应时,消耗20%硫酸的质量是 g。
⑵计算生铁样品中铁的质量分数。(精确到0.1%)
⑶恰好完全反应时,所得溶液中溶质的质量分数为多少 (精确到1%)
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B D A D C C B B C A C A B C B
⑴变浑浊 ⑵a液面下降,b液面上升
⑴不饱和 21 ⑵C ⑶50 33.3%
18.⑴氯化钠 ⑵20% ⑶加入硝酸钾(合理即可) ⑷降温结晶,再过滤
19.⑴= 70 ⑵甲 ⑶n/(n+m1)×100% t>t1
⑴3 ⑵左 ⑶搅拌,加快溶解
⑷ ⑸B ⑹100
⑴温度、溶剂的质量 温度 不同
⑵温度 溶质的质量和溶剂的质量 温度
⑴C(2分)
⑵解:设可以配制0.5%的过氧乙酸溶液的质量为y,则
500g×20%=y×0.5%
y=20000g=20kg
答:可以配制成20千克的0.5%的过氧乙酸溶液
⑴49(2分)
⑵解:设生铁样品中铁的质量为x,生成硫酸亚铁的质量为y,生成氢气的质量为z。
Fe+H2SO4===FeSO4+H2↑ (2分)
56 98 152 2
x 49g×20% y z
=== (1分)
解得:x=5.6g,y=15.2g,z=0.2g (1分)
生铁样品中铁的质量分数:
×100%≈94.9% (1分)
答:生铁样品中铁的质量分数约为94.9%。
⑶恰好完全反应时所得溶液的质量为:5.6g+49g-0.2g=54.4g (1分)
所得溶液中溶质的质量分数为:×100%≈28% (1分)
答:所得溶液中溶质的质量分数约为28%
同课章节目录
