3.2.1原子——2021-2022学年人教版九年级上册(word版 含解析)
文档属性
| 名称 | 3.2.1原子——2021-2022学年人教版九年级上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 236.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-25 00:00:00 | ||
图片预览


文档简介
3.2.1原子
一、单项选择题(共15小题;共30分)
1. 【 石景山一模 】下列原子中的粒子,带负电荷的是
A. 电子 B. 中子 C. 质子 D. 原子核
2. 高铁上装有烟雾传感器,主体是放有镅( )的电离室,这种镅原子的原子核内有 个质子和 个中子,该原子的核外电子数为
A. B. C. D.
3. 下列关于原子结构的叙述正确的是 。
A. 一切原子的原子核都由质子和中子构成
B. 在原子中,核电荷数一定等于质子数或核外电子数
C. 原子核内质子数一定等于中子数
D. 原子是不能再分的粒子
4. 下列粒子中,不带电的是
A. 原子核 B. 质子 C. 中子 D. 电子
5. 已知氧元素的原子结构示意图为,下列原子结构示意图所表示的元素与氧元素的化学性质相似的是
A. B.
C. D.
6. 下列粒子在化学反应中容易得到电子的是
A. B.
C. D.
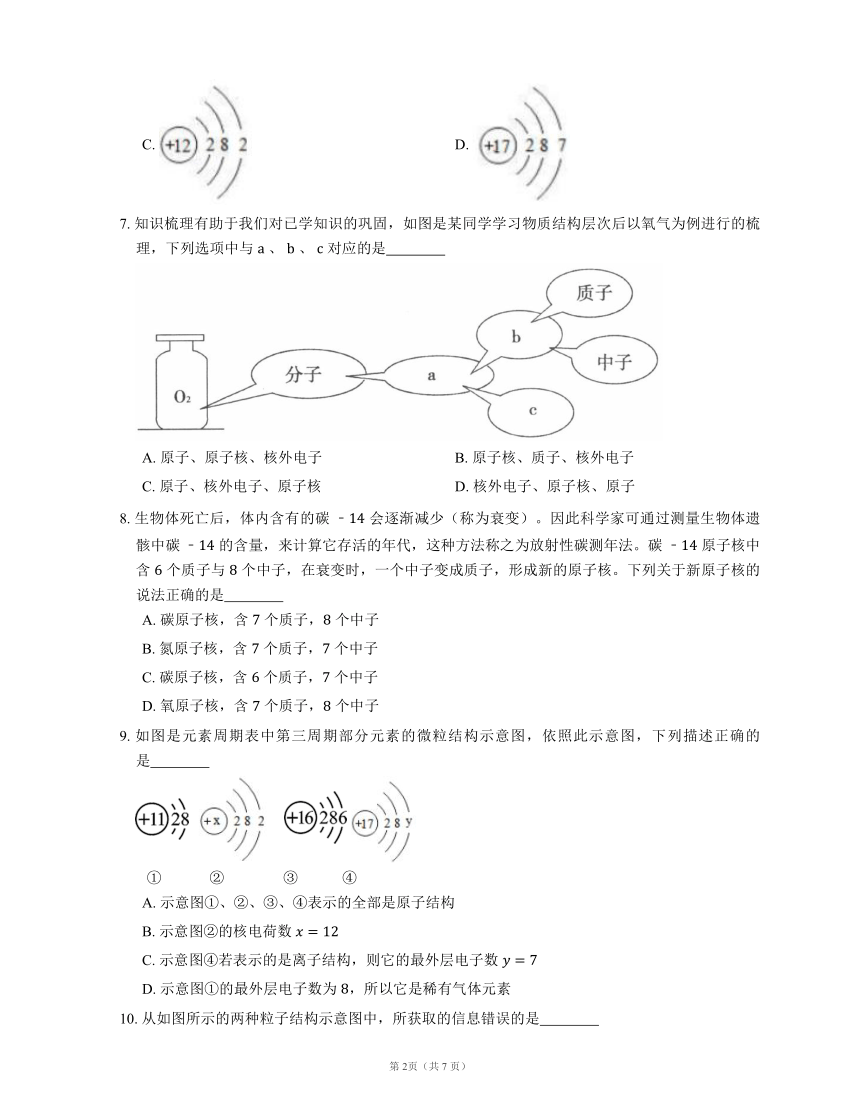
7. 知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与 、 、 对应的是
A. 原子、原子核、核外电子 B. 原子核、质子、核外电子
C. 原子、核外电子、原子核 D. 核外电子、原子核、原子
8. 生物体死亡后,体内含有的碳 会逐渐减少(称为衰变)。因此科学家可通过测量生物体遗骸中碳 的含量,来计算它存活的年代,这种方法称之为放射性碳测年法。碳 原子核中含 个质子与 个中子,在衰变时,一个中子变成质子,形成新的原子核。下列关于新原子核的说法正确的是
A. 碳原子核,含 个质子, 个中子
B. 氮原子核,含 个质子, 个中子
C. 碳原子核,含 个质子, 个中子
D. 氧原子核,含 个质子, 个中子
9. 如图是元素周期表中第三周期部分元素的微粒结构示意图,依照此示意图,下列描述正确的是
① ② ③ ④
A. 示意图①、②、③、④表示的全部是原子结构
B. 示意图②的核电荷数
C. 示意图④若表示的是离子结构,则它的最外层电子数
D. 示意图①的最外层电子数为 ,所以它是稀有气体元素
10. 从如图所示的两种粒子结构示意图中,所获取的信息错误的是
① ②
A. 微粒①带一个单位正电荷,微粒②表示原子
B. 它们的核外电子数相同
C. 它们属于不同种元素
D. 它们所属的元素位于第二周期
11. 如图是氯元素的原子结构示意图,下列叙述正确的是
A. 氯原子第一电子层有 个电子
B. 氯原子核内有 个质子
C. 氯原子在化学反应中容易失去电子
D. 氯与铝形成物质的化学式为
12. 下列原子结构示意图中,表示相对稳定结构的是
A. B.
C. D.
13. 与元素化学性质关系最密切的是原子的
A. 质子数 B. 核外电子总数 C. 电子层数 D. 最外层电子数
14. 有关氧原子的描述正确的是
A. 一个氧原子的质量是
B. 氧原子和 氧分子含有相同的原子个数
C. 氧原子的摩尔质量在数值上等于氧原子的质量
D. 氧原子的相对原子质量就是 氧原子的质量
15. 核外电子分层排布的主要原因是
A. 电子的能量不同 B. 电子的大小不同
C. 电子的数量不同 D. 电子的质量不同
二、非选择题(共4小题;共36分)
16. 中国科学院院士张青莲教授曾主持测定了铟、铱、锑等九种元素相对原子质量的新值,被国际原子量委员会采用为国际新标准。其中锑元素原子结构示意图如图所示。
(1)锑原子的核电荷数是 。
(2)锑原子最外层有 个电子。
17. 原子结构最外层电子数的得失电子情况:
(1)最外层电子数 ,易 电子,形成带 电的粒子;
(2)最外层电子数 ,易 电子,形成带 电的粒子;
(3)最外层电子数 (只有一层为 ),不易得失电子,属于 结构。
18. 某元素原子结构示意图为如图,请回答:
(1)表示的意义 。
(2)弧线表示 。
(3)弧线上的数字表示 。
(4)该元素的原子最外层电子数是 。
(5)该元素原子核外共有 层电子层。
(6)该元素原子在化学反应中易 电子(填“获得”或“失去”)。
19. 征服原子 揭开原子的神秘面纱
伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是 一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。
(1) 年,近代化学之父,英国科学家道尔顿()在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
年,意大利化学家阿伏伽德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
年,汤姆森通过实验发现了 ,进一步发展了原子。分子论。汤姆森主要是纠正了“道尔顿原子论” 中的观点。
年,声瑟福又通过实验,推测原子是由 构成,并提出了沿用至今的现代原子结构理论。
(2)道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样。对实验现象进行解释的过程叫做 。
原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了 来表达他们的理论成果。
答案
第一部分
1. A
2. A
3. B
【解析】绝大多数原子的原子核是由质子和中子构成,但不是一切原子的原子核里都有质子和中子,普通氢原子核内只有一个质子而没有中子,所以A项和C项错误;对于D项来说,原子是化学变化中最小的微粒,在化学变化中确实不可以再分,但在其他变化(如核反应)中可以再分。在原子中,核电荷数 质子数 核外电子数,所以整个原子不显电性。
4. C
5. C
【解析】元素的化学性质与原子的最外层电子数关系密切。一般来说,原子的最外层电子数相同,则元素化学性质相似,故选C。
6. D
【解析】A、该原子的最外层已达 个电子,结构比较稳定,化学性质不活泼。故不易得失电子。
B、该原子的最外层有 个电子,在化学反应中易失去 个电子而达 电子的稳定结构,所以B不正确。
C、该原子的最外层有 个电子,在化学反应中易失去 个电子而达 电子的稳定结构,所以C不正确。
D、该原子的最外层有 个电子,最外层电子数越多越容易得到电子(除稀有气体外),在化学反应中易得到 个电子而达 电子的稳定结构,所以D正确。
故选:D。
7. A
【解析】分子都是由原子构成的。
8. B
【解析】由于碳 原子核中含 个质子与 个中子,在衰变时,一个中子变成质子,形成新的原子核,所以该原子核内的质子数成为 ,因此该原子核成为氮原子的原子核,其核内质子数是 中子数也是 ;
故选B
9. B
【解析】A、由于原子中质子数等于核外电子数,所以可知①不属于原子;
B、根据原子中质子数等于核外电子数,所以 ;
C、 号元素的核外电子情况是最外层有 个电子,化学反应中易得到 个电子而成为 个电子的稳定结构,所以示意图④若表示的是离子结构,则它的最外层电子数 ;
D、稀有气体的原子最外层电子数是 (或 ),而①表示的是钠离子的结构示意图,不是稀有气体元素。
10. D
【解析】A、由粒子结构示意图可知①核电荷数 质子数 核外电子数 ,为阳离子,带一个单位正电荷;②核电荷数 质子数 核外电子数 ,为原子;故说法正确;
B、由粒子结构示意图可知①②核外电子数相同;故说法正确;
C、依据不同种元素最本质的区别是质子数不同,它们属于不同种元素,故说法正确;
D、由于①是离子,根据其质子数可以判断应属于第三周期,②属于第二正确周期,因此不属于同一周期;故说法错误;
故选:D。
11. B
【解析】A、由氯元素的原子结构图的意义可知,氯原子第一电子层有 个电子,故选项说法错误。
B、由氯元素的原子结构图的意义可知,氯原子核内有 个质子,故选项说法正确。
C、氯原子的最外层电子数为 ,大于 ,在化学反应中容易得到 个电子形成 个电子的稳定结构,故选项说法错误。
D、氯原子的最外层电子数为 ,易形成带一个单位负电荷的阴离子,化合价为 价,铝显 价,形成的物质的化学式是 ,故选项说法错误。
12. D
【解析】A、该原子的最外层电子数为 ,在化学反应中易失去 个电子而形成阳离子,故选项错误。
B、该原子的最外层电子数为 ,在化学反应中易得到 个电子而形成阴离子,故选项错误。
C、该原子的最外层电子数为 ,在化学反应中易失去 个电子而形成阳离子,故选项错误。
D、该原子的最外层电子数为 ,属于相对稳定结构,故选项正确。
故选:D。
13. D
【解析】元素性质与原子核外电子的排布,特别是最外层上的电子数目有密切关系,决定元素化学性质的是最外层电子数。
A、决定元素化学性质的是最外层电子数,而不是质子数,故选项错误。
B、决定元素化学性质的是最外层电子数,而不是核外电子总数,故选项错误。
C、决定元素化学性质的是最外层电子数,而不是电子层数,故选项错误。
D、决定元素化学性质的是最外层电子数,故选项正确。故选:D。
14. B
【解析】A、氧原子质量很小,相对原子质量是相对可以说明原子的大小,但非真实质量,错误。
B、氧原子质量相等,所以 氧原子和 氧分子所含氧原子个数相等,正确。
C、氧原子的摩尔质量数值上等于氧原子的相对原子质量,错误。
D、氧原子的相对原子质量数值上等于 氧原子的质量,错误。
15. A
【解析】核外电子分层排布的主要原因是电子的能量不同,在原子核外能量低的电子排在离核较近的区域,而能量较高的电子排在离核较远的区域,故A项正确。
第二部分
16. (1)
【解析】由锑的原子结构示意图可知,锑原子的质子数为 ,由于质子数 核电荷数,所以锑原子的核电荷数也是 。
(2)
【解析】由锑的原子结构示意图可知,锑原子最外层有 个电子。
17. (1) 失去;正
(2) 得到;负
(3) 相对稳定
18. (1) 原子核及核内质子数是
【解析】由元素原子结构示意图可知:表示的意义是:原子核及核内质子数是 。
(2) 电子层
【解析】弧线表示电子层,
(3) 电子数
【解析】弧线上的数字表示该层的电子数。
(4)
【解析】该元素的原子最外层电子数是 。
(5)
【解析】该元素原子核外共有 层电子层,
(6) 失去
【解析】该元素原子的最外层电子数是 ,小于 ,在化学反应中易失去电子。
19. (1) 电子;原子不可再分;原子核和核外电子
(2) 推理;模型
第1页(共1 页)
一、单项选择题(共15小题;共30分)
1. 【 石景山一模 】下列原子中的粒子,带负电荷的是
A. 电子 B. 中子 C. 质子 D. 原子核
2. 高铁上装有烟雾传感器,主体是放有镅( )的电离室,这种镅原子的原子核内有 个质子和 个中子,该原子的核外电子数为
A. B. C. D.
3. 下列关于原子结构的叙述正确的是 。
A. 一切原子的原子核都由质子和中子构成
B. 在原子中,核电荷数一定等于质子数或核外电子数
C. 原子核内质子数一定等于中子数
D. 原子是不能再分的粒子
4. 下列粒子中,不带电的是
A. 原子核 B. 质子 C. 中子 D. 电子
5. 已知氧元素的原子结构示意图为,下列原子结构示意图所表示的元素与氧元素的化学性质相似的是
A. B.
C. D.
6. 下列粒子在化学反应中容易得到电子的是
A. B.
C. D.
7. 知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与 、 、 对应的是
A. 原子、原子核、核外电子 B. 原子核、质子、核外电子
C. 原子、核外电子、原子核 D. 核外电子、原子核、原子
8. 生物体死亡后,体内含有的碳 会逐渐减少(称为衰变)。因此科学家可通过测量生物体遗骸中碳 的含量,来计算它存活的年代,这种方法称之为放射性碳测年法。碳 原子核中含 个质子与 个中子,在衰变时,一个中子变成质子,形成新的原子核。下列关于新原子核的说法正确的是
A. 碳原子核,含 个质子, 个中子
B. 氮原子核,含 个质子, 个中子
C. 碳原子核,含 个质子, 个中子
D. 氧原子核,含 个质子, 个中子
9. 如图是元素周期表中第三周期部分元素的微粒结构示意图,依照此示意图,下列描述正确的是
① ② ③ ④
A. 示意图①、②、③、④表示的全部是原子结构
B. 示意图②的核电荷数
C. 示意图④若表示的是离子结构,则它的最外层电子数
D. 示意图①的最外层电子数为 ,所以它是稀有气体元素
10. 从如图所示的两种粒子结构示意图中,所获取的信息错误的是
① ②
A. 微粒①带一个单位正电荷,微粒②表示原子
B. 它们的核外电子数相同
C. 它们属于不同种元素
D. 它们所属的元素位于第二周期
11. 如图是氯元素的原子结构示意图,下列叙述正确的是
A. 氯原子第一电子层有 个电子
B. 氯原子核内有 个质子
C. 氯原子在化学反应中容易失去电子
D. 氯与铝形成物质的化学式为
12. 下列原子结构示意图中,表示相对稳定结构的是
A. B.
C. D.
13. 与元素化学性质关系最密切的是原子的
A. 质子数 B. 核外电子总数 C. 电子层数 D. 最外层电子数
14. 有关氧原子的描述正确的是
A. 一个氧原子的质量是
B. 氧原子和 氧分子含有相同的原子个数
C. 氧原子的摩尔质量在数值上等于氧原子的质量
D. 氧原子的相对原子质量就是 氧原子的质量
15. 核外电子分层排布的主要原因是
A. 电子的能量不同 B. 电子的大小不同
C. 电子的数量不同 D. 电子的质量不同
二、非选择题(共4小题;共36分)
16. 中国科学院院士张青莲教授曾主持测定了铟、铱、锑等九种元素相对原子质量的新值,被国际原子量委员会采用为国际新标准。其中锑元素原子结构示意图如图所示。
(1)锑原子的核电荷数是 。
(2)锑原子最外层有 个电子。
17. 原子结构最外层电子数的得失电子情况:
(1)最外层电子数 ,易 电子,形成带 电的粒子;
(2)最外层电子数 ,易 电子,形成带 电的粒子;
(3)最外层电子数 (只有一层为 ),不易得失电子,属于 结构。
18. 某元素原子结构示意图为如图,请回答:
(1)表示的意义 。
(2)弧线表示 。
(3)弧线上的数字表示 。
(4)该元素的原子最外层电子数是 。
(5)该元素原子核外共有 层电子层。
(6)该元素原子在化学反应中易 电子(填“获得”或“失去”)。
19. 征服原子 揭开原子的神秘面纱
伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是 一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。
(1) 年,近代化学之父,英国科学家道尔顿()在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
年,意大利化学家阿伏伽德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
年,汤姆森通过实验发现了 ,进一步发展了原子。分子论。汤姆森主要是纠正了“道尔顿原子论” 中的观点。
年,声瑟福又通过实验,推测原子是由 构成,并提出了沿用至今的现代原子结构理论。
(2)道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样。对实验现象进行解释的过程叫做 。
原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了 来表达他们的理论成果。
答案
第一部分
1. A
2. A
3. B
【解析】绝大多数原子的原子核是由质子和中子构成,但不是一切原子的原子核里都有质子和中子,普通氢原子核内只有一个质子而没有中子,所以A项和C项错误;对于D项来说,原子是化学变化中最小的微粒,在化学变化中确实不可以再分,但在其他变化(如核反应)中可以再分。在原子中,核电荷数 质子数 核外电子数,所以整个原子不显电性。
4. C
5. C
【解析】元素的化学性质与原子的最外层电子数关系密切。一般来说,原子的最外层电子数相同,则元素化学性质相似,故选C。
6. D
【解析】A、该原子的最外层已达 个电子,结构比较稳定,化学性质不活泼。故不易得失电子。
B、该原子的最外层有 个电子,在化学反应中易失去 个电子而达 电子的稳定结构,所以B不正确。
C、该原子的最外层有 个电子,在化学反应中易失去 个电子而达 电子的稳定结构,所以C不正确。
D、该原子的最外层有 个电子,最外层电子数越多越容易得到电子(除稀有气体外),在化学反应中易得到 个电子而达 电子的稳定结构,所以D正确。
故选:D。
7. A
【解析】分子都是由原子构成的。
8. B
【解析】由于碳 原子核中含 个质子与 个中子,在衰变时,一个中子变成质子,形成新的原子核,所以该原子核内的质子数成为 ,因此该原子核成为氮原子的原子核,其核内质子数是 中子数也是 ;
故选B
9. B
【解析】A、由于原子中质子数等于核外电子数,所以可知①不属于原子;
B、根据原子中质子数等于核外电子数,所以 ;
C、 号元素的核外电子情况是最外层有 个电子,化学反应中易得到 个电子而成为 个电子的稳定结构,所以示意图④若表示的是离子结构,则它的最外层电子数 ;
D、稀有气体的原子最外层电子数是 (或 ),而①表示的是钠离子的结构示意图,不是稀有气体元素。
10. D
【解析】A、由粒子结构示意图可知①核电荷数 质子数 核外电子数 ,为阳离子,带一个单位正电荷;②核电荷数 质子数 核外电子数 ,为原子;故说法正确;
B、由粒子结构示意图可知①②核外电子数相同;故说法正确;
C、依据不同种元素最本质的区别是质子数不同,它们属于不同种元素,故说法正确;
D、由于①是离子,根据其质子数可以判断应属于第三周期,②属于第二正确周期,因此不属于同一周期;故说法错误;
故选:D。
11. B
【解析】A、由氯元素的原子结构图的意义可知,氯原子第一电子层有 个电子,故选项说法错误。
B、由氯元素的原子结构图的意义可知,氯原子核内有 个质子,故选项说法正确。
C、氯原子的最外层电子数为 ,大于 ,在化学反应中容易得到 个电子形成 个电子的稳定结构,故选项说法错误。
D、氯原子的最外层电子数为 ,易形成带一个单位负电荷的阴离子,化合价为 价,铝显 价,形成的物质的化学式是 ,故选项说法错误。
12. D
【解析】A、该原子的最外层电子数为 ,在化学反应中易失去 个电子而形成阳离子,故选项错误。
B、该原子的最外层电子数为 ,在化学反应中易得到 个电子而形成阴离子,故选项错误。
C、该原子的最外层电子数为 ,在化学反应中易失去 个电子而形成阳离子,故选项错误。
D、该原子的最外层电子数为 ,属于相对稳定结构,故选项正确。
故选:D。
13. D
【解析】元素性质与原子核外电子的排布,特别是最外层上的电子数目有密切关系,决定元素化学性质的是最外层电子数。
A、决定元素化学性质的是最外层电子数,而不是质子数,故选项错误。
B、决定元素化学性质的是最外层电子数,而不是核外电子总数,故选项错误。
C、决定元素化学性质的是最外层电子数,而不是电子层数,故选项错误。
D、决定元素化学性质的是最外层电子数,故选项正确。故选:D。
14. B
【解析】A、氧原子质量很小,相对原子质量是相对可以说明原子的大小,但非真实质量,错误。
B、氧原子质量相等,所以 氧原子和 氧分子所含氧原子个数相等,正确。
C、氧原子的摩尔质量数值上等于氧原子的相对原子质量,错误。
D、氧原子的相对原子质量数值上等于 氧原子的质量,错误。
15. A
【解析】核外电子分层排布的主要原因是电子的能量不同,在原子核外能量低的电子排在离核较近的区域,而能量较高的电子排在离核较远的区域,故A项正确。
第二部分
16. (1)
【解析】由锑的原子结构示意图可知,锑原子的质子数为 ,由于质子数 核电荷数,所以锑原子的核电荷数也是 。
(2)
【解析】由锑的原子结构示意图可知,锑原子最外层有 个电子。
17. (1) 失去;正
(2) 得到;负
(3) 相对稳定
18. (1) 原子核及核内质子数是
【解析】由元素原子结构示意图可知:表示的意义是:原子核及核内质子数是 。
(2) 电子层
【解析】弧线表示电子层,
(3) 电子数
【解析】弧线上的数字表示该层的电子数。
(4)
【解析】该元素的原子最外层电子数是 。
(5)
【解析】该元素原子核外共有 层电子层,
(6) 失去
【解析】该元素原子的最外层电子数是 ,小于 ,在化学反应中易失去电子。
19. (1) 电子;原子不可再分;原子核和核外电子
(2) 推理;模型
第1页(共1 页)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
