第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 176.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-26 00:00:00 | ||
图片预览


文档简介
人教版九年级化学下册
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题2分,共24分)
1.如果把家庭中的①食盐、②纯碱、③面粉、④芝麻油、⑤蔗糖、⑥白酒,分别加入适量水并充分搅拌,能够得到的溶液是( )
A、①④⑥ B、①②⑤⑥ C、②③⑥ D、①②③⑤
2.已知50℃时氯化铵的溶解度为50g,则在50℃时的氯化铵饱和溶液中,溶质质量∶溶剂质量∶溶液质量等于( )
A. 1∶2∶3 B. 2∶3∶1 C. 3∶1∶2 D. 1∶3∶2
3.下列除垢或除污过程中利用乳化作用的是( )
A.自来水洗手 B.食醋除水垢
C.汽油除油污 D.洗洁精除油污
4.下列有关溶液的叙述错误的是( )
A.长期放置后不会分层的液体一定是溶液
B.衣服上的油污用汽油或用加了洗涤剂的水可除去
C.一瓶合格的生理盐水密封一段时间,不会出现浑浊
D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率
5.下列洗涤方式应用乳化作用的是( )
A.用汽油除去衣服上的油污 B.用水洗去盘子中的水果渣
C.用洗洁精洗餐具上的油污 D.用盐酸清洗水壶的水垢
6.将60 ℃的硝酸钾溶液降温至20 ℃,有晶体析出。有关该过程的说法错误的是( )
A.60 ℃时的溶液一定是硝酸钾饱和溶液
B.20 ℃时的溶液一定是硝酸钾饱和溶液
C.硝酸钾的溶解度随温度降低而减小
D.硝酸钾晶体可采用降温结晶的方法得到
7.30 ℃时将等质量的两份饱和石灰水,一份冷却到20 ℃,另一份加入少量生石灰,温度仍保持在30 ℃,则两种情况下均不改变的是( )
A.溶剂的质量 B.溶质的质量
C.溶质的溶解度 D.溶液中溶质的质量分数
8.实验室欲配制50克溶质质量分数为15%的氯化钠溶液,下列有关叙述正确的是( )
A.配制该溶液的步骤是称量和溶解
B.配制过程中用到的仪器只有天平、烧杯和玻璃棒
C.溶解氯化钠固体时,玻璃棒的作用是加快溶解速率
D.转移溶液时,用蒸馏水洗涤烧杯2~3次,将洗涤液一并倒入试剂瓶
9.医院里常用溶质分数为5%的双氧水(H2O2)溶液清洗受伤病人的伤口,若要配制5%的双氧水溶液600g,需要30%的高浓度双氧水的质量为( )
A.30g B.100g C.200g D.400g
10.t ℃时,向一只盛有0.15 g熟石灰的烧杯中加入50 g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体。下列相关叙述正确的是( )
A. 升高温度,上层清液变为不饱和溶液
B. t ℃时,熟石灰的溶解度为0.3 g
C. 烧杯中溶液的质量小于50.15 g
D. 上层清液中溶质质量分数大于0.3%
11.下列物质之间的质量关系,能用右图表示的是( )
A.向一定质量的水中加入蔗糖
B.向一定质量的NaCl饱和溶液中加入KNO3
C.向一定质量的KNO3饱和溶液中加入KNO3
D.向一定质量的Ca(OH)2饱和溶液中加入CaO
12.下列不能达到实验目的的是( )
选项 实验目的 操作
A 鉴别固体硫酸铜和氯化钠 加水溶解观察颜色
B 区分硝酸铵和氢氧化钠 加适量水测量温度变化
C 区分20 ℃时氯化钠的饱和溶液与水 分别加入一定量的氯化钾
D 将某温度下的氢氧化钙的不饱和溶液变为饱和溶液 加入适量氧化钙
二、填空题(每空2分,作图2分,共42分)
13.分别指出下列溶液中的溶质和溶剂,用相关物质的化学式填空:
(1)浓硫酸中的溶质是____________。
(2)石灰水中的溶质是。
(3)35%的酒精溶液中溶质是________________,溶剂是________________。
(4)铁与稀硫酸恰好完全反应后的溶液中,溶质是________,溶剂是________。
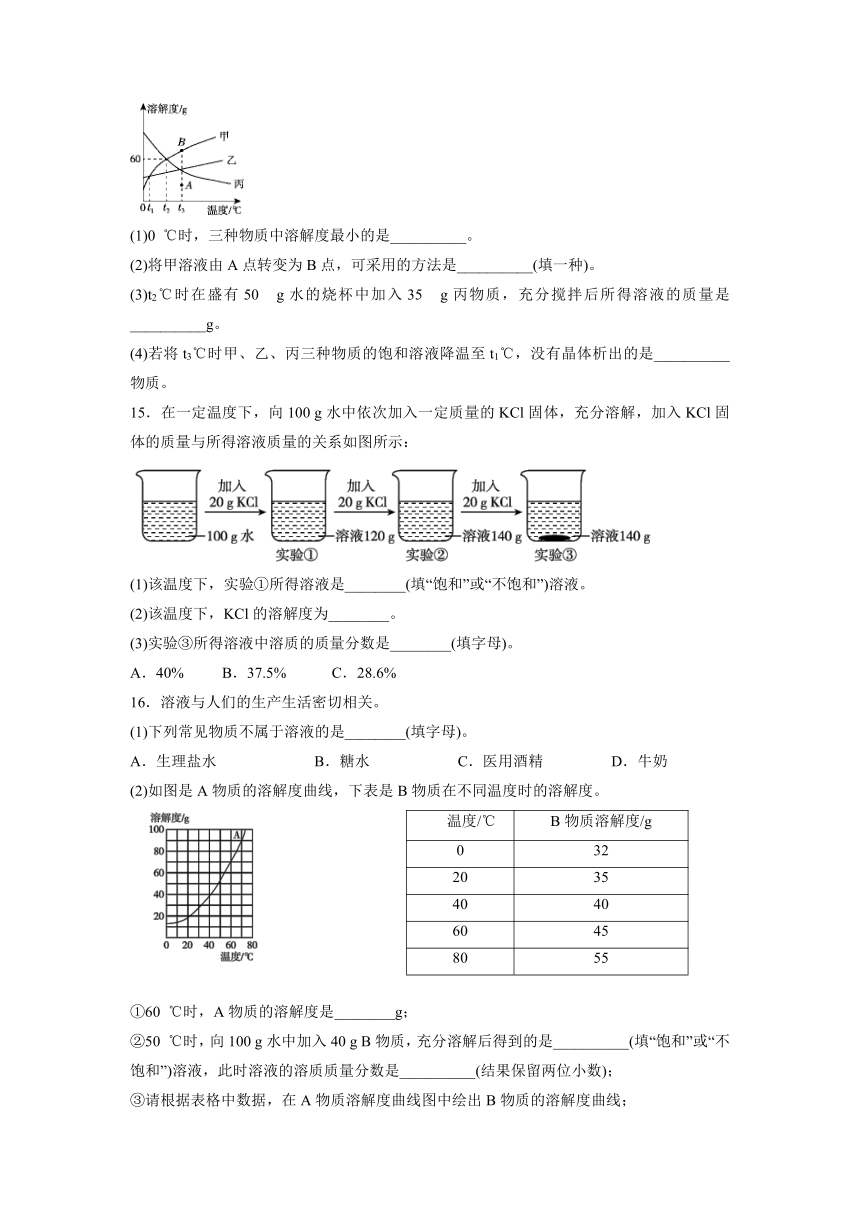
14.如图是甲、乙、丙三种固体物质的溶解度曲线,根据图示回答:
(1)0 ℃时,三种物质中溶解度最小的是__________。
(2)将甲溶液由A点转变为B点,可采用的方法是__________(填一种)。
(3)t2℃时在盛有50 g水的烧杯中加入35 g丙物质,充分搅拌后所得溶液的质量是__________g。
(4)若将t3℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,没有晶体析出的是__________物质。
15.在一定温度下,向100 g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是________(填“饱和”或“不饱和”)溶液。
(2)该温度下,KCl的溶解度为________。
(3)实验③所得溶液中溶质的质量分数是________(填字母)。
A.40% B.37.5% C.28.6%
16.溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是________(填字母)。
A.生理盐水 B.糖水 C.医用酒精 D.牛奶
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。
温度/℃ B物质溶解度/g
0 32
20 35
40 40
60 45
80 55
①60 ℃时,A物质的溶解度是________g;
②50 ℃时,向100 g水中加入40 g B物质,充分溶解后得到的是__________(填“饱和”或“不饱和”)溶液,此时溶液的溶质质量分数是__________(结果保留两位小数);
③请根据表格中数据,在A物质溶解度曲线图中绘出B物质的溶解度曲线;
④A、B两种物质溶解度相同时的温度是________℃。
(3)生活中常用75%的酒精消毒液对手和皮肤进行消毒。请分析酒精浓度与杀死细菌的时间对比表(如下表所示)中的数据,酒精消毒液最合适的浓度应为________。根据酒精的物理性质,你认为两者浓度差异的主要原因是________________________________________。
酒精浓度(%) 大肠杆菌 金黄色葡萄球菌 溶血性链球菌
90 15小时 30分钟 5分钟
80 1小时 30分钟 5分钟
70 30秒 5分钟 10秒
60 20秒 30分钟 10秒
50 20秒 2小时 20秒
40 22分钟 4小时 2分钟
三、实验探究题(每空2分,共28分)
17.某化学兴趣小组进行溶液的配制和粗盐的初步提纯实验。
(1)配制200g质量分数为8%的氢氧化钠溶液:
①计算:需要氢氧化钠固体的质量为 克,需要水的体积为 mL(水的密度近似看作1g/mL)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后 (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③用 量取所需要的水,倒入盛有氢氧化钠固体的烧杯中,用 搅拌,使其溶解,并冷却到室温。
④将配制好的溶液放入试剂瓶,塞好橡胶塞并 ,放到指定的地方。
(2)粗盐的初步提纯:称取5.0克粗盐,用药匙逐渐加入到10mL水中,直到粗盐不再溶解为止。还需进行的实验操作步骤的顺序为:称量剩余粗盐、 (填编号)。
A.过滤 B.计算产率 C.蒸发 D.称量精盐
18.某实验小组如图所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
(1)图甲中仪器a的名称是 。
(2)完成此实验正确的操作顺序是(填序号) 。
①溶解 ②把配好的溶液装入试剂瓶 ③称量 ④计算
(3)按实验要求,图甲中还缺少的玻璃仪器是(填名称) 。
(4)小婧按图乙的操作称氯化钠,小民发现小婧的操作有错误,你认为小婧操作中的错误是 。她称取的氯化钠实际质量为 g。
(5)小民所取蒸镏水的体积如图丙所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为(水的密度约为1g/cm3) 。
四、综合应用题(共6分)
19. 某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34 g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8 g,将烧杯内剩余物质过滤、洗涤、干燥后得滤渣3 g。请根据要求回答下列问题:
(1)生成氧气的质量是________g。
(2)瓶内过氧化氢溶液中溶质的质量分数是多少?
(3)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100 g,需加入水的质量是多少?
参考答案
一、选择题
1-6BADACA 7-12DCACBC
二、填空题
13.(1)H2SO4 (2)Ca(OH)2 (3)C2H5OH H2O (4)FeSO4 H2O
14.(1)甲 (2)增加溶质(或恒温蒸发溶剂) (3)80 (4)丙
15.(1)不饱和 (2)40 g (3)C
16.(1)D (2)①70 ②不饱和 28. 57% ③如图所示。
④ 42 (3)70% 酒精易挥发,实际配制的浓度要大些
三、实验探究题
17. (1)①16 184 ②左 BA 氢氧化钠易潮解(或氢氧化钠具有腐蚀性)
③量筒 玻璃棒 ④贴上标签
(2)ACDB
18. (1)烧杯
(2) ④③①②
(3) 玻璃棒
(4)左盘应放食盐右盘放砝码
(5)18%
四、综合应用题
19. 解: (1)3. 2
(2)设34 g过氧化氢溶液中含溶质的质量为x。
2H2O2 2H2O+O2↑
68 32
x 3.2 g
=
x=6. 8 g
过氧化氢溶液中溶质的质量分数为×100%=20%。
(3)配制100 g溶质质量分数为3%的过氧化氢溶液, 需要20%过氧化氢溶液的质量为100 g×3%÷20%=15 g
需加水的质量为100 g-15 g=85 g
答: (2)瓶内过氧化氢溶液中溶质的质量分数为20%。(3)需加入水的质量为85 g。
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题2分,共24分)
1.如果把家庭中的①食盐、②纯碱、③面粉、④芝麻油、⑤蔗糖、⑥白酒,分别加入适量水并充分搅拌,能够得到的溶液是( )
A、①④⑥ B、①②⑤⑥ C、②③⑥ D、①②③⑤
2.已知50℃时氯化铵的溶解度为50g,则在50℃时的氯化铵饱和溶液中,溶质质量∶溶剂质量∶溶液质量等于( )
A. 1∶2∶3 B. 2∶3∶1 C. 3∶1∶2 D. 1∶3∶2
3.下列除垢或除污过程中利用乳化作用的是( )
A.自来水洗手 B.食醋除水垢
C.汽油除油污 D.洗洁精除油污
4.下列有关溶液的叙述错误的是( )
A.长期放置后不会分层的液体一定是溶液
B.衣服上的油污用汽油或用加了洗涤剂的水可除去
C.一瓶合格的生理盐水密封一段时间,不会出现浑浊
D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率
5.下列洗涤方式应用乳化作用的是( )
A.用汽油除去衣服上的油污 B.用水洗去盘子中的水果渣
C.用洗洁精洗餐具上的油污 D.用盐酸清洗水壶的水垢
6.将60 ℃的硝酸钾溶液降温至20 ℃,有晶体析出。有关该过程的说法错误的是( )
A.60 ℃时的溶液一定是硝酸钾饱和溶液
B.20 ℃时的溶液一定是硝酸钾饱和溶液
C.硝酸钾的溶解度随温度降低而减小
D.硝酸钾晶体可采用降温结晶的方法得到
7.30 ℃时将等质量的两份饱和石灰水,一份冷却到20 ℃,另一份加入少量生石灰,温度仍保持在30 ℃,则两种情况下均不改变的是( )
A.溶剂的质量 B.溶质的质量
C.溶质的溶解度 D.溶液中溶质的质量分数
8.实验室欲配制50克溶质质量分数为15%的氯化钠溶液,下列有关叙述正确的是( )
A.配制该溶液的步骤是称量和溶解
B.配制过程中用到的仪器只有天平、烧杯和玻璃棒
C.溶解氯化钠固体时,玻璃棒的作用是加快溶解速率
D.转移溶液时,用蒸馏水洗涤烧杯2~3次,将洗涤液一并倒入试剂瓶
9.医院里常用溶质分数为5%的双氧水(H2O2)溶液清洗受伤病人的伤口,若要配制5%的双氧水溶液600g,需要30%的高浓度双氧水的质量为( )
A.30g B.100g C.200g D.400g
10.t ℃时,向一只盛有0.15 g熟石灰的烧杯中加入50 g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体。下列相关叙述正确的是( )
A. 升高温度,上层清液变为不饱和溶液
B. t ℃时,熟石灰的溶解度为0.3 g
C. 烧杯中溶液的质量小于50.15 g
D. 上层清液中溶质质量分数大于0.3%
11.下列物质之间的质量关系,能用右图表示的是( )
A.向一定质量的水中加入蔗糖
B.向一定质量的NaCl饱和溶液中加入KNO3
C.向一定质量的KNO3饱和溶液中加入KNO3
D.向一定质量的Ca(OH)2饱和溶液中加入CaO
12.下列不能达到实验目的的是( )
选项 实验目的 操作
A 鉴别固体硫酸铜和氯化钠 加水溶解观察颜色
B 区分硝酸铵和氢氧化钠 加适量水测量温度变化
C 区分20 ℃时氯化钠的饱和溶液与水 分别加入一定量的氯化钾
D 将某温度下的氢氧化钙的不饱和溶液变为饱和溶液 加入适量氧化钙
二、填空题(每空2分,作图2分,共42分)
13.分别指出下列溶液中的溶质和溶剂,用相关物质的化学式填空:
(1)浓硫酸中的溶质是____________。
(2)石灰水中的溶质是。
(3)35%的酒精溶液中溶质是________________,溶剂是________________。
(4)铁与稀硫酸恰好完全反应后的溶液中,溶质是________,溶剂是________。
14.如图是甲、乙、丙三种固体物质的溶解度曲线,根据图示回答:
(1)0 ℃时,三种物质中溶解度最小的是__________。
(2)将甲溶液由A点转变为B点,可采用的方法是__________(填一种)。
(3)t2℃时在盛有50 g水的烧杯中加入35 g丙物质,充分搅拌后所得溶液的质量是__________g。
(4)若将t3℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,没有晶体析出的是__________物质。
15.在一定温度下,向100 g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是________(填“饱和”或“不饱和”)溶液。
(2)该温度下,KCl的溶解度为________。
(3)实验③所得溶液中溶质的质量分数是________(填字母)。
A.40% B.37.5% C.28.6%
16.溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是________(填字母)。
A.生理盐水 B.糖水 C.医用酒精 D.牛奶
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。
温度/℃ B物质溶解度/g
0 32
20 35
40 40
60 45
80 55
①60 ℃时,A物质的溶解度是________g;
②50 ℃时,向100 g水中加入40 g B物质,充分溶解后得到的是__________(填“饱和”或“不饱和”)溶液,此时溶液的溶质质量分数是__________(结果保留两位小数);
③请根据表格中数据,在A物质溶解度曲线图中绘出B物质的溶解度曲线;
④A、B两种物质溶解度相同时的温度是________℃。
(3)生活中常用75%的酒精消毒液对手和皮肤进行消毒。请分析酒精浓度与杀死细菌的时间对比表(如下表所示)中的数据,酒精消毒液最合适的浓度应为________。根据酒精的物理性质,你认为两者浓度差异的主要原因是________________________________________。
酒精浓度(%) 大肠杆菌 金黄色葡萄球菌 溶血性链球菌
90 15小时 30分钟 5分钟
80 1小时 30分钟 5分钟
70 30秒 5分钟 10秒
60 20秒 30分钟 10秒
50 20秒 2小时 20秒
40 22分钟 4小时 2分钟
三、实验探究题(每空2分,共28分)
17.某化学兴趣小组进行溶液的配制和粗盐的初步提纯实验。
(1)配制200g质量分数为8%的氢氧化钠溶液:
①计算:需要氢氧化钠固体的质量为 克,需要水的体积为 mL(水的密度近似看作1g/mL)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后 (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③用 量取所需要的水,倒入盛有氢氧化钠固体的烧杯中,用 搅拌,使其溶解,并冷却到室温。
④将配制好的溶液放入试剂瓶,塞好橡胶塞并 ,放到指定的地方。
(2)粗盐的初步提纯:称取5.0克粗盐,用药匙逐渐加入到10mL水中,直到粗盐不再溶解为止。还需进行的实验操作步骤的顺序为:称量剩余粗盐、 (填编号)。
A.过滤 B.计算产率 C.蒸发 D.称量精盐
18.某实验小组如图所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
(1)图甲中仪器a的名称是 。
(2)完成此实验正确的操作顺序是(填序号) 。
①溶解 ②把配好的溶液装入试剂瓶 ③称量 ④计算
(3)按实验要求,图甲中还缺少的玻璃仪器是(填名称) 。
(4)小婧按图乙的操作称氯化钠,小民发现小婧的操作有错误,你认为小婧操作中的错误是 。她称取的氯化钠实际质量为 g。
(5)小民所取蒸镏水的体积如图丙所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为(水的密度约为1g/cm3) 。
四、综合应用题(共6分)
19. 某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34 g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8 g,将烧杯内剩余物质过滤、洗涤、干燥后得滤渣3 g。请根据要求回答下列问题:
(1)生成氧气的质量是________g。
(2)瓶内过氧化氢溶液中溶质的质量分数是多少?
(3)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100 g,需加入水的质量是多少?
参考答案
一、选择题
1-6BADACA 7-12DCACBC
二、填空题
13.(1)H2SO4 (2)Ca(OH)2 (3)C2H5OH H2O (4)FeSO4 H2O
14.(1)甲 (2)增加溶质(或恒温蒸发溶剂) (3)80 (4)丙
15.(1)不饱和 (2)40 g (3)C
16.(1)D (2)①70 ②不饱和 28. 57% ③如图所示。
④ 42 (3)70% 酒精易挥发,实际配制的浓度要大些
三、实验探究题
17. (1)①16 184 ②左 BA 氢氧化钠易潮解(或氢氧化钠具有腐蚀性)
③量筒 玻璃棒 ④贴上标签
(2)ACDB
18. (1)烧杯
(2) ④③①②
(3) 玻璃棒
(4)左盘应放食盐右盘放砝码
(5)18%
四、综合应用题
19. 解: (1)3. 2
(2)设34 g过氧化氢溶液中含溶质的质量为x。
2H2O2 2H2O+O2↑
68 32
x 3.2 g
=
x=6. 8 g
过氧化氢溶液中溶质的质量分数为×100%=20%。
(3)配制100 g溶质质量分数为3%的过氧化氢溶液, 需要20%过氧化氢溶液的质量为100 g×3%÷20%=15 g
需加水的质量为100 g-15 g=85 g
答: (2)瓶内过氧化氢溶液中溶质的质量分数为20%。(3)需加入水的质量为85 g。
同课章节目录
