4.2物质组成的表示随堂练习-2021-2022学年九年级化学鲁教版上册(word版 含解析)
文档属性
| 名称 | 4.2物质组成的表示随堂练习-2021-2022学年九年级化学鲁教版上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 113.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-26 00:00:00 | ||
图片预览




文档简介
4.2物质组成的表示
一、选择题(共16题)
1.化合物的化学式为R2O3,它的相对分子质量是160,则R的相对原子质量是
A.112 B.56
C.114 D.72
2.对下列事实的解释正确的是
A.事实:过氧化氢溶液是混合物 解释:含有不同种分子
B.事实:吹胀气球 解释:气球内分子间间隔增大
C.事实:加热红色的氧化汞能生成汞和氧气 解释:分子可以再分,原子不能再分
D.事实:水和过氧化氢的化学性质不同 解释:分子是保持物质性质的最小粒子
3.下列化学用语与表示的意义不相符的是
A.Al2O3:氧化铝 B.Mg+2:镁离子
C.2H2O:两个水分子 D.:氧气中氧元素的化合价为零
4.下面是从小芳同学笔记中摘录的部分化学用语,你认为正确的是
A.3O—3个氧元素 B.O3—3个氧原子
C.SO3—1个三氧化硫分子 D.—1个铁离子
5.高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂,它在整个对水的消毒和净化过程中,不产生任何对人体有害的物质,高铁酸钠被科学家们公认为绿色消毒剂。高铁酸钠(Na2FeO4)中铁元素的化合价是
A.+2 B.+3 C.+4 D.+6
6.蓝莓中含有的花青素(化学式为C15H11O6)具有缓解眼睛疲劳、保护视力的作用。酸能使花青素溶液变成红色,碱能使花青素溶液变成蓝色,下列说法不正确的是
A.一个花青素分子中共有32个原子 B.花青素溶液遇酸溶液变成红色发生了化学反应
C.花青素中氧元素的质量分数最小 D.花青素分子中碳、氢、氧原子个数比为15:11:6
7.有关“物质的量”说法正确的是
A.32克氧气的物质的量是1 B.1molH2O中约含6.02×1023个氢原子
C.1molCO2的质量是44g/mol D.1molSO3比1molSO2多6.02×1023个氧原子
8.有关元素、原子、分子和离子,下列说法正确的是
A.原子可以构成分子,不能直接构成物质
B.分子是保持物质性质的最小粒子
C.元素的化学性质与原子的最外层电子数有关
D.微粒得到或失去电子变成离子
9.酸奶中含有的乳酸菌(C3H6O3)能帮助消化。下列说法错误的是()
A.乳酸菌中 C、H、O 三种元素均为人体必需的常量元素
B.乳酸菌分子由 3 个碳原子、6 个氢原子、3 个氧原子构成
C.乳酸菌中氧元素的质量分数最大
D.乳酸菌中碳、氢、氧元素质量比为6 :1: 8
10.近年用红外激光技术研究液氢,发现液氢中含有H3+,则H3+属于
A.单质 B.分子 C.原子 D.离子
11.可以表示一个原子,还可以表示一种物质的是
A.CO B.H2 C.Cl D.Cu
12.化学符号表示不同的意义,下列化学符号中,表示2个氧原子的是
A.O2 B.2O C.2O2 D.CO2
13.关于葡萄糖(C6H12O6)的组成和构成说法正确的是
A.葡萄糖的相对分子质量是180克
B.葡萄糖中碳、氢、氧三种元素质量比为1:2:1
C.葡萄糖由24个原子构成
D.葡萄糖是由碳、氢、氧三种元素组成的
14.“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体,如图为该反应的微观示意图 ,其中不同的球代表不同的原子,下列说法中,不正确的是( )
A.分子在化学变化中可分
B.此反应一定有单质生成
C.原子在化学变化中不可分
D.参加反应的物质中各元素化合价都没有发生改变
15.学会分析,寻找规律试分析NaCl,x,HClO,KClO3,KClO4的排列顺序规律,可知X代表的物质是
A.HCl B.Ca(ClO)2 C.Cl2 D.Cl2O
16.《中学生守则》规定:中学生不能吸烟。其原因之一是香烟燃烧时放出多种有毒物质和有害气体,其中元素间的质量比是3∶4的物质是
A.CO B.CO2 C.NO D.SO2
二、综合题(共6题)
17.央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊。在熬制明胶过程中添加重铬酸钾(K2Cr2O7),导致生产的药用胶囊重金属铬超标。根据化学式回答下列问题:
(1)请画出钾元素原子结构示意图_______。
(2)该物质由______种元素组成。
(3)钾、铬、氧三种元素的质量比为_______(要求填最简整数比)。
(4)铬元素的质量分数为________( 写出计算步骤, 结果保留到0.1%)。
18.如图是某口服液标签的部分内容。
××口服液 有效成分:硫酸亚铁(FeSO4) ……
(1)该口服液能为人体提供的一种微量元素是________,人体缺乏该元素会引发的病症是________。
(2)硫酸亚铁的相对分子质量是________,硫酸亚铁中铁、硫、氧三种元素的质量比是________。
19.无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。现有西红柿无土栽培营养液中,含硝酸钾(KNO3)的溶质质量分数为5%,请填空:
(1)硝酸钾由 _____ 种元素组成,其中氮、氧两种元素质量比为(最简整数比) _____ ;
(2)某同学练习配制该无土栽培营养液80g,需KNO3_______ g.
下图是该同学配制的实验操作示意图:
(3)量取所需要的水应选择 ____ (选填“10mL”“50mL”或“100mL”)量筒.用上述图示的序号表示配制溶液的操作顺序: ____ ;
(4)要使该溶液的质量分数增大一倍,可以采用增加溶质和 ____ 等方法。请你选取其中一种方法通过计算说明(要有解题过程和必要的文字说明;所选方法如有小数,请保留小数点后两位数)
20.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
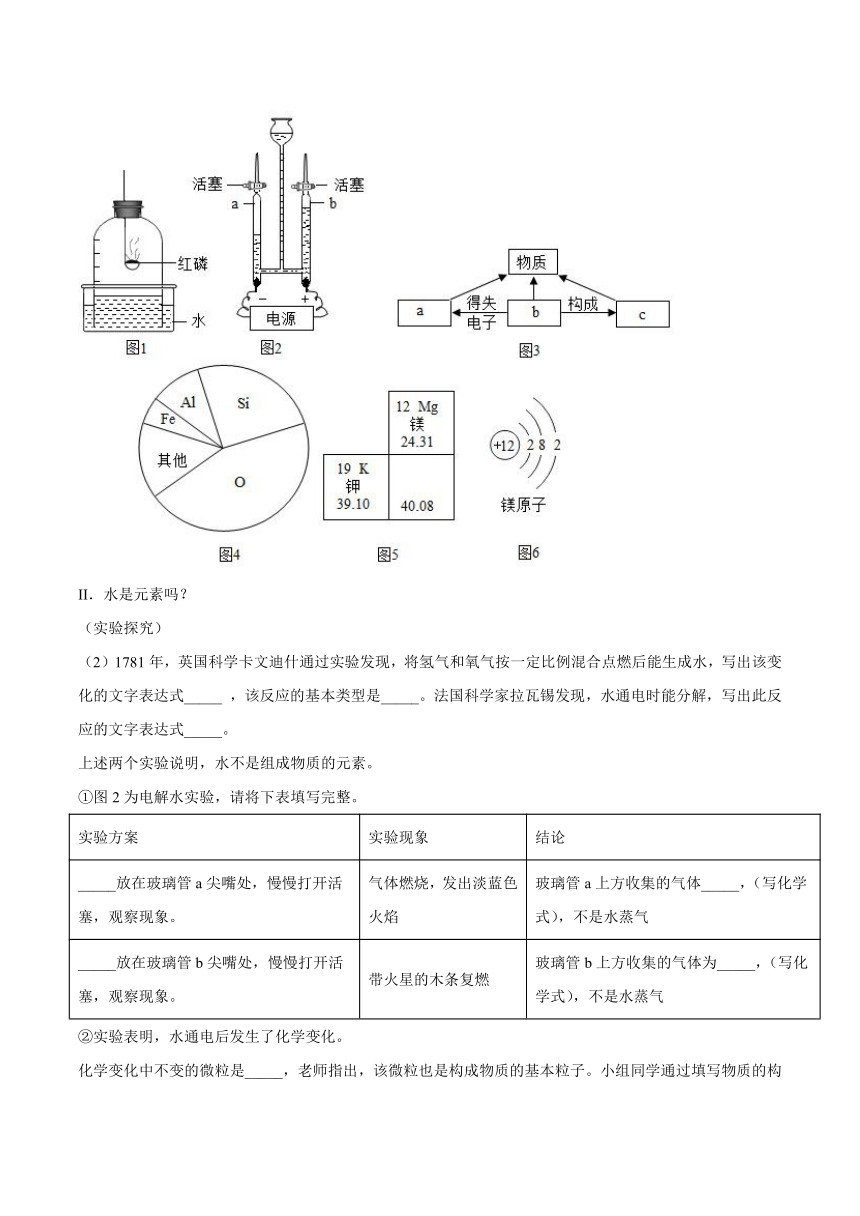
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
21.2021年5月,“天问一号”搭载祝融号火星车成功着陆火星。
(1)火星车使用新型镁锂合金实现了探测器的轻量化,画出锂原子的结构示意图________。
(2)火星车热控材料——纳米气凝胶的主要成分是二氧化硅,化学式为________,其中硅元素的化合价为________。
(3)火星车的动力来源于太阳能,人类正在利用和开发的新能源还有________(写一种)。
(4)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是________。
(5)若为满足人类未来在火星上生活,下列研究设想不合理的是 (填字母序号)。
A.将CO2转化为O2,提高O2含量 B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术 D.利用火星上的金属矿物冶炼金属
22.化学用语可准确、简洁地记录、表达、交流化学信息.请用化学符号表示:
(1)2个过氧化氢分子____________;
(2)表示的粒子____________
(3)3个锌原子____________;
(4)氯化亚铁中铁元素化合价是+2价____________
(5)2个硫酸根离子____________;
(6)电解水中的最小粒子____________、____________.
参考答案
1.B
【详解】
根据化合物的化学式为R2O3,相对分子质量为160,设R的相对原子质量为x,则2x +16×3=160,解得x=56;故选B。
2.A
【详解】
A、由不同种物质组成的是混合物,过氧化氢溶液是混合物,从微观上看过氧化氢溶液中含有过氧化氢分子、水分子两种不同分子,此选项正确;
B、吹胀气球,是因为分子间有间隔,气体增多,分子间隔变小,此选项错误;
C、加热红色的氧化汞能生成汞和氧气,是因为氧化汞分子分裂成了汞原子和氧原子,然后氧原子重新组合形成氧分子,该事实说明在化学变化中分子是可以再分、原子不能再分,此选项错误;
D、由分子构成的物质,分子是保持物质化学性质的最小粒子,水和过氧化氢的化学性质不同的原因是分子的构成不同,此选项错误。
故选A。
3.B
【解析】
A、氧化铝表示为Al2O3,正确但不符合题意,错误;B、镁离子表示为Mg2+,题目中是错误的,错误符合题意,正确;C、两个水分子表示为2H2O,正确但不符合题意,错误;D、氧气中氧元素的化合价为零表示为,正确但不符合题意,错误。故选B。
4.C
【详解】
A、元素符号前面的数字表示原子个数,故3O表示3个氧原子,不符合题意。
B、元素符号右下角的数字表示分子内的原子个数,O3中的3表示一个臭氧分子中含有3个氧原子,不符合题意。
C、SO3表示1个三氧化硫分子,符合题意。
D、元素符号正上方的数字和正负号表示元素的化合价表示铁元素的化合价为+3价;1个铁离子的符号应为:Fe3+,不符合题意。
故选:C。
5.D
【详解】
高铁酸钠(Na2FeO4)中钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合物中化合价代数和为零的原则,设该化合物中铁元素的化合价为x,,故x=+6,故选D。
6.C
【详解】
A、一个花青素分子中共有15+11+6=32个原子。错误。
B、花青素溶液遇酸溶液变成红色是花青素与酸发生了反应生成了红色物质,发生了化学变化。正确。
C、花青素中C、H、O元素的质量比为(12×15):11:(16×6)=60:11:96,所以氢元素的质量分数最小。错误。
D、花青素分子中碳、氢、氧原子个数比为15:11:6,正确。
故选C。
7.D
【详解】
A. 32克氧气的物质的量是1 mol,选项A错误;
B.一个水分子中有两氢原子,所以1molH2O中约含12.04×1023个氢原子,选项B错误;
C. 1molCO2的质量是44g,选项C错误;
D. 一个三氧化硫分子比一个二氧化硫分子多一个氧原子,所以1molSO3比1molSO2多6.02×1023个氧原子,选项D正确。选D。
8.C
【详解】
A、原子可以构成分子,也可以直接构成物质,如铁由铁原子构成,不符合题意;
B、由分子构成的构成,分子是保持物质化学性质的最小粒子,由原子构成的物质,原子是保持物质化学性质的最小粒子,由离子构成的物质,离子是保持物质化学性质的最小粒子,不符合题意;
C、元素的化学性质与原子的最外层电子数有关,最外层电子数相同,化学性质相似,符合题意;
D、原子可通过得失电子变成离子,离子可通过失得电子变成原子,不符合题意。
故选C。
9.B
【详解】
A.乳酸菌中 C、H、O 三种元素均为人体必需的常量元素,选项正确;
B.一个乳酸菌分子由 3 个碳原子、6 个氢原子、3 个氧原子构成,选项错误;
C.乳酸菌中碳、氢、氧三种元素的质量比:(12×3):(1×6):(16×3)=6:1:8,氧元素的质量分数最大,选项正确;
D.乳酸菌中碳、氢、氧三种元素的质量比:(12×3):(1×6):(16×3)=6:1:8,选项正确。
故选B。
10.D
【详解】
根据离子的表示方法,可知H3+属于离子;故选D.
11.D
【详解】
A、该符号是一氧化碳的化学式,不是元素符号,故选项不符合题意;
B、该符号是氢气的化学式,不是元素符号,故选项不符合题意;
C、Cl可表示氯元素,表示一个氯原子,但不能表示一种物质,故选项不符合题意;
D、Cu属于金属元素,可表示铜元素,表示一个铜原子,还能表示铜这一物质,故选项符合题意。
故选D。
12.B
【详解】
试题分析:A、O2表示一个氧分子中含有2个氧原子,错误,B、在元素符号前面加数字,表示原子个数,故2O表示2个氧原子,正确,C、在化学式前面加数字,表示分子个数,2O2表示2个氧分子,错误,D、CO2表示一个二氧化碳分子中含有2个氧原子,错误,故选B
13.D
【详解】
A、葡萄糖的化学式为:C6H12O6,它的相对分子质量为:12×6+12+16×6=180,故不符合题意;
B、葡萄糖中碳、氢、氧三种元素质量比为:(12×6):12:(16×6)=6:1:8,故不符合题意;
C、一个葡萄糖分子是由6+12+6=24个原子构成,故不符合题意;
D、葡萄糖是由碳、氢、氧三种元素组成的,故符合题意。
14.D
【详解】
A、由微观图可知,反应前后分子构成发生改变,即分子在化学变化前后不同,说明化学变化中分子可分,选项正确;
B、反应生成物中有一种生成物的分子由2个相同的原子构成,该物质为单质,选项正确;
C、反应前后的四种分子中,分子构成虽然不同,但在变化前后构成分子的原子种类没变,说明原子在化学变化中不可分,选项正确;
D、由微观示意图可知,生成物中有单质生成,一定有化合价的变化,选项错误。故选D。
15.C
【详解】
A、氢元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1,个选项错误;
B、钙元素显+2价,氧元素显-2价,设氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+2)+2y+(-2)×2=0,则y=+1,故选项错误;
C、单质中元素的化合价为0,因此氯气中氯元素化合价为0,氯元素化合价在-1和+1之间,符合要求,故选项正确;
D、氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:2·z+(-2)=0,则z=+1,故选项错误。
故选:C。
16.A
【详解】
本题主要考查元素质量比的计算。根据题意,香烟燃烧时放出多种有毒物质和致癌物质,且两种元素间的质量比是3:4,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答。
A、CO中碳元素和氧元素的质量比为12:16=3:4,故选项正确.
B、CO2中硫元素和氧元素的质量比为12:(16×2)=6:16,故选项错误.
C、NO中氮元素和氧元素的质量比为14:16=7:8,故选项错误..
D、SO2中硫元素和氧元素的质量比为32:(16×2)=1:1,故选项错误
故选A
17. 三 39∶52∶56 35.4%(详见解析)
【详解】
(1)在钾原子中,核内质子数为19,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,第四层上有1个电子,其原子结构示意图为;
(2)根据重铬酸钾(K2Cr2O7)的化学式可知,在重铬酸钾中,含有钾元素、铬元素、氧元素三种元素;
(3)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比=(39×2):(52×2):(16×7)=39:52:56;
(4)铬元素的质量分数=。
18.(1)铁 ;贫血
(2)152;7∶4∶8
【详解】
(1)标签中的信息可知该物质的有效成分为硫酸亚铁,缺铁会造成缺铁性贫血;
(2)硫酸亚铁的化学式为:FeSO4,所以硫酸亚铁的相对分子质量为:56+32+16×4=152,硫酸亚铁中铁、硫、氧三种元素的质量比是:56:32:64=7:4:8。
19.3 7:24 4 100mL ④①②⑤③ 采用蒸发水的方法使其溶质的质量分数增大一倍,设需要蒸发水的质量为x,则
=10% x=40g;
采用加入溶质的方法使其溶质的质量分数增大一倍,设需要加入硝酸钾的质量为y,则
=10% y=4.44g。
答:可蒸发掉40g水或加入4.44g硝酸钾
【详解】
(1)根据硝酸钾的化学式可知,硝酸钾由钾、氮、氧3种元素组成,其中氮、氧两种元素质量比=14:16×3=7:24;
(2)配制该无土栽培营养液80g,需KNO3的质量=80g×5%=4g;
(3)配制该无土栽培营养液80g,需KNO3=80g×5%=4g,需水的质量=80g-4g=76g,则水的体积为76mL,应选用100mL量筒;由配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,可知配制溶液的操作顺序是:④①②⑤③;
(4)采用蒸发水的方法使其溶质的质量分数增大一倍,设需要蒸发水的质量为x,则
=10% x=40g;
采用加入溶质的方法使其溶质的质量分数增大一倍,设需要加入硝酸钾的质量为y,则
=10% y=4.44g。
答:可蒸发掉40g水或加入4.44g硝酸钾。
20.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
21.
(1)
(2) SiO2 +4价
(3)地热能(或潮汐能、风能、生物质能、核能等)
(4)分别伸入燃着的木条检验(或倒入适量澄清石灰水,振荡)(或其他合理答案)
(5)B
【解析】
(1)
锂原子是3号元素,核外3个电子,锂原子的结构示意图为;
(2)
火星车热控材料——纳米气凝胶的主要成分是二氧化硅,化学式为SiO2,氧元素的化合价为-2价,根据化合物中元素正负化合价代数和为0,可得硅元素的化合价为+4价;
(3)
火星车的动力来源于太阳能,人类正在利用和开发的新能源还有地热能(或潮汐能、风能、生物质能、核能等);
(4)
火星低层大气的主要成分中含量最多的是二氧化碳,为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是分别伸入燃着的木条检验(或倒入适量澄清石灰水,振荡);
(5)
A、将CO2转化为O2,提高O2含量,人类生活需要氧气,研究设想合理;
B、将CO2分解转化为N2,提高N2含量,根据质量守恒定律,CO2分解不会生成N2,研究设想不合理;
C、寻找水的存在和开发水循环技术,研究设想合理;
D、利用火星上的金属矿物冶炼金属,研究设想合理;
故选B。
22.2H2O2; S2- 3Zn 2SO42- H O
【详解】
(1)过氧化氢的化学式为H2O2,它表示过氧化氢这种物质,还表示一个过氧化氢分子,那么2个过氧化氢分子,要在化学式左边加2,即2H2O2;(2)该图是原子结构示意图,其核电荷数是16,是硫元素,该图中16<2+8+8,是硫元素的阴离子,带两个单位的负电荷,离子电荷要写在符号的右上角,而且数字在前,正负号在后,即S2-;(3)锌元素符号为Zn,它表示锌元素、锌单质、一个锌原子,那么3个锌原子,就要在元素符号左边加上3,即3Zn;(4)氯化亚铁的化学式为FeCl2,其中铁元素显+2价,就要把+2写在铁元素符号的正上方,即;(5)硫酸根离子的符号是SO42-,那么2个硫酸根离子,就要在该符号左边加上2,即2SO42-;(6)原子是化学变化中的最小粒子,在电解水反应中,有两种原子,即氢原子和氧原子,它们都是用元素符号来表示,即H、O。
一、选择题(共16题)
1.化合物的化学式为R2O3,它的相对分子质量是160,则R的相对原子质量是
A.112 B.56
C.114 D.72
2.对下列事实的解释正确的是
A.事实:过氧化氢溶液是混合物 解释:含有不同种分子
B.事实:吹胀气球 解释:气球内分子间间隔增大
C.事实:加热红色的氧化汞能生成汞和氧气 解释:分子可以再分,原子不能再分
D.事实:水和过氧化氢的化学性质不同 解释:分子是保持物质性质的最小粒子
3.下列化学用语与表示的意义不相符的是
A.Al2O3:氧化铝 B.Mg+2:镁离子
C.2H2O:两个水分子 D.:氧气中氧元素的化合价为零
4.下面是从小芳同学笔记中摘录的部分化学用语,你认为正确的是
A.3O—3个氧元素 B.O3—3个氧原子
C.SO3—1个三氧化硫分子 D.—1个铁离子
5.高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂,它在整个对水的消毒和净化过程中,不产生任何对人体有害的物质,高铁酸钠被科学家们公认为绿色消毒剂。高铁酸钠(Na2FeO4)中铁元素的化合价是
A.+2 B.+3 C.+4 D.+6
6.蓝莓中含有的花青素(化学式为C15H11O6)具有缓解眼睛疲劳、保护视力的作用。酸能使花青素溶液变成红色,碱能使花青素溶液变成蓝色,下列说法不正确的是
A.一个花青素分子中共有32个原子 B.花青素溶液遇酸溶液变成红色发生了化学反应
C.花青素中氧元素的质量分数最小 D.花青素分子中碳、氢、氧原子个数比为15:11:6
7.有关“物质的量”说法正确的是
A.32克氧气的物质的量是1 B.1molH2O中约含6.02×1023个氢原子
C.1molCO2的质量是44g/mol D.1molSO3比1molSO2多6.02×1023个氧原子
8.有关元素、原子、分子和离子,下列说法正确的是
A.原子可以构成分子,不能直接构成物质
B.分子是保持物质性质的最小粒子
C.元素的化学性质与原子的最外层电子数有关
D.微粒得到或失去电子变成离子
9.酸奶中含有的乳酸菌(C3H6O3)能帮助消化。下列说法错误的是()
A.乳酸菌中 C、H、O 三种元素均为人体必需的常量元素
B.乳酸菌分子由 3 个碳原子、6 个氢原子、3 个氧原子构成
C.乳酸菌中氧元素的质量分数最大
D.乳酸菌中碳、氢、氧元素质量比为6 :1: 8
10.近年用红外激光技术研究液氢,发现液氢中含有H3+,则H3+属于
A.单质 B.分子 C.原子 D.离子
11.可以表示一个原子,还可以表示一种物质的是
A.CO B.H2 C.Cl D.Cu
12.化学符号表示不同的意义,下列化学符号中,表示2个氧原子的是
A.O2 B.2O C.2O2 D.CO2
13.关于葡萄糖(C6H12O6)的组成和构成说法正确的是
A.葡萄糖的相对分子质量是180克
B.葡萄糖中碳、氢、氧三种元素质量比为1:2:1
C.葡萄糖由24个原子构成
D.葡萄糖是由碳、氢、氧三种元素组成的
14.“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体,如图为该反应的微观示意图 ,其中不同的球代表不同的原子,下列说法中,不正确的是( )
A.分子在化学变化中可分
B.此反应一定有单质生成
C.原子在化学变化中不可分
D.参加反应的物质中各元素化合价都没有发生改变
15.学会分析,寻找规律试分析NaCl,x,HClO,KClO3,KClO4的排列顺序规律,可知X代表的物质是
A.HCl B.Ca(ClO)2 C.Cl2 D.Cl2O
16.《中学生守则》规定:中学生不能吸烟。其原因之一是香烟燃烧时放出多种有毒物质和有害气体,其中元素间的质量比是3∶4的物质是
A.CO B.CO2 C.NO D.SO2
二、综合题(共6题)
17.央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊。在熬制明胶过程中添加重铬酸钾(K2Cr2O7),导致生产的药用胶囊重金属铬超标。根据化学式回答下列问题:
(1)请画出钾元素原子结构示意图_______。
(2)该物质由______种元素组成。
(3)钾、铬、氧三种元素的质量比为_______(要求填最简整数比)。
(4)铬元素的质量分数为________( 写出计算步骤, 结果保留到0.1%)。
18.如图是某口服液标签的部分内容。
××口服液 有效成分:硫酸亚铁(FeSO4) ……
(1)该口服液能为人体提供的一种微量元素是________,人体缺乏该元素会引发的病症是________。
(2)硫酸亚铁的相对分子质量是________,硫酸亚铁中铁、硫、氧三种元素的质量比是________。
19.无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。现有西红柿无土栽培营养液中,含硝酸钾(KNO3)的溶质质量分数为5%,请填空:
(1)硝酸钾由 _____ 种元素组成,其中氮、氧两种元素质量比为(最简整数比) _____ ;
(2)某同学练习配制该无土栽培营养液80g,需KNO3_______ g.
下图是该同学配制的实验操作示意图:
(3)量取所需要的水应选择 ____ (选填“10mL”“50mL”或“100mL”)量筒.用上述图示的序号表示配制溶液的操作顺序: ____ ;
(4)要使该溶液的质量分数增大一倍,可以采用增加溶质和 ____ 等方法。请你选取其中一种方法通过计算说明(要有解题过程和必要的文字说明;所选方法如有小数,请保留小数点后两位数)
20.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
21.2021年5月,“天问一号”搭载祝融号火星车成功着陆火星。
(1)火星车使用新型镁锂合金实现了探测器的轻量化,画出锂原子的结构示意图________。
(2)火星车热控材料——纳米气凝胶的主要成分是二氧化硅,化学式为________,其中硅元素的化合价为________。
(3)火星车的动力来源于太阳能,人类正在利用和开发的新能源还有________(写一种)。
(4)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是________。
(5)若为满足人类未来在火星上生活,下列研究设想不合理的是 (填字母序号)。
A.将CO2转化为O2,提高O2含量 B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术 D.利用火星上的金属矿物冶炼金属
22.化学用语可准确、简洁地记录、表达、交流化学信息.请用化学符号表示:
(1)2个过氧化氢分子____________;
(2)表示的粒子____________
(3)3个锌原子____________;
(4)氯化亚铁中铁元素化合价是+2价____________
(5)2个硫酸根离子____________;
(6)电解水中的最小粒子____________、____________.
参考答案
1.B
【详解】
根据化合物的化学式为R2O3,相对分子质量为160,设R的相对原子质量为x,则2x +16×3=160,解得x=56;故选B。
2.A
【详解】
A、由不同种物质组成的是混合物,过氧化氢溶液是混合物,从微观上看过氧化氢溶液中含有过氧化氢分子、水分子两种不同分子,此选项正确;
B、吹胀气球,是因为分子间有间隔,气体增多,分子间隔变小,此选项错误;
C、加热红色的氧化汞能生成汞和氧气,是因为氧化汞分子分裂成了汞原子和氧原子,然后氧原子重新组合形成氧分子,该事实说明在化学变化中分子是可以再分、原子不能再分,此选项错误;
D、由分子构成的物质,分子是保持物质化学性质的最小粒子,水和过氧化氢的化学性质不同的原因是分子的构成不同,此选项错误。
故选A。
3.B
【解析】
A、氧化铝表示为Al2O3,正确但不符合题意,错误;B、镁离子表示为Mg2+,题目中是错误的,错误符合题意,正确;C、两个水分子表示为2H2O,正确但不符合题意,错误;D、氧气中氧元素的化合价为零表示为,正确但不符合题意,错误。故选B。
4.C
【详解】
A、元素符号前面的数字表示原子个数,故3O表示3个氧原子,不符合题意。
B、元素符号右下角的数字表示分子内的原子个数,O3中的3表示一个臭氧分子中含有3个氧原子,不符合题意。
C、SO3表示1个三氧化硫分子,符合题意。
D、元素符号正上方的数字和正负号表示元素的化合价表示铁元素的化合价为+3价;1个铁离子的符号应为:Fe3+,不符合题意。
故选:C。
5.D
【详解】
高铁酸钠(Na2FeO4)中钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合物中化合价代数和为零的原则,设该化合物中铁元素的化合价为x,,故x=+6,故选D。
6.C
【详解】
A、一个花青素分子中共有15+11+6=32个原子。错误。
B、花青素溶液遇酸溶液变成红色是花青素与酸发生了反应生成了红色物质,发生了化学变化。正确。
C、花青素中C、H、O元素的质量比为(12×15):11:(16×6)=60:11:96,所以氢元素的质量分数最小。错误。
D、花青素分子中碳、氢、氧原子个数比为15:11:6,正确。
故选C。
7.D
【详解】
A. 32克氧气的物质的量是1 mol,选项A错误;
B.一个水分子中有两氢原子,所以1molH2O中约含12.04×1023个氢原子,选项B错误;
C. 1molCO2的质量是44g,选项C错误;
D. 一个三氧化硫分子比一个二氧化硫分子多一个氧原子,所以1molSO3比1molSO2多6.02×1023个氧原子,选项D正确。选D。
8.C
【详解】
A、原子可以构成分子,也可以直接构成物质,如铁由铁原子构成,不符合题意;
B、由分子构成的构成,分子是保持物质化学性质的最小粒子,由原子构成的物质,原子是保持物质化学性质的最小粒子,由离子构成的物质,离子是保持物质化学性质的最小粒子,不符合题意;
C、元素的化学性质与原子的最外层电子数有关,最外层电子数相同,化学性质相似,符合题意;
D、原子可通过得失电子变成离子,离子可通过失得电子变成原子,不符合题意。
故选C。
9.B
【详解】
A.乳酸菌中 C、H、O 三种元素均为人体必需的常量元素,选项正确;
B.一个乳酸菌分子由 3 个碳原子、6 个氢原子、3 个氧原子构成,选项错误;
C.乳酸菌中碳、氢、氧三种元素的质量比:(12×3):(1×6):(16×3)=6:1:8,氧元素的质量分数最大,选项正确;
D.乳酸菌中碳、氢、氧三种元素的质量比:(12×3):(1×6):(16×3)=6:1:8,选项正确。
故选B。
10.D
【详解】
根据离子的表示方法,可知H3+属于离子;故选D.
11.D
【详解】
A、该符号是一氧化碳的化学式,不是元素符号,故选项不符合题意;
B、该符号是氢气的化学式,不是元素符号,故选项不符合题意;
C、Cl可表示氯元素,表示一个氯原子,但不能表示一种物质,故选项不符合题意;
D、Cu属于金属元素,可表示铜元素,表示一个铜原子,还能表示铜这一物质,故选项符合题意。
故选D。
12.B
【详解】
试题分析:A、O2表示一个氧分子中含有2个氧原子,错误,B、在元素符号前面加数字,表示原子个数,故2O表示2个氧原子,正确,C、在化学式前面加数字,表示分子个数,2O2表示2个氧分子,错误,D、CO2表示一个二氧化碳分子中含有2个氧原子,错误,故选B
13.D
【详解】
A、葡萄糖的化学式为:C6H12O6,它的相对分子质量为:12×6+12+16×6=180,故不符合题意;
B、葡萄糖中碳、氢、氧三种元素质量比为:(12×6):12:(16×6)=6:1:8,故不符合题意;
C、一个葡萄糖分子是由6+12+6=24个原子构成,故不符合题意;
D、葡萄糖是由碳、氢、氧三种元素组成的,故符合题意。
14.D
【详解】
A、由微观图可知,反应前后分子构成发生改变,即分子在化学变化前后不同,说明化学变化中分子可分,选项正确;
B、反应生成物中有一种生成物的分子由2个相同的原子构成,该物质为单质,选项正确;
C、反应前后的四种分子中,分子构成虽然不同,但在变化前后构成分子的原子种类没变,说明原子在化学变化中不可分,选项正确;
D、由微观示意图可知,生成物中有单质生成,一定有化合价的变化,选项错误。故选D。
15.C
【详解】
A、氢元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1,个选项错误;
B、钙元素显+2价,氧元素显-2价,设氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+2)+2y+(-2)×2=0,则y=+1,故选项错误;
C、单质中元素的化合价为0,因此氯气中氯元素化合价为0,氯元素化合价在-1和+1之间,符合要求,故选项正确;
D、氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:2·z+(-2)=0,则z=+1,故选项错误。
故选:C。
16.A
【详解】
本题主要考查元素质量比的计算。根据题意,香烟燃烧时放出多种有毒物质和致癌物质,且两种元素间的质量比是3:4,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答。
A、CO中碳元素和氧元素的质量比为12:16=3:4,故选项正确.
B、CO2中硫元素和氧元素的质量比为12:(16×2)=6:16,故选项错误.
C、NO中氮元素和氧元素的质量比为14:16=7:8,故选项错误..
D、SO2中硫元素和氧元素的质量比为32:(16×2)=1:1,故选项错误
故选A
17. 三 39∶52∶56 35.4%(详见解析)
【详解】
(1)在钾原子中,核内质子数为19,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,第四层上有1个电子,其原子结构示意图为;
(2)根据重铬酸钾(K2Cr2O7)的化学式可知,在重铬酸钾中,含有钾元素、铬元素、氧元素三种元素;
(3)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比=(39×2):(52×2):(16×7)=39:52:56;
(4)铬元素的质量分数=。
18.(1)铁 ;贫血
(2)152;7∶4∶8
【详解】
(1)标签中的信息可知该物质的有效成分为硫酸亚铁,缺铁会造成缺铁性贫血;
(2)硫酸亚铁的化学式为:FeSO4,所以硫酸亚铁的相对分子质量为:56+32+16×4=152,硫酸亚铁中铁、硫、氧三种元素的质量比是:56:32:64=7:4:8。
19.3 7:24 4 100mL ④①②⑤③ 采用蒸发水的方法使其溶质的质量分数增大一倍,设需要蒸发水的质量为x,则
=10% x=40g;
采用加入溶质的方法使其溶质的质量分数增大一倍,设需要加入硝酸钾的质量为y,则
=10% y=4.44g。
答:可蒸发掉40g水或加入4.44g硝酸钾
【详解】
(1)根据硝酸钾的化学式可知,硝酸钾由钾、氮、氧3种元素组成,其中氮、氧两种元素质量比=14:16×3=7:24;
(2)配制该无土栽培营养液80g,需KNO3的质量=80g×5%=4g;
(3)配制该无土栽培营养液80g,需KNO3=80g×5%=4g,需水的质量=80g-4g=76g,则水的体积为76mL,应选用100mL量筒;由配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,可知配制溶液的操作顺序是:④①②⑤③;
(4)采用蒸发水的方法使其溶质的质量分数增大一倍,设需要蒸发水的质量为x,则
=10% x=40g;
采用加入溶质的方法使其溶质的质量分数增大一倍,设需要加入硝酸钾的质量为y,则
=10% y=4.44g。
答:可蒸发掉40g水或加入4.44g硝酸钾。
20.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
21.
(1)
(2) SiO2 +4价
(3)地热能(或潮汐能、风能、生物质能、核能等)
(4)分别伸入燃着的木条检验(或倒入适量澄清石灰水,振荡)(或其他合理答案)
(5)B
【解析】
(1)
锂原子是3号元素,核外3个电子,锂原子的结构示意图为;
(2)
火星车热控材料——纳米气凝胶的主要成分是二氧化硅,化学式为SiO2,氧元素的化合价为-2价,根据化合物中元素正负化合价代数和为0,可得硅元素的化合价为+4价;
(3)
火星车的动力来源于太阳能,人类正在利用和开发的新能源还有地热能(或潮汐能、风能、生物质能、核能等);
(4)
火星低层大气的主要成分中含量最多的是二氧化碳,为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是分别伸入燃着的木条检验(或倒入适量澄清石灰水,振荡);
(5)
A、将CO2转化为O2,提高O2含量,人类生活需要氧气,研究设想合理;
B、将CO2分解转化为N2,提高N2含量,根据质量守恒定律,CO2分解不会生成N2,研究设想不合理;
C、寻找水的存在和开发水循环技术,研究设想合理;
D、利用火星上的金属矿物冶炼金属,研究设想合理;
故选B。
22.2H2O2; S2- 3Zn 2SO42- H O
【详解】
(1)过氧化氢的化学式为H2O2,它表示过氧化氢这种物质,还表示一个过氧化氢分子,那么2个过氧化氢分子,要在化学式左边加2,即2H2O2;(2)该图是原子结构示意图,其核电荷数是16,是硫元素,该图中16<2+8+8,是硫元素的阴离子,带两个单位的负电荷,离子电荷要写在符号的右上角,而且数字在前,正负号在后,即S2-;(3)锌元素符号为Zn,它表示锌元素、锌单质、一个锌原子,那么3个锌原子,就要在元素符号左边加上3,即3Zn;(4)氯化亚铁的化学式为FeCl2,其中铁元素显+2价,就要把+2写在铁元素符号的正上方,即;(5)硫酸根离子的符号是SO42-,那么2个硫酸根离子,就要在该符号左边加上2,即2SO42-;(6)原子是化学变化中的最小粒子,在电解水反应中,有两种原子,即氢原子和氧原子,它们都是用元素符号来表示,即H、O。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
