2.3原子的构成随堂练习—2021_2022学年九年级化学鲁教版上册(word版 含解析)
文档属性
| 名称 | 2.3原子的构成随堂练习—2021_2022学年九年级化学鲁教版上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 163.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-26 00:00:00 | ||
图片预览



文档简介
2.3原子的构成
一、选择题(共16题)
1.法国化学家德维尔在实验室中意外地发现一种新原子。已知该原子的原子核中含有27个微粒,其中14个微粒不带电,则该原子的质子数为( )
A.13 B.14 C.26 D.40
2.下列物质由原子构成的是
A.氨气 B.氦气 C.硫酸铜 D.C60
3.元素的化学性质主要决定于原子的
A.核外电子数 B.核电荷数 C.最外层电子数 D.中子数
4.下列叙述正确的是①原子由质子和中子构成 ②原子不显电性 ③原子不能再分 ④原子的质子数决定元素种类 ⑤原子可以构成分子,也可直接构成物质( )
A.①②④ B.②④⑤ C.③④ D.①②③⑤
5.下列各组物质中,都由分子构成的一组是( )
A.金和硅 B.水和氨气 C.汞和氯化钠 D.干冰和硫酸铜
6.下列物质中,由离子构成的是
A.氧气 B.石墨 C.烧碱 D.氧化汞
7.下列关于分子、原子的说法中,错误的是
A.湿衣服晾干是水分子运动的结果 B.化学变化中原子的种类不变
C.气体可压缩是因为分子间有间隔 D.原子是不可再分的最小粒子
8.下列图示中(“”表示氢原子,“”表示氧原子),能表示保持水的化学性质的粒子的是
A. B. C. D.
9.某种碳原子可用于检测人体中的幽门螺旋杆菌,该原子的原子核内含有6个质子和8个中子,则该原子的核外电子数为
A.14 B.8 C.6 D.2
10.质量相等的氮气、氧气、一氧化碳与二氧化硫中,分子数最少的是( )
A.氮气 B.氧气 C.一氧化碳 D.二氧化硫
11.如图为镍的原子结构示意图,关于该原子的叙述错误的是
A.核电荷数为28
B.核外有4个电子层
C.质子数大于核外电子数
D.易失去2个电子
12.家庭装修材料中的有害物质会影响人体的健康。如某些花岗岩石材中就含有放射性元素氡。若一种氡原子的核外电子数为86,相对原子质量为222,这种氡原子中子数为( )
A.50 B.86 C.136 D.222
13.下列各组物质中,都由分子构成的一组是
A.氩气和水 B.金和金刚石 C.铜和氯化钠 D.氢气和水
14.铀235(其原子核内有92个质子,相对原子质量为235)是核电站的主要燃料。下列有关说法正确的是
A.铀属于非金属元素 B.该原子的核电荷数为92
C.该原子核内有51个中子 D.该原子核外有143个电子
15.下列物质中,由原子直接构成的是
A.C60 B.金刚石 C.氮气 D.氯化钠
16.下列叙述中错误的是
A.水分子是保持水的化学性质的最小粒子
B.水是由氢元素和氧元素组成的氧化物
C.电解水生成氢气和氧气的体积比为2:1
D.液态水变成水蒸气的过程中水分子变大了
二、综合题(共5题)
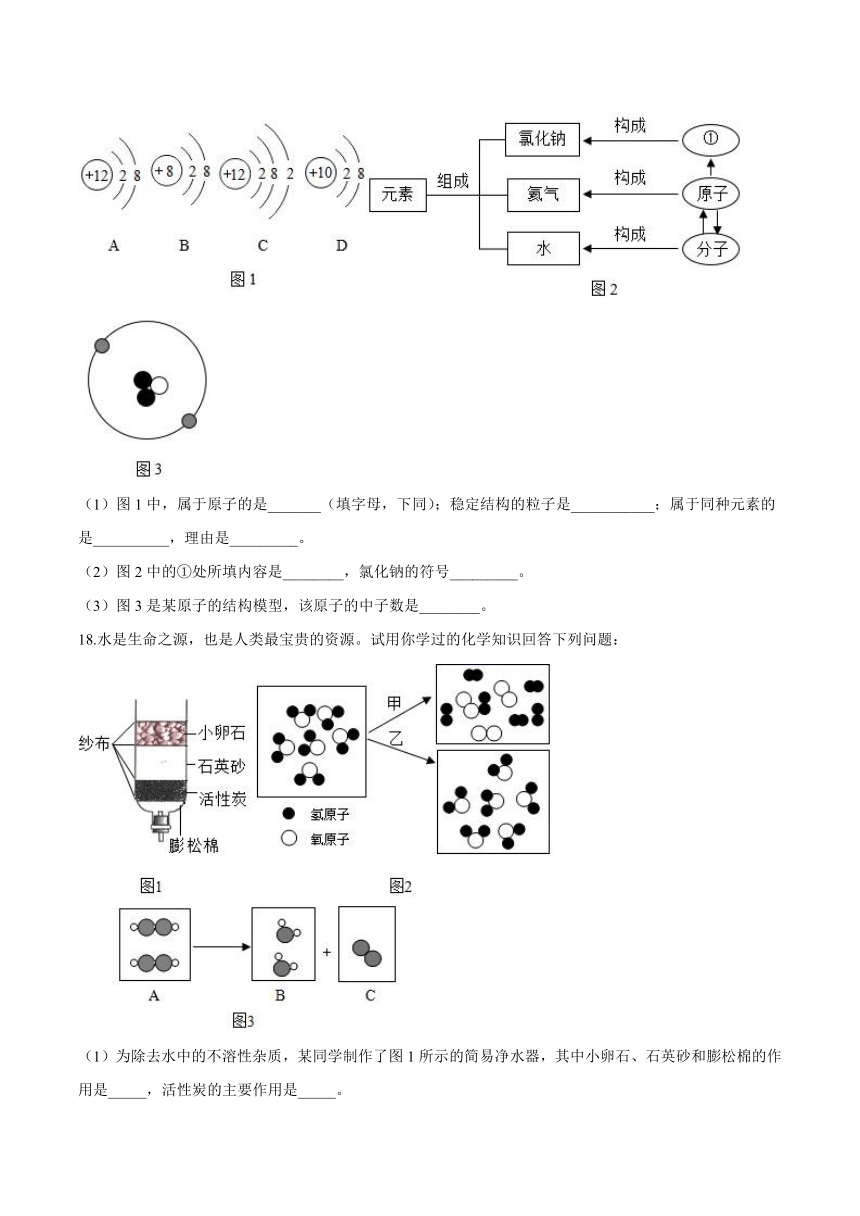
17.“宏观一微观一符号”是化学视角认识物质的方法。根据下列图示回答问题:
(1)图1中,属于原子的是_______(填字母,下同);稳定结构的粒子是___________;属于同种元素的是__________,理由是_________。
(2)图2中的①处所填内容是________,氯化钠的符号_________。
(3)图3是某原子的结构模型,该原子的中子数是________。
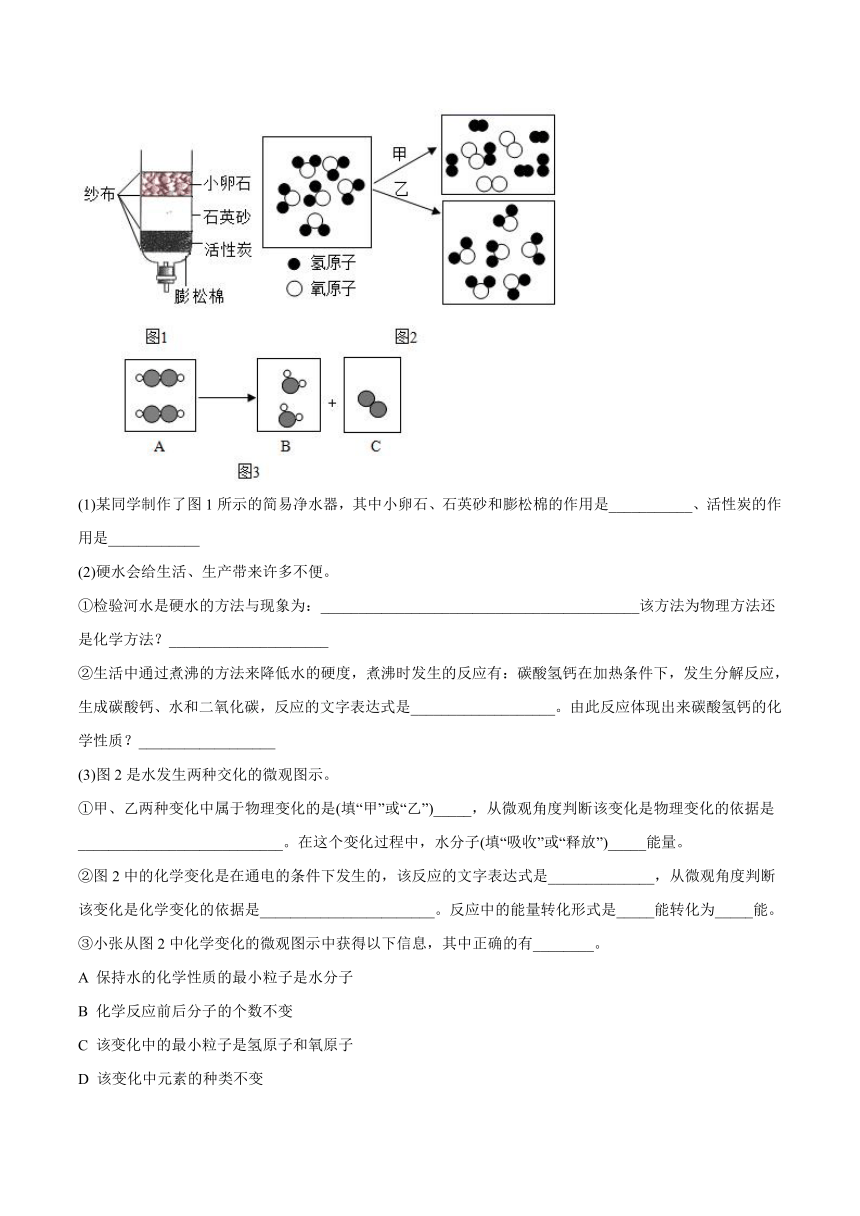
18.水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识回答下列问题:
(1)为除去水中的不溶性杂质,某同学制作了图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是_____,活性炭的主要作用是_____。
(2)硬水会给生活、生产带来许多不便。
①检验河水是硬水的方法与现象为:_____。
②生活中可以通过煮沸的方法来降低水的硬度,煮沸时发生的反应之一是:碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,该反应的文字表达式是_____。
(3)图2是水发生两种交化的微观图示。
①甲、乙两种变化中属于物理变化的是(填“甲”或“乙”)_____,从微观角度判断该变化是物理变化的依据是_____。在这个变化过程中,水分子(填“吸收”或“释放”)_____能量。
②图2中的化学变化是在通电的条件下发生的,该反应的文字表达式是_____,从微观角度判断该变化是化学变化的依据是_____。反应中的能量转化形式是_____能转化为_____能。
③小张从图2中化学变化的微观图示中获得以下信息,其中正确的有_____。
A 保持水的化学性质的最小粒子是水分子
B 化学反应前后分子的个数不变
C 该变化中的最小粒子是氢原子和氧原子
D 该变化中元素的种类不变
(4)图3为某化学变化的微观示意图,分别表示氧原子和氢原子。
①物质A是过氧化氢,A的化学式是_____。
②写出该反应的文字表达式_____,该反应属于基本反应类型中的_____反应,判断的依据是_____。
③A、B、C三种物质中属于单质的是(填字母,下同)_____,属于化合物的是_____。
④关于过氧化氢及其水溶液的部分描述如下:
a.过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶,c.过氧化氢的水溶液俗称双氧水,d.双氧水常用于伤口消毒、环境消毒和食品消毒,e.常温下,能缓慢分解成水和氧气。
上述描述中,属于过氧化氢或双氧水物理性质的有(填序号,下同)_____;属于化学性质的有_____;属于用途的有_____。从元素组成的角度看,过氧化氢和水的相同点是_____。二者性质有根大的差异,从微观角度看,原因是_____。
19.水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识回答下列问题:
(1)某同学制作了图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是___________、活性炭的作用是____________
(2)硬水会给生活、生产带来许多不便。
①检验河水是硬水的方法与现象为:__________________________________________该方法为物理方法还是化学方法?_____________________
②生活中通过煮沸的方法来降低水的硬度,煮沸时发生的反应有:碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,反应的文字表达式是___________________。由此反应体现出来碳酸氢钙的化学性质?__________________
(3)图2是水发生两种交化的微观图示。
①甲、乙两种变化中属于物理变化的是(填“甲”或“乙”)_____,从微观角度判断该变化是物理变化的依据是___________________________。在这个变化过程中,水分子(填“吸收”或“释放”)_____能量。
②图2中的化学变化是在通电的条件下发生的,该反应的文字表达式是______________,从微观角度判断该变化是化学变化的依据是_______________________。反应中的能量转化形式是_____能转化为_____能。
③小张从图2中化学变化的微观图示中获得以下信息,其中正确的有________。
A 保持水的化学性质的最小粒子是水分子
B 化学反应前后分子的个数不变
C 该变化中的最小粒子是氢原子和氧原子
D 该变化中元素的种类不变
(4)图3为某化学变化的微观示意图,分别表示氧原子和氢原子。
①物质A是过氧化氢,A的化学式是_________。
②A、B、C三种物质中属于单质的是(填字母,下同)_____,属于化合物的是_____。
③关于过氧化氢及其水溶液的部分描述如下:
a 过氧化氢是淡蓝色的黏稠液体,b 易溶于水,能与水以任意比例互溶,c 过氧化氢的水溶液俗称双氧水,d 双氧水常用于伤口消毒、环境消毒和食品消毒,e 常温下,能缓慢分解成水和氧气。
上述描述中,属于过氧化氢或双氧水物理性质的有(填序号,下同)_____________;属于化学性质的有_________;属于用途的有_________。从元素组成的角度看,过氧化氢和水的相同点是_____________。二者性质有很大的差异,从微观角度看,原因是_______________________。
20.根据所学知识回答问题:
(1)小明自制了如图所示的实验装置,对水通电进行实验探究。
①与A量筒中的电极相连接的是电池的___________极,A量筒中产生的气体是___________,检验此气体的方法是______________________。说明此气体的化学性质是___________,该反应的文字表达式是___________,反应类型是___________。该检验过程中能量是如何转化的?___________。
②若在正极上产生了20mL的气体,则在负极上约产生___________mL气体。
③写出水电解反应的文字表达式:___________,反应的基本类型是___________。
(2)水的微观结构:构成水的粒子可表示为___________(填字母代号,下同),该变化中,最小的微粒符号为___________ ,保持氢气化学性质的最小微粒可表示为___________。上述实验证明化学反应的实质是:___________。
(3)水的性质:
①人体发热时,常用冰块来降温,这是利用了水的___________(填“物理”或“化学”)性质。
②常温下,水能与氧化钠反应生成氢氧化钠。请写出其文字表达式及反应类型是___________,___________。
(4)水的净化。兴趣小组的同学取学校附近河水样品,利用下图所示的实验过程对该水样进行了净化处理。请回答下列问题:
①加入的物质A是___________,其作用是___________,为除去水样2中的一些异味和色素,加入的物质B是___________,其作用是___________。
②取少量水样3于试管中,加入少量肥皂水并振荡,发现___________,说明水样3是硬水,其中含较多的___________。生活中,可通过___________的方法,将其转化为软水。
③操作②是采用紫外线灯照射,发生___________变化。水样4因为含有___________,所以不是纯水,但可通过___________的方法获得纯水。
21.学科思想在化学素养发展中起着重要的作用。水是生命之源,人类的日常生活与工农业生产都离不开水。
Ⅰ.认识水。
(1)我国生活饮用水水质标准规定“铜<1.0mg/L,铁<0.3mg/L”,其中的铜、铁是指_______(选填“元素”或“单质”)。
(2)如图是电解水实验装置,b连接电源的_______极(选填“正”或“负”)。
(3)下图为水变化的微观示意图,图中“、”分别代表氧原子和氢原子,请依据图示回答以下问题:
①保持物质A化学性质的微粒是_______(填化学符号)。
②变化1中的“一定条件”可能是_______(写出一项即可)。
③变化2的符号表达式为_______,反应中不变的微粒是_______(填化学符号)。
Ⅱ.利用水。
化学兴趣小组收集了一瓶浑浊的长江水,模拟自来水厂进行水的净化过程。其实验过程如下所示,请回答以下问题。
(4)操作1的名称是_______。
(5)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是_______。
(6)操作3是消毒杀菌。二氧化氯(ClO2)是常用的净水消毒剂之一、已知:可用氯酸钾和草酸在一定条件下反应可生成二氧化氯、碳酸钾和其他物质。其中碳酸钾中碳酸根离子的化学符号为_______。
(7)为了判断净化水是硬水或软水,可加入_______,日常生活中常将水加热煮沸除了杀菌消毒之外,还起到的作用是_______。
参考答案
1.A
【详解】
原子一般是由质子、中子、电子构成的,其中中子不带电,一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,已知该元素的一个原子中14个微粒不带电,也就是说有14个中子,质子数有27﹣14=13,故质子数为13,故选A。
2.B
【详解】
A、氨气是由氨分子构成的一种化合物,选项错误;
B、氦气是由氦原子直接构成的一种单质,选项正确;
C、硫酸铜是由铜离子与硫酸根离子构成的一种盐,选项错误;
D、C60是由C60分子构成的一种单质,选项错误,故选B。
3.C
【详解】
元素的化学性质与其原子的核外电子排布,特别是最外层电子的个数关系最为密切,所以元素的化学性质主要决定于原子的最外层电子数;
故选C。
4.B
【详解】
①原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,故错误;
②原子核带正电,所带的正电荷数(即核电荷数,也就是质子数)与核外的电子数相等,所带电性相反,电量相等,相互抵消,所以原子不显电性,故正确;
③原子能再分为原子核和核外电子,故错误;
④由元素的定义可知决定元素种类的是核电荷数或核内质子数,故正确;
⑤原子可以构成分子,也可直接构成物质(例如金属、稀有气体等由原子直接构成),故正确;
所以②④⑤正确。
5.B
【详解】
A、金属于金属单质,是由金原子直接构成的;硅属于固态非金属单质,是由硅原子直接构成的,故选项错误;
B、水是由非金属元素组成的化合物,是由水分子构成的;氨气是由氨分子构成的,故选项正确;
C、汞属于金属单质,是由汞原子直接构成的;氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,故选项错误;
D、干冰是固态的二氧化碳,二氧化碳是由非金属元素组成的化合物,是由二氧化碳分子构成的;硫酸铜是由铜离子和硫酸根离子构成的,故选项错误。
故选B。
6.C
【详解】
A、氧气由氧分子构成,不符合题意;
B、石墨由碳原子构成,不符合题意;
C、烧碱是氢氧化钠的俗称,氢氧化钠由钠离子和氢氧根离子构成,符合题意;
D、氧化汞由氧化汞分子构成,不符合题意。
故选C。
7.D
【详解】
A、湿衣服晾干是水分子运动的结果,正确;B、在化学变化中,原子的种类不变,原子是化学变化中的最小粒子,正确;C、气体可压缩是因为分子间有间隔,正确;D、原子是化学变化中的最小粒子,在化学变化中不能再分,错误。故选D。
8.D
【详解】
水由水分子构成,所以水的化学性质由水分子保持;根据水的化学式H2O,可知水分子由两个氢原子和一个氧原子构成,故D图示的微粒能保持水的化学性质。
故选D
9.C
【详解】
在原子中,质子数=核外电子数=6。
故选C。
10.D
【详解】
氮气的相对分子质量为:14×2=28;
氧气的相对分子质量为:16×2=32;
一氧化碳的相对分子质量为:12+16=28;
二氧化硫的相对分子质量为:32+16×2=64。
质量相等的氮气、氧气、一氧化碳与二氧化硫中,分子的相对分子质量与分子数目成反比,所以二氧化硫所含分子数最少,故选D。
11.C
【详解】
由原子结构示意图可判断:
A、它的核电荷数为28,故A说法正确;
B、该原子的电子层数为4,故B说法正确;
C、它的质子数等核外电子数,故C说法错误;
D、该原子的最外层电子数是2,小于4,它易失去2个电子,故D说法正确。
故选:C。
12.C
【详解】
原子中质子数=核外电子数,氡原子的核外电子数为86,则氡原子的质子数为86,相对原子质量≈质子数+中子数,故该氡原子中子数为:222-86=136,故选C。
13.D
【详解】
A、氩气是由氩原子构成的,水是由水分子构成的,不符合题意;
B、金是由金原子构成,金刚石是由碳原子直接构成,不符合题意;
C、铜是由铜原子构成的,氯化钠是由钠离子和氯离子构成的,不符合题意;
D、氢气是由氢气分子构成的,水是由水分子构成的,符合题意。
故选D。
14.B
【详解】
A、铀带“钅”字旁,属于金属元素,故选项说法错误.
B、由题意,铀235原子核内有92个质子,由原子中:核电荷数=核内质子数=核外电子数,则该原子的核电荷数为92,故选项说法正确.
C、由题意,铀235原子核内有92个质子,相对原子质量为235,该原子核内有235﹣92=143个中子,故选项说法错误.
D、由题意,铀235原子核内有92个质子,由原子中:核电荷数=核内质子数=核外电子数,该原子核外有92个电子,故选项说法错误.
故选B.
15.B
【详解】
A、C60是由C60分子构成的,故选项错误。
B、金刚石属于固态非金属单质,是由碳原子直接构成的,故选项正确。
C、氮气属于气态非金属单质,是由氮分子直接构成的,故选项错误。
D、氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,故选项错误。
故选:B。
16.D
【详解】
A.分子是保持物质的化学性质的最小粒子,A正确。D.液态水变成水蒸气的过程中水分子之间的距离变大了,水分子大小不变。
17.(1)
【分析】
(1)
图1中,粒子C、D中,质子数等于核外电子数,属于原子是CD;A、B、D粒子的最外层电子数均为8,是具有相对稳定结构的粒子;质子数决定元素的种类,由粒子的结构示意图可知,A、C的质子数相同,属于同种元素的粒子,故填:CD;ABD;AC;质子数相同。
(2)
氯化钠是由钠离子与氯离子构成的,所以图2中的①处所填内容是离子;氯化钠中钠元素的化合价为+1价,氯元素的化合价为-1价,其化学式为NaCl,故填:离子;NaCl。
(3)
原子中,质子数=核外电子数,由结构示意图可知,该原子核内的3个粒子有2个质子,1个中子,所以该原子的中子数是1,故填:1(或一或1个或一个)。
18.过滤 吸附 向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水 碳酸氢钙碳酸钙+水+二氧化碳 乙 分子种类没有改变 吸收 水氢气+氧气 分子种类发生了改变,生成了新的分子 电 化学 ACD H2O2 过氧化氢→水+氧气 分解 由一种物质生成两种新物质 C AB ab e d 组成元素相同 分子结构不同
【详解】
(1)图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是过滤,活性炭的主要作用是吸附,除去水中的色素和异味;故填:过滤;吸附;
(2)①用肥皂水可以鉴别硬水和软水,向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水;故填:向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水;
②碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,故填:碳酸氢钙碳酸钙+水+二氧化碳;
(3)①由图2甲可知,分子发生了变化,生成了新的分子,发生了化学变化,乙中分子种类没有改变,发生的属于物理变化;乙中水分子吸收能量,分子间隔变大;故填:乙;分子种类没有改变;吸收;
②图2中的甲是水在通电的条件下生成氢气和氧气,该变化中分子种类发生了改变,生成了新的分子,变化由电能转化为化学能;故填:水氢气+氧气;分子种类发生了改变,生成了新的分子;电;化学;
③A.保持水的化学性质的最小粒子是水分子,正确;
B.化学反应前后分子的个数改变,错误;
C.该变化中的最小粒子是氢原子和氧原子,正确;
D.该变化中元素的种类不变,正确。
故填:ACD;
(4)①由分子结构模型可知,一个过氧化氢分子是由2个氢原子和2个氧原子构成的,其化学式为H2O2;故填:H2O2;
②图示变化为:过氧化氢生成水和氧气,该反应是由一种物质生成两种新物质,属于分解反应;故填:过氧化氢→水+氧气;分解;由一种物质生成两种新物质;
③AB的分子是由不同种原子构成的,属于化合物;C的分子是由同种原子构成的,属于单质;故填:C;AB;
④不需要发生化学变化就能表现出来的性质属于物质的物理性质,如过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶;需要发生化学变化才能表现出来的性质属于物质的化学性质,如e。常温下,能缓慢分解成水和氧气;双氧水的用途有:d.双氧水常用于伤口消毒、环境消毒和食品消毒;从元素组成的角度看,过氧化氢和水的相同点是组成元素相同。二者性质有根大的差异,从微观角度看,原因是分子结构不同;故填:ab;e;d;组成元素相同;分子结构不同。
19.过滤 吸附 向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水 化学方法 碳酸氢钙碳酸钙+水+二氧化碳 不稳定性 乙 分子种类没有改变 吸收 水氢气+氧气 分子种类发生了改变,生成了新的分子 电 化学 ACD H2O2 C AB ab e d 组成元素相同 分子结构不同
【详解】
(1)图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是过滤,活性炭的主要作用是吸附,除去水中的色素和异味;
(2)①用肥皂水可以鉴别硬水和软水,向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水,水中的钙镁离子和肥皂水生成新物质,属于化学变化;
②碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,碳酸氢钙碳酸钙+水+二氧化碳;此反应体现出来碳酸氢钙的化学性质是不稳定性;
(3)①由图2甲可知,分子发生了变化,生成了新的分子,发生了化学变化,乙中分子种类没有改变,发生的属于物理变化;乙中水分子吸收能量,分子间隔变大;
②图2中的甲是水在通电的条件下生成氢气和氧气,水氢气+氧气;该变化中分子种类发生了改变,生成了新的分子,变化由电能转化为化学能;
③A.保持水的化学性质的最小粒子是水分子,正确;
B.由图示可知,化学反应前后分子的个数改变,错误;
C.该变化中的最小粒子是氢原子和氧原子,正确;
D.该变化中元素的种类不变,正确;
故选ACD;
(4)①由分子结构模型可知,一个过氧化氢分子是由2个氢原子和2个氧原子构成的,其化学式为H2O2;
②图示变化为:过氧化氢生成水和氧气;AB的分子是由不同种原子构成的,属于化合物;C的分子是由同种原子构成的,属于单质;
③不需要发生化学变化就能表现出来的性质属于物质的物理性质,如a过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶;需要发生化学变化才能表现出来的性质属于物质的化学性质,如e常温下,能缓慢分解成水和氧气;双氧水的用途有:d.双氧水常用于伤口消毒、环境消毒和食品消毒;从元素组成的角度看,过氧化氢和水的相同点是都是由氢氧元素组成。二者性质有根大的差异,从微观角度看,原因是分子结构不同。
20.
(1) 负 氢气2 用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气 可燃性 氢气+氧气水 化合反应 化学能 光能和热能 40mL 水氢气+氧气 分解反应
(2) C EF B 在化学变化中,分子分为原子,原子重新组合为新的分子
(3) 物理 水+氧化钠 氢氧化钠 化合反应
(4) 明矾 加速悬浮杂质的沉降 活性炭 吸附水中的色素和异味 浮渣多、泡沫少 可溶性钙、镁化合物 加热煮沸 化学 可溶性杂质 蒸馏
【分析】
(1)
①在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,A量筒中产生的气体较多,是氢气,与电池的负极相连;
氢气具有可燃性,检验氢气的方法是:用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气;说明氢气具有可燃性;
氢气燃烧生成水,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
该检验过程中,氢气燃烧生成水,化学能转化为热能和光能;
②在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,若在正极上产生了20mL的气体,则在负极上约产生40mL气体;
③水在通电的条件下反应生成氢气和氧气,该反应的文字表达式为:;
该反应符合“一变多”的特点,属于分解反应;
(2)
水由水分子构成,每个水分子由2个氢原子和1个氧原子构成,故表示为C;
原子是化学变化中的最小粒子,该变化中,最小的微粒符号为氢原子和氧原子,故填:EF;
氢气由氢分子构成,保持氢气化学性质的最小微粒为氢分子,每个氢分子由2个氢原子构成,表示为:B;
该实验证明化学反应的实质是:在化学变化中,分子分为原子,原子重新组合为新的分子;
(3)
①人体发热时,常用冰块来降温,是因为冰融化吸热,不需要通过化学变化就能表现出来,这是利用了水的物理性质;
②常温下,水能与氧化钠反应生成氢氧化钠,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
(4)
①加入的物质A是明矾,明矾溶于水形成的胶状物具有吸附性,可以吸附水中悬浮的杂质。加速其沉降;
为除去水样2中的一些异味和色素,加入的物质B是活性炭,活性炭具有吸附性,可以吸附水中的色素和异味;
②通常用肥皂水来区分硬水和软水,肥皂水在硬水中易起浮渣,在软水中泡沫较多,故取少量水样3于试管中,加入少量肥皂水并振荡,发现浮渣多、泡沫少,说明水样3是硬水,其中含较多的可溶性钙、镁化合物;
可溶性钙、镁化合物在加热时,能形成沉淀,故生活中,可通过煮沸的方法将其转化为软水;
③操作②是采用紫外线灯照射,发生了蛋白质变性,有新物质生成,属于化学变化;
水样4中因为含有可溶性杂质,不是纯水,属于混合物,可通过蒸馏的方法获得纯水,蒸馏可除去所有杂质。
22.(1)元素(2)负(3) H2O 加热(升温等) H和O (4)过滤
(5)活性炭(6)(7) 肥皂水 将硬水软化(降低水的硬度等)
【分析】
(1)我国生活饮用水水质标准规定“铜<1.0mg/L,铁<0.3mg/L”,其中的铜、铁是指元素;
(2)如图是电解水实验装置,氢负氧正,且生成氢气和氧气的体积比为2:1;b连接电源的负极;
(3)①保持物质A化学性质的微粒是水分子,符号为H2O;
②变化1中的“一定条件”可能是加热(升温等);
③观察反应的微观示意图,可知反应物是水,生成物是氢气和氧气,该反应的符号表达式为:,反应中不变的微粒是氢原子和氧原子,其符号为:H和O;
(4)过滤可将难溶性固体和液体分离,操作1的名称是过滤;
(5)操作2是吸附,活性炭具有吸附性,可以吸附异味和色素;
(6)碳酸钾中碳酸根离子的化学符号为CO32-;
(7)为了鉴别软水和硬水,可加入肥皂水,产生较多浮渣的是硬水,较少浮渣的水软水,将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,煮沸可将可溶性钙镁化合物转化沉沉淀面降低水的硬度,还起到的作用是软化硬水。
一、选择题(共16题)
1.法国化学家德维尔在实验室中意外地发现一种新原子。已知该原子的原子核中含有27个微粒,其中14个微粒不带电,则该原子的质子数为( )
A.13 B.14 C.26 D.40
2.下列物质由原子构成的是
A.氨气 B.氦气 C.硫酸铜 D.C60
3.元素的化学性质主要决定于原子的
A.核外电子数 B.核电荷数 C.最外层电子数 D.中子数
4.下列叙述正确的是①原子由质子和中子构成 ②原子不显电性 ③原子不能再分 ④原子的质子数决定元素种类 ⑤原子可以构成分子,也可直接构成物质( )
A.①②④ B.②④⑤ C.③④ D.①②③⑤
5.下列各组物质中,都由分子构成的一组是( )
A.金和硅 B.水和氨气 C.汞和氯化钠 D.干冰和硫酸铜
6.下列物质中,由离子构成的是
A.氧气 B.石墨 C.烧碱 D.氧化汞
7.下列关于分子、原子的说法中,错误的是
A.湿衣服晾干是水分子运动的结果 B.化学变化中原子的种类不变
C.气体可压缩是因为分子间有间隔 D.原子是不可再分的最小粒子
8.下列图示中(“”表示氢原子,“”表示氧原子),能表示保持水的化学性质的粒子的是
A. B. C. D.
9.某种碳原子可用于检测人体中的幽门螺旋杆菌,该原子的原子核内含有6个质子和8个中子,则该原子的核外电子数为
A.14 B.8 C.6 D.2
10.质量相等的氮气、氧气、一氧化碳与二氧化硫中,分子数最少的是( )
A.氮气 B.氧气 C.一氧化碳 D.二氧化硫
11.如图为镍的原子结构示意图,关于该原子的叙述错误的是
A.核电荷数为28
B.核外有4个电子层
C.质子数大于核外电子数
D.易失去2个电子
12.家庭装修材料中的有害物质会影响人体的健康。如某些花岗岩石材中就含有放射性元素氡。若一种氡原子的核外电子数为86,相对原子质量为222,这种氡原子中子数为( )
A.50 B.86 C.136 D.222
13.下列各组物质中,都由分子构成的一组是
A.氩气和水 B.金和金刚石 C.铜和氯化钠 D.氢气和水
14.铀235(其原子核内有92个质子,相对原子质量为235)是核电站的主要燃料。下列有关说法正确的是
A.铀属于非金属元素 B.该原子的核电荷数为92
C.该原子核内有51个中子 D.该原子核外有143个电子
15.下列物质中,由原子直接构成的是
A.C60 B.金刚石 C.氮气 D.氯化钠
16.下列叙述中错误的是
A.水分子是保持水的化学性质的最小粒子
B.水是由氢元素和氧元素组成的氧化物
C.电解水生成氢气和氧气的体积比为2:1
D.液态水变成水蒸气的过程中水分子变大了
二、综合题(共5题)
17.“宏观一微观一符号”是化学视角认识物质的方法。根据下列图示回答问题:
(1)图1中,属于原子的是_______(填字母,下同);稳定结构的粒子是___________;属于同种元素的是__________,理由是_________。
(2)图2中的①处所填内容是________,氯化钠的符号_________。
(3)图3是某原子的结构模型,该原子的中子数是________。
18.水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识回答下列问题:
(1)为除去水中的不溶性杂质,某同学制作了图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是_____,活性炭的主要作用是_____。
(2)硬水会给生活、生产带来许多不便。
①检验河水是硬水的方法与现象为:_____。
②生活中可以通过煮沸的方法来降低水的硬度,煮沸时发生的反应之一是:碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,该反应的文字表达式是_____。
(3)图2是水发生两种交化的微观图示。
①甲、乙两种变化中属于物理变化的是(填“甲”或“乙”)_____,从微观角度判断该变化是物理变化的依据是_____。在这个变化过程中,水分子(填“吸收”或“释放”)_____能量。
②图2中的化学变化是在通电的条件下发生的,该反应的文字表达式是_____,从微观角度判断该变化是化学变化的依据是_____。反应中的能量转化形式是_____能转化为_____能。
③小张从图2中化学变化的微观图示中获得以下信息,其中正确的有_____。
A 保持水的化学性质的最小粒子是水分子
B 化学反应前后分子的个数不变
C 该变化中的最小粒子是氢原子和氧原子
D 该变化中元素的种类不变
(4)图3为某化学变化的微观示意图,分别表示氧原子和氢原子。
①物质A是过氧化氢,A的化学式是_____。
②写出该反应的文字表达式_____,该反应属于基本反应类型中的_____反应,判断的依据是_____。
③A、B、C三种物质中属于单质的是(填字母,下同)_____,属于化合物的是_____。
④关于过氧化氢及其水溶液的部分描述如下:
a.过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶,c.过氧化氢的水溶液俗称双氧水,d.双氧水常用于伤口消毒、环境消毒和食品消毒,e.常温下,能缓慢分解成水和氧气。
上述描述中,属于过氧化氢或双氧水物理性质的有(填序号,下同)_____;属于化学性质的有_____;属于用途的有_____。从元素组成的角度看,过氧化氢和水的相同点是_____。二者性质有根大的差异,从微观角度看,原因是_____。
19.水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识回答下列问题:
(1)某同学制作了图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是___________、活性炭的作用是____________
(2)硬水会给生活、生产带来许多不便。
①检验河水是硬水的方法与现象为:__________________________________________该方法为物理方法还是化学方法?_____________________
②生活中通过煮沸的方法来降低水的硬度,煮沸时发生的反应有:碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,反应的文字表达式是___________________。由此反应体现出来碳酸氢钙的化学性质?__________________
(3)图2是水发生两种交化的微观图示。
①甲、乙两种变化中属于物理变化的是(填“甲”或“乙”)_____,从微观角度判断该变化是物理变化的依据是___________________________。在这个变化过程中,水分子(填“吸收”或“释放”)_____能量。
②图2中的化学变化是在通电的条件下发生的,该反应的文字表达式是______________,从微观角度判断该变化是化学变化的依据是_______________________。反应中的能量转化形式是_____能转化为_____能。
③小张从图2中化学变化的微观图示中获得以下信息,其中正确的有________。
A 保持水的化学性质的最小粒子是水分子
B 化学反应前后分子的个数不变
C 该变化中的最小粒子是氢原子和氧原子
D 该变化中元素的种类不变
(4)图3为某化学变化的微观示意图,分别表示氧原子和氢原子。
①物质A是过氧化氢,A的化学式是_________。
②A、B、C三种物质中属于单质的是(填字母,下同)_____,属于化合物的是_____。
③关于过氧化氢及其水溶液的部分描述如下:
a 过氧化氢是淡蓝色的黏稠液体,b 易溶于水,能与水以任意比例互溶,c 过氧化氢的水溶液俗称双氧水,d 双氧水常用于伤口消毒、环境消毒和食品消毒,e 常温下,能缓慢分解成水和氧气。
上述描述中,属于过氧化氢或双氧水物理性质的有(填序号,下同)_____________;属于化学性质的有_________;属于用途的有_________。从元素组成的角度看,过氧化氢和水的相同点是_____________。二者性质有很大的差异,从微观角度看,原因是_______________________。
20.根据所学知识回答问题:
(1)小明自制了如图所示的实验装置,对水通电进行实验探究。
①与A量筒中的电极相连接的是电池的___________极,A量筒中产生的气体是___________,检验此气体的方法是______________________。说明此气体的化学性质是___________,该反应的文字表达式是___________,反应类型是___________。该检验过程中能量是如何转化的?___________。
②若在正极上产生了20mL的气体,则在负极上约产生___________mL气体。
③写出水电解反应的文字表达式:___________,反应的基本类型是___________。
(2)水的微观结构:构成水的粒子可表示为___________(填字母代号,下同),该变化中,最小的微粒符号为___________ ,保持氢气化学性质的最小微粒可表示为___________。上述实验证明化学反应的实质是:___________。
(3)水的性质:
①人体发热时,常用冰块来降温,这是利用了水的___________(填“物理”或“化学”)性质。
②常温下,水能与氧化钠反应生成氢氧化钠。请写出其文字表达式及反应类型是___________,___________。
(4)水的净化。兴趣小组的同学取学校附近河水样品,利用下图所示的实验过程对该水样进行了净化处理。请回答下列问题:
①加入的物质A是___________,其作用是___________,为除去水样2中的一些异味和色素,加入的物质B是___________,其作用是___________。
②取少量水样3于试管中,加入少量肥皂水并振荡,发现___________,说明水样3是硬水,其中含较多的___________。生活中,可通过___________的方法,将其转化为软水。
③操作②是采用紫外线灯照射,发生___________变化。水样4因为含有___________,所以不是纯水,但可通过___________的方法获得纯水。
21.学科思想在化学素养发展中起着重要的作用。水是生命之源,人类的日常生活与工农业生产都离不开水。
Ⅰ.认识水。
(1)我国生活饮用水水质标准规定“铜<1.0mg/L,铁<0.3mg/L”,其中的铜、铁是指_______(选填“元素”或“单质”)。
(2)如图是电解水实验装置,b连接电源的_______极(选填“正”或“负”)。
(3)下图为水变化的微观示意图,图中“、”分别代表氧原子和氢原子,请依据图示回答以下问题:
①保持物质A化学性质的微粒是_______(填化学符号)。
②变化1中的“一定条件”可能是_______(写出一项即可)。
③变化2的符号表达式为_______,反应中不变的微粒是_______(填化学符号)。
Ⅱ.利用水。
化学兴趣小组收集了一瓶浑浊的长江水,模拟自来水厂进行水的净化过程。其实验过程如下所示,请回答以下问题。
(4)操作1的名称是_______。
(5)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是_______。
(6)操作3是消毒杀菌。二氧化氯(ClO2)是常用的净水消毒剂之一、已知:可用氯酸钾和草酸在一定条件下反应可生成二氧化氯、碳酸钾和其他物质。其中碳酸钾中碳酸根离子的化学符号为_______。
(7)为了判断净化水是硬水或软水,可加入_______,日常生活中常将水加热煮沸除了杀菌消毒之外,还起到的作用是_______。
参考答案
1.A
【详解】
原子一般是由质子、中子、电子构成的,其中中子不带电,一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,已知该元素的一个原子中14个微粒不带电,也就是说有14个中子,质子数有27﹣14=13,故质子数为13,故选A。
2.B
【详解】
A、氨气是由氨分子构成的一种化合物,选项错误;
B、氦气是由氦原子直接构成的一种单质,选项正确;
C、硫酸铜是由铜离子与硫酸根离子构成的一种盐,选项错误;
D、C60是由C60分子构成的一种单质,选项错误,故选B。
3.C
【详解】
元素的化学性质与其原子的核外电子排布,特别是最外层电子的个数关系最为密切,所以元素的化学性质主要决定于原子的最外层电子数;
故选C。
4.B
【详解】
①原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,故错误;
②原子核带正电,所带的正电荷数(即核电荷数,也就是质子数)与核外的电子数相等,所带电性相反,电量相等,相互抵消,所以原子不显电性,故正确;
③原子能再分为原子核和核外电子,故错误;
④由元素的定义可知决定元素种类的是核电荷数或核内质子数,故正确;
⑤原子可以构成分子,也可直接构成物质(例如金属、稀有气体等由原子直接构成),故正确;
所以②④⑤正确。
5.B
【详解】
A、金属于金属单质,是由金原子直接构成的;硅属于固态非金属单质,是由硅原子直接构成的,故选项错误;
B、水是由非金属元素组成的化合物,是由水分子构成的;氨气是由氨分子构成的,故选项正确;
C、汞属于金属单质,是由汞原子直接构成的;氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,故选项错误;
D、干冰是固态的二氧化碳,二氧化碳是由非金属元素组成的化合物,是由二氧化碳分子构成的;硫酸铜是由铜离子和硫酸根离子构成的,故选项错误。
故选B。
6.C
【详解】
A、氧气由氧分子构成,不符合题意;
B、石墨由碳原子构成,不符合题意;
C、烧碱是氢氧化钠的俗称,氢氧化钠由钠离子和氢氧根离子构成,符合题意;
D、氧化汞由氧化汞分子构成,不符合题意。
故选C。
7.D
【详解】
A、湿衣服晾干是水分子运动的结果,正确;B、在化学变化中,原子的种类不变,原子是化学变化中的最小粒子,正确;C、气体可压缩是因为分子间有间隔,正确;D、原子是化学变化中的最小粒子,在化学变化中不能再分,错误。故选D。
8.D
【详解】
水由水分子构成,所以水的化学性质由水分子保持;根据水的化学式H2O,可知水分子由两个氢原子和一个氧原子构成,故D图示的微粒能保持水的化学性质。
故选D
9.C
【详解】
在原子中,质子数=核外电子数=6。
故选C。
10.D
【详解】
氮气的相对分子质量为:14×2=28;
氧气的相对分子质量为:16×2=32;
一氧化碳的相对分子质量为:12+16=28;
二氧化硫的相对分子质量为:32+16×2=64。
质量相等的氮气、氧气、一氧化碳与二氧化硫中,分子的相对分子质量与分子数目成反比,所以二氧化硫所含分子数最少,故选D。
11.C
【详解】
由原子结构示意图可判断:
A、它的核电荷数为28,故A说法正确;
B、该原子的电子层数为4,故B说法正确;
C、它的质子数等核外电子数,故C说法错误;
D、该原子的最外层电子数是2,小于4,它易失去2个电子,故D说法正确。
故选:C。
12.C
【详解】
原子中质子数=核外电子数,氡原子的核外电子数为86,则氡原子的质子数为86,相对原子质量≈质子数+中子数,故该氡原子中子数为:222-86=136,故选C。
13.D
【详解】
A、氩气是由氩原子构成的,水是由水分子构成的,不符合题意;
B、金是由金原子构成,金刚石是由碳原子直接构成,不符合题意;
C、铜是由铜原子构成的,氯化钠是由钠离子和氯离子构成的,不符合题意;
D、氢气是由氢气分子构成的,水是由水分子构成的,符合题意。
故选D。
14.B
【详解】
A、铀带“钅”字旁,属于金属元素,故选项说法错误.
B、由题意,铀235原子核内有92个质子,由原子中:核电荷数=核内质子数=核外电子数,则该原子的核电荷数为92,故选项说法正确.
C、由题意,铀235原子核内有92个质子,相对原子质量为235,该原子核内有235﹣92=143个中子,故选项说法错误.
D、由题意,铀235原子核内有92个质子,由原子中:核电荷数=核内质子数=核外电子数,该原子核外有92个电子,故选项说法错误.
故选B.
15.B
【详解】
A、C60是由C60分子构成的,故选项错误。
B、金刚石属于固态非金属单质,是由碳原子直接构成的,故选项正确。
C、氮气属于气态非金属单质,是由氮分子直接构成的,故选项错误。
D、氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,故选项错误。
故选:B。
16.D
【详解】
A.分子是保持物质的化学性质的最小粒子,A正确。D.液态水变成水蒸气的过程中水分子之间的距离变大了,水分子大小不变。
17.(1)
【分析】
(1)
图1中,粒子C、D中,质子数等于核外电子数,属于原子是CD;A、B、D粒子的最外层电子数均为8,是具有相对稳定结构的粒子;质子数决定元素的种类,由粒子的结构示意图可知,A、C的质子数相同,属于同种元素的粒子,故填:CD;ABD;AC;质子数相同。
(2)
氯化钠是由钠离子与氯离子构成的,所以图2中的①处所填内容是离子;氯化钠中钠元素的化合价为+1价,氯元素的化合价为-1价,其化学式为NaCl,故填:离子;NaCl。
(3)
原子中,质子数=核外电子数,由结构示意图可知,该原子核内的3个粒子有2个质子,1个中子,所以该原子的中子数是1,故填:1(或一或1个或一个)。
18.过滤 吸附 向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水 碳酸氢钙碳酸钙+水+二氧化碳 乙 分子种类没有改变 吸收 水氢气+氧气 分子种类发生了改变,生成了新的分子 电 化学 ACD H2O2 过氧化氢→水+氧气 分解 由一种物质生成两种新物质 C AB ab e d 组成元素相同 分子结构不同
【详解】
(1)图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是过滤,活性炭的主要作用是吸附,除去水中的色素和异味;故填:过滤;吸附;
(2)①用肥皂水可以鉴别硬水和软水,向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水;故填:向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水;
②碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,故填:碳酸氢钙碳酸钙+水+二氧化碳;
(3)①由图2甲可知,分子发生了变化,生成了新的分子,发生了化学变化,乙中分子种类没有改变,发生的属于物理变化;乙中水分子吸收能量,分子间隔变大;故填:乙;分子种类没有改变;吸收;
②图2中的甲是水在通电的条件下生成氢气和氧气,该变化中分子种类发生了改变,生成了新的分子,变化由电能转化为化学能;故填:水氢气+氧气;分子种类发生了改变,生成了新的分子;电;化学;
③A.保持水的化学性质的最小粒子是水分子,正确;
B.化学反应前后分子的个数改变,错误;
C.该变化中的最小粒子是氢原子和氧原子,正确;
D.该变化中元素的种类不变,正确。
故填:ACD;
(4)①由分子结构模型可知,一个过氧化氢分子是由2个氢原子和2个氧原子构成的,其化学式为H2O2;故填:H2O2;
②图示变化为:过氧化氢生成水和氧气,该反应是由一种物质生成两种新物质,属于分解反应;故填:过氧化氢→水+氧气;分解;由一种物质生成两种新物质;
③AB的分子是由不同种原子构成的,属于化合物;C的分子是由同种原子构成的,属于单质;故填:C;AB;
④不需要发生化学变化就能表现出来的性质属于物质的物理性质,如过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶;需要发生化学变化才能表现出来的性质属于物质的化学性质,如e。常温下,能缓慢分解成水和氧气;双氧水的用途有:d.双氧水常用于伤口消毒、环境消毒和食品消毒;从元素组成的角度看,过氧化氢和水的相同点是组成元素相同。二者性质有根大的差异,从微观角度看,原因是分子结构不同;故填:ab;e;d;组成元素相同;分子结构不同。
19.过滤 吸附 向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水 化学方法 碳酸氢钙碳酸钙+水+二氧化碳 不稳定性 乙 分子种类没有改变 吸收 水氢气+氧气 分子种类发生了改变,生成了新的分子 电 化学 ACD H2O2 C AB ab e d 组成元素相同 分子结构不同
【详解】
(1)图1所示的简易净水器,其中小卵石、石英砂和膨松棉的作用是过滤,活性炭的主要作用是吸附,除去水中的色素和异味;
(2)①用肥皂水可以鉴别硬水和软水,向水样中加入肥皂水搅拌,产生泡沫多的是软水,泡沫少的是硬水,水中的钙镁离子和肥皂水生成新物质,属于化学变化;
②碳酸氢钙在加热条件下,发生分解反应,生成碳酸钙、水和二氧化碳,碳酸氢钙碳酸钙+水+二氧化碳;此反应体现出来碳酸氢钙的化学性质是不稳定性;
(3)①由图2甲可知,分子发生了变化,生成了新的分子,发生了化学变化,乙中分子种类没有改变,发生的属于物理变化;乙中水分子吸收能量,分子间隔变大;
②图2中的甲是水在通电的条件下生成氢气和氧气,水氢气+氧气;该变化中分子种类发生了改变,生成了新的分子,变化由电能转化为化学能;
③A.保持水的化学性质的最小粒子是水分子,正确;
B.由图示可知,化学反应前后分子的个数改变,错误;
C.该变化中的最小粒子是氢原子和氧原子,正确;
D.该变化中元素的种类不变,正确;
故选ACD;
(4)①由分子结构模型可知,一个过氧化氢分子是由2个氢原子和2个氧原子构成的,其化学式为H2O2;
②图示变化为:过氧化氢生成水和氧气;AB的分子是由不同种原子构成的,属于化合物;C的分子是由同种原子构成的,属于单质;
③不需要发生化学变化就能表现出来的性质属于物质的物理性质,如a过氧化氢是淡蓝色的黏稠液体,b.易溶于水,能与水以任意比例互溶;需要发生化学变化才能表现出来的性质属于物质的化学性质,如e常温下,能缓慢分解成水和氧气;双氧水的用途有:d.双氧水常用于伤口消毒、环境消毒和食品消毒;从元素组成的角度看,过氧化氢和水的相同点是都是由氢氧元素组成。二者性质有根大的差异,从微观角度看,原因是分子结构不同。
20.
(1) 负 氢气2 用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气 可燃性 氢气+氧气水 化合反应 化学能 光能和热能 40mL 水氢气+氧气 分解反应
(2) C EF B 在化学变化中,分子分为原子,原子重新组合为新的分子
(3) 物理 水+氧化钠 氢氧化钠 化合反应
(4) 明矾 加速悬浮杂质的沉降 活性炭 吸附水中的色素和异味 浮渣多、泡沫少 可溶性钙、镁化合物 加热煮沸 化学 可溶性杂质 蒸馏
【分析】
(1)
①在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,A量筒中产生的气体较多,是氢气,与电池的负极相连;
氢气具有可燃性,检验氢气的方法是:用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气;说明氢气具有可燃性;
氢气燃烧生成水,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
该检验过程中,氢气燃烧生成水,化学能转化为热能和光能;
②在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,若在正极上产生了20mL的气体,则在负极上约产生40mL气体;
③水在通电的条件下反应生成氢气和氧气,该反应的文字表达式为:;
该反应符合“一变多”的特点,属于分解反应;
(2)
水由水分子构成,每个水分子由2个氢原子和1个氧原子构成,故表示为C;
原子是化学变化中的最小粒子,该变化中,最小的微粒符号为氢原子和氧原子,故填:EF;
氢气由氢分子构成,保持氢气化学性质的最小微粒为氢分子,每个氢分子由2个氢原子构成,表示为:B;
该实验证明化学反应的实质是:在化学变化中,分子分为原子,原子重新组合为新的分子;
(3)
①人体发热时,常用冰块来降温,是因为冰融化吸热,不需要通过化学变化就能表现出来,这是利用了水的物理性质;
②常温下,水能与氧化钠反应生成氢氧化钠,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
(4)
①加入的物质A是明矾,明矾溶于水形成的胶状物具有吸附性,可以吸附水中悬浮的杂质。加速其沉降;
为除去水样2中的一些异味和色素,加入的物质B是活性炭,活性炭具有吸附性,可以吸附水中的色素和异味;
②通常用肥皂水来区分硬水和软水,肥皂水在硬水中易起浮渣,在软水中泡沫较多,故取少量水样3于试管中,加入少量肥皂水并振荡,发现浮渣多、泡沫少,说明水样3是硬水,其中含较多的可溶性钙、镁化合物;
可溶性钙、镁化合物在加热时,能形成沉淀,故生活中,可通过煮沸的方法将其转化为软水;
③操作②是采用紫外线灯照射,发生了蛋白质变性,有新物质生成,属于化学变化;
水样4中因为含有可溶性杂质,不是纯水,属于混合物,可通过蒸馏的方法获得纯水,蒸馏可除去所有杂质。
22.(1)元素(2)负(3) H2O 加热(升温等) H和O (4)过滤
(5)活性炭(6)(7) 肥皂水 将硬水软化(降低水的硬度等)
【分析】
(1)我国生活饮用水水质标准规定“铜<1.0mg/L,铁<0.3mg/L”,其中的铜、铁是指元素;
(2)如图是电解水实验装置,氢负氧正,且生成氢气和氧气的体积比为2:1;b连接电源的负极;
(3)①保持物质A化学性质的微粒是水分子,符号为H2O;
②变化1中的“一定条件”可能是加热(升温等);
③观察反应的微观示意图,可知反应物是水,生成物是氢气和氧气,该反应的符号表达式为:,反应中不变的微粒是氢原子和氧原子,其符号为:H和O;
(4)过滤可将难溶性固体和液体分离,操作1的名称是过滤;
(5)操作2是吸附,活性炭具有吸附性,可以吸附异味和色素;
(6)碳酸钾中碳酸根离子的化学符号为CO32-;
(7)为了鉴别软水和硬水,可加入肥皂水,产生较多浮渣的是硬水,较少浮渣的水软水,将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,煮沸可将可溶性钙镁化合物转化沉沉淀面降低水的硬度,还起到的作用是软化硬水。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
