第八单元课题3金属资源的利用和保护同步练习—2021-2022学年九年级化学人教版下册(无答案)
文档属性
| 名称 | 第八单元课题3金属资源的利用和保护同步练习—2021-2022学年九年级化学人教版下册(无答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 149.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-27 00:00:00 | ||
图片预览

文档简介
课题3金属资源的利用和保护
课时1铁的冶炼
一、选择题
1.下列有关金属的说法,正确的是( )
A.多数金属以单质的形式存在
B.在地壳中含量最高的金属元素是铁
C.常见的铁矿石有赤铁矿和磁铁矿
D.人类每年从自然界中提取量最大的金属是铝
2.用下列矿石冶炼金属时,排放的废气容易引起酸雨的是( )
A.赤铁矿(主要成分Fe2O3) B.磁铁矿(主要成分Fe3O4)
C.黄铁矿(主要成分FeS2) D.菱铁矿(主要成分FeCO3)
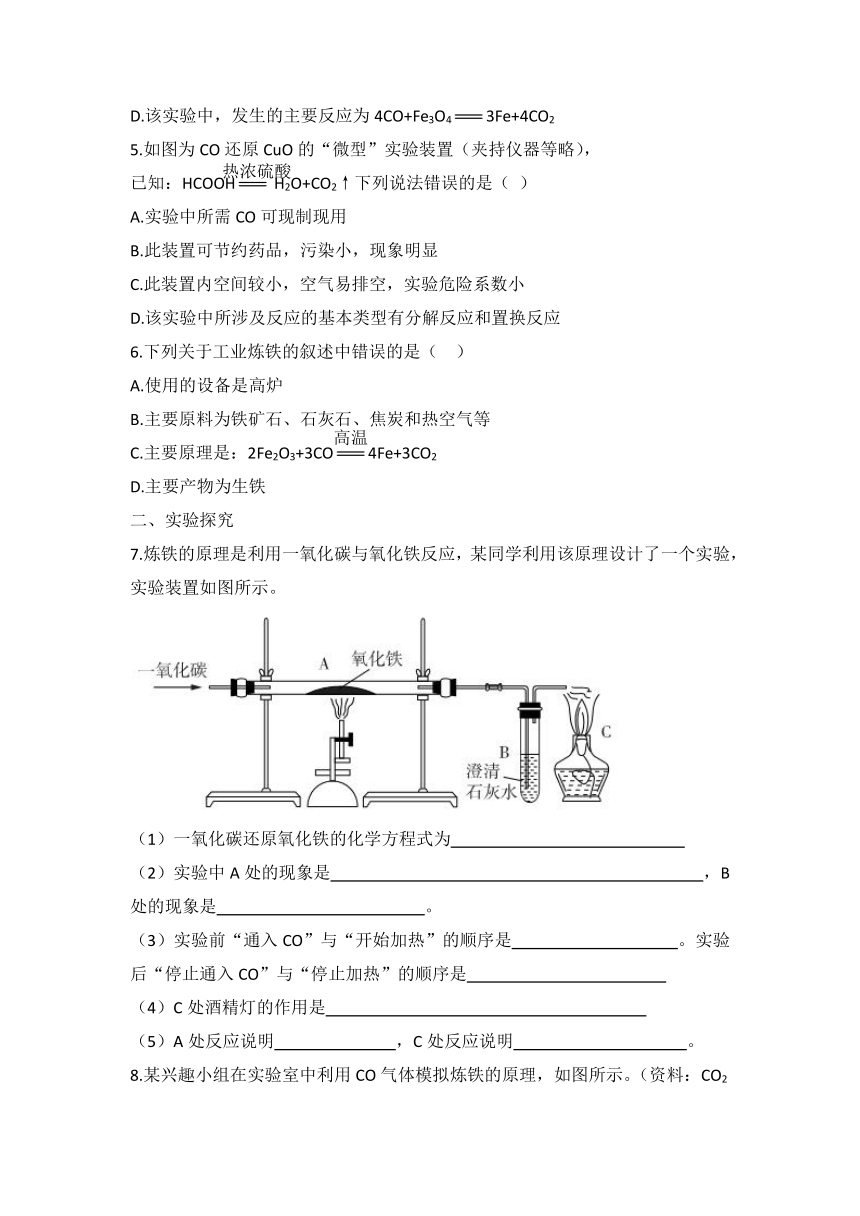
3.下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内CO和Fe2O3发生化学反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红棕色
D.该模拟实验缺少尾气处理装置,会污染空气
4.实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、铁等固体物质。关于该实验,下列说法正确的是( )
A.实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳
B.实验过程中,试管中澄清石灰水变浑浊,证明该反应有二氧化碳生成
(
高温
)C.实验结束后,玻璃管中红棕色的氧化铁粉末变成黑色,该产物一定是铁
D.该实验中,发生的主要反应为4CO+Fe3O4=3Fe+4CO2
(
热浓硫酸
)5.如图为CO还原CuO的“微型”实验装置(夹持仪器等略),
已知:HCOOH= H2O+CO2↑下列说法错误的是( )
A.实验中所需CO可现制现用
B.此装置可节约药品,污染小,现象明显
C.此装置内空间较小,空气易排空,实验危险系数小
D.该实验中所涉及反应的基本类型有分解反应和置换反应
6.下列关于工业炼铁的叙述中错误的是( )
A.使用的设备是高炉
(
高温
)B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是:2Fe2O3+3CO=4Fe+3CO2
D.主要产物为生铁
二、实验探究
7.炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置如图所示。
(1)一氧化碳还原氧化铁的化学方程式为
(2)实验中A处的现象是 ,B处的现象是 。
(3)实验前“通入CO”与“开始加热”的顺序是 。实验后“停止通入CO”与“停止加热”的顺序是
(4)C处酒精灯的作用是
(5)A处反应说明 ,C处反应说明 。
8.某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如图所示。(资料:CO2能与NaOH溶液反应)
(1)为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应
(2)装置A玻璃管中发生反应的化学方程式是
(3)装置B除了吸收CO2气体外,还有 。
三、综合应用
9.工业上炼铁炼钢的主要流程如下图。
(
高温
)已知生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(
高温
)(1)反应:①2Fe2O3+3CO=4Fe+3CO2
②2Fe2O3+3C=4Fe+3CO
。属于置换反应的是 ,用3C于高炉炼铁的原理是 。(均填序号)
(2)炼铁的固体原料需经过粉碎,其目的是
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是 。炉渣中含有硅酸钙(CaSiO4),其中硅元素的化合价是 。
(4)炼钢炉中,通入纯氧的目的是
10. 2019年1月3日嫦娥四号探测器成功着陆在月球背面,并通过“鹊桥”中继星传回了近距离拍摄的月背影像图,揭开了月背的神秘面纱。“鹊桥”号上伞状通信天线是用表面镀金的钼丝编织而成的金属网。这种镀金钼丝纤维只有头发丝四分之一细,其性能稳定。“编”出来的金属网既强韧,受得住发射飞行外力“折腾”,又能在太空中收放自如,可以说是“刚柔并济”。
(1)钼能制成细丝,是利用了钼的 。
(2)钼丝表面镀金,原因之一是利用了金的化学性质 。
(3)我国的钼矿储量非常丰富,用辉钼矿(MoS2)制备钼的过程如下:
①完成过程I中反应的化学方程式:2 MoS2+7O2=2MoO3+4
②过程Ⅱ分两个阶段:
第一阶段反应中反应物与生成物的化学计量数之比为1:1:1:1。
写出下列化学方程式:
第一阶段
第二阶段 ,该反应的基本反应类型为 反应。
11.如图所示的炼铁高炉内发生了许多化学反应,根据图示回答下列问题:
(1)将铁从铁矿石中还原出来铁矿石、焦炭、石灰石的物质是 (填化学高护气体,高如气体式);该物质在B区生成,写出相关反应的化学方程式:
。开始生成生铁。
(2)高炉炼铁时焦炭的作用
①
②
(3)为什么高炉中生铁出口低于炉渣出口?
答:
(4)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是 ,发生反应的化学方程式为 ,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质是 (填化学式)。
四、计算题
12. [2020四川凉山州中考]某炼钢厂每天需消耗5000t含Fe,0,76%的赤铁矿,该厂理论上可日产含Fe98%的生铁的质量是多少?(保留至小数点后一位)
(
通电
)13. 19世纪初,铝的发现得益于电解技术的应用。电解铝的反应为:
2Al2O3=4Al+3O2↑,现有含Al2O351%的铝土矿200t,经上述反应后可制得铝多少吨?(假设上述各步反应中铝元素一共损失10%,计算结果精确到小数点后一位)
课时1铁的冶炼
一、选择题
1.下列有关金属的说法,正确的是( )
A.多数金属以单质的形式存在
B.在地壳中含量最高的金属元素是铁
C.常见的铁矿石有赤铁矿和磁铁矿
D.人类每年从自然界中提取量最大的金属是铝
2.用下列矿石冶炼金属时,排放的废气容易引起酸雨的是( )
A.赤铁矿(主要成分Fe2O3) B.磁铁矿(主要成分Fe3O4)
C.黄铁矿(主要成分FeS2) D.菱铁矿(主要成分FeCO3)
3.下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内CO和Fe2O3发生化学反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红棕色
D.该模拟实验缺少尾气处理装置,会污染空气
4.实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、铁等固体物质。关于该实验,下列说法正确的是( )
A.实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳
B.实验过程中,试管中澄清石灰水变浑浊,证明该反应有二氧化碳生成
(
高温
)C.实验结束后,玻璃管中红棕色的氧化铁粉末变成黑色,该产物一定是铁
D.该实验中,发生的主要反应为4CO+Fe3O4=3Fe+4CO2
(
热浓硫酸
)5.如图为CO还原CuO的“微型”实验装置(夹持仪器等略),
已知:HCOOH= H2O+CO2↑下列说法错误的是( )
A.实验中所需CO可现制现用
B.此装置可节约药品,污染小,现象明显
C.此装置内空间较小,空气易排空,实验危险系数小
D.该实验中所涉及反应的基本类型有分解反应和置换反应
6.下列关于工业炼铁的叙述中错误的是( )
A.使用的设备是高炉
(
高温
)B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是:2Fe2O3+3CO=4Fe+3CO2
D.主要产物为生铁
二、实验探究
7.炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置如图所示。
(1)一氧化碳还原氧化铁的化学方程式为
(2)实验中A处的现象是 ,B处的现象是 。
(3)实验前“通入CO”与“开始加热”的顺序是 。实验后“停止通入CO”与“停止加热”的顺序是
(4)C处酒精灯的作用是
(5)A处反应说明 ,C处反应说明 。
8.某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如图所示。(资料:CO2能与NaOH溶液反应)
(1)为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应
(2)装置A玻璃管中发生反应的化学方程式是
(3)装置B除了吸收CO2气体外,还有 。
三、综合应用
9.工业上炼铁炼钢的主要流程如下图。
(
高温
)已知生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(
高温
)(1)反应:①2Fe2O3+3CO=4Fe+3CO2
②2Fe2O3+3C=4Fe+3CO
。属于置换反应的是 ,用3C于高炉炼铁的原理是 。(均填序号)
(2)炼铁的固体原料需经过粉碎,其目的是
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是 。炉渣中含有硅酸钙(CaSiO4),其中硅元素的化合价是 。
(4)炼钢炉中,通入纯氧的目的是
10. 2019年1月3日嫦娥四号探测器成功着陆在月球背面,并通过“鹊桥”中继星传回了近距离拍摄的月背影像图,揭开了月背的神秘面纱。“鹊桥”号上伞状通信天线是用表面镀金的钼丝编织而成的金属网。这种镀金钼丝纤维只有头发丝四分之一细,其性能稳定。“编”出来的金属网既强韧,受得住发射飞行外力“折腾”,又能在太空中收放自如,可以说是“刚柔并济”。
(1)钼能制成细丝,是利用了钼的 。
(2)钼丝表面镀金,原因之一是利用了金的化学性质 。
(3)我国的钼矿储量非常丰富,用辉钼矿(MoS2)制备钼的过程如下:
①完成过程I中反应的化学方程式:2 MoS2+7O2=2MoO3+4
②过程Ⅱ分两个阶段:
第一阶段反应中反应物与生成物的化学计量数之比为1:1:1:1。
写出下列化学方程式:
第一阶段
第二阶段 ,该反应的基本反应类型为 反应。
11.如图所示的炼铁高炉内发生了许多化学反应,根据图示回答下列问题:
(1)将铁从铁矿石中还原出来铁矿石、焦炭、石灰石的物质是 (填化学高护气体,高如气体式);该物质在B区生成,写出相关反应的化学方程式:
。开始生成生铁。
(2)高炉炼铁时焦炭的作用
①
②
(3)为什么高炉中生铁出口低于炉渣出口?
答:
(4)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是 ,发生反应的化学方程式为 ,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质是 (填化学式)。
四、计算题
12. [2020四川凉山州中考]某炼钢厂每天需消耗5000t含Fe,0,76%的赤铁矿,该厂理论上可日产含Fe98%的生铁的质量是多少?(保留至小数点后一位)
(
通电
)13. 19世纪初,铝的发现得益于电解技术的应用。电解铝的反应为:
2Al2O3=4Al+3O2↑,现有含Al2O351%的铝土矿200t,经上述反应后可制得铝多少吨?(假设上述各步反应中铝元素一共损失10%,计算结果精确到小数点后一位)
同课章节目录
