8.1金属材料同步练习-2021-2022学年九年级化学人教版下册(word版含解析)
文档属性
| 名称 | 8.1金属材料同步练习-2021-2022学年九年级化学人教版下册(word版含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 216.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-28 00:00:00 | ||
图片预览



文档简介
8.1、金属材料
一、选择题(共16题)
1.生活中的下列物品,其制作材料属于合金的是( )
A.金刚石钻头 B.钢化玻璃杯 C.不锈钢锅 D.瓷器
2.下列可回收的生活垃圾中,属于金属材料的是
A.铝制易拉罐 B.废旧塑料桶 C.旧报纸 D.玻璃瓶
3.物质的性质决定其用途,下列说法不正确的是
A.甲烷作燃料,是因为甲烷具有可燃性 B.铜作导线,是因为铜具有良好的导电性
C.洗洁精洗涤油污,是因为洗洁精能溶解油污 D.活性炭除冰箱异味,是因为活性炭具有吸附性
4.下列物品所使用的主要材料属于合金的是
A.青花瓷瓶 B.橡胶充气艇 C.青铜宝剑 D.金刚石
5.下列关于合金的说法不正确的是( )
A.不锈钢在一定的条件下也会生锈 B.合金的熔点一般低于各成分金属
C.合金一定是由多种金属熔合而成 D.控制条件可制成性能不同的合金
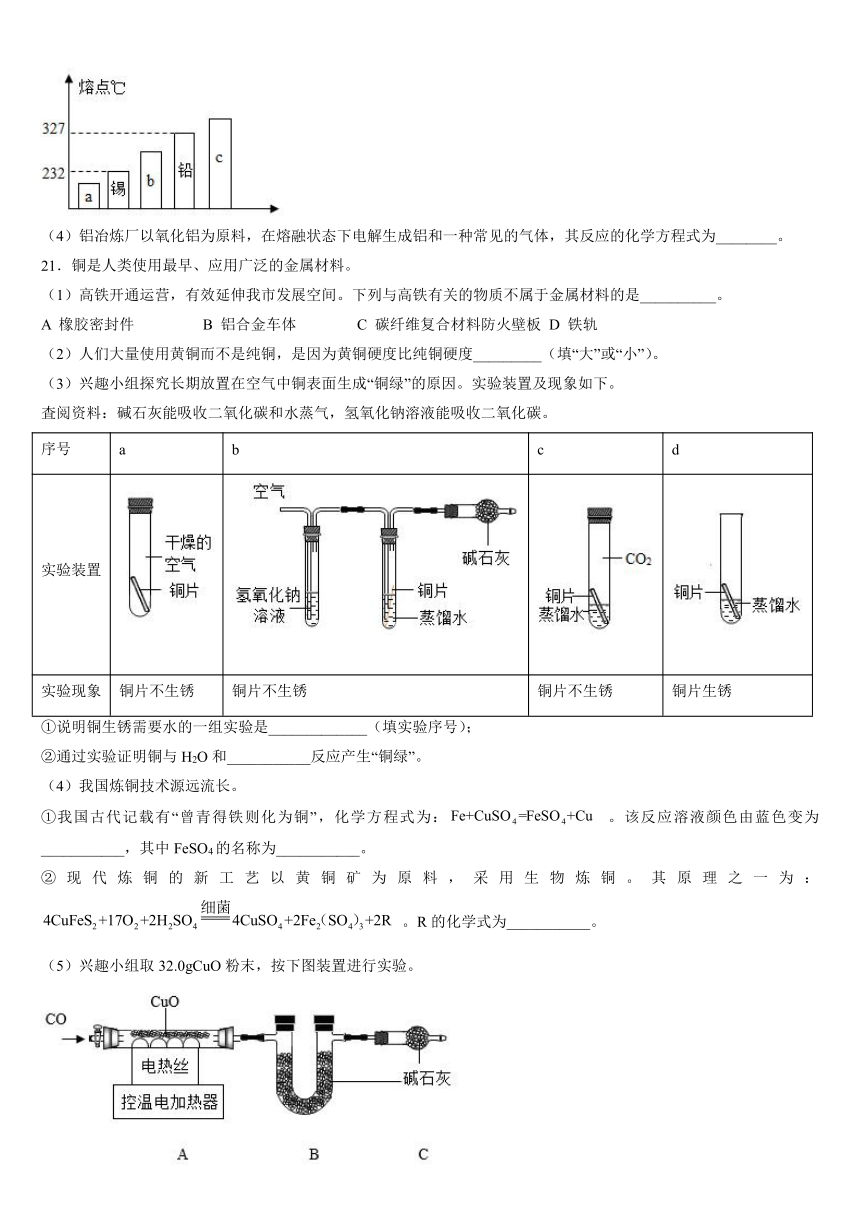
6.下图所示的实验不能达到实验目的的是( )
A.实验一:验证CO2的部分性质 B.实验二:验证空气中氧气含量
C.实验三:验证O2是否收集满 D.实验四:比较黄铜与纯铜的硬度
7.锡、铅的熔点分别是232℃和327℃。焊锡是锡铅合金,焊锡的熔点小于200℃,把铅加入锡中制成合金的主要目的是( )
A.增加强度 B.降低熔点 C.增加延展性 D.增加耐磨性
8.目前哈尔滨地铁工程已有一定的规模,待哈尔滨地铁网络全部建成以后,地铁将成为城市最主要的交通工具,下列有关认识不正确的是( )
A.地铁作为环保的交通工具,可以很大限度地实现节能减排
B.建地铁可节省人们的出行时间,有效缓解交通压力
C.生铁和钢是含碳量不同的两种铁合金
D.生铁的硬度比钢大,钢轨是用生铁铺设的
9.生活中的下列现象,属于化学变化的是( )
A.用石墨制金刚石 B.干冰升华 C.铁杵磨成针 D.铜和锌制成合金
10.铝、铜、锡、铁等金属本质上的共同点是
A.都具有银白色的金属光泽
B.熔点都很高
C.密度、硬度都很大
D.都具有良好的延展性、导电性、导热性
11.下列物质属于纯净物的是
A.雪碧饮料
B.生铁
C.二氧化碳
D.高锰酸钾加热制氧气后的剩余固体
12.关于合金的说法正确的是
A.合金是一种纯净物
B.合金中只含有金属元素
C.合金的强度、硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好
D.铁锈是一种合金
13.下列有关实验现象叙述错误的是
A.将二氧化碳通入燃着的两支高低不同蜡烛的烧杯中,蜡烛由低到高依次熄灭
B.铁丝在氧气中燃烧,火星四射,生成黑色固体
C.用黄铜片(铜锌合金)和铜片相互刻画,黄铜片上留有划痕
D.硫在空气中燃烧产生微弱的淡蓝色火焰,生成有刺激性气味的气体
14.氨基钠(NaNH2)是合成维生素A的原料.工业上将钠于97~100℃熔融,向反应容器中缓慢通入无水的液氨(NH3),再加热至350~360℃生成氨基钠和氢气.下列说法中,不正确的是( )
A.单质钠的化合价为0价 B.钠的熔点比铁的熔点低
C.维生素A是由Na、N、H元素组成的 D.该反应属于置换反应
15.下列实验方案,不能达到相应实验目的是( )
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.铝锂合金是航空飞行器较理想的结构材料之一。铝锂合金具有的以下性质中,与该应用无关的是( )
A.硬度大 B.耐腐蚀 C.密度小 D.易导电
二、非选择题(共8题)
17.近一年,丹东上线的公交汽车都由动力单一燃油改为电和气电能和燃气混合动力。
(1)这种做法的目的是______答一点。
(2)汽车尾部都有内置铜丝拖地的带子。这是利用铜能______这一性质。
(3)汽车尾气的主要成分是一氧化碳和一氧化氮。处理尾气的方法是在催化剂作用下可生成空气中最多的气体和一种氧化物。请写出该反应的化学方程式:______。
18.铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由______构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和______性。
(3)实验室:细铁丝在氧气中燃烧的现象是______,放热。该反应的化学方程式是______。在做这个实验是集气瓶的底部要留少量水,其目的是______。
19.青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。如图是一种照明用台灯。
(1)如图中标示的各部件中,用金属材料制成的是_____(填序号)。
(2)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的_____性。
(3)铜质插头是利用了金属铜的_____性。
20.人类的生产、生活离不开金属。
(1)家用热水瓶内胆壁的银白色金属是________(填符号,下同);液体金属是__________;地壳中含量最高的金属元素是_______,人体中含量最多的金属元素是________。
(2)镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是_____(任写一个化学方程式)。该合金属于______(填“混合物”或“纯净物”),它是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于________(填“物理”或“化学”)变化。
(3)合金的很多性能与组成它们的纯金属不同。如图能表示锡铅合金的是________(填序号“a”“b”或“c”)。
(4)铝冶炼厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为________。
21.铜是人类使用最早、应用广泛的金属材料。
(1)高铁开通运营,有效延伸我市发展空间。下列与高铁有关的物质不属于金属材料的是__________。
A 橡胶密封件 B 铝合金车体 C 碳纤维复合材料防火壁板 D 铁轨
(2)人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度_________(填“大”或“小”)。
(3)兴趣小组探究长期放置在空气中铜表面生成“铜绿”的原因。实验装置及现象如下。
査阅资料:碱石灰能吸收二氧化碳和水蒸气,氢氧化钠溶液能吸收二氧化碳。
序号 a b c d
实验装置
实验现象 铜片不生锈 铜片不生锈 铜片不生锈 铜片生锈
①说明铜生锈需要水的一组实验是_____________(填实验序号);
②通过实验证明铜与H2O和___________反应产生“铜绿”。
(4)我国炼铜技术源远流长。
①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为___________,其中FeSO4的名称为___________。
②现代炼铜的新工艺以黄铜矿为原料,采用生物炼铜。其原理之一为: 。R的化学式为___________。
(5)兴趣小组取32.0gCuO粉末,按下图装置进行实验。
①实验时,应先___________(填“加热样品”或“通一段时间CO”)。
②从环境保护角度,该装置缺少___________。
③若加热一段时间后,测得装置B增重11.0g,此时固体中铜元素与氧元素的质量比为___________,若缺少C装置测得数据将___________(填“偏大”、“偏小”或“不变”)。
④若32.0gCuO完全被还原成Cu,装置B增重多少克?(写计算过程)____
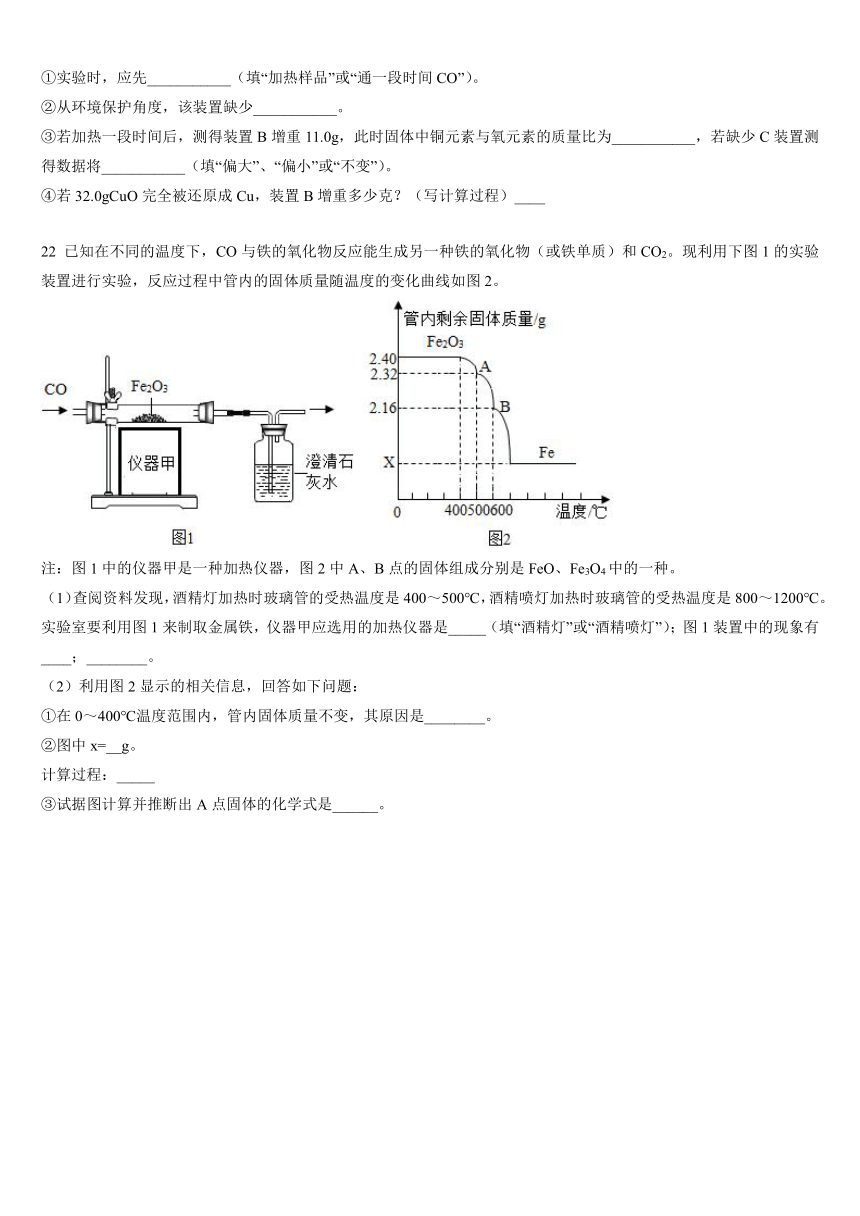
22 已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.C
【详解】
A、 金刚石钻头,是由碳元素组成的,不属于合金,故选项错误;B、玻璃杯是硅酸盐产品,不属于合金,故选项错误;C、不锈钢是钢的一种,是铁的合金,故选项正确;D、陶瓷是用泥土烧制而成的,属于无机非金属材料,不属于合金,故选项错误。故选C。
2.A
【解析】
金属材料包括纯金属以及它们的合金,故选A。
3.C
【详解】
A、甲烷具有可燃性,可用来作燃料,故选项说法正确;
B、因为铜具有较好的导电性,所以可作导线,故原选项说法正确;
C、洗洁精可去除油污,是因为它具有乳化作用,不能将油污溶解,故选项说法错误;
D、活性炭具有的吸附性是去除冰箱异味的主要原因,故原选项说法正确。
故选C。
4.C
【详解】
A、青花瓷瓶属于硅酸盐材料,即无机非金属材料,不符合题意。
B、橡胶充气艇属于有机高分子材料,不符合题意。
C、青铜宝剑是铜和锡的合金,符合题意。
D、金刚石是由碳元素组成的单质,不属于合金,不符合题意。
故选:C。
5.C
【详解】
A、不锈钢在一定的条件下也会生锈,故选项正确;
B、合金的熔点一般比各成分金属低,故选项正确;
C、合金不一定是金属和金属熔合而成,合金可以是金属与非金属熔合而成的物质,故选项错误;
D、控制条件可制成性能不同的合金,例如控制铁的合金中的含碳量,可以制得性能不同的生铁和钢,故选项正确。
故选C。
B 7.B 8.D
9.A
【详解】
A、用石墨制金刚石,产生了新的物质,属于化学变化;
B、干冰升华是固态二氧化碳变为气态二氧化碳,没有产生新的物质,不属于化学变化;
C、铁杵磨成针只是铁的形状改变了,没有产生新的物质,不属于化学变化;
D、铜和锌制成合金是铜和锌按照一定方法制成的,没有产生新的物质,不属于化学变化。
故选A。
10.D
【详解】
A.都具有银白色的金属光泽,不是金属的共性,如铜呈紫红色,故选项错误。
B.熔点都很高,不是金属的共性,如钠的熔点较低,故选项错误。
C.密度、硬度都很大不是金属的共性,如钠的密度和硬度较小,故选项错误。
D.金属都具有良好的延展性、导电性、导热性,属于金属共性,故选项正确。故选:D。
11.C
【详解】
A、雪碧饮料中含有水、碳酸等物质属于混合物,故选项不符合题意。
B、生铁中含有铁和碳等物质,因此属于混合物,故选项不符合题意。
C、二氧化碳是由二氧化碳一种物质组成,属于纯净物,故选项符合题意。
D、高锰酸钾加热制氧气后的剩余物是锰酸钾、二氧化锰,属于混合物,故选项不符合题意。
故选:C。
12.C
【详解】
A. 合金是由多种物质混合而成的,属于混合物,此选项错误;
B. 合金是金属与其它金属或非金属经高温熔合在一起的具有金属特性的物质,合金中可能含有非金属元素,此选项错误;
C. 金属制成合金后,性能发生了改变,合金的强度、硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好,此选项正确;
D. 铁锈不是合金,此选项错误。
故选C。
13.C 14.C
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.D
【分析】
合金的硬度大于其成分金属,熔点低于其成分金属,抗腐蚀性优于其成分金属,根据铝锂合金是航空飞行器较理想的结构材料之一来分析其所具备的特点。
【详解】
铝锂合金是航空飞行器较理想的结构材料之一,说明其耐腐蚀强、密度小、硬度大、强度高,和其易导电性无关。
故选:D。
17.(1)减少环境污染 (2) 导电 (3)2CO+2NO2CO2+N2
18.(1) 铁元素 铁原子 (2)导热(3) 剧烈燃烧,火星四射,放出热量,生成黑色固体 防止生成的高温融熔物溅落瓶底,使集气瓶炸裂
19.(1)①②④(2)延展(3)导电
20.Ag Hg Al Ca 纯净物 化学 a
【详解】
(1).该银白色金属是银:Ag;
液体金属是汞:Hg;
地壳中含量最高的金属元素是铝:Al;
人体中含量最多的金属元素是钙:Ca。
(2).合金中的Mg会和氧气发生反应:;
该镁铝合金具有化学式,有固定的组成,属于纯净物;
储氢过程中生成了MgH2和Al,属于化学变化过程。
(3).合金的熔点比组成合金的纯金属的低,所以a能表示锡铅合金。
(4). 。
21.AC 大 a d O2和CO2 浅绿色 硫酸亚铁 H2O 通一段时间CO 尾气处理装置(尾气处理方法也得分) 32:3 偏大 设反应生成CO2的质量为x,则
解得:x=17.6g。
答:装置B增重的质量等于生成CO2的质量为17.6g。
【详解】
(1)A、橡胶密封件属于合成材料;
B、铝合金车体属于合金,为金属材料;
C、碳纤维复合材料防火壁板属于复合材料;
D、铁轨属于合金,是金属材料;
故填:AC。
(2)合金硬度通常比它的组成纯金属的硬度大,人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度大。
(3)①实验a铜片在干燥的空气中不生锈,d中铜片同时与空气和水接触,铜片生锈,说明铜生锈需要水的一组实验是ad;
②实验a铜片在干燥的空气中不生锈,b中铜片不与二氧化碳接触,不生锈,c中铜片不与氧气接触,不生锈,d中铜片同时与氧气、二氧化碳和水接触,铜片生锈,通过实验证明铜与H2O和O2和CO2反应产生“铜绿”。
(4)①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为浅绿色,其中FeSO4的名称为硫酸亚铁。
②根据,反应前铜原子4个、铁原子4个、硫原子10个、氧原子42个、氢原子4个,反应后铜原子4个、铁原子4个、硫原子10个、氧原子40个,则2R中含2个氧原子、4个氢原子,R的化学式为H2O。
(5)①实验时,应先通一段时间CO,排尽装置内空气,防止爆炸。
②从环境保护角度,该装置缺少尾气处理装置,因为一氧化碳有毒,会污染空气。
③若加热一段时间后,测得装置B增重11.0g,说明反应生成二氧化碳的质量为11g,根据可知,二氧化碳中的氧元素一半来自氧化铜,一半来自一氧化碳,则剩余氧化铜中氧元素质量为,固体中铜元素质量不变,为,此时固体中铜元素与氧元素的质量比为,若缺少C装置,空气中二氧化碳进入B中,测得数据将偏大。
④见答案。
22.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
一、选择题(共16题)
1.生活中的下列物品,其制作材料属于合金的是( )
A.金刚石钻头 B.钢化玻璃杯 C.不锈钢锅 D.瓷器
2.下列可回收的生活垃圾中,属于金属材料的是
A.铝制易拉罐 B.废旧塑料桶 C.旧报纸 D.玻璃瓶
3.物质的性质决定其用途,下列说法不正确的是
A.甲烷作燃料,是因为甲烷具有可燃性 B.铜作导线,是因为铜具有良好的导电性
C.洗洁精洗涤油污,是因为洗洁精能溶解油污 D.活性炭除冰箱异味,是因为活性炭具有吸附性
4.下列物品所使用的主要材料属于合金的是
A.青花瓷瓶 B.橡胶充气艇 C.青铜宝剑 D.金刚石
5.下列关于合金的说法不正确的是( )
A.不锈钢在一定的条件下也会生锈 B.合金的熔点一般低于各成分金属
C.合金一定是由多种金属熔合而成 D.控制条件可制成性能不同的合金
6.下图所示的实验不能达到实验目的的是( )
A.实验一:验证CO2的部分性质 B.实验二:验证空气中氧气含量
C.实验三:验证O2是否收集满 D.实验四:比较黄铜与纯铜的硬度
7.锡、铅的熔点分别是232℃和327℃。焊锡是锡铅合金,焊锡的熔点小于200℃,把铅加入锡中制成合金的主要目的是( )
A.增加强度 B.降低熔点 C.增加延展性 D.增加耐磨性
8.目前哈尔滨地铁工程已有一定的规模,待哈尔滨地铁网络全部建成以后,地铁将成为城市最主要的交通工具,下列有关认识不正确的是( )
A.地铁作为环保的交通工具,可以很大限度地实现节能减排
B.建地铁可节省人们的出行时间,有效缓解交通压力
C.生铁和钢是含碳量不同的两种铁合金
D.生铁的硬度比钢大,钢轨是用生铁铺设的
9.生活中的下列现象,属于化学变化的是( )
A.用石墨制金刚石 B.干冰升华 C.铁杵磨成针 D.铜和锌制成合金
10.铝、铜、锡、铁等金属本质上的共同点是
A.都具有银白色的金属光泽
B.熔点都很高
C.密度、硬度都很大
D.都具有良好的延展性、导电性、导热性
11.下列物质属于纯净物的是
A.雪碧饮料
B.生铁
C.二氧化碳
D.高锰酸钾加热制氧气后的剩余固体
12.关于合金的说法正确的是
A.合金是一种纯净物
B.合金中只含有金属元素
C.合金的强度、硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好
D.铁锈是一种合金
13.下列有关实验现象叙述错误的是
A.将二氧化碳通入燃着的两支高低不同蜡烛的烧杯中,蜡烛由低到高依次熄灭
B.铁丝在氧气中燃烧,火星四射,生成黑色固体
C.用黄铜片(铜锌合金)和铜片相互刻画,黄铜片上留有划痕
D.硫在空气中燃烧产生微弱的淡蓝色火焰,生成有刺激性气味的气体
14.氨基钠(NaNH2)是合成维生素A的原料.工业上将钠于97~100℃熔融,向反应容器中缓慢通入无水的液氨(NH3),再加热至350~360℃生成氨基钠和氢气.下列说法中,不正确的是( )
A.单质钠的化合价为0价 B.钠的熔点比铁的熔点低
C.维生素A是由Na、N、H元素组成的 D.该反应属于置换反应
15.下列实验方案,不能达到相应实验目的是( )
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.铝锂合金是航空飞行器较理想的结构材料之一。铝锂合金具有的以下性质中,与该应用无关的是( )
A.硬度大 B.耐腐蚀 C.密度小 D.易导电
二、非选择题(共8题)
17.近一年,丹东上线的公交汽车都由动力单一燃油改为电和气电能和燃气混合动力。
(1)这种做法的目的是______答一点。
(2)汽车尾部都有内置铜丝拖地的带子。这是利用铜能______这一性质。
(3)汽车尾气的主要成分是一氧化碳和一氧化氮。处理尾气的方法是在催化剂作用下可生成空气中最多的气体和一种氧化物。请写出该反应的化学方程式:______。
18.铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由______构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和______性。
(3)实验室:细铁丝在氧气中燃烧的现象是______,放热。该反应的化学方程式是______。在做这个实验是集气瓶的底部要留少量水,其目的是______。
19.青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。如图是一种照明用台灯。
(1)如图中标示的各部件中,用金属材料制成的是_____(填序号)。
(2)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的_____性。
(3)铜质插头是利用了金属铜的_____性。
20.人类的生产、生活离不开金属。
(1)家用热水瓶内胆壁的银白色金属是________(填符号,下同);液体金属是__________;地壳中含量最高的金属元素是_______,人体中含量最多的金属元素是________。
(2)镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是_____(任写一个化学方程式)。该合金属于______(填“混合物”或“纯净物”),它是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于________(填“物理”或“化学”)变化。
(3)合金的很多性能与组成它们的纯金属不同。如图能表示锡铅合金的是________(填序号“a”“b”或“c”)。
(4)铝冶炼厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为________。
21.铜是人类使用最早、应用广泛的金属材料。
(1)高铁开通运营,有效延伸我市发展空间。下列与高铁有关的物质不属于金属材料的是__________。
A 橡胶密封件 B 铝合金车体 C 碳纤维复合材料防火壁板 D 铁轨
(2)人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度_________(填“大”或“小”)。
(3)兴趣小组探究长期放置在空气中铜表面生成“铜绿”的原因。实验装置及现象如下。
査阅资料:碱石灰能吸收二氧化碳和水蒸气,氢氧化钠溶液能吸收二氧化碳。
序号 a b c d
实验装置
实验现象 铜片不生锈 铜片不生锈 铜片不生锈 铜片生锈
①说明铜生锈需要水的一组实验是_____________(填实验序号);
②通过实验证明铜与H2O和___________反应产生“铜绿”。
(4)我国炼铜技术源远流长。
①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为___________,其中FeSO4的名称为___________。
②现代炼铜的新工艺以黄铜矿为原料,采用生物炼铜。其原理之一为: 。R的化学式为___________。
(5)兴趣小组取32.0gCuO粉末,按下图装置进行实验。
①实验时,应先___________(填“加热样品”或“通一段时间CO”)。
②从环境保护角度,该装置缺少___________。
③若加热一段时间后,测得装置B增重11.0g,此时固体中铜元素与氧元素的质量比为___________,若缺少C装置测得数据将___________(填“偏大”、“偏小”或“不变”)。
④若32.0gCuO完全被还原成Cu,装置B增重多少克?(写计算过程)____
22 已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.C
【详解】
A、 金刚石钻头,是由碳元素组成的,不属于合金,故选项错误;B、玻璃杯是硅酸盐产品,不属于合金,故选项错误;C、不锈钢是钢的一种,是铁的合金,故选项正确;D、陶瓷是用泥土烧制而成的,属于无机非金属材料,不属于合金,故选项错误。故选C。
2.A
【解析】
金属材料包括纯金属以及它们的合金,故选A。
3.C
【详解】
A、甲烷具有可燃性,可用来作燃料,故选项说法正确;
B、因为铜具有较好的导电性,所以可作导线,故原选项说法正确;
C、洗洁精可去除油污,是因为它具有乳化作用,不能将油污溶解,故选项说法错误;
D、活性炭具有的吸附性是去除冰箱异味的主要原因,故原选项说法正确。
故选C。
4.C
【详解】
A、青花瓷瓶属于硅酸盐材料,即无机非金属材料,不符合题意。
B、橡胶充气艇属于有机高分子材料,不符合题意。
C、青铜宝剑是铜和锡的合金,符合题意。
D、金刚石是由碳元素组成的单质,不属于合金,不符合题意。
故选:C。
5.C
【详解】
A、不锈钢在一定的条件下也会生锈,故选项正确;
B、合金的熔点一般比各成分金属低,故选项正确;
C、合金不一定是金属和金属熔合而成,合金可以是金属与非金属熔合而成的物质,故选项错误;
D、控制条件可制成性能不同的合金,例如控制铁的合金中的含碳量,可以制得性能不同的生铁和钢,故选项正确。
故选C。
B 7.B 8.D
9.A
【详解】
A、用石墨制金刚石,产生了新的物质,属于化学变化;
B、干冰升华是固态二氧化碳变为气态二氧化碳,没有产生新的物质,不属于化学变化;
C、铁杵磨成针只是铁的形状改变了,没有产生新的物质,不属于化学变化;
D、铜和锌制成合金是铜和锌按照一定方法制成的,没有产生新的物质,不属于化学变化。
故选A。
10.D
【详解】
A.都具有银白色的金属光泽,不是金属的共性,如铜呈紫红色,故选项错误。
B.熔点都很高,不是金属的共性,如钠的熔点较低,故选项错误。
C.密度、硬度都很大不是金属的共性,如钠的密度和硬度较小,故选项错误。
D.金属都具有良好的延展性、导电性、导热性,属于金属共性,故选项正确。故选:D。
11.C
【详解】
A、雪碧饮料中含有水、碳酸等物质属于混合物,故选项不符合题意。
B、生铁中含有铁和碳等物质,因此属于混合物,故选项不符合题意。
C、二氧化碳是由二氧化碳一种物质组成,属于纯净物,故选项符合题意。
D、高锰酸钾加热制氧气后的剩余物是锰酸钾、二氧化锰,属于混合物,故选项不符合题意。
故选:C。
12.C
【详解】
A. 合金是由多种物质混合而成的,属于混合物,此选项错误;
B. 合金是金属与其它金属或非金属经高温熔合在一起的具有金属特性的物质,合金中可能含有非金属元素,此选项错误;
C. 金属制成合金后,性能发生了改变,合金的强度、硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好,此选项正确;
D. 铁锈不是合金,此选项错误。
故选C。
13.C 14.C
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.D
【分析】
合金的硬度大于其成分金属,熔点低于其成分金属,抗腐蚀性优于其成分金属,根据铝锂合金是航空飞行器较理想的结构材料之一来分析其所具备的特点。
【详解】
铝锂合金是航空飞行器较理想的结构材料之一,说明其耐腐蚀强、密度小、硬度大、强度高,和其易导电性无关。
故选:D。
17.(1)减少环境污染 (2) 导电 (3)2CO+2NO2CO2+N2
18.(1) 铁元素 铁原子 (2)导热(3) 剧烈燃烧,火星四射,放出热量,生成黑色固体 防止生成的高温融熔物溅落瓶底,使集气瓶炸裂
19.(1)①②④(2)延展(3)导电
20.Ag Hg Al Ca 纯净物 化学 a
【详解】
(1).该银白色金属是银:Ag;
液体金属是汞:Hg;
地壳中含量最高的金属元素是铝:Al;
人体中含量最多的金属元素是钙:Ca。
(2).合金中的Mg会和氧气发生反应:;
该镁铝合金具有化学式,有固定的组成,属于纯净物;
储氢过程中生成了MgH2和Al,属于化学变化过程。
(3).合金的熔点比组成合金的纯金属的低,所以a能表示锡铅合金。
(4). 。
21.AC 大 a d O2和CO2 浅绿色 硫酸亚铁 H2O 通一段时间CO 尾气处理装置(尾气处理方法也得分) 32:3 偏大 设反应生成CO2的质量为x,则
解得:x=17.6g。
答:装置B增重的质量等于生成CO2的质量为17.6g。
【详解】
(1)A、橡胶密封件属于合成材料;
B、铝合金车体属于合金,为金属材料;
C、碳纤维复合材料防火壁板属于复合材料;
D、铁轨属于合金,是金属材料;
故填:AC。
(2)合金硬度通常比它的组成纯金属的硬度大,人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度大。
(3)①实验a铜片在干燥的空气中不生锈,d中铜片同时与空气和水接触,铜片生锈,说明铜生锈需要水的一组实验是ad;
②实验a铜片在干燥的空气中不生锈,b中铜片不与二氧化碳接触,不生锈,c中铜片不与氧气接触,不生锈,d中铜片同时与氧气、二氧化碳和水接触,铜片生锈,通过实验证明铜与H2O和O2和CO2反应产生“铜绿”。
(4)①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为浅绿色,其中FeSO4的名称为硫酸亚铁。
②根据,反应前铜原子4个、铁原子4个、硫原子10个、氧原子42个、氢原子4个,反应后铜原子4个、铁原子4个、硫原子10个、氧原子40个,则2R中含2个氧原子、4个氢原子,R的化学式为H2O。
(5)①实验时,应先通一段时间CO,排尽装置内空气,防止爆炸。
②从环境保护角度,该装置缺少尾气处理装置,因为一氧化碳有毒,会污染空气。
③若加热一段时间后,测得装置B增重11.0g,说明反应生成二氧化碳的质量为11g,根据可知,二氧化碳中的氧元素一半来自氧化铜,一半来自一氧化碳,则剩余氧化铜中氧元素质量为,固体中铜元素质量不变,为,此时固体中铜元素与氧元素的质量比为,若缺少C装置,空气中二氧化碳进入B中,测得数据将偏大。
④见答案。
22.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
同课章节目录
