5.2物质组成的表示——化学式课后练习-2021-2022学年九年级化学京改版(2013)九年级上册(word版 含解析)
文档属性
| 名称 | 5.2物质组成的表示——化学式课后练习-2021-2022学年九年级化学京改版(2013)九年级上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 166.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-28 00:00:00 | ||
图片预览




文档简介
5.2物质组成的表示——化学式
一、选择题(共16题)
1.下列日常生活中的下列各组物质,前者属于混合物,后者属于单质的是
A.氯化钠 铁 B.空气 水 C.医用酒精 氢气 D.冰水混合物 臭氧
2.酸奶中含有的乳酸菌(C3H6O3)能帮助消化。下列说法错误的是( )
A.乳酸菌属于化合物
B.乳酸菌由3个碳原子、6个氢原子、3个氧原子构成
C.乳酸菌由碳元素、氢元素、氧元素组成
D.乳酸菌中碳、氢、氧元素原子个数比为1:2:1
3.下列化学用语对应关系正确的是
A.水银—Ag B.铝—AL C.氨气—NH4 D.氯化氢—HCl
4.氧气(O2)、二氧化碳(CO2)、双氧水(H2O2)是初中常见的物质,这三种物质中都含有
A.氧元素 B.2个氧原子 C.氧气 D.氧分子
5.75%的酒精是小范围消毒的理想试剂。关于酒精溶质(C2H6O),说法正确的是
A.C2H6O中含有8个原子
B.C2H6O分子由三种元素组成
C.C2H6O中,碳、氧元素质量比为3:2
D.C2H6O属于氧化物
6.港珠澳大桥被评为“新的世界七大奇迹”之一。整座大桥对防腐蚀技术提出了很高的要求,大桥外侧使用的涂料是具有防潮防霉等性能的产品——氟碳涂料,成分为PEVE氟树脂,是由乙烯基乙醚单体和氟乙烯单体交替联接构成。下列有关乙烯基乙醚(化学式为C4H8O)说法正确的是
A.它由4个碳原子、8个氢原子和1个氧原子构成
B.其中氢元素质量分数最大
C.它的相对分子质量为72g
D.它由碳、氢、氧三种元素组成
7.我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为H25N34O3Cl),该物质是超高能材料,在航空航天上可作推进剂。下列有关该物质的说法不正确的是 ( )
A.全氮阴离子盐是由四种非金属元素组成
B.全氮阴离子盐中氮元素与氧元素的原子个数比为34:3
C.全氮阴离子盐中氯元素的质量分数大于氧元素的质量分数
D.584.5g该物质中氢元素的质量为25g
8.下列化学用语书写正确的是( )
A.镁元素 MG B.氧离子O﹣2 C.水银Hg D.2个氮原子N2
9.下列化学用语与所表达的意义对应正确的是( )
A.Fe2+:铁离子 B.2Ne:2个氖元素
C.O2中氧的化合价为-2价 D.2个氮原子:2N
10.根据常见元素的化合价,下列物质相应的化学式正确的是( )
A.氧化钙 B.碳酸钠 C.氯化镁MgCl D.氢氧化钾KOH
11.在金星的大气中含有C2O3气体(分子结构如图),关于该气体的说法,正确的是( )
A.该气体是由2个碳元素和3个氧元素组成的
B.该气体是由多原子构成的
C.一个三氧化二碳分子含有35个质子
D.该气体的一个分子是由2个碳原子和3个氧原子构成的
12.研究发现,达菲(Tamiflu)对甲型 H1N1 流感病毒有抑制作用,从香料八角中提取的莽草酸(C7H10O5)是合成达菲(C16H31O8N2P)的原料之一。下列对莽草酸的说法不正确是
A.是氧化物 B.由碳、氢、氧元素组成
C.由分子构成 D.碳、氢、氧原子个数比为 7∶10∶5
13.氮与氧两元素组成的氧化物,其中氮元素与氧元素的质量比为7:20,则该氧化物的化学式是( )
A.NO B. C. D.
14.过氧化氢的化学式为H2O2,下列有关过氧化氢的说法正确的是
A.过氧化氢是由氢气和氧气组成的 B.过氧化氢是由2个氢原子和2个氧原子构成的
C.过氧化氢在常温下可缓慢分解出氧气 D.过氧化氢中氢元素和氧元素的质量比为1:1
15.维生素的化学式为,下列关于维生素的说法正确的是
A.碳元素的质量分数最大 B.含有3个元素
C.相对分子质量是396g D.H、O元素的质量比为44:1
16.传统中医名方连花清瘟胶囊可用于治疗流感,其成分之一是没食子酸(化学式为:C7H6O5),下列说法正确的是
A.没食子酸是氧化物 B.没食子酸中碳、氢、氧元素的质量比为7:6:5
C.没食子酸中含有18个原子 D.没食子酸中由三种元素组成
二、综合题(共6题)
17.空气是宝贵的自然资源,下图是以空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去)。请按要求回答相关问题:
(1)图中空气分离属于_________变化(填“物理”或“化学”)。
(2)写出“X→NH3”反应的符号表达式____________。
(3)如图为某化肥样品的标签,根据图标签计算:
①该袋化肥中氮元素的质量至少为__________kg。 (结果保留至0.1)
②若杂质中不含氮元素,则该化肥中纯尿素的质量分数至少是__________。(列式计算,结果保留至0.1 %)
18.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
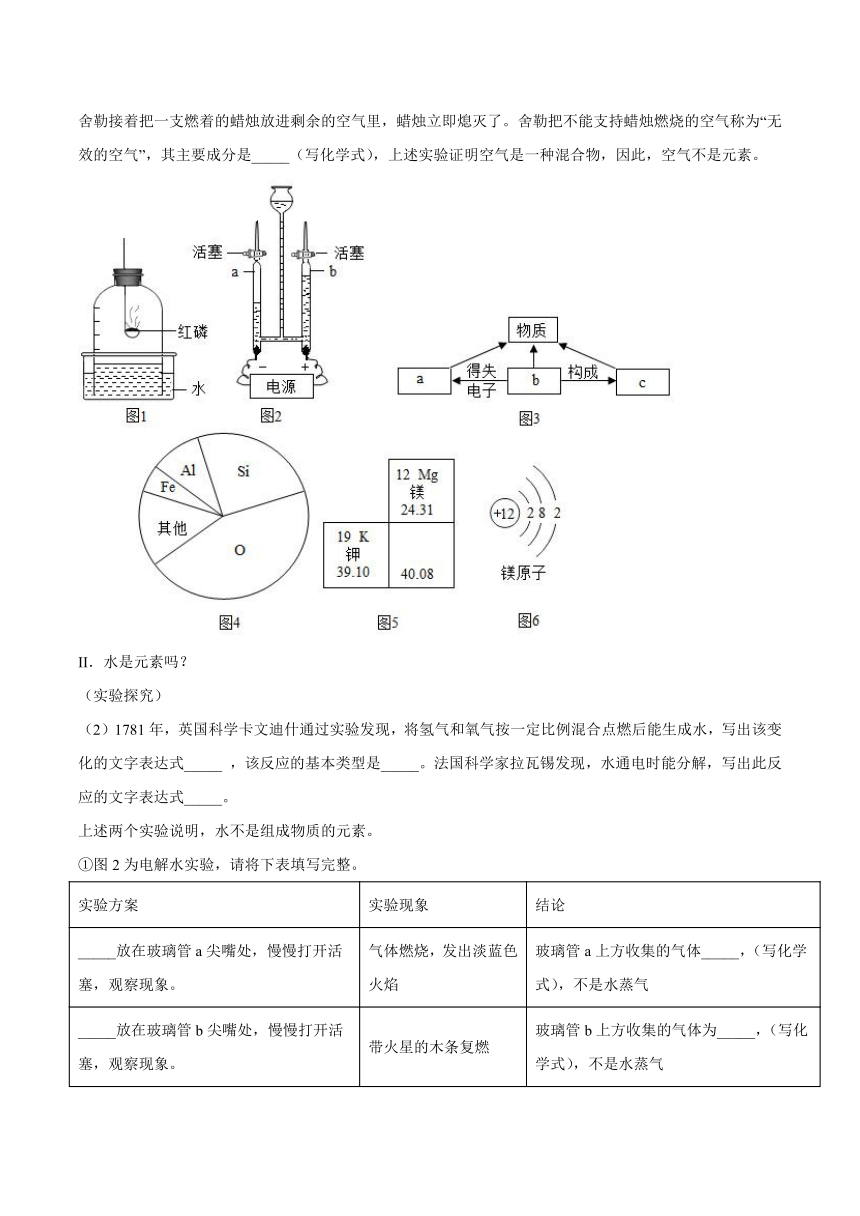
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
19.学校化学兴趣小组欲利用下列装置进行相关实验探究,请你分析并填空。
(1)写出图中标号②的仪器名称____________________。
(2)下列哪种方法可以得到平稳的氧气流?__________(填序号)
①把二氧化锰加入装有过氧化氢溶液的试管中
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(3)某同学选用A发生装置完成实验室制取氧气,该装置中仪器①略向下倾斜的原因是:___________。
(4)收集较纯净的氧气时,选用的收集装置是______________;用A和该装置制氧气实验结束时的正确操作是______________________;D装置不能用于收集氧气的原因是________________________。
(5)检验一瓶气体是否为氧气的方法是_________________________。
(6)糖类是人类食物的重要成分,在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成CO2和H2O,同时放出能量(已知每克葡萄糖放出约16kJ的能量)。请回答:
①葡萄糖的相对分子质量为____________________;
②葡萄糖中碳、氢、氧的质量比为__________________(写最简整数比);
③一般人每行走lkm,大约需消耗170kJ的能量。假设这些能量全部来自葡萄糖,请问:小明同学步行5km,大约需消耗多少克葡萄糖____________(写出计算过程,结果取整数)。
20.水是生命活动不可缺少的物质。请回答相关的问题。
Ⅰ、探究水的组成实验
(1)为证明水不是由“水元素”组成的,1785年,拉瓦锡在高温的条件下,用水蒸气与红热的铁反应,将水转化为氢气,同时生成四氧化三铁。模拟实验装置如图1所示。
①该反应的化学符号表达式为______。
②加热铁粉前,应先通入水蒸气一段时间,理由是______。
(2)电解水实验的简易装置如图2所示,a中收集到的气体是______(填化学式);从该实验得到关于水的组成的结论是______;从能量变化角度看,该过程是将______能转化为______能。
Ⅱ、水的净化
化学兴趣小组收集了一瓶浑浊的京杭大运河的河水,模拟自来水厂进行水的净化过程。其实验过程如下所示,请回答以下问题。
(3)自来水厂常用明矾作絮凝剂,明矾[KAl(SO4)m·12H2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝,则m=______,氢氧化铝的化学式为______。
(4)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是______。
(5)将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,还起到的作用是______。欲使净化水转化为纯水,则可采取的方法是______。
21.如图是某口服液标签的部分内容。
××口服液 有效成分:硫酸亚铁(FeSO4) ……
(1)该口服液能为人体提供的一种微量元素是________,人体缺乏该元素会引发的病症是________。
(2)硫酸亚铁的相对分子质量是________,硫酸亚铁中铁、硫、氧三种元素的质量比是________。
22.根据下列装置示意图回答问题:
(1)仪器②的名称是__________。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时应选用的发生装置是______,写出该反应的文字(或符号)表达式__________。
(3)实验室利用装置A加热高锰酸钾制氧气时,需要进行改进的地方是___________。
(4)若用C装置收集氧气,验满的方法是_______。
(5)用F装置做硫在氧气中燃烧的实验,观察到的现象有________,集气瓶底部装少量水的目的是________。
(6)2020年全球爆发新型冠状肺炎的传染病,莽草酸(化学式C7H10O5)是制取抗流感药物“达菲”的主要原料。请计算:34.8g莽草酸中含有氧元素的质量为________g。
参考答案
1.C
【解析】
试题分析:由一种物质组成的物质是纯净物;由两种或两种以上的物质组成的物质是混合物。由一种元素组成的纯净物是单质。空气、医用酒精、都是多种物质组成的混合物;水是化合物,氢气是单质。
2.B
【详解】
A、乳酸菌是由三种元素组成的纯净物,属于化合物,故A正确;
B、一个乳酸菌分子由3个碳原子、6个氢原子、3个氧原子构成,故B不正确;
C、乳酸菌的化学式中含有三种元素符号,乳酸菌由碳元素、氢元素、氧元素组成,故C正确;
D、乳酸菌中碳、氢、氧元素原子个数比为,故D正确。故选B。
3.D
【详解】
A、水银是金属汞的俗称,其化学式为Hg,故选项化学用语错误;
B、铝属于金属单质,直接用元素符号表示其化学式,其化学式为Al,故选项化学用语错误;
C、氨气的化学式为:NH3,故选项化学用语错误;
D、氯化氢的化学式为:HCl,故选项化学用语正确。故选D。
4.A
【详解】
氧气(O2)是由氧气分子构成,是由氧元素组成;二氧化碳(CO2)是由二氧化碳分子构成,是由碳、氧元素组成;双氧水(H2O2)是由过氧化氢分子构成,是由氢、氧元素组成。这三种物质中都含有氧元素。
故选:A。
5.C
【详解】
A、C2H6O是由 C2H6O分子构成的,1个C2H6O分子中含有8个原子,故选项说法错误。
B、分子是由原子构成的,C2H6O是由碳、氢和氧三种元素组成的,故选项说法错误。
C、C2H6O中,碳、氧元素质量比为(12×2):(16×1)=3:2,故选项说法正确。
D、C2H6O是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
故选:C。
6.D
【详解】
A、1个乙烯基乙醚分子是由4个碳原子、8个氢原子和1个氧原子构成的。A错误;
B、乙烯基乙醚中碳、氢、氧元素的质量比为(12×4):(1×8):16=6:1:2,其中碳元素的质量分数最大。B错误;
C、相对分子质量的单位是“1”,不是“g”,通常省略不写。C错误;
D、乙烯基乙醚是由碳、氢、氧三种元素组成的。D正确。
故选D。
7.C
【详解】
A、由全氮阴离子盐化学式H25N34O3Cl可知,全氮阴离子盐是由H、N、O、Cl四种非金属元素组成,不符合题意;
B、由全氮阴离子盐化学式H25N34O3Cl可知,全氮阴离子盐中氮元素与氧元素的原子个数比为34:3,不符合题意;
C、全氮阴离子盐中氯元素与氧元素的质量比为35.5:(16×3)=35.5:48,故氯元素的质量分数小于氧元素的质量分数,符合题意;
D、584.5g该物质中氢元素的质量为:,不符合题意。
故选C。
8.C
【详解】
A、镁元素的元素符号为Mg,故选项化学用语书写错误.
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.氧离子的离子符号为O2﹣,故选项化学用语书写错误.
C、水银属于金属单质,直接用元素符号表示其化学式,其化学式为Hg,故选项化学用语书写正确.
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N,故选项化学用语书写错误.
故选C.
9.D
【详解】
A、Fe2+表示亚铁离子,错误;
B、标在元素符号前的数字表示原子的个数,2Ne表示2个氖原子,错误;
C、单质中元素的化合价为0,O2中氧的化合价为0,错误;
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N,正确;
故选D。
10.D
【详解】
A、氧化钙中,钙元素显+2价,氧元素显-2价,所以其化学式为CaO,故错误;
B、碳酸钠中,钠元素显+1价,碳酸根显-2价,所以其化学式为Na2CO3,故错误;
C、氯化镁中,镁元素显+2价,氯元素显-1价,所以其化学式为MgCl2,故错误;
D、氢氧化钾中,钾元素显+1价,氢氧根显-1价,所以其化学式为KOH,故正确。
故选D。
11.D
【详解】
A、元素只论种类不论个数,故A错误;
B、该气体由分子构成,不是由原子构成,故B错误;
C、一个碳原子中有6个质子,一个氧原子中有8个质子,故一个三氧化二碳中有36个质子,故C错误;
D、根据结构图可知,一个三氧化二碳分子由2个碳原子和3个氧原子构成,故D正确。故选D。
12.A
【详解】
A、莽草酸是含有碳、氢、氧三种元素的化合物,不属于氧化物,故选项说法错误。
B、由莽草酸的化学式可知,莽草酸是由碳、氢、氧元素组成的,故选项说法正确。
C、莽草酸由莽草酸分子构成,故选项说法正确。
D、由莽草酸的化学式可知,1个莽草酸分子是由7个碳原子、10个氢原子和5个氧原子构成的,一个莽草酸分子中碳、氢、氧原子个数比为7:10:5,故选项说法正确。
故选A。
13.D
【详解】
某氧化物由氮元素与氧元素组成,设此氧化物的化学式为NxOy,由氮元素与氧元素的质量比为7:20,
则14x:16y=7:20,则x:y=2:5;则此氧化物的化学式为N2O5。
故选D。
14.C
【详解】
A、分子是由原子构成的,过氧化氢分子是由氢原子和氧原子构成,不含氢气和氧气,故选项说法错误。
B、过氧化氢是由过氧化氢分子构成的,1个过氧化氢分子是由2个氢原子和2个氧原子构成的,故选项说法错误。
C、过氧化氢在常温下可缓慢分解出氧气,故选项说法正确。
D、过氧化氢中氢元素和氧元素的质量比为(1×2):(16×2)≠1:1,故选项说法错误。
故选:C。
15.A
【详解】
A、维生素 D2中,碳、氢、氧元素的质量比为:::336:44:16,可见其中碳元素的质量分数最大,符合题意;
B、元素是宏观概念,只讲种类、不讲个数,不符合题意;
C、维生素 D2的相对分子质量为:12×28+44+16=396,相对分子质量单位是“1”,不是“克”,常常省略不写,不符合题意;
D、维生素 D2中,氢、氧元素的质量比为:(1×44):(16×1)=11:4,不符合题意。
故选A。
16.D
【详解】
A、氧化物是由两种元素组成,其中一种为氧元素的化合物,没食子酸的化学式为:C7H6O5,由三种元素组成,则没食子酸不是氧化物,故A不正确;
B、没食子酸中碳、氢、氧元素的质量比为,故B不正确;
C、没食子酸的化学式为:C7H6O5,由三种元素组成,1个没食子酸分子中含有个原子,故C不正确;
D、没食子酸的化学式为:C7H6O5,没食子酸由碳元素、氢元素和氧元素共三种元素组成,故D正确。
故选D。
17.物理; N2+3H22NH3 23.2 99.4%(详见解析)
【详解】
(1)分离空气的原理是利用液态氮和液态氧沸点的不同,没有新物质生成,是物理变化;
(2)空气的主要成分是氮气和氧气,空气分离可以得到氮气和氧气,X为氮气,其化学式为N2,氮气和氢气反应生成氨气,反应的化学方程式为:N2+3H2 2NH3;
(3)①由题意,净含量为50kg,含氮量≥46.4%,该袋化肥中氮元素的质量至少=50kg×46.4%=23.2kg;
②纯尿素中氮元素的质量分数=,若杂质中不含氮元素,则该化肥中纯尿素的质量分数至少=。
18.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
19.集气瓶 ② 防止试管壁上的冷凝水倒流,造成热的试管炸裂 E 先将导气管移出水槽,再停止加热 氧气的密度比空气大,不能用向下排空气法收集 用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气。否则,不是 180 6:1:8 53g
【详解】
(1)由图示可知②是集气瓶;
(2)可以得到平稳的氧气流的方法是:把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中,这样反应物过氧化氢是一部分一部分反应的,气流平稳;如果把二氧化锰直接加入过氧化氢溶液中,大量的过氧化氢迅速反应,短时间产生大量氧气。 选②。
(3)某同学选用A发生装置制取氧气,仪器①略向下倾斜的原因是:防止试管壁上的冷凝水倒流,造成热的试管炸裂;
(4)收集较纯净的氧气时,应用排水法收集,选用的收集装置是E;用A和该装置制氧气实验结束时的正确操作是先将导气管移出水槽,再停止加热,防止水倒吸引起试管炸裂;D装置不能用于收集氧气的原因是:氧气的密度比空气大,不能用向下排空气法收集。
(5)由于氧气具有助燃性,检验气体是否为氧气的方法:用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气,否则,不是。
(6)①葡萄糖的相对分子质量是:12×6+1×12+16×6=180;
②由葡萄糖的化学式C6H12O6可知,葡萄糖中碳、氢、氧的质量比为:(12×6):(1×12):(16×6)=6:1:8;
③步行5km,大约需消耗葡萄糖为: ≈53g
故答案为:
(1)集气瓶;
(2)②;
(3)防止试管壁上的冷凝水倒流,造成热的试管炸裂;
(4)E; 先将导气管移出水槽,再停止加热;氧气的密度比空气大,不能用向下排空气法收集;
(5)用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气。否则,不是;
(6)①180,②6:1:8,③步行5km消耗葡萄糖的质量为53g。
20.
(1) Fe+H2OFe3O4+H2 排出空气,防止铁粉被空气中的氧气氧化
(2) H2 水是由氢元素和氧元素组成的 电 化学
(3) 2 Al(OH)3
(4)活性炭
(5) 降低水的硬度 蒸馏
【解析】
(1)
①铁粉和水蒸气反应的符号表达式为:Fe+H2O Fe3O4+H2;
②铁粉在加热时会被空气中的氧气氧化,故先通入水蒸气,排尽空气,防止铁粉被氧化;
(2)
电解水时生成的氢气和氧气的体积比为2:1,故气体多的是氢气,则a管为氢气(H2);电解水生成氢气和氧气则可知水是由氢元素和氧元素组成的;该过程中是将电能转化成化学能;
(3)
明矾的化学式为:KAl(SO4)2·12H2O,故m为2;氢氧化铝的化学式为:Al(OH)3;
(4)
活性炭可吸附色素和异味;
(5)
生活中降低水的硬度的方法是:煮沸;但要得到纯水可采用的方法是:蒸馏。
21.(1)铁 ;贫血
(2)152;7∶4∶8
【详解】
(1)标签中的信息可知该物质的有效成分为硫酸亚铁,缺铁会造成缺铁性贫血;
(2)硫酸亚铁的化学式为:FeSO4,所以硫酸亚铁的相对分子质量为:56+32+16×4=152,硫酸亚铁中铁、硫、氧三种元素的质量比是:56:32:64=7:4:8。
22.
(1)集气瓶
(2) B (或)
(3)在试管口放一团棉花
(4)将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满
(5) 发出蓝紫色火焰 吸收二氧化硫,防止污染空气(答案合理即可)
(6)16g
34.8g莽草酸中含有氧元素的质量为34.8g××100%=16g;
答:34.8g莽草酸中含有氧元素的质量为16g。
【解析】
(1)
由图可知,仪器②的名称是集气瓶,故填:集气瓶;
(2)
实验室用过氧化氢溶液和二氧化锰制取氧气,属于固液常温型,选择的发生装置为B;过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,反应的文字(符号)表达式为(或),故填:B;(或);
(3)
实验室利用装置A加热高锰酸钾制氧气时,为防止加热时高锰酸钾进入导管,应在试管口放置一团棉花,故填:在试管口放一团棉花;
(4)
氧气具有助燃性,能使带火星的木条复燃,若用C装置收集氧气,验满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满,故填:将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满;
(5)
硫在氧气中燃烧发出明亮的蓝紫色火焰,所以用F装置做硫在氧气中燃烧的实验,观察到的现象有发出蓝紫色火焰;二氧化硫有毒,直接排放会污染空气,因此集气瓶底部装少量水的目的是吸收二氧化硫,防止污染空气,故填:发出蓝紫色火焰;吸收二氧化硫,防止污染空气;
(6)
见答案。
一、选择题(共16题)
1.下列日常生活中的下列各组物质,前者属于混合物,后者属于单质的是
A.氯化钠 铁 B.空气 水 C.医用酒精 氢气 D.冰水混合物 臭氧
2.酸奶中含有的乳酸菌(C3H6O3)能帮助消化。下列说法错误的是( )
A.乳酸菌属于化合物
B.乳酸菌由3个碳原子、6个氢原子、3个氧原子构成
C.乳酸菌由碳元素、氢元素、氧元素组成
D.乳酸菌中碳、氢、氧元素原子个数比为1:2:1
3.下列化学用语对应关系正确的是
A.水银—Ag B.铝—AL C.氨气—NH4 D.氯化氢—HCl
4.氧气(O2)、二氧化碳(CO2)、双氧水(H2O2)是初中常见的物质,这三种物质中都含有
A.氧元素 B.2个氧原子 C.氧气 D.氧分子
5.75%的酒精是小范围消毒的理想试剂。关于酒精溶质(C2H6O),说法正确的是
A.C2H6O中含有8个原子
B.C2H6O分子由三种元素组成
C.C2H6O中,碳、氧元素质量比为3:2
D.C2H6O属于氧化物
6.港珠澳大桥被评为“新的世界七大奇迹”之一。整座大桥对防腐蚀技术提出了很高的要求,大桥外侧使用的涂料是具有防潮防霉等性能的产品——氟碳涂料,成分为PEVE氟树脂,是由乙烯基乙醚单体和氟乙烯单体交替联接构成。下列有关乙烯基乙醚(化学式为C4H8O)说法正确的是
A.它由4个碳原子、8个氢原子和1个氧原子构成
B.其中氢元素质量分数最大
C.它的相对分子质量为72g
D.它由碳、氢、氧三种元素组成
7.我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为H25N34O3Cl),该物质是超高能材料,在航空航天上可作推进剂。下列有关该物质的说法不正确的是 ( )
A.全氮阴离子盐是由四种非金属元素组成
B.全氮阴离子盐中氮元素与氧元素的原子个数比为34:3
C.全氮阴离子盐中氯元素的质量分数大于氧元素的质量分数
D.584.5g该物质中氢元素的质量为25g
8.下列化学用语书写正确的是( )
A.镁元素 MG B.氧离子O﹣2 C.水银Hg D.2个氮原子N2
9.下列化学用语与所表达的意义对应正确的是( )
A.Fe2+:铁离子 B.2Ne:2个氖元素
C.O2中氧的化合价为-2价 D.2个氮原子:2N
10.根据常见元素的化合价,下列物质相应的化学式正确的是( )
A.氧化钙 B.碳酸钠 C.氯化镁MgCl D.氢氧化钾KOH
11.在金星的大气中含有C2O3气体(分子结构如图),关于该气体的说法,正确的是( )
A.该气体是由2个碳元素和3个氧元素组成的
B.该气体是由多原子构成的
C.一个三氧化二碳分子含有35个质子
D.该气体的一个分子是由2个碳原子和3个氧原子构成的
12.研究发现,达菲(Tamiflu)对甲型 H1N1 流感病毒有抑制作用,从香料八角中提取的莽草酸(C7H10O5)是合成达菲(C16H31O8N2P)的原料之一。下列对莽草酸的说法不正确是
A.是氧化物 B.由碳、氢、氧元素组成
C.由分子构成 D.碳、氢、氧原子个数比为 7∶10∶5
13.氮与氧两元素组成的氧化物,其中氮元素与氧元素的质量比为7:20,则该氧化物的化学式是( )
A.NO B. C. D.
14.过氧化氢的化学式为H2O2,下列有关过氧化氢的说法正确的是
A.过氧化氢是由氢气和氧气组成的 B.过氧化氢是由2个氢原子和2个氧原子构成的
C.过氧化氢在常温下可缓慢分解出氧气 D.过氧化氢中氢元素和氧元素的质量比为1:1
15.维生素的化学式为,下列关于维生素的说法正确的是
A.碳元素的质量分数最大 B.含有3个元素
C.相对分子质量是396g D.H、O元素的质量比为44:1
16.传统中医名方连花清瘟胶囊可用于治疗流感,其成分之一是没食子酸(化学式为:C7H6O5),下列说法正确的是
A.没食子酸是氧化物 B.没食子酸中碳、氢、氧元素的质量比为7:6:5
C.没食子酸中含有18个原子 D.没食子酸中由三种元素组成
二、综合题(共6题)
17.空气是宝贵的自然资源,下图是以空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去)。请按要求回答相关问题:
(1)图中空气分离属于_________变化(填“物理”或“化学”)。
(2)写出“X→NH3”反应的符号表达式____________。
(3)如图为某化肥样品的标签,根据图标签计算:
①该袋化肥中氮元素的质量至少为__________kg。 (结果保留至0.1)
②若杂质中不含氮元素,则该化肥中纯尿素的质量分数至少是__________。(列式计算,结果保留至0.1 %)
18.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
19.学校化学兴趣小组欲利用下列装置进行相关实验探究,请你分析并填空。
(1)写出图中标号②的仪器名称____________________。
(2)下列哪种方法可以得到平稳的氧气流?__________(填序号)
①把二氧化锰加入装有过氧化氢溶液的试管中
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(3)某同学选用A发生装置完成实验室制取氧气,该装置中仪器①略向下倾斜的原因是:___________。
(4)收集较纯净的氧气时,选用的收集装置是______________;用A和该装置制氧气实验结束时的正确操作是______________________;D装置不能用于收集氧气的原因是________________________。
(5)检验一瓶气体是否为氧气的方法是_________________________。
(6)糖类是人类食物的重要成分,在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成CO2和H2O,同时放出能量(已知每克葡萄糖放出约16kJ的能量)。请回答:
①葡萄糖的相对分子质量为____________________;
②葡萄糖中碳、氢、氧的质量比为__________________(写最简整数比);
③一般人每行走lkm,大约需消耗170kJ的能量。假设这些能量全部来自葡萄糖,请问:小明同学步行5km,大约需消耗多少克葡萄糖____________(写出计算过程,结果取整数)。
20.水是生命活动不可缺少的物质。请回答相关的问题。
Ⅰ、探究水的组成实验
(1)为证明水不是由“水元素”组成的,1785年,拉瓦锡在高温的条件下,用水蒸气与红热的铁反应,将水转化为氢气,同时生成四氧化三铁。模拟实验装置如图1所示。
①该反应的化学符号表达式为______。
②加热铁粉前,应先通入水蒸气一段时间,理由是______。
(2)电解水实验的简易装置如图2所示,a中收集到的气体是______(填化学式);从该实验得到关于水的组成的结论是______;从能量变化角度看,该过程是将______能转化为______能。
Ⅱ、水的净化
化学兴趣小组收集了一瓶浑浊的京杭大运河的河水,模拟自来水厂进行水的净化过程。其实验过程如下所示,请回答以下问题。
(3)自来水厂常用明矾作絮凝剂,明矾[KAl(SO4)m·12H2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝,则m=______,氢氧化铝的化学式为______。
(4)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是______。
(5)将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,还起到的作用是______。欲使净化水转化为纯水,则可采取的方法是______。
21.如图是某口服液标签的部分内容。
××口服液 有效成分:硫酸亚铁(FeSO4) ……
(1)该口服液能为人体提供的一种微量元素是________,人体缺乏该元素会引发的病症是________。
(2)硫酸亚铁的相对分子质量是________,硫酸亚铁中铁、硫、氧三种元素的质量比是________。
22.根据下列装置示意图回答问题:
(1)仪器②的名称是__________。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时应选用的发生装置是______,写出该反应的文字(或符号)表达式__________。
(3)实验室利用装置A加热高锰酸钾制氧气时,需要进行改进的地方是___________。
(4)若用C装置收集氧气,验满的方法是_______。
(5)用F装置做硫在氧气中燃烧的实验,观察到的现象有________,集气瓶底部装少量水的目的是________。
(6)2020年全球爆发新型冠状肺炎的传染病,莽草酸(化学式C7H10O5)是制取抗流感药物“达菲”的主要原料。请计算:34.8g莽草酸中含有氧元素的质量为________g。
参考答案
1.C
【解析】
试题分析:由一种物质组成的物质是纯净物;由两种或两种以上的物质组成的物质是混合物。由一种元素组成的纯净物是单质。空气、医用酒精、都是多种物质组成的混合物;水是化合物,氢气是单质。
2.B
【详解】
A、乳酸菌是由三种元素组成的纯净物,属于化合物,故A正确;
B、一个乳酸菌分子由3个碳原子、6个氢原子、3个氧原子构成,故B不正确;
C、乳酸菌的化学式中含有三种元素符号,乳酸菌由碳元素、氢元素、氧元素组成,故C正确;
D、乳酸菌中碳、氢、氧元素原子个数比为,故D正确。故选B。
3.D
【详解】
A、水银是金属汞的俗称,其化学式为Hg,故选项化学用语错误;
B、铝属于金属单质,直接用元素符号表示其化学式,其化学式为Al,故选项化学用语错误;
C、氨气的化学式为:NH3,故选项化学用语错误;
D、氯化氢的化学式为:HCl,故选项化学用语正确。故选D。
4.A
【详解】
氧气(O2)是由氧气分子构成,是由氧元素组成;二氧化碳(CO2)是由二氧化碳分子构成,是由碳、氧元素组成;双氧水(H2O2)是由过氧化氢分子构成,是由氢、氧元素组成。这三种物质中都含有氧元素。
故选:A。
5.C
【详解】
A、C2H6O是由 C2H6O分子构成的,1个C2H6O分子中含有8个原子,故选项说法错误。
B、分子是由原子构成的,C2H6O是由碳、氢和氧三种元素组成的,故选项说法错误。
C、C2H6O中,碳、氧元素质量比为(12×2):(16×1)=3:2,故选项说法正确。
D、C2H6O是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
故选:C。
6.D
【详解】
A、1个乙烯基乙醚分子是由4个碳原子、8个氢原子和1个氧原子构成的。A错误;
B、乙烯基乙醚中碳、氢、氧元素的质量比为(12×4):(1×8):16=6:1:2,其中碳元素的质量分数最大。B错误;
C、相对分子质量的单位是“1”,不是“g”,通常省略不写。C错误;
D、乙烯基乙醚是由碳、氢、氧三种元素组成的。D正确。
故选D。
7.C
【详解】
A、由全氮阴离子盐化学式H25N34O3Cl可知,全氮阴离子盐是由H、N、O、Cl四种非金属元素组成,不符合题意;
B、由全氮阴离子盐化学式H25N34O3Cl可知,全氮阴离子盐中氮元素与氧元素的原子个数比为34:3,不符合题意;
C、全氮阴离子盐中氯元素与氧元素的质量比为35.5:(16×3)=35.5:48,故氯元素的质量分数小于氧元素的质量分数,符合题意;
D、584.5g该物质中氢元素的质量为:,不符合题意。
故选C。
8.C
【详解】
A、镁元素的元素符号为Mg,故选项化学用语书写错误.
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.氧离子的离子符号为O2﹣,故选项化学用语书写错误.
C、水银属于金属单质,直接用元素符号表示其化学式,其化学式为Hg,故选项化学用语书写正确.
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N,故选项化学用语书写错误.
故选C.
9.D
【详解】
A、Fe2+表示亚铁离子,错误;
B、标在元素符号前的数字表示原子的个数,2Ne表示2个氖原子,错误;
C、单质中元素的化合价为0,O2中氧的化合价为0,错误;
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N,正确;
故选D。
10.D
【详解】
A、氧化钙中,钙元素显+2价,氧元素显-2价,所以其化学式为CaO,故错误;
B、碳酸钠中,钠元素显+1价,碳酸根显-2价,所以其化学式为Na2CO3,故错误;
C、氯化镁中,镁元素显+2价,氯元素显-1价,所以其化学式为MgCl2,故错误;
D、氢氧化钾中,钾元素显+1价,氢氧根显-1价,所以其化学式为KOH,故正确。
故选D。
11.D
【详解】
A、元素只论种类不论个数,故A错误;
B、该气体由分子构成,不是由原子构成,故B错误;
C、一个碳原子中有6个质子,一个氧原子中有8个质子,故一个三氧化二碳中有36个质子,故C错误;
D、根据结构图可知,一个三氧化二碳分子由2个碳原子和3个氧原子构成,故D正确。故选D。
12.A
【详解】
A、莽草酸是含有碳、氢、氧三种元素的化合物,不属于氧化物,故选项说法错误。
B、由莽草酸的化学式可知,莽草酸是由碳、氢、氧元素组成的,故选项说法正确。
C、莽草酸由莽草酸分子构成,故选项说法正确。
D、由莽草酸的化学式可知,1个莽草酸分子是由7个碳原子、10个氢原子和5个氧原子构成的,一个莽草酸分子中碳、氢、氧原子个数比为7:10:5,故选项说法正确。
故选A。
13.D
【详解】
某氧化物由氮元素与氧元素组成,设此氧化物的化学式为NxOy,由氮元素与氧元素的质量比为7:20,
则14x:16y=7:20,则x:y=2:5;则此氧化物的化学式为N2O5。
故选D。
14.C
【详解】
A、分子是由原子构成的,过氧化氢分子是由氢原子和氧原子构成,不含氢气和氧气,故选项说法错误。
B、过氧化氢是由过氧化氢分子构成的,1个过氧化氢分子是由2个氢原子和2个氧原子构成的,故选项说法错误。
C、过氧化氢在常温下可缓慢分解出氧气,故选项说法正确。
D、过氧化氢中氢元素和氧元素的质量比为(1×2):(16×2)≠1:1,故选项说法错误。
故选:C。
15.A
【详解】
A、维生素 D2中,碳、氢、氧元素的质量比为:::336:44:16,可见其中碳元素的质量分数最大,符合题意;
B、元素是宏观概念,只讲种类、不讲个数,不符合题意;
C、维生素 D2的相对分子质量为:12×28+44+16=396,相对分子质量单位是“1”,不是“克”,常常省略不写,不符合题意;
D、维生素 D2中,氢、氧元素的质量比为:(1×44):(16×1)=11:4,不符合题意。
故选A。
16.D
【详解】
A、氧化物是由两种元素组成,其中一种为氧元素的化合物,没食子酸的化学式为:C7H6O5,由三种元素组成,则没食子酸不是氧化物,故A不正确;
B、没食子酸中碳、氢、氧元素的质量比为,故B不正确;
C、没食子酸的化学式为:C7H6O5,由三种元素组成,1个没食子酸分子中含有个原子,故C不正确;
D、没食子酸的化学式为:C7H6O5,没食子酸由碳元素、氢元素和氧元素共三种元素组成,故D正确。
故选D。
17.物理; N2+3H22NH3 23.2 99.4%(详见解析)
【详解】
(1)分离空气的原理是利用液态氮和液态氧沸点的不同,没有新物质生成,是物理变化;
(2)空气的主要成分是氮气和氧气,空气分离可以得到氮气和氧气,X为氮气,其化学式为N2,氮气和氢气反应生成氨气,反应的化学方程式为:N2+3H2 2NH3;
(3)①由题意,净含量为50kg,含氮量≥46.4%,该袋化肥中氮元素的质量至少=50kg×46.4%=23.2kg;
②纯尿素中氮元素的质量分数=,若杂质中不含氮元素,则该化肥中纯尿素的质量分数至少=。
18.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
19.集气瓶 ② 防止试管壁上的冷凝水倒流,造成热的试管炸裂 E 先将导气管移出水槽,再停止加热 氧气的密度比空气大,不能用向下排空气法收集 用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气。否则,不是 180 6:1:8 53g
【详解】
(1)由图示可知②是集气瓶;
(2)可以得到平稳的氧气流的方法是:把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中,这样反应物过氧化氢是一部分一部分反应的,气流平稳;如果把二氧化锰直接加入过氧化氢溶液中,大量的过氧化氢迅速反应,短时间产生大量氧气。 选②。
(3)某同学选用A发生装置制取氧气,仪器①略向下倾斜的原因是:防止试管壁上的冷凝水倒流,造成热的试管炸裂;
(4)收集较纯净的氧气时,应用排水法收集,选用的收集装置是E;用A和该装置制氧气实验结束时的正确操作是先将导气管移出水槽,再停止加热,防止水倒吸引起试管炸裂;D装置不能用于收集氧气的原因是:氧气的密度比空气大,不能用向下排空气法收集。
(5)由于氧气具有助燃性,检验气体是否为氧气的方法:用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气,否则,不是。
(6)①葡萄糖的相对分子质量是:12×6+1×12+16×6=180;
②由葡萄糖的化学式C6H12O6可知,葡萄糖中碳、氢、氧的质量比为:(12×6):(1×12):(16×6)=6:1:8;
③步行5km,大约需消耗葡萄糖为: ≈53g
故答案为:
(1)集气瓶;
(2)②;
(3)防止试管壁上的冷凝水倒流,造成热的试管炸裂;
(4)E; 先将导气管移出水槽,再停止加热;氧气的密度比空气大,不能用向下排空气法收集;
(5)用带火星的木条伸入集气瓶内,若木条复燃,说明瓶内气体是氧气。否则,不是;
(6)①180,②6:1:8,③步行5km消耗葡萄糖的质量为53g。
20.
(1) Fe+H2OFe3O4+H2 排出空气,防止铁粉被空气中的氧气氧化
(2) H2 水是由氢元素和氧元素组成的 电 化学
(3) 2 Al(OH)3
(4)活性炭
(5) 降低水的硬度 蒸馏
【解析】
(1)
①铁粉和水蒸气反应的符号表达式为:Fe+H2O Fe3O4+H2;
②铁粉在加热时会被空气中的氧气氧化,故先通入水蒸气,排尽空气,防止铁粉被氧化;
(2)
电解水时生成的氢气和氧气的体积比为2:1,故气体多的是氢气,则a管为氢气(H2);电解水生成氢气和氧气则可知水是由氢元素和氧元素组成的;该过程中是将电能转化成化学能;
(3)
明矾的化学式为:KAl(SO4)2·12H2O,故m为2;氢氧化铝的化学式为:Al(OH)3;
(4)
活性炭可吸附色素和异味;
(5)
生活中降低水的硬度的方法是:煮沸;但要得到纯水可采用的方法是:蒸馏。
21.(1)铁 ;贫血
(2)152;7∶4∶8
【详解】
(1)标签中的信息可知该物质的有效成分为硫酸亚铁,缺铁会造成缺铁性贫血;
(2)硫酸亚铁的化学式为:FeSO4,所以硫酸亚铁的相对分子质量为:56+32+16×4=152,硫酸亚铁中铁、硫、氧三种元素的质量比是:56:32:64=7:4:8。
22.
(1)集气瓶
(2) B (或)
(3)在试管口放一团棉花
(4)将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满
(5) 发出蓝紫色火焰 吸收二氧化硫,防止污染空气(答案合理即可)
(6)16g
34.8g莽草酸中含有氧元素的质量为34.8g××100%=16g;
答:34.8g莽草酸中含有氧元素的质量为16g。
【解析】
(1)
由图可知,仪器②的名称是集气瓶,故填:集气瓶;
(2)
实验室用过氧化氢溶液和二氧化锰制取氧气,属于固液常温型,选择的发生装置为B;过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,反应的文字(符号)表达式为(或),故填:B;(或);
(3)
实验室利用装置A加热高锰酸钾制氧气时,为防止加热时高锰酸钾进入导管,应在试管口放置一团棉花,故填:在试管口放一团棉花;
(4)
氧气具有助燃性,能使带火星的木条复燃,若用C装置收集氧气,验满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满,故填:将带火星的木条放在集气瓶口,若木条复燃,则证明氧气收集满;
(5)
硫在氧气中燃烧发出明亮的蓝紫色火焰,所以用F装置做硫在氧气中燃烧的实验,观察到的现象有发出蓝紫色火焰;二氧化硫有毒,直接排放会污染空气,因此集气瓶底部装少量水的目的是吸收二氧化硫,防止污染空气,故填:发出蓝紫色火焰;吸收二氧化硫,防止污染空气;
(6)
见答案。
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
