5.1初步认识化学元素课后练习-2021-2022学年九年级化学京改版(2013)上册(word版 含解析)
文档属性
| 名称 | 5.1初步认识化学元素课后练习-2021-2022学年九年级化学京改版(2013)上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 102.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-28 13:37:26 | ||
图片预览



文档简介
5.1初步认识化学元素
一、选择题(共16题)
1.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。下列说法错误的是( )
A.碘的相对原子质量为126.9,原子核内质子数为53
B.碘元素位于第五周期,其原子最外层有7个电子
C.碘元素属于非金属元素,碘原子在化学反应中容易得到电子
D.碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为﹣1价
2.菠菜是一种富含铁的蔬菜,这里的“铁”指的是
A.原子 B.离子 C.分子 D.元素
3.下列说法不正确的是
A.催化剂在化学反应前后,质量和性质都不变
B.地壳中质量分数最大的元素是氧
C.空气中体积分数最大的气体是氮气
D.只含有一种元素的物质可能是纯净物
4.2019年是元素周期表年,下列元素中属于非金属元素的是
A.Na B.Mg C.S D.Zn
5.下列推理你认为正确的是
A.如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同
B.如果两种粒子含有的质子数相同;则这两种粒子一定属于同一种元素
C.如果物质中只含有一种元素,则这种物质一定是纯净物
D.如果化学变化中构成物质的分子改变,则组成物质的元素也一定变
6.下列说法正确的是
A.纯净物是由同种分子(或原子)构成的
B.含有氧元素的化合物,不一定是氧化物
C.化合反应一定是由两种物质参加反应,生成一种物质
D.由不同种元素组成的物质一定是化合物
7.既能表示一种元素,还能表示由这种元素组成的单质的符号是
A.Cu B.H C.O D.N
8.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
A.氮气、五氧化二磷、干冰 B.红磷、冰水混合物、四氧化三铁
C.铁、高锰酸钾、空气 D.臭氧、二氧化碳、牛奶
9.下列各组物质,按混合物、单质顺序排列的是
A.海水、干冰
B.冰水、水银
C.食醋、蒸馏水
D.煤、金刚石
10.第11号元素和第17号元素位于同一周期的原因是
A.质子数相同 B.中子数相同 C.原子的电子层数相同 D.最外层电子数相同
11.核燃料中钚在中子的撞击下,原子核发生分裂,产生锶及一些粒子和射线。锶元素在元素周期表中显示的信息和粒子结构示意图如图所示。以下表述中正确的是
A.图2、图3都属于锶元素
B.图3所表示粒子的化学符号是Sr
C.锶原子的中子数为38
D.锶原子的相对原子质量是87.62g
12.生活中常接触到的“加铁酱油”“含氟牙膏”中的铁、氟是指
A.单质 B.元素 C.原子 D.分子
13.分类法是化学学习的重要方法之一.下列各组物质按照单质、化合物、混合物的顺序排列的是( )
A.水银、碳酸钙、冰水混合物 B.液氧、水、粗盐
C.水、食盐、海水 D.钙片、氯化镁、矿泉水
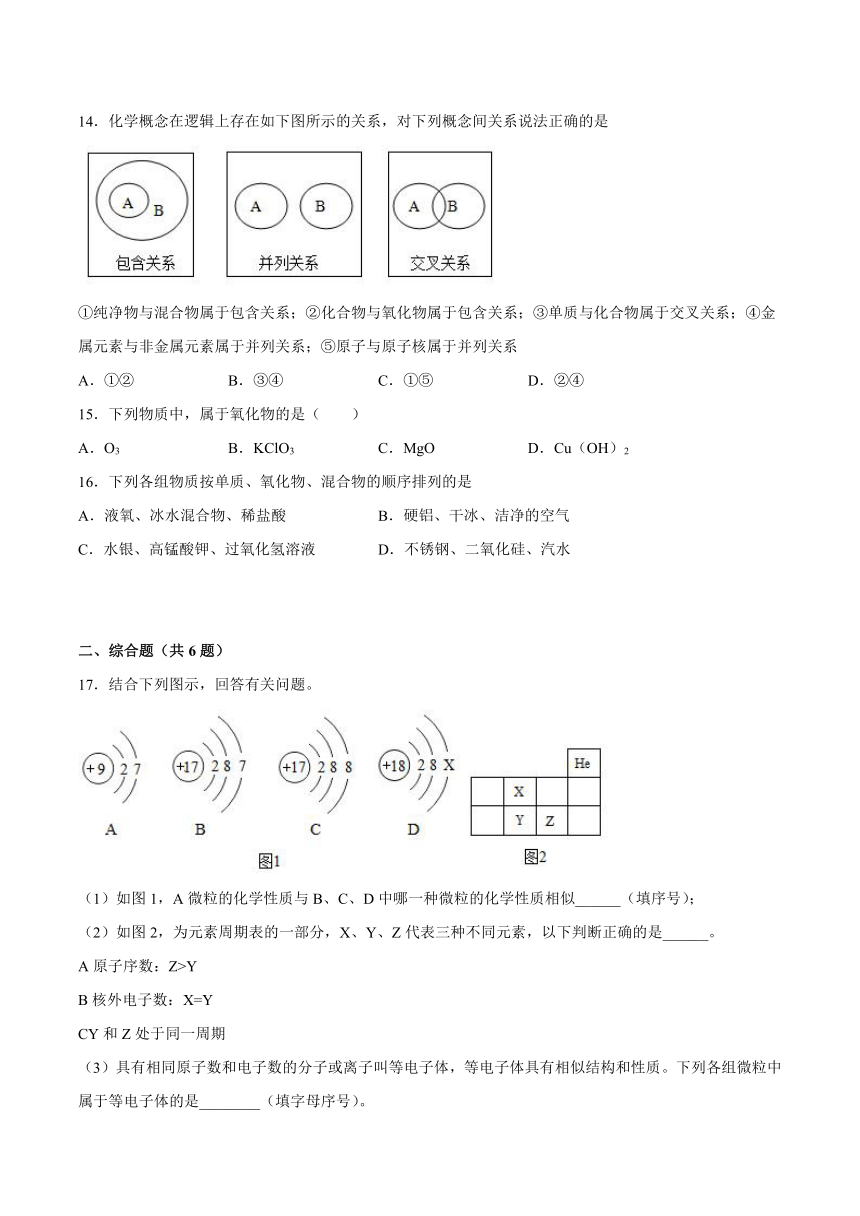
14.化学概念在逻辑上存在如下图所示的关系,对下列概念间关系说法正确的是
①纯净物与混合物属于包含关系;②化合物与氧化物属于包含关系;③单质与化合物属于交叉关系;④金属元素与非金属元素属于并列关系;⑤原子与原子核属于并列关系
A.①② B.③④ C.①⑤ D.②④
15.下列物质中,属于氧化物的是( )
A.O3 B.KClO3 C.MgO D.Cu(OH)2
16.下列各组物质按单质、氧化物、混合物的顺序排列的是
A.液氧、冰水混合物、稀盐酸 B.硬铝、干冰、洁净的空气
C.水银、高锰酸钾、过氧化氢溶液 D.不锈钢、二氧化硅、汽水
二、综合题(共6题)
17.结合下列图示,回答有关问题。
(1)如图1,A微粒的化学性质与B、C、D中哪一种微粒的化学性质相似______(填序号);
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是______。
A原子序数:Z>Y
B核外电子数:X=Y
CY和Z处于同一周期
(3)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似结构和性质。下列各组微粒中属于等电子体的是________(填字母序号)。
A NH3和H2O B CO和N2 C H2O2和H2O D CO 和SO2。
18.生活中处处有化学,请回答下列问题.
(1)人体中所含最多的金属元素是________________(写名称);
(2)相对分子质量最小的氧化物________________(写化学式);
(3)自然界中最坚硬的物质是________________(写名称);
(4)通过“铜绿”性质研究实验,我们可以观察到以下现象:
①向“铜绿”中加入稀盐酸,可以发现产生大量________________,绿色粉末逐渐消失,溶液变成________________色。
②加热“铜绿”,可以发现绿色粉末变成________色,试管壁上有水珠生成。
19.图A是钾元素在元素周期表中的部分信息,图B是钾原子的结构示意图,据此回答问题。
(1)钾的相对原子质量是__________;
(2)钾原子的最外层电子数是__________;
(3)由原子核外电子层数与元素所在周期表中周期数相同可知,钾元素在元素周期表中应该排在第__________周期;
(4)该元素属于__________元素(选填 “金属”或“非金属”);
(5)该元素的原子在化学反应中容易__________电子(选填 “得到”或“失去”)。
20.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1所示,X是___________________________________________;Y是___________________________________________。
(2)从宏观角度看,汞由________________________________________组成;从微观角度看,汞由__________________________________________构成。
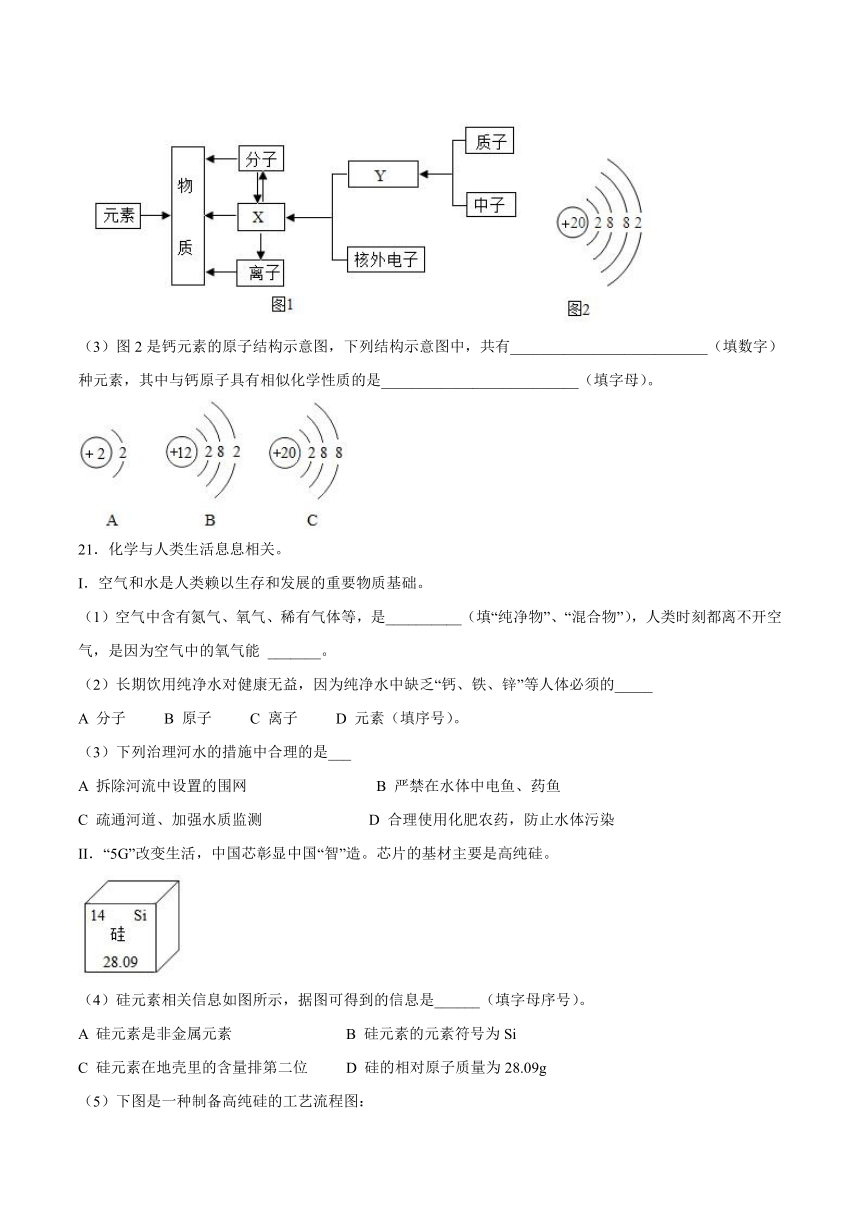
(3)图2是钙元素的原子结构示意图,下列结构示意图中,共有__________________________(填数字)种元素,其中与钙原子具有相似化学性质的是__________________________(填字母)。
21.化学与人类生活息息相关。
I.空气和水是人类赖以生存和发展的重要物质基础。
(1)空气中含有氮气、氧气、稀有气体等,是__________(填“纯净物”、“混合物”),人类时刻都离不开空气,是因为空气中的氧气能 _______。
(2)长期饮用纯净水对健康无益,因为纯净水中缺乏“钙、铁、锌”等人体必须的_____
A 分子 B 原子 C 离子 D 元素(填序号)。
(3)下列治理河水的措施中合理的是___
A 拆除河流中设置的围网 B 严禁在水体中电鱼、药鱼
C 疏通河道、加强水质监测 D 合理使用化肥农药,防止水体污染
II.“5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅。
(4)硅元素相关信息如图所示,据图可得到的信息是______(填字母序号)。
A 硅元素是非金属元素 B 硅元素的元素符号为Si
C 硅元素在地壳里的含量排第二位 D 硅的相对原子质量为28.09g
(5)下图是一种制备高纯硅的工艺流程图:
①反应Ⅰ所用的镁在化学反应中易______电子(填“得”或“失”),镁和SiO2发生的是否是化合反应______(填“是”或“否”);反应Ⅱ要在无氧气的环境中进行,原因是_____(答出一种即可);
②操作Ⅰ的名称是_______,进行该操作时液面应______(填“高于”或“低于”)滤纸边缘,进行该操作需要用到玻璃棒,其作用是________;
③上述已知生产流程中,可以循环利用的物质是_______。
22.下表是元素周期表中第2、3周期的元素,请回答有关问题。
(1)下列各组具有相似化学性质的元素是 _____ (填字母序号)
A Na、Cl
B O、S
C F、Cl
D Al、Ar
(2)写出一条第三周期元素原子的核外电子排布规律 _____ 。
(3)地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物的化学式为 _____ 。
(4)某离子的结构示意图为 当x-y=8时,该粒子的符号为 _____ .
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是 _____ (填字母序号)
A NO和O2 B CO和N2 C SO3和CO2 D PO43- 和SO42-
参考答案
1.D
【详解】
A、由元素周期表中提供的碘元素的部分信息及碘原子的结构示意图,可知碘的相对原子质量为126.9,原子核内质子数为53,故A正确;
B、由碘原子的结构示意图,可知碘原子核外共有5个电子层,位于第五周期,最外层有7个电子,故B正确;
C、由汉语名称“碘”,可知其为非金属元素;由碘原子的结构示意图,可知在化学反应中容易得到电子,故C正确;
D、根据化合价原则“正负化合价的代数和为零”,设KIO3中碘元素的化合价为x,则(+1)+x+3×(-2)=0,故x=+5价,故KIO3中碘元素的化合价为-1价,说法错误,故D错误。
故选D。
2.D
【详解】
在菠菜中,铁是以无机盐的形式存在的,这里的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。故选D。
3.A
【详解】
A、催化剂在化学反应前后质量和化学性质(而不是性质)都不变,故选项说法错误;B、地壳中质量分数最大的元素是氧,故选项说法正确;C、空气中体积分数最大的气体是氮气,故选项说法正确;D、只含有一种元素的物质可能是纯净物,例如氧气等,故选项说法正确。故选A。
4.C
【详解】
A、Na为钠元素的元素符号,带“钅”字旁,属于金属元素,故A错误;
B、Mg为镁元素的元素符号,带“钅”字旁,属于金属元素,故B错误;
C、S为硫元素的元素符号,带“石”字旁,属于固态非金属元素,故C正确;
D、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故D错误。故选C。
5.A
【详解】
A、同一元素的质子数相同;如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同,正确;
B、含有的质子数相同的两种粒子不一定属于同一种元素,例如氖原子和水分子质子数相同,不是同一元素,错误;
C、物质中只含有一种元素,这种物质不一定是纯净物,例如氧气和臭氧组成的混合物,错误;
D、化学变化中构成物质的分子改变,组成物质的元素一定不变,例如氧气转化为臭氧,错误。
故选A。
6.B
【详解】
A、纯净物是由相同的微粒构成的,如氯化钠是纯净物,氯化钠中只含有钠离子和氯离子,故A错误;
B、含有氧元素的化合物,不一定是氧化物,例如NaOH,其中含有氧元素,但是不属于氧化物,故B正确;
C、化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,故C错误;
D、由不同种元素组成的物质不一定是化合物,还有可能是混合物,故D错误;
故选择B
7.A
【详解】
A、Cu是金属铜的元素符号,它即可以表示铜的元素符号,又可以表示金属铜,故正确;
B、H只能表示元素符号,不能表示单质,故错误;
C、O不能表示单质,故错误;
D、N不能表示单质,故错误。故选A.
8.D
【详解】
A、氮气属于单质,五氧化二磷、干冰均属于氧化物,故A不正确;
B、红磷属于单质,冰水混合物、四氧化三铁均属于氧化物,故B不正确;
C、铁属于单质,高锰酸钾不属于氧化物,空气属于混合物,故C不正确;
D、臭氧属于单质,二氧化碳属于氧化物,牛奶属于混合物,故D正确。故选D。
9.D
【详解】
A、海水包括水、氯化钠等,属于混合物。干冰是固态的二氧化碳,是纯净物中的化合物。故A错误;
B、冰水是水的两种形态,属于同种物质,是纯净物。水银是金属汞,是单质。故B错误;
C、食醋中包括水、醋酸等,属于混合物。蒸馏水指的是水,是化合物。故C错误;
D、煤的主要成分是碳,也包括硫等其他杂质,属于混合物。金刚石是碳单质。故D正确。
故选D。
10.C
【详解】
第11号元素和第17号元素的原子核外都有三个电子层,即两种元素原子的电子层数相同,所以第11号元素和第17号元素位于元素周期表中的同一周期,故选C。
11.A
【解析】
试题分析:从图示看:图2和3都属于锶元素,因为其中的质子数都是38;图3所表示粒子的化学符号是Sr2+;锶原子的中子数为=88-38=40;锶原子的相对原子质量是87.62。故选A.
12.B
【详解】
“加铁酱油”、“含氟牙膏”等用品中的“铁”、“氟”不是以单质、分子、原子、离子等形式存在,而是指元素,故选B。
13.B
【解析】:由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物。 A. 水银是单质、碳酸钙、冰水混合物 都是化合物; B. 液氧是单质、水是化合物、粗盐是混合物;C. 水是化合物、食盐是主要成分为氯化钠的混合物、海水是混合物; D.钙片属于混合物;氯化镁属于化合物,矿泉水属于混合物。
14.D
【详解】
①物质按含有物质种类的多少可分为纯净物与混合物,是并列关系,故此选项错误;②化合物有多种元素组成,其中氧化物是含有氧元素和另外一种元素的化合物,是包含关系,故此选项正确;③纯净物按元素的含有情况可分为化合物与单质,故是并列关系,故此选项错误;④元素分为金属元素和非金属元素,因此金属元素与非金属元素属于并列关系,故此选项正确;⑤原子分为原子核和核外电子,所以原子与原子核属于包含关系,故此选项错误。故选D。
15.C
【详解】
A、O3是一种只有氧元素组成的物质,则属于单质,故错误;
B、KClO3中含有三种元素,属于化合物,但不属于氧化物,故错误;
C、MgO是一种含有Mg和O两种元素且有氧元素的化合物,则属于氧化物,故正确;
D、Cu(OH)2是由金属离子和氢氧根离子构成的化合物,则属于碱,故错误。
故选:C。
16.A
【详解】
A、液氧(液态的氧气)是由氧元素组成的纯净物,属于单质;冰水混合物中只有水,是由氢、氧两种元素组成的化合物,属于氧化物;稀盐酸是氯化氢水溶液,属于混合物。符合题意;
B、硬铝是合金,属于混合物;干冰(固态二氧化碳)是由碳、氧两种元素组成化合物,属于氧化物;洁净的空气中含有氧气、氮气等物质,属于混合物。不符合题意;
C、水银是由汞元素组成的纯净物,属于单质;高锰酸钾是由三种元素组成的化合物,不是氧化物,过氧化氢溶液中含有过氧化氢和水,属于混合物,不符合题意;
D、不锈钢是合金,属于混合物;二氧化硅是由硅、氧两种元素组成化合物,属于氧化物;汽水中含有水、二氧化碳等物质,属于混合物,不符合题意。
故选A。
17.B A、C B
【详解】
(1)粒子的最外层电子数决定其化学性质,A微粒与B微粒的最外层电子数相同,故A微粒的化学性质与B相似;
(2)A、根据元素周期表可知,原子序数:Z>Y,符合题意;
B、X与Y的最外层电子数相同,核外电子数:Y>X,不符合题意;
C、Y和Z的核外电子层数都是3,故Y和Z处于同一周期,符合题意。
故选AC。
(3)A、NH3和H2O的原子数不相同,不是等电子体,不符合题意;
B、CO和N2都有2个原子数,14个电子数,是等电子体,符合题意;
C、H2O2和H2O原子数和电子数都不相同,不是等电子体,不符合题意;
D、CO和SO2原子数和电子数都不相同,不是等电子体,不符合题意;
故选B。
18.钙; H2O; 金刚石; 气泡; 蓝绿; 黑
【详解】
(1)人体中含有最多的金属元素是钙(Ca);(2)相对分子质量最小的氧化物是水(H2O);(3)自然界最坚硬的是金刚石;(4)铜绿中加入稀盐酸会产生气泡(二氧化碳),2价铜离子为蓝绿色,所以溶液为蓝绿色,加热后Cu氧化变为氧化铜,变为黑色。
19.39.10 1 四 金属 失去
【详解】
(1)在元素周期表中,下方的数字表示该元素的相对原子质量,故填:39.10;(2)读图可知钾原子最外层电子数为1;(3)已知原子核外的电子层数与元素所在周期表中的周期数相同,镁元素的原子核外有3个电子层,则镁元素在元素周期表中应该排在第3周期;(4)镁元素带“钅”字旁,属于金属元素;(2)由镁原子结构示意图为可以看出:最外层弧线上的数字是2,最外层电子数是2,在化学反应中易失去2个电子而形成阳离子。
20.原子 原子核 汞元素 汞原子 3 B
【详解】
(1)构成物质的微粒有分子、原子、离子,所以X是原子;原子由原子核和核外电子构成,所以Y为原子核。
(2)物质由元素组成,汞是由汞元素组成的单质;汞由汞原子直接构成。
(3)元素的种类由该元素原子中质子数决定,图中A、B、C3种粒子的质子数各不相同,所以共有3种元素。
元素的化学性质由原子核外最外层电子数决定。钙原子的最外层电子数为2,化学反应中容易失去2个电子。A为氦原子的结构示意图,最外层虽然也有2个电子,但它是第一层,是一种相对稳定结构,B中最外层(第三层)上有2个电子,与钙原子化学性质相似。故选B。
21.混合物 供给呼吸 D ABCD AB 失 否 防止氢气高温时发生爆炸 过滤 低于 引流 HCl
【详解】
(1)空气中含有氮气、氧气、稀有气体等,是混合物,人类时刻都离不开空气,是因为空气中的氧气能供给呼吸。
(2)长期饮用纯净水对健康无益,因为纯净水中缺乏“钙、铁、锌”等人体必须的元素,故选D。
(3)A、拆除河流中设置的围网有利于河水治理,故A正确;
B、严禁在水体中电鱼、药鱼有利于河水治理,故B正确;
C、疏通河道、加强水质监测有利于河水治理,故C正确;
D、合理使用化肥农药,防止水体污染有利于河水治理,故D正确。故选ABCD。
(4)硅元素相关信息如图所示,据图可得到如下信息:
A、硅元素是非金属元素,正确;
B、硅元素的元素符号为Si,正确;
C、硅元素在地壳里的含量排第二位,不同从图中得到,错误;
D、硅的相对原子质量为28.09,单位错误。
故选AB。
(5)①镁的最外层电子数是2,反应Ⅰ所用的镁在化学反应中易失电子(填“得”或“失”),镁和SiO2生成氧化镁和硅,发生的不是化合反应,填“否”;反应Ⅱ要在无氧气的环境中进行,是为了防止氢气高温时发生爆炸;
②操作Ⅰ是分离难溶固体和液体,操作的名称是过滤,进行该操作时液面应低于滤纸边缘,进行该操作需要用到玻璃棒,其作用是引流;
③上述已知生产流程中,可以循环利用的物质是HCl。
22.BC 从左往右,最外层电子数依次增大(合理即可) Al2O3. S2- BD
【详解】
(1)
A、Na和Cl的最外层电子数不同,不具有相似的化学性质;
B、O和S的最外层电子数相同,具有相似的化学性质;
C、F和Cl的最外层电子数相同,具有相似的化学性质;
D、Al和Ar的最外层电子数不同,不具有相似的化学性质;
故填:BC;
(2)第三周期元素原子的核外电子排布规律是:从左往右,最外层电子数依次增大(合理即可)
故填:从左往右,最外层电子数依次增大(合理即可);
(3)地壳中含量最多的金属元素是Al元素,在化合物中显+3价;地壳中含量最多的非金属元素O元素,Al元素显正价,故氧元素在该化合物中显-2价,故这二者组成的化合物的化学式为Al2O3。
(4)当x-y=8时,说明带有的是2个单位的负电荷,y=8,该粒子的核内质子数为16,故是硫离子,故填:S2-;
(5)A.NO和O2 的原子数都是2,电子数分别是15和16,不属于等电子体;
B.CO和N2的原子数都是2,电子数都是14,属于等电子体;
C.SO3和CO2的原子数和电子数都不同,不属于等电子体;
D.PO43-和SO42-的原子个数和电子个数都相等,属于等电子体。
故选:BD。
一、选择题(共16题)
1.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。下列说法错误的是( )
A.碘的相对原子质量为126.9,原子核内质子数为53
B.碘元素位于第五周期,其原子最外层有7个电子
C.碘元素属于非金属元素,碘原子在化学反应中容易得到电子
D.碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为﹣1价
2.菠菜是一种富含铁的蔬菜,这里的“铁”指的是
A.原子 B.离子 C.分子 D.元素
3.下列说法不正确的是
A.催化剂在化学反应前后,质量和性质都不变
B.地壳中质量分数最大的元素是氧
C.空气中体积分数最大的气体是氮气
D.只含有一种元素的物质可能是纯净物
4.2019年是元素周期表年,下列元素中属于非金属元素的是
A.Na B.Mg C.S D.Zn
5.下列推理你认为正确的是
A.如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同
B.如果两种粒子含有的质子数相同;则这两种粒子一定属于同一种元素
C.如果物质中只含有一种元素,则这种物质一定是纯净物
D.如果化学变化中构成物质的分子改变,则组成物质的元素也一定变
6.下列说法正确的是
A.纯净物是由同种分子(或原子)构成的
B.含有氧元素的化合物,不一定是氧化物
C.化合反应一定是由两种物质参加反应,生成一种物质
D.由不同种元素组成的物质一定是化合物
7.既能表示一种元素,还能表示由这种元素组成的单质的符号是
A.Cu B.H C.O D.N
8.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
A.氮气、五氧化二磷、干冰 B.红磷、冰水混合物、四氧化三铁
C.铁、高锰酸钾、空气 D.臭氧、二氧化碳、牛奶
9.下列各组物质,按混合物、单质顺序排列的是
A.海水、干冰
B.冰水、水银
C.食醋、蒸馏水
D.煤、金刚石
10.第11号元素和第17号元素位于同一周期的原因是
A.质子数相同 B.中子数相同 C.原子的电子层数相同 D.最外层电子数相同
11.核燃料中钚在中子的撞击下,原子核发生分裂,产生锶及一些粒子和射线。锶元素在元素周期表中显示的信息和粒子结构示意图如图所示。以下表述中正确的是
A.图2、图3都属于锶元素
B.图3所表示粒子的化学符号是Sr
C.锶原子的中子数为38
D.锶原子的相对原子质量是87.62g
12.生活中常接触到的“加铁酱油”“含氟牙膏”中的铁、氟是指
A.单质 B.元素 C.原子 D.分子
13.分类法是化学学习的重要方法之一.下列各组物质按照单质、化合物、混合物的顺序排列的是( )
A.水银、碳酸钙、冰水混合物 B.液氧、水、粗盐
C.水、食盐、海水 D.钙片、氯化镁、矿泉水
14.化学概念在逻辑上存在如下图所示的关系,对下列概念间关系说法正确的是
①纯净物与混合物属于包含关系;②化合物与氧化物属于包含关系;③单质与化合物属于交叉关系;④金属元素与非金属元素属于并列关系;⑤原子与原子核属于并列关系
A.①② B.③④ C.①⑤ D.②④
15.下列物质中,属于氧化物的是( )
A.O3 B.KClO3 C.MgO D.Cu(OH)2
16.下列各组物质按单质、氧化物、混合物的顺序排列的是
A.液氧、冰水混合物、稀盐酸 B.硬铝、干冰、洁净的空气
C.水银、高锰酸钾、过氧化氢溶液 D.不锈钢、二氧化硅、汽水
二、综合题(共6题)
17.结合下列图示,回答有关问题。
(1)如图1,A微粒的化学性质与B、C、D中哪一种微粒的化学性质相似______(填序号);
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是______。
A原子序数:Z>Y
B核外电子数:X=Y
CY和Z处于同一周期
(3)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似结构和性质。下列各组微粒中属于等电子体的是________(填字母序号)。
A NH3和H2O B CO和N2 C H2O2和H2O D CO 和SO2。
18.生活中处处有化学,请回答下列问题.
(1)人体中所含最多的金属元素是________________(写名称);
(2)相对分子质量最小的氧化物________________(写化学式);
(3)自然界中最坚硬的物质是________________(写名称);
(4)通过“铜绿”性质研究实验,我们可以观察到以下现象:
①向“铜绿”中加入稀盐酸,可以发现产生大量________________,绿色粉末逐渐消失,溶液变成________________色。
②加热“铜绿”,可以发现绿色粉末变成________色,试管壁上有水珠生成。
19.图A是钾元素在元素周期表中的部分信息,图B是钾原子的结构示意图,据此回答问题。
(1)钾的相对原子质量是__________;
(2)钾原子的最外层电子数是__________;
(3)由原子核外电子层数与元素所在周期表中周期数相同可知,钾元素在元素周期表中应该排在第__________周期;
(4)该元素属于__________元素(选填 “金属”或“非金属”);
(5)该元素的原子在化学反应中容易__________电子(选填 “得到”或“失去”)。
20.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1所示,X是___________________________________________;Y是___________________________________________。
(2)从宏观角度看,汞由________________________________________组成;从微观角度看,汞由__________________________________________构成。
(3)图2是钙元素的原子结构示意图,下列结构示意图中,共有__________________________(填数字)种元素,其中与钙原子具有相似化学性质的是__________________________(填字母)。
21.化学与人类生活息息相关。
I.空气和水是人类赖以生存和发展的重要物质基础。
(1)空气中含有氮气、氧气、稀有气体等,是__________(填“纯净物”、“混合物”),人类时刻都离不开空气,是因为空气中的氧气能 _______。
(2)长期饮用纯净水对健康无益,因为纯净水中缺乏“钙、铁、锌”等人体必须的_____
A 分子 B 原子 C 离子 D 元素(填序号)。
(3)下列治理河水的措施中合理的是___
A 拆除河流中设置的围网 B 严禁在水体中电鱼、药鱼
C 疏通河道、加强水质监测 D 合理使用化肥农药,防止水体污染
II.“5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅。
(4)硅元素相关信息如图所示,据图可得到的信息是______(填字母序号)。
A 硅元素是非金属元素 B 硅元素的元素符号为Si
C 硅元素在地壳里的含量排第二位 D 硅的相对原子质量为28.09g
(5)下图是一种制备高纯硅的工艺流程图:
①反应Ⅰ所用的镁在化学反应中易______电子(填“得”或“失”),镁和SiO2发生的是否是化合反应______(填“是”或“否”);反应Ⅱ要在无氧气的环境中进行,原因是_____(答出一种即可);
②操作Ⅰ的名称是_______,进行该操作时液面应______(填“高于”或“低于”)滤纸边缘,进行该操作需要用到玻璃棒,其作用是________;
③上述已知生产流程中,可以循环利用的物质是_______。
22.下表是元素周期表中第2、3周期的元素,请回答有关问题。
(1)下列各组具有相似化学性质的元素是 _____ (填字母序号)
A Na、Cl
B O、S
C F、Cl
D Al、Ar
(2)写出一条第三周期元素原子的核外电子排布规律 _____ 。
(3)地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物的化学式为 _____ 。
(4)某离子的结构示意图为 当x-y=8时,该粒子的符号为 _____ .
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是 _____ (填字母序号)
A NO和O2 B CO和N2 C SO3和CO2 D PO43- 和SO42-
参考答案
1.D
【详解】
A、由元素周期表中提供的碘元素的部分信息及碘原子的结构示意图,可知碘的相对原子质量为126.9,原子核内质子数为53,故A正确;
B、由碘原子的结构示意图,可知碘原子核外共有5个电子层,位于第五周期,最外层有7个电子,故B正确;
C、由汉语名称“碘”,可知其为非金属元素;由碘原子的结构示意图,可知在化学反应中容易得到电子,故C正确;
D、根据化合价原则“正负化合价的代数和为零”,设KIO3中碘元素的化合价为x,则(+1)+x+3×(-2)=0,故x=+5价,故KIO3中碘元素的化合价为-1价,说法错误,故D错误。
故选D。
2.D
【详解】
在菠菜中,铁是以无机盐的形式存在的,这里的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。故选D。
3.A
【详解】
A、催化剂在化学反应前后质量和化学性质(而不是性质)都不变,故选项说法错误;B、地壳中质量分数最大的元素是氧,故选项说法正确;C、空气中体积分数最大的气体是氮气,故选项说法正确;D、只含有一种元素的物质可能是纯净物,例如氧气等,故选项说法正确。故选A。
4.C
【详解】
A、Na为钠元素的元素符号,带“钅”字旁,属于金属元素,故A错误;
B、Mg为镁元素的元素符号,带“钅”字旁,属于金属元素,故B错误;
C、S为硫元素的元素符号,带“石”字旁,属于固态非金属元素,故C正确;
D、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故D错误。故选C。
5.A
【详解】
A、同一元素的质子数相同;如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同,正确;
B、含有的质子数相同的两种粒子不一定属于同一种元素,例如氖原子和水分子质子数相同,不是同一元素,错误;
C、物质中只含有一种元素,这种物质不一定是纯净物,例如氧气和臭氧组成的混合物,错误;
D、化学变化中构成物质的分子改变,组成物质的元素一定不变,例如氧气转化为臭氧,错误。
故选A。
6.B
【详解】
A、纯净物是由相同的微粒构成的,如氯化钠是纯净物,氯化钠中只含有钠离子和氯离子,故A错误;
B、含有氧元素的化合物,不一定是氧化物,例如NaOH,其中含有氧元素,但是不属于氧化物,故B正确;
C、化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,故C错误;
D、由不同种元素组成的物质不一定是化合物,还有可能是混合物,故D错误;
故选择B
7.A
【详解】
A、Cu是金属铜的元素符号,它即可以表示铜的元素符号,又可以表示金属铜,故正确;
B、H只能表示元素符号,不能表示单质,故错误;
C、O不能表示单质,故错误;
D、N不能表示单质,故错误。故选A.
8.D
【详解】
A、氮气属于单质,五氧化二磷、干冰均属于氧化物,故A不正确;
B、红磷属于单质,冰水混合物、四氧化三铁均属于氧化物,故B不正确;
C、铁属于单质,高锰酸钾不属于氧化物,空气属于混合物,故C不正确;
D、臭氧属于单质,二氧化碳属于氧化物,牛奶属于混合物,故D正确。故选D。
9.D
【详解】
A、海水包括水、氯化钠等,属于混合物。干冰是固态的二氧化碳,是纯净物中的化合物。故A错误;
B、冰水是水的两种形态,属于同种物质,是纯净物。水银是金属汞,是单质。故B错误;
C、食醋中包括水、醋酸等,属于混合物。蒸馏水指的是水,是化合物。故C错误;
D、煤的主要成分是碳,也包括硫等其他杂质,属于混合物。金刚石是碳单质。故D正确。
故选D。
10.C
【详解】
第11号元素和第17号元素的原子核外都有三个电子层,即两种元素原子的电子层数相同,所以第11号元素和第17号元素位于元素周期表中的同一周期,故选C。
11.A
【解析】
试题分析:从图示看:图2和3都属于锶元素,因为其中的质子数都是38;图3所表示粒子的化学符号是Sr2+;锶原子的中子数为=88-38=40;锶原子的相对原子质量是87.62。故选A.
12.B
【详解】
“加铁酱油”、“含氟牙膏”等用品中的“铁”、“氟”不是以单质、分子、原子、离子等形式存在,而是指元素,故选B。
13.B
【解析】:由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物。 A. 水银是单质、碳酸钙、冰水混合物 都是化合物; B. 液氧是单质、水是化合物、粗盐是混合物;C. 水是化合物、食盐是主要成分为氯化钠的混合物、海水是混合物; D.钙片属于混合物;氯化镁属于化合物,矿泉水属于混合物。
14.D
【详解】
①物质按含有物质种类的多少可分为纯净物与混合物,是并列关系,故此选项错误;②化合物有多种元素组成,其中氧化物是含有氧元素和另外一种元素的化合物,是包含关系,故此选项正确;③纯净物按元素的含有情况可分为化合物与单质,故是并列关系,故此选项错误;④元素分为金属元素和非金属元素,因此金属元素与非金属元素属于并列关系,故此选项正确;⑤原子分为原子核和核外电子,所以原子与原子核属于包含关系,故此选项错误。故选D。
15.C
【详解】
A、O3是一种只有氧元素组成的物质,则属于单质,故错误;
B、KClO3中含有三种元素,属于化合物,但不属于氧化物,故错误;
C、MgO是一种含有Mg和O两种元素且有氧元素的化合物,则属于氧化物,故正确;
D、Cu(OH)2是由金属离子和氢氧根离子构成的化合物,则属于碱,故错误。
故选:C。
16.A
【详解】
A、液氧(液态的氧气)是由氧元素组成的纯净物,属于单质;冰水混合物中只有水,是由氢、氧两种元素组成的化合物,属于氧化物;稀盐酸是氯化氢水溶液,属于混合物。符合题意;
B、硬铝是合金,属于混合物;干冰(固态二氧化碳)是由碳、氧两种元素组成化合物,属于氧化物;洁净的空气中含有氧气、氮气等物质,属于混合物。不符合题意;
C、水银是由汞元素组成的纯净物,属于单质;高锰酸钾是由三种元素组成的化合物,不是氧化物,过氧化氢溶液中含有过氧化氢和水,属于混合物,不符合题意;
D、不锈钢是合金,属于混合物;二氧化硅是由硅、氧两种元素组成化合物,属于氧化物;汽水中含有水、二氧化碳等物质,属于混合物,不符合题意。
故选A。
17.B A、C B
【详解】
(1)粒子的最外层电子数决定其化学性质,A微粒与B微粒的最外层电子数相同,故A微粒的化学性质与B相似;
(2)A、根据元素周期表可知,原子序数:Z>Y,符合题意;
B、X与Y的最外层电子数相同,核外电子数:Y>X,不符合题意;
C、Y和Z的核外电子层数都是3,故Y和Z处于同一周期,符合题意。
故选AC。
(3)A、NH3和H2O的原子数不相同,不是等电子体,不符合题意;
B、CO和N2都有2个原子数,14个电子数,是等电子体,符合题意;
C、H2O2和H2O原子数和电子数都不相同,不是等电子体,不符合题意;
D、CO和SO2原子数和电子数都不相同,不是等电子体,不符合题意;
故选B。
18.钙; H2O; 金刚石; 气泡; 蓝绿; 黑
【详解】
(1)人体中含有最多的金属元素是钙(Ca);(2)相对分子质量最小的氧化物是水(H2O);(3)自然界最坚硬的是金刚石;(4)铜绿中加入稀盐酸会产生气泡(二氧化碳),2价铜离子为蓝绿色,所以溶液为蓝绿色,加热后Cu氧化变为氧化铜,变为黑色。
19.39.10 1 四 金属 失去
【详解】
(1)在元素周期表中,下方的数字表示该元素的相对原子质量,故填:39.10;(2)读图可知钾原子最外层电子数为1;(3)已知原子核外的电子层数与元素所在周期表中的周期数相同,镁元素的原子核外有3个电子层,则镁元素在元素周期表中应该排在第3周期;(4)镁元素带“钅”字旁,属于金属元素;(2)由镁原子结构示意图为可以看出:最外层弧线上的数字是2,最外层电子数是2,在化学反应中易失去2个电子而形成阳离子。
20.原子 原子核 汞元素 汞原子 3 B
【详解】
(1)构成物质的微粒有分子、原子、离子,所以X是原子;原子由原子核和核外电子构成,所以Y为原子核。
(2)物质由元素组成,汞是由汞元素组成的单质;汞由汞原子直接构成。
(3)元素的种类由该元素原子中质子数决定,图中A、B、C3种粒子的质子数各不相同,所以共有3种元素。
元素的化学性质由原子核外最外层电子数决定。钙原子的最外层电子数为2,化学反应中容易失去2个电子。A为氦原子的结构示意图,最外层虽然也有2个电子,但它是第一层,是一种相对稳定结构,B中最外层(第三层)上有2个电子,与钙原子化学性质相似。故选B。
21.混合物 供给呼吸 D ABCD AB 失 否 防止氢气高温时发生爆炸 过滤 低于 引流 HCl
【详解】
(1)空气中含有氮气、氧气、稀有气体等,是混合物,人类时刻都离不开空气,是因为空气中的氧气能供给呼吸。
(2)长期饮用纯净水对健康无益,因为纯净水中缺乏“钙、铁、锌”等人体必须的元素,故选D。
(3)A、拆除河流中设置的围网有利于河水治理,故A正确;
B、严禁在水体中电鱼、药鱼有利于河水治理,故B正确;
C、疏通河道、加强水质监测有利于河水治理,故C正确;
D、合理使用化肥农药,防止水体污染有利于河水治理,故D正确。故选ABCD。
(4)硅元素相关信息如图所示,据图可得到如下信息:
A、硅元素是非金属元素,正确;
B、硅元素的元素符号为Si,正确;
C、硅元素在地壳里的含量排第二位,不同从图中得到,错误;
D、硅的相对原子质量为28.09,单位错误。
故选AB。
(5)①镁的最外层电子数是2,反应Ⅰ所用的镁在化学反应中易失电子(填“得”或“失”),镁和SiO2生成氧化镁和硅,发生的不是化合反应,填“否”;反应Ⅱ要在无氧气的环境中进行,是为了防止氢气高温时发生爆炸;
②操作Ⅰ是分离难溶固体和液体,操作的名称是过滤,进行该操作时液面应低于滤纸边缘,进行该操作需要用到玻璃棒,其作用是引流;
③上述已知生产流程中,可以循环利用的物质是HCl。
22.BC 从左往右,最外层电子数依次增大(合理即可) Al2O3. S2- BD
【详解】
(1)
A、Na和Cl的最外层电子数不同,不具有相似的化学性质;
B、O和S的最外层电子数相同,具有相似的化学性质;
C、F和Cl的最外层电子数相同,具有相似的化学性质;
D、Al和Ar的最外层电子数不同,不具有相似的化学性质;
故填:BC;
(2)第三周期元素原子的核外电子排布规律是:从左往右,最外层电子数依次增大(合理即可)
故填:从左往右,最外层电子数依次增大(合理即可);
(3)地壳中含量最多的金属元素是Al元素,在化合物中显+3价;地壳中含量最多的非金属元素O元素,Al元素显正价,故氧元素在该化合物中显-2价,故这二者组成的化合物的化学式为Al2O3。
(4)当x-y=8时,说明带有的是2个单位的负电荷,y=8,该粒子的核内质子数为16,故是硫离子,故填:S2-;
(5)A.NO和O2 的原子数都是2,电子数分别是15和16,不属于等电子体;
B.CO和N2的原子数都是2,电子数都是14,属于等电子体;
C.SO3和CO2的原子数和电子数都不同,不属于等电子体;
D.PO43-和SO42-的原子个数和电子个数都相等,属于等电子体。
故选:BD。
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
