第七章 有机化合物 单元测试
文档属性
| 名称 | 第七章 有机化合物 单元测试 |

|
|
| 格式 | docx | ||
| 文件大小 | 127.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-29 00:00:00 | ||
图片预览




文档简介
第七章《有机化合物》测试卷
一、单选题(共15小题)
1.某有机物的结构简式为。下列关于该有机物的叙述中,不正确的是( )
A. 能与NaHCO3发生反应并放出二氧化碳
B. 能在催化剂作用下与HCl发生加成反应
C. 不能使酸性KMnO4溶液和溴水褪色
D. 在浓硫酸作催化剂条件下能和乙醇发生酯化反应生成酯
2.食品店里出售的冰淇淋是硬化油,它是以多种植物油为原料来制取的,制作过程发生的反应是( )
A. 水解反应
B. 取代反应
C. 加成反应
D. 氧化反应
3.维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能都特别好的氟橡胶。它的结构简式为,合成它的单体为( )
A. CH2==CF2—CF2和CF==CF3
B. CH2==CF2和CF2==CF—CF3
C. CH2==CF2—CF2==CF—CF3
D. CH2==CF2—CF2—CF==CF3
4.丁烷(C4H10)失去1个氢原子后得到丁基(—C4H9),丁基的结构共有( )
A. 2种
B. 3种
C. 4种
D. 5种
5.测得某乙酸乙酯和乙酸的混合物中含氢的质量分数为7.8%,则此混合物中含氧元素的质量分数为( )
A. 56.4%
B. 49.8%
C. 45.4%
D. 15.6%
6.青苹果汁遇碘溶液显蓝色,熟苹果能还原新制的氢氧化铜浊液,这说明( )
A. 青苹果中只含淀粉不含糖类
B. 苹果转熟时淀粉水解为单糖
C. 熟苹果中只含糖类不含淀粉
D. 苹果转熟时单糖聚合成淀粉
7.关于苯乙烯的下列叙述中,正确的是( )
A. 1 mol苯乙烯只能与1 mol氢气发生加成反应
B. 苯乙烯不能使酸性高锰酸钾溶液褪色
C. 苯乙烯不能使溴水溶液褪色
D. 苯乙烯分子中8个碳原子有可能都在同一平面上
8.以下是分离乙酸乙酯、乙酸、乙醇的混合物的流程图,图中圆括号内是适当的试剂,方括号内是适当的分离方法,方框内是有关物质的名称。下列说法正确的是( )
A. a为氢氧化钠溶液,b是盐酸
B. ①、②、③均为蒸馏
C. A是乙酸乙酯,①为分液
D. b是硫酸,②为分液
9.已知二氯苯有3种同分异构体,则四氯苯的同分异构体有( )
A. 2种
B. 3种
C. 4种
D. 5种
10.在我国的南海、东海海底已发现天然气的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”的开采,有助于解决人类面临的能源危机。下列说法不正确的是( )
A. 可燃冰的主要成分是甲烷
B. 可燃冰的形成说明甲烷易溶于水
C. 常温常压下可燃冰极易挥发
D. 可燃冰是一种极具潜力的能源
11.设阿伏加德罗常数的值为NA,下列说法正确的是( )
A. 1 mol苯乙烯中含有的C==C键数为4NA
B. 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C. 0.1 mol CnH2n+2中含有的C—C键数为0.1nNA
D. 标准状况下,2.24 L CCl4中含有的分子数为0.1NA
12.相对分子质量为198的烷烃分子式是( )
A. C12H22O2
B. C15H18
C. C16H34
D. C14H30
13.下列衣料不能用加酶洗衣粉洗涤的是( )
A. 棉织品
B. 蚕丝制品
C. 晴纶织品
D. 人造丝织品
14.下列各反应属于加成反应的是( )
A. CH4+2O2CO2+2H2O
B. CH3CH==CH2+Br2―→CH3CHBr—CH2Br
C. CH3CH2CH3+Cl2CH3CH2CH2Cl+HCl
D. CH3CH2CH2CH3CH2==CH2+CH3—CH3
15.葡萄糖的结构简式为
CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,
其对应的性质中不正确的是( )
A. 葡萄糖在一定条件下能水解
B. 可与乙酸发生取代反应
C. 能发生银镜反应
D. 葡萄糖的分子式是C6H12O6
二、实验题(共3小题)
16.将下图所示的装置放置在光亮的地方(日光没有直接照射),回答下列问题:
(1)一段时间后观察到的实验现象:量筒中________;水槽中________。
(2)饱和食盐水的pH________(填变大、变小或不变)。
(3)得到的气态产物有________、________。
(4)油状液滴的成分可能是_________________________________。
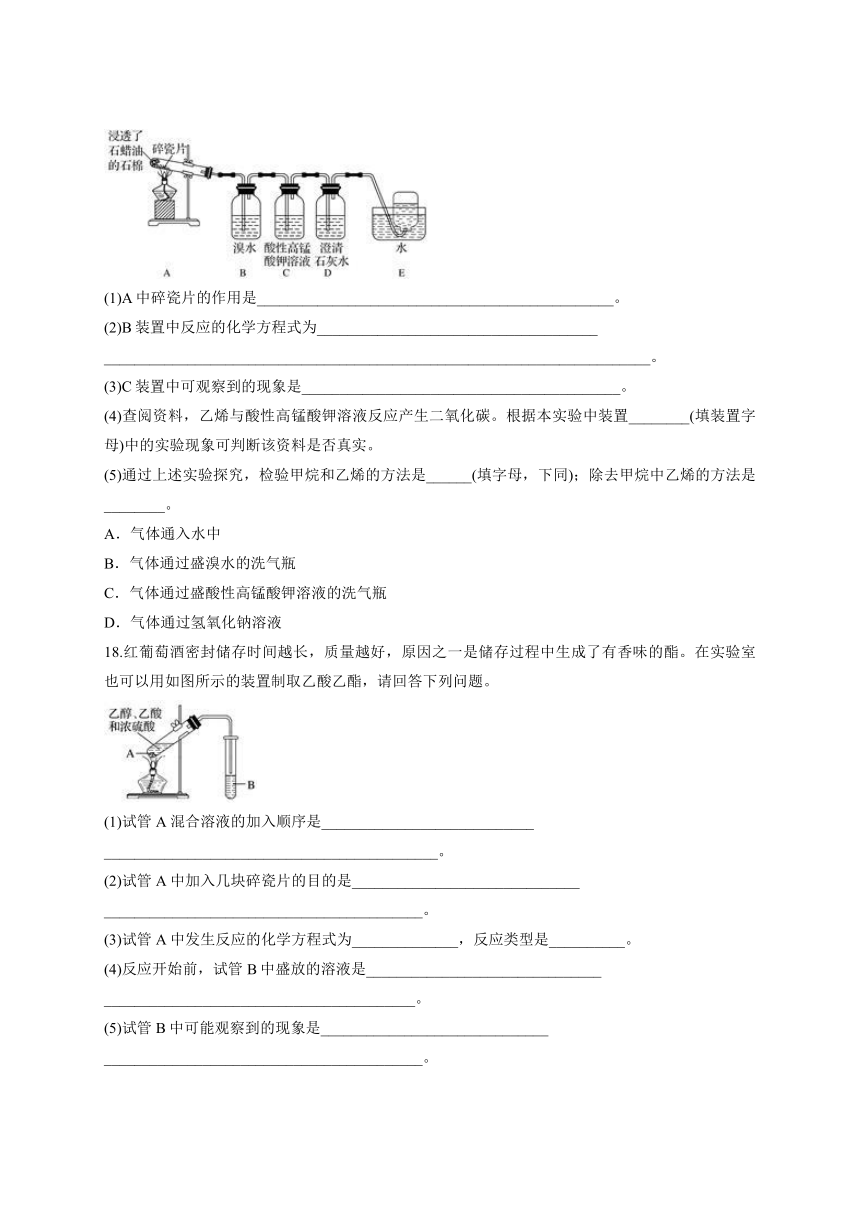
17.下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验。请回答下列问题:
(1)A中碎瓷片的作用是_______________________________________________。
(2)B装置中反应的化学方程式为_____________________________________
________________________________________________________________________。
(3)C装置中可观察到的现象是__________________________________________。
(4)查阅资料,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填装置字母)中的实验现象可判断该资料是否真实。
(5)通过上述实验探究,检验甲烷和乙烯的方法是______(填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
18.红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题。
(1)试管A混合溶液的加入顺序是____________________________
____________________________________________。
(2)试管A中加入几块碎瓷片的目的是______________________________
__________________________________________。
(3)试管A中发生反应的化学方程式为______________,反应类型是__________。
(4)反应开始前,试管B中盛放的溶液是_______________________________
_________________________________________。
(5)试管B中可能观察到的现象是______________________________
__________________________________________。
(6)将试管B中的物质分离得到乙酸乙酯,必须使用的仪器是________,具体操作是将乙酸乙酯从该仪器的________________________(填“下口放出”或“上口倒出”)。
三、计算题(共3小题)
19.某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56 L混合气体通入足量的溴水中,溴水的质量增重35 g。
(1)计算确定混合气体中烃的化学式。
(2)混合气体中两种烃的物质的量之比。
20.实验室测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。若实验时消耗2.9 mL的无水乙醇(密度为0.8 g·mL-1),测量排出水的体积后折算成标准状况下H2的体积为560 mL。根据以上数据计算乙醇分子中可被置换的氢原子个数是多少
21.(1)0.1 mol某烃完全燃烧,将燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9 g,浓碱液增重17.6 g。则该烃的分子式为________________,写出其所有可能的结构简式:__________________________________
____________。
(2)2.2 g某气态烃在O2中完全燃烧,生成6.6 g CO2和3.6 g H2O,在标准状况下,该气态烃的密度为1.964 3 g·L-1,则其分子式为_________________________。
(3)在120 ℃、101 kPa下,某气态烃和一定质量的O2的混合气体在点燃条件下完全反应后再恢复到原来的温度和压强时,气体的体积减小,则该烃分子中的氢原子个数________(填序号)。
A.小于4 B.大于4
C.等于4 D.无法判断
四、填空题(共3小题)
22.回答下问题:
(1)糖尿病是“富贵病”,请设计实验检验病人尿液中的葡萄糖,设计要求:①实验所用的化学药品是________;②实验的现象与结论是_____________________________________。
(2)鉴别三种溶液中分别含有蛋白质、淀粉和肥皂_________________________________。
23.有下列结构的物质:①CH3(CH2)3CH3
②CH3CH2CH2CH2CH3
③CH3CH2CH2CH2CH2CH3
于同系物的是________;属于同分异构体的是__________________________;
属于同种物质的是________。
A.①② B.②③
C.③④⑤⑥⑦ D.①③
E.③④⑤⑦ F.④⑥
24.写出下列各种烷烃的分子式:
(1)在标况下,相对分子质量最大的气态烷烃________。
(2)在标况下,相对分子质量最小的液态烷烃________。
(3)在标况下,相对分子质量最小的固态烷烃________。
(4)含碳质量分数最低的烷烃________。
(5)与二氧化碳密度相同的烷烃________。
(6)碳、氢质量比为5∶1的烷烃________。
答案解析
1.【答案】C
【解析】该有机物分子中含有、—COOH两种官能团,其中—COOH能和NaHCO3反应放出CO2,能在浓硫酸作催化剂条件下发生酯化反应生成酯;能使酸性KMnO4溶液褪色,也能和Br2及HCl发生加成反应。
2.【答案】C
【解析】植物油(液态油)能氢气发生加成反应,转化为硬化油冰淇淋(固态脂肪)。
3.【答案】B
【解析】由链节可知,主碳链为4个碳原子,而且都为单键,其单体必为两种含双键的物质,据加聚反应的特点,可推知两种单体分别为CH2==CF2和CF2==CF—CF3。
4.【答案】C
【解析】丁烷(C4H10)有两种结构:CH3CH2CH2CH3和H3CCHCH3CH3,它们分子中各有两种氢原子,因此失去1个氢原子后得到丁基(—C4H9)的结构共有4种。
5.【答案】C
【解析】 分析解题的基点:混合物中碳、氢原子个数比恒定。
乙酸乙酯(C4H8O2)与乙酸(C2H4O2)分子中的碳、氢原子个数比都是1∶2,碳、氢元素的质量比为6∶1,碳元素的质量分数为6×7.8%,氧元素的质量分数为1-7×7.8%= 45.4%。
6.【答案】B
【解析】青苹果中含有多糖淀粉,遇碘溶液显蓝色;苹果转熟时,部分淀粉水解转化为葡萄糖,葡萄糖具有还原性,能与新制的氢氧化铜浊液反应生成红色沉淀。
7.【答案】D
【解析】苯乙烯分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,能与溴水发生加成反应,能使酸性高锰酸钾溶液、溴水褪色;苯乙烯分子中的苯环和碳碳双键都能与氢气发生加成反应,1 mol苯乙烯最多能与4 mol氢气加成。
8.【答案】C
【解析】 分析解题的基点:乙酸乙酯(含乙醇和乙酸)的净化与分离。乙酸乙酯不溶于饱和碳酸钠溶液,乙酸和乙醇易溶于饱和碳酸钠溶液,常先加饱和碳酸钠溶液进行萃取,分液得到乙酸乙酯;然后将乙酸钠和乙醇的水溶液加热蒸馏,得到乙醇;最后在留下的残液(乙酸钠溶液)中加入稀硫酸,蒸馏得到乙酸。即a为饱和碳酸钠溶液,b为盐酸或硫酸;①为分液,②为蒸馏,③为蒸馏;A为乙酸乙酯,C为乙酸钠溶液,E为乙醇。
9.【答案】B
【解析】在二氯苯中有2个氯原子和4个氢原子,四氯苯中有4个氯原子和2个氢原子,如果把2个氢原子看成2个氯原子,4个氯原子看成4个氢原子,这样,两者的结构就完全相同,也应为3种。
10.【答案】B
【解析】可燃冰是天然气水合物,主要成分是甲烷,在海底的高压、低温条件下与水形成的水合物。常温常压下,可燃冰极易变为甲烷气体,是一种很好的清洁能源。
11.【答案】B
【解析】1 mol苯乙烯中含有的C==C键数为NA,A项错误;2.8 g乙烯和丙烯的混合气体中所含碳原子为2.8 g÷M(CH2)=0.2 mol,B项正确;0.1 mol CnH2n+2中含有的C—C键数为0.1(n-1)NA,C项错误;标准状况下,CCl4是液体,不能只根据其体积求其物质的量,D项错误。
12.【答案】D
【解析】根据烷烃的通式CnH2n+2(相对分子质量为14n+2),计算求出相对分子质量为198烷烃分子中碳原子数为14,分子式为C14H30。
13.【答案】B
【解析】酶是蛋白质,加酶洗衣粉,能将衣服上汗渍、血迹及人体排放的蛋白质分解而除去,所以衣料中主要成分是蛋白质的制品都不能用加酶洗衣粉。棉织品的主要成分是纤维素,可用加酶洗衣粉洗;加酶洗衣粉含有生物催化剂酶,可以催化蛋白质发生水解反应,蚕丝制品属于蛋白质,所以不能用加酶洗衣粉;腈纶织品的主要成分是合成纤维,可用加酶洗衣粉洗;人造丝织品的成分是一种丝质的人造纤维,属于纤维素,可用加酶洗衣粉洗。
14.【答案】B
【解析】CH4在O2中燃烧,是氧化反应,A项错误;CH3CH==CH2与Br2发生的是加成反应,B项正确;CH3CH2CH3与Cl2在光照条件下发生取代反应,C项错误;CH3CH2CH2CH3发生的是分解反应,D项错误。
15.【答案】A
【解析】葡萄糖是单糖,故不能水解。葡萄糖含有羟基,可与乙酸发生酯化反应(取代反应的一种);含有醛基,能发生银镜反应;由葡萄糖的结构简式可知,葡萄糖的分子式是C6H12O6。
16.【答案】(1)气体颜色变浅,液面上升,有油状液滴出现 有白色晶体析出
(2)变小
(3)CH3Cl HCl(或一氯甲烷、氯化氢)
(4)CH2Cl2,CHCl3,CCl4(或二氯甲烷、三氯甲烷、四氯化碳)
【解析】甲烷与氯气在光照条件下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳、氯化氢5种物质。氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,溶液的pH变小。
17.【答案】(1)催化作用 (2)CH2==CH2+Br2―→BrCH2—CH2Br
(3)溶液紫(或紫红)色褪去 (4)D (5)BC B
【解析】(1)碎瓷片可作石蜡油分解反应的催化剂。
(2)乙烯和溴水发生加成反应,反应的化学方程式为CH2==CH2+Br2―→BrCH2—CH2Br。
(3)乙烯能够被酸性高锰酸钾溶液氧化,因此现象是溶液紫红色褪去。
(4)CO2能使澄清石灰水变浑浊,如果D装置中澄清石灰水变浑浊,说明乙烯与酸性高锰酸钾溶液反应产生二氧化碳。
(5)检验甲烷和乙烯,利用乙烯能使溴水或酸性高锰酸钾溶液褪色而甲烷不能,B、C正确;除去甲烷中的乙烯,不能引入新杂质,故不能用酸性高锰酸钾溶液,因乙烯会转化为CO2气体,可以利用溴水除去乙烯,B项正确。
18.【答案】(1)先加入乙醇、再加入浓硫酸、最后加入乙酸
(2)防止液体暴沸
(3)CH3COOH+CH3CH2OHCH3COOC2H5+H2O 酯化反应(或取代反应)
(4)饱和碳酸钠溶液
(5)液面上有透明不溶于水、具有香味的油状液体生成
(6)分液漏斗 上口倒出
【解析】分析解题的基点:乙酸乙酯制取实验的相关问题。
①药品加入顺序:先加入乙醇、再加入浓硫酸、最后加入乙酸;
②浓硫酸的作用:催化剂和吸水剂;
③产品乙酸乙酯的收集与净化:饱和碳酸钠溶液的作用;
④玻璃导管不能插入碳酸钠溶液液面下:防止倒吸;
⑤观察到的现象:上层为油状液体,具有果香气味;
⑥分离乙酸乙酯的方法与仪器:分液漏斗;
⑦制取反应原理:化学方程式、可逆反应;
⑧实验装置的改进:球形干燥管(起冷凝作用并能防止倒吸)。
19.【答案】(1)CH4、C4H8
(2)3∶1
【解析】混合气体的平均相对分子质量为13×2=26,必有甲烷,混合气体的物质的量为56 L÷22.4 L·mol-1=2.5 mol,混合气体的质量为2.5 mol×26 g·mol-1=65 g,甲烷的物质的量为(65 g-35 g)÷16 g·mol-1=1.875 mol,
设烯烃的分子式为CnH2n,
(2.5 mol-1.875 mol)×14ng·mol-1=35 g,
解得n=4,化学式为C4H8,
甲烷与丁烯的物质的量之比为1.875 mol∶(2.5 mol-1.875 mol)=3∶1
20.【答案】乙醇分子中的6个氢原子中只有1个可被置换。
【解析】设生成1 mol H2需C2H6O的物质的量为x
C2H6O ~ H2
x 22 400 mL
0.05 mol 560 mL
x≈ 2
说明生成1 mol H2需2 mol乙醇跟Na反应,也就是说一个乙醇分子中的6个氢原子中
只有1个可被置换。
21.【答案】(1)C4H10 CH3—CH2—CH2—CH3、
(2)C3H8 (3)A
【解析】(1)0.1 mol该烃中所含碳原子的物质的量为n(C)==0.4 mol,所含氢原子的物质的量为n(H)=×2=1 mol,则1 mol该烃分子中含4 mol碳原子、10 mol氢原子,即其分子式为C4H10。该烃的结构简式有2种:,
(2)该气态烃的摩尔质量为22.4 L·mol-1×1.964 3 g·L-1≈44 g·mol-1,即相对分子质量为44,该气态烃中n(C)∶n(H)=()∶(×2)=3∶8,即最简式为C3H8,因该气态烃的相对分子质量为44,故该烃的分子式为C3H8。
(3)设该烃的分子式为CxHy,则有CxHy+(x+)O2xCO2+H2O,因为反应后气体的体积减小,则1+x+>x+,即y<4。
22.【答案】(1)①新制氢氧化铜悬浊液(或银氨溶液) ②产生红色沉淀(或产生银镜),证明含有醛基
(2)分别取少量三种溶液,滴加碘水变蓝的是淀粉溶液,其余两种溶液同时加热,生产沉淀的是蛋白质,剩余的是肥皂溶液
【解析】(1)“糖尿病”人的尿样中能检查出葡萄糖,葡萄糖中含有醛基,通过检验醛基即可检验葡萄糖,加入新制的氢氧化铜悬浊液,加热后,若有红色沉淀产生,说明含有醛基。
(2)淀粉遇碘水变蓝色;肥皂的成分是硬脂酸钠,能与酸发生反应生成不溶于水的硬脂酸沉淀;加热时,蛋白质能变性产生沉淀。
23.【答案】BD E AF
【解析】7种物质均为烷烃,若碳原子数不同,则互为同系物;若碳原子数相同,而结构不同,则互为同分异构体;若碳原子数相同,且结构也相同,则为同一种物质。7种物质的分子式分别为①C5H12、②C5H12、③C6H14、④C6H14、⑤C6H14、⑥C6H14、⑦C6H14。所以①②中任一物质与③④⑤⑥⑦中任一物质均属于同系物;①②结构相同,属于同种物质,④⑥结构相同,属于同种物质;③④⑤⑦或③⑤⑥⑦互为同分异构体。
24.【答案】(1)C4H10 (2)C5H12 (3)C17H36 (4)CH4 (5)C3H8 (6)C5H12
【解析】①相对分子质量最大的气态烷烃是丁烷,相对分子质量最小的液态烷烃是戊烷,相对分子质量最小的固态烷烃是十七烷。
②烷烃随着分子中碳原子数的增加,其含碳量增大,故含碳质量分数最低的是甲烷。
③根据烷烃通式确定分子式:12n+2n+2=44,n=3;12n∶(2n+2)=5∶1,n=5。
一、单选题(共15小题)
1.某有机物的结构简式为。下列关于该有机物的叙述中,不正确的是( )
A. 能与NaHCO3发生反应并放出二氧化碳
B. 能在催化剂作用下与HCl发生加成反应
C. 不能使酸性KMnO4溶液和溴水褪色
D. 在浓硫酸作催化剂条件下能和乙醇发生酯化反应生成酯
2.食品店里出售的冰淇淋是硬化油,它是以多种植物油为原料来制取的,制作过程发生的反应是( )
A. 水解反应
B. 取代反应
C. 加成反应
D. 氧化反应
3.维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能都特别好的氟橡胶。它的结构简式为,合成它的单体为( )
A. CH2==CF2—CF2和CF==CF3
B. CH2==CF2和CF2==CF—CF3
C. CH2==CF2—CF2==CF—CF3
D. CH2==CF2—CF2—CF==CF3
4.丁烷(C4H10)失去1个氢原子后得到丁基(—C4H9),丁基的结构共有( )
A. 2种
B. 3种
C. 4种
D. 5种
5.测得某乙酸乙酯和乙酸的混合物中含氢的质量分数为7.8%,则此混合物中含氧元素的质量分数为( )
A. 56.4%
B. 49.8%
C. 45.4%
D. 15.6%
6.青苹果汁遇碘溶液显蓝色,熟苹果能还原新制的氢氧化铜浊液,这说明( )
A. 青苹果中只含淀粉不含糖类
B. 苹果转熟时淀粉水解为单糖
C. 熟苹果中只含糖类不含淀粉
D. 苹果转熟时单糖聚合成淀粉
7.关于苯乙烯的下列叙述中,正确的是( )
A. 1 mol苯乙烯只能与1 mol氢气发生加成反应
B. 苯乙烯不能使酸性高锰酸钾溶液褪色
C. 苯乙烯不能使溴水溶液褪色
D. 苯乙烯分子中8个碳原子有可能都在同一平面上
8.以下是分离乙酸乙酯、乙酸、乙醇的混合物的流程图,图中圆括号内是适当的试剂,方括号内是适当的分离方法,方框内是有关物质的名称。下列说法正确的是( )
A. a为氢氧化钠溶液,b是盐酸
B. ①、②、③均为蒸馏
C. A是乙酸乙酯,①为分液
D. b是硫酸,②为分液
9.已知二氯苯有3种同分异构体,则四氯苯的同分异构体有( )
A. 2种
B. 3种
C. 4种
D. 5种
10.在我国的南海、东海海底已发现天然气的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”的开采,有助于解决人类面临的能源危机。下列说法不正确的是( )
A. 可燃冰的主要成分是甲烷
B. 可燃冰的形成说明甲烷易溶于水
C. 常温常压下可燃冰极易挥发
D. 可燃冰是一种极具潜力的能源
11.设阿伏加德罗常数的值为NA,下列说法正确的是( )
A. 1 mol苯乙烯中含有的C==C键数为4NA
B. 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C. 0.1 mol CnH2n+2中含有的C—C键数为0.1nNA
D. 标准状况下,2.24 L CCl4中含有的分子数为0.1NA
12.相对分子质量为198的烷烃分子式是( )
A. C12H22O2
B. C15H18
C. C16H34
D. C14H30
13.下列衣料不能用加酶洗衣粉洗涤的是( )
A. 棉织品
B. 蚕丝制品
C. 晴纶织品
D. 人造丝织品
14.下列各反应属于加成反应的是( )
A. CH4+2O2CO2+2H2O
B. CH3CH==CH2+Br2―→CH3CHBr—CH2Br
C. CH3CH2CH3+Cl2CH3CH2CH2Cl+HCl
D. CH3CH2CH2CH3CH2==CH2+CH3—CH3
15.葡萄糖的结构简式为
CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,
其对应的性质中不正确的是( )
A. 葡萄糖在一定条件下能水解
B. 可与乙酸发生取代反应
C. 能发生银镜反应
D. 葡萄糖的分子式是C6H12O6
二、实验题(共3小题)
16.将下图所示的装置放置在光亮的地方(日光没有直接照射),回答下列问题:
(1)一段时间后观察到的实验现象:量筒中________;水槽中________。
(2)饱和食盐水的pH________(填变大、变小或不变)。
(3)得到的气态产物有________、________。
(4)油状液滴的成分可能是_________________________________。
17.下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验。请回答下列问题:
(1)A中碎瓷片的作用是_______________________________________________。
(2)B装置中反应的化学方程式为_____________________________________
________________________________________________________________________。
(3)C装置中可观察到的现象是__________________________________________。
(4)查阅资料,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填装置字母)中的实验现象可判断该资料是否真实。
(5)通过上述实验探究,检验甲烷和乙烯的方法是______(填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
18.红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题。
(1)试管A混合溶液的加入顺序是____________________________
____________________________________________。
(2)试管A中加入几块碎瓷片的目的是______________________________
__________________________________________。
(3)试管A中发生反应的化学方程式为______________,反应类型是__________。
(4)反应开始前,试管B中盛放的溶液是_______________________________
_________________________________________。
(5)试管B中可能观察到的现象是______________________________
__________________________________________。
(6)将试管B中的物质分离得到乙酸乙酯,必须使用的仪器是________,具体操作是将乙酸乙酯从该仪器的________________________(填“下口放出”或“上口倒出”)。
三、计算题(共3小题)
19.某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56 L混合气体通入足量的溴水中,溴水的质量增重35 g。
(1)计算确定混合气体中烃的化学式。
(2)混合气体中两种烃的物质的量之比。
20.实验室测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。若实验时消耗2.9 mL的无水乙醇(密度为0.8 g·mL-1),测量排出水的体积后折算成标准状况下H2的体积为560 mL。根据以上数据计算乙醇分子中可被置换的氢原子个数是多少
21.(1)0.1 mol某烃完全燃烧,将燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9 g,浓碱液增重17.6 g。则该烃的分子式为________________,写出其所有可能的结构简式:__________________________________
____________。
(2)2.2 g某气态烃在O2中完全燃烧,生成6.6 g CO2和3.6 g H2O,在标准状况下,该气态烃的密度为1.964 3 g·L-1,则其分子式为_________________________。
(3)在120 ℃、101 kPa下,某气态烃和一定质量的O2的混合气体在点燃条件下完全反应后再恢复到原来的温度和压强时,气体的体积减小,则该烃分子中的氢原子个数________(填序号)。
A.小于4 B.大于4
C.等于4 D.无法判断
四、填空题(共3小题)
22.回答下问题:
(1)糖尿病是“富贵病”,请设计实验检验病人尿液中的葡萄糖,设计要求:①实验所用的化学药品是________;②实验的现象与结论是_____________________________________。
(2)鉴别三种溶液中分别含有蛋白质、淀粉和肥皂_________________________________。
23.有下列结构的物质:①CH3(CH2)3CH3
②CH3CH2CH2CH2CH3
③CH3CH2CH2CH2CH2CH3
于同系物的是________;属于同分异构体的是__________________________;
属于同种物质的是________。
A.①② B.②③
C.③④⑤⑥⑦ D.①③
E.③④⑤⑦ F.④⑥
24.写出下列各种烷烃的分子式:
(1)在标况下,相对分子质量最大的气态烷烃________。
(2)在标况下,相对分子质量最小的液态烷烃________。
(3)在标况下,相对分子质量最小的固态烷烃________。
(4)含碳质量分数最低的烷烃________。
(5)与二氧化碳密度相同的烷烃________。
(6)碳、氢质量比为5∶1的烷烃________。
答案解析
1.【答案】C
【解析】该有机物分子中含有、—COOH两种官能团,其中—COOH能和NaHCO3反应放出CO2,能在浓硫酸作催化剂条件下发生酯化反应生成酯;能使酸性KMnO4溶液褪色,也能和Br2及HCl发生加成反应。
2.【答案】C
【解析】植物油(液态油)能氢气发生加成反应,转化为硬化油冰淇淋(固态脂肪)。
3.【答案】B
【解析】由链节可知,主碳链为4个碳原子,而且都为单键,其单体必为两种含双键的物质,据加聚反应的特点,可推知两种单体分别为CH2==CF2和CF2==CF—CF3。
4.【答案】C
【解析】丁烷(C4H10)有两种结构:CH3CH2CH2CH3和H3CCHCH3CH3,它们分子中各有两种氢原子,因此失去1个氢原子后得到丁基(—C4H9)的结构共有4种。
5.【答案】C
【解析】 分析解题的基点:混合物中碳、氢原子个数比恒定。
乙酸乙酯(C4H8O2)与乙酸(C2H4O2)分子中的碳、氢原子个数比都是1∶2,碳、氢元素的质量比为6∶1,碳元素的质量分数为6×7.8%,氧元素的质量分数为1-7×7.8%= 45.4%。
6.【答案】B
【解析】青苹果中含有多糖淀粉,遇碘溶液显蓝色;苹果转熟时,部分淀粉水解转化为葡萄糖,葡萄糖具有还原性,能与新制的氢氧化铜浊液反应生成红色沉淀。
7.【答案】D
【解析】苯乙烯分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,能与溴水发生加成反应,能使酸性高锰酸钾溶液、溴水褪色;苯乙烯分子中的苯环和碳碳双键都能与氢气发生加成反应,1 mol苯乙烯最多能与4 mol氢气加成。
8.【答案】C
【解析】 分析解题的基点:乙酸乙酯(含乙醇和乙酸)的净化与分离。乙酸乙酯不溶于饱和碳酸钠溶液,乙酸和乙醇易溶于饱和碳酸钠溶液,常先加饱和碳酸钠溶液进行萃取,分液得到乙酸乙酯;然后将乙酸钠和乙醇的水溶液加热蒸馏,得到乙醇;最后在留下的残液(乙酸钠溶液)中加入稀硫酸,蒸馏得到乙酸。即a为饱和碳酸钠溶液,b为盐酸或硫酸;①为分液,②为蒸馏,③为蒸馏;A为乙酸乙酯,C为乙酸钠溶液,E为乙醇。
9.【答案】B
【解析】在二氯苯中有2个氯原子和4个氢原子,四氯苯中有4个氯原子和2个氢原子,如果把2个氢原子看成2个氯原子,4个氯原子看成4个氢原子,这样,两者的结构就完全相同,也应为3种。
10.【答案】B
【解析】可燃冰是天然气水合物,主要成分是甲烷,在海底的高压、低温条件下与水形成的水合物。常温常压下,可燃冰极易变为甲烷气体,是一种很好的清洁能源。
11.【答案】B
【解析】1 mol苯乙烯中含有的C==C键数为NA,A项错误;2.8 g乙烯和丙烯的混合气体中所含碳原子为2.8 g÷M(CH2)=0.2 mol,B项正确;0.1 mol CnH2n+2中含有的C—C键数为0.1(n-1)NA,C项错误;标准状况下,CCl4是液体,不能只根据其体积求其物质的量,D项错误。
12.【答案】D
【解析】根据烷烃的通式CnH2n+2(相对分子质量为14n+2),计算求出相对分子质量为198烷烃分子中碳原子数为14,分子式为C14H30。
13.【答案】B
【解析】酶是蛋白质,加酶洗衣粉,能将衣服上汗渍、血迹及人体排放的蛋白质分解而除去,所以衣料中主要成分是蛋白质的制品都不能用加酶洗衣粉。棉织品的主要成分是纤维素,可用加酶洗衣粉洗;加酶洗衣粉含有生物催化剂酶,可以催化蛋白质发生水解反应,蚕丝制品属于蛋白质,所以不能用加酶洗衣粉;腈纶织品的主要成分是合成纤维,可用加酶洗衣粉洗;人造丝织品的成分是一种丝质的人造纤维,属于纤维素,可用加酶洗衣粉洗。
14.【答案】B
【解析】CH4在O2中燃烧,是氧化反应,A项错误;CH3CH==CH2与Br2发生的是加成反应,B项正确;CH3CH2CH3与Cl2在光照条件下发生取代反应,C项错误;CH3CH2CH2CH3发生的是分解反应,D项错误。
15.【答案】A
【解析】葡萄糖是单糖,故不能水解。葡萄糖含有羟基,可与乙酸发生酯化反应(取代反应的一种);含有醛基,能发生银镜反应;由葡萄糖的结构简式可知,葡萄糖的分子式是C6H12O6。
16.【答案】(1)气体颜色变浅,液面上升,有油状液滴出现 有白色晶体析出
(2)变小
(3)CH3Cl HCl(或一氯甲烷、氯化氢)
(4)CH2Cl2,CHCl3,CCl4(或二氯甲烷、三氯甲烷、四氯化碳)
【解析】甲烷与氯气在光照条件下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳、氯化氢5种物质。氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,溶液的pH变小。
17.【答案】(1)催化作用 (2)CH2==CH2+Br2―→BrCH2—CH2Br
(3)溶液紫(或紫红)色褪去 (4)D (5)BC B
【解析】(1)碎瓷片可作石蜡油分解反应的催化剂。
(2)乙烯和溴水发生加成反应,反应的化学方程式为CH2==CH2+Br2―→BrCH2—CH2Br。
(3)乙烯能够被酸性高锰酸钾溶液氧化,因此现象是溶液紫红色褪去。
(4)CO2能使澄清石灰水变浑浊,如果D装置中澄清石灰水变浑浊,说明乙烯与酸性高锰酸钾溶液反应产生二氧化碳。
(5)检验甲烷和乙烯,利用乙烯能使溴水或酸性高锰酸钾溶液褪色而甲烷不能,B、C正确;除去甲烷中的乙烯,不能引入新杂质,故不能用酸性高锰酸钾溶液,因乙烯会转化为CO2气体,可以利用溴水除去乙烯,B项正确。
18.【答案】(1)先加入乙醇、再加入浓硫酸、最后加入乙酸
(2)防止液体暴沸
(3)CH3COOH+CH3CH2OHCH3COOC2H5+H2O 酯化反应(或取代反应)
(4)饱和碳酸钠溶液
(5)液面上有透明不溶于水、具有香味的油状液体生成
(6)分液漏斗 上口倒出
【解析】分析解题的基点:乙酸乙酯制取实验的相关问题。
①药品加入顺序:先加入乙醇、再加入浓硫酸、最后加入乙酸;
②浓硫酸的作用:催化剂和吸水剂;
③产品乙酸乙酯的收集与净化:饱和碳酸钠溶液的作用;
④玻璃导管不能插入碳酸钠溶液液面下:防止倒吸;
⑤观察到的现象:上层为油状液体,具有果香气味;
⑥分离乙酸乙酯的方法与仪器:分液漏斗;
⑦制取反应原理:化学方程式、可逆反应;
⑧实验装置的改进:球形干燥管(起冷凝作用并能防止倒吸)。
19.【答案】(1)CH4、C4H8
(2)3∶1
【解析】混合气体的平均相对分子质量为13×2=26,必有甲烷,混合气体的物质的量为56 L÷22.4 L·mol-1=2.5 mol,混合气体的质量为2.5 mol×26 g·mol-1=65 g,甲烷的物质的量为(65 g-35 g)÷16 g·mol-1=1.875 mol,
设烯烃的分子式为CnH2n,
(2.5 mol-1.875 mol)×14ng·mol-1=35 g,
解得n=4,化学式为C4H8,
甲烷与丁烯的物质的量之比为1.875 mol∶(2.5 mol-1.875 mol)=3∶1
20.【答案】乙醇分子中的6个氢原子中只有1个可被置换。
【解析】设生成1 mol H2需C2H6O的物质的量为x
C2H6O ~ H2
x 22 400 mL
0.05 mol 560 mL
x≈ 2
说明生成1 mol H2需2 mol乙醇跟Na反应,也就是说一个乙醇分子中的6个氢原子中
只有1个可被置换。
21.【答案】(1)C4H10 CH3—CH2—CH2—CH3、
(2)C3H8 (3)A
【解析】(1)0.1 mol该烃中所含碳原子的物质的量为n(C)==0.4 mol,所含氢原子的物质的量为n(H)=×2=1 mol,则1 mol该烃分子中含4 mol碳原子、10 mol氢原子,即其分子式为C4H10。该烃的结构简式有2种:,
(2)该气态烃的摩尔质量为22.4 L·mol-1×1.964 3 g·L-1≈44 g·mol-1,即相对分子质量为44,该气态烃中n(C)∶n(H)=()∶(×2)=3∶8,即最简式为C3H8,因该气态烃的相对分子质量为44,故该烃的分子式为C3H8。
(3)设该烃的分子式为CxHy,则有CxHy+(x+)O2xCO2+H2O,因为反应后气体的体积减小,则1+x+>x+,即y<4。
22.【答案】(1)①新制氢氧化铜悬浊液(或银氨溶液) ②产生红色沉淀(或产生银镜),证明含有醛基
(2)分别取少量三种溶液,滴加碘水变蓝的是淀粉溶液,其余两种溶液同时加热,生产沉淀的是蛋白质,剩余的是肥皂溶液
【解析】(1)“糖尿病”人的尿样中能检查出葡萄糖,葡萄糖中含有醛基,通过检验醛基即可检验葡萄糖,加入新制的氢氧化铜悬浊液,加热后,若有红色沉淀产生,说明含有醛基。
(2)淀粉遇碘水变蓝色;肥皂的成分是硬脂酸钠,能与酸发生反应生成不溶于水的硬脂酸沉淀;加热时,蛋白质能变性产生沉淀。
23.【答案】BD E AF
【解析】7种物质均为烷烃,若碳原子数不同,则互为同系物;若碳原子数相同,而结构不同,则互为同分异构体;若碳原子数相同,且结构也相同,则为同一种物质。7种物质的分子式分别为①C5H12、②C5H12、③C6H14、④C6H14、⑤C6H14、⑥C6H14、⑦C6H14。所以①②中任一物质与③④⑤⑥⑦中任一物质均属于同系物;①②结构相同,属于同种物质,④⑥结构相同,属于同种物质;③④⑤⑦或③⑤⑥⑦互为同分异构体。
24.【答案】(1)C4H10 (2)C5H12 (3)C17H36 (4)CH4 (5)C3H8 (6)C5H12
【解析】①相对分子质量最大的气态烷烃是丁烷,相对分子质量最小的液态烷烃是戊烷,相对分子质量最小的固态烷烃是十七烷。
②烷烃随着分子中碳原子数的增加,其含碳量增大,故含碳质量分数最低的是甲烷。
③根据烷烃通式确定分子式:12n+2n+2=44,n=3;12n∶(2n+2)=5∶1,n=5。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
