第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 366.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-28 00:00:00 | ||
图片预览


文档简介
人教版九年级化学下册
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题3分,共36分)
1.化学让我们鉴赏了溶液的颜色美,下列物质加入水中能形成有色溶液的是( )
A.碳酸钙 B.高锰酸钾 C.植物油 D.氯化钠
2.下列有关溶液的说法正确的是( )
A. 将植物油加入水中搅拌,可得到溶液
B. 溶液一定是无色透明的液体
C. 蔗糖溶液中,蔗糖是溶质,水是溶剂
D. 饱和溶液中一定不能再溶解其他物质
3.实验室配制氯化钠溶液的操作中,正确的是( )
4.下列加速溶解的措施中,能改变固体溶解度的是( )
A. 把固体研细 B. 加热 C. 搅拌 D.振荡
5.在一瓶NaCl饱和溶液中,当温度不变时,加入少量NaCl晶体,则( )
A. 溶液的质量增大 B. 晶体的质量不变
C. 晶体的质量增大 D. 晶体溶解一部分
6.甲是60 ℃的蔗糖溶液,按如图所示进行操作,以下分析错误的是( )
A. 甲一定是不饱和溶液
B. 丙和丁一定是饱和溶液
C. 乙的溶质质量分数一定比甲大
D. 甲和丙的溶质质量分数一定不相等
7.常温下,对100 mL氯化钠饱和溶液进行如图所示实验。下列分析错误的是( )
A. 实验1后,甲、乙中溶液的溶质质量分数相等
B. 实验2后,乙中比甲中氯化钠的溶解度大
C. 实验2后,甲中溶液为氯化钠的不饱和溶液
D. 实验2后,甲、乙中溶液所含溶质质量相等
8.下列说法正确的是( )
A.均一.稳定的液体都是溶液
B.稀溶液一定是不饱和的溶液
C.悬浊液.乳浊液是不均匀的.不稳定的混合物,静置分层
D.澄清的石灰水中通入适量的二氧化碳后形成的液体为溶液
9.若研究温度对食盐溶解快慢的影响,应选用进行对照实验的两个装置是( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
10.下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是( )
温度/℃ 0 10 20 T 30 40 50
甲 13.3 20.9 31.6 39.1 45.8 63.9 85.5
乙 29.4 33.3 37.2 39.1 41.1 45.8 50.4
丙 35.7 35.8 36.0 36.2 36.3 36.6 37.0
A.三种物质的溶解度大小:甲>乙>丙
B.随着温度变化,甲的溶解度变化最小
C.30 ℃时,100 g丙的饱和溶液中,溶质的质量为36.3 g
D.分别将50 ℃时甲、乙的饱和溶液降温至T ℃,两种溶液中溶质的质量分数相等
11.如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是( )
A.t1℃时,等质量的甲、丙溶液中所含溶质的质量分数为丙>甲
B.t2℃时,20 g丙溶解于50 g水中能形成70 g溶液
C.分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙
D.若要将组成在N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
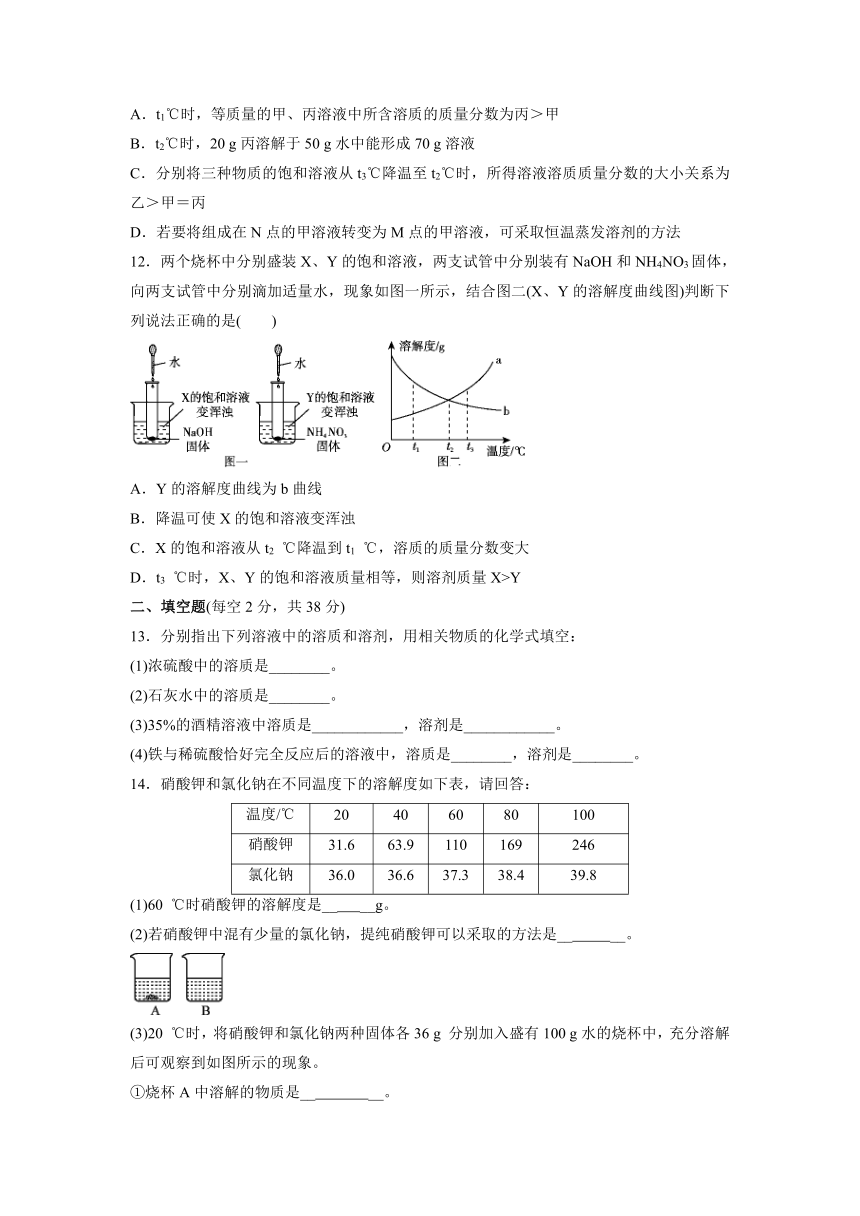
12.两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二(X、Y的溶解度曲线图)判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2 ℃降温到t1 ℃,溶质的质量分数变大
D.t3 ℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
二、填空题(每空2分,共38分)
13.分别指出下列溶液中的溶质和溶剂,用相关物质的化学式填空:
(1)浓硫酸中的溶质是________。
(2)石灰水中的溶质是________。
(3)35%的酒精溶液中溶质是____________,溶剂是____________。
(4)铁与稀硫酸恰好完全反应后的溶液中,溶质是________,溶剂是________。
14.硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答:
温度/℃ 20 40 60 80 100
硝酸钾 31.6 63.9 110 169 246
氯化钠 36.0 36.6 37.3 38.4 39.8
(1)60 ℃时硝酸钾的溶解度是__ __g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是__ __。
(3)20 ℃时,将硝酸钾和氯化钠两种固体各36 g 分别加入盛有100 g水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是__ __。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解,溶液变为饱和溶液,则溶液中溶质的质量分数__ __(填“变大”“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80 ℃,则A、B中溶质的质量__ __(填“一定”或“不一定”)相等。
15.下表是KNO3 、NaCl在不同温度下的溶解度:
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
KNO3/g 13.3 20.9 32 45.8 64 85.5 110 138 169 202 246
NaCl/g 35.7 35.8 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8
(1)以上两种物质的溶解度受温度变化影响较小的是________。
(2)30 ℃时,KNO3 的溶解度是________g。
(3)KNO3 溶液中含有少量NaCl时,可通过________________的方法提纯KNO3。
(4)对(3)析出的晶体和剩余溶液描述正确的是________(填写编号)。
Ⅰ.剩余溶液一定是KNO3的饱和溶液
Ⅱ.剩余溶液一定是NaCl溶液
Ⅲ.上述方法可以将两者完全分离
Ⅳ.析出的晶体中一定只含有KNO3
16.已知甲物质的溶解度与温度的关系如下表所示:
温度/℃ 10 20 30 40
溶解度/g 10.0 18.0 36.0 56.0
按如图步骤进行操作:
(1)甲属于_________ (填“易”或“可”)溶性物质,它的溶解度随温度的升高而增大 。
(2)在A~E的溶液中,属于不饱和溶液的是___________ (填字母,下同),与B溶液的溶质质量分数相同的是___________ 。
(3)要使E中未溶的甲物质全部溶解,至少需要加入30 ℃的水________ g。
三、实验探究题(每空2分,共20分)
17.下列是“粗盐中难溶性杂质的去除”的实验操作示意图:
(1)仪器a的名称: ________。
(2)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是_______________________。
(3)操作B中还需用到的仪器是____________________。
(4)操作C中,倒入液体时液面要低于滤纸边缘,主要是为了防止______(填序号)。
A. 过滤速度慢
B. 滤纸破损
C. 不溶性杂质未经过滤就进入滤液
(5)操作C完成后滤液中还含有少量的氯化钙,写出除去氯化钙的化学方程式: _________________________________________________________________。
(6)图中部分操作有错误,其中会导致精盐产率明显偏低的操作编号是________,说明引起产率偏低的原因__________________。
18.根据下面实验报告填空:
探究目的: 。
实验用品:药匙、烧杯、玻璃棒、温度计、氢氧化钠固体、水。
操作过程如下图所示:
(1)图示③中的操作存在一处错误,应改正为: 。
(2)图示③中错误操作改正后,上述实验能否达到实验目的?为什么?
、
四、综合应用题(共6分)
19. 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如右图所示。试计算:
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液中溶质的质量分数。
参考答案
一、选择题
1-6BCDBBD 7-12BCBDDD
二、填空题
13. (1)H2SO4 (2)Ca(OH)2 (3)C2H5OH H2O (4)FeSO4 H2O
14. (1)110 (2)降温结晶 (3)①硝酸钾 ②不变 ③一定
15. (1)NaCl (2)45. 8 (3)降温结晶(或冷却热饱和溶液) (4)Ⅰ
15. (1)易 (2)C、D A (3)50
三、实验探究题
17. (1)铁架台
(2)防止药品腐蚀托盘, 使称量更准确
(3)胶头滴管
(4)C
(5)Na2CO3+CaCl2===CaCO3↓+2NaCl
(6)D D中未用玻璃棒搅拌, 造成液滴飞溅, 精盐的产率偏低
18. 探究目的:物质溶解时,溶液的温度有何变化?
(1)用玻璃棒搅拌至全部溶解
(2)不能 应先测量水在溶解前的温度。
四、综合应用题
19. 解:设锌质量为x,H2SO4质量为y,ZnSO4质量为z
Zn + H2SO4══ ZnSO4 + H2↑
65 98 161 2
x y z 0.1g
65:2=X:0.1g x=3.25g
65:98=y:0.1g y=4.9g
65:161=z:0.1g z=8.05g
(1)即黄铜中Cu的质量分数为×100%=66.7%
(2) 4.9g / 9.8% =50g
(3) ×100%=15.1%
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题3分,共36分)
1.化学让我们鉴赏了溶液的颜色美,下列物质加入水中能形成有色溶液的是( )
A.碳酸钙 B.高锰酸钾 C.植物油 D.氯化钠
2.下列有关溶液的说法正确的是( )
A. 将植物油加入水中搅拌,可得到溶液
B. 溶液一定是无色透明的液体
C. 蔗糖溶液中,蔗糖是溶质,水是溶剂
D. 饱和溶液中一定不能再溶解其他物质
3.实验室配制氯化钠溶液的操作中,正确的是( )
4.下列加速溶解的措施中,能改变固体溶解度的是( )
A. 把固体研细 B. 加热 C. 搅拌 D.振荡
5.在一瓶NaCl饱和溶液中,当温度不变时,加入少量NaCl晶体,则( )
A. 溶液的质量增大 B. 晶体的质量不变
C. 晶体的质量增大 D. 晶体溶解一部分
6.甲是60 ℃的蔗糖溶液,按如图所示进行操作,以下分析错误的是( )
A. 甲一定是不饱和溶液
B. 丙和丁一定是饱和溶液
C. 乙的溶质质量分数一定比甲大
D. 甲和丙的溶质质量分数一定不相等
7.常温下,对100 mL氯化钠饱和溶液进行如图所示实验。下列分析错误的是( )
A. 实验1后,甲、乙中溶液的溶质质量分数相等
B. 实验2后,乙中比甲中氯化钠的溶解度大
C. 实验2后,甲中溶液为氯化钠的不饱和溶液
D. 实验2后,甲、乙中溶液所含溶质质量相等
8.下列说法正确的是( )
A.均一.稳定的液体都是溶液
B.稀溶液一定是不饱和的溶液
C.悬浊液.乳浊液是不均匀的.不稳定的混合物,静置分层
D.澄清的石灰水中通入适量的二氧化碳后形成的液体为溶液
9.若研究温度对食盐溶解快慢的影响,应选用进行对照实验的两个装置是( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
10.下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是( )
温度/℃ 0 10 20 T 30 40 50
甲 13.3 20.9 31.6 39.1 45.8 63.9 85.5
乙 29.4 33.3 37.2 39.1 41.1 45.8 50.4
丙 35.7 35.8 36.0 36.2 36.3 36.6 37.0
A.三种物质的溶解度大小:甲>乙>丙
B.随着温度变化,甲的溶解度变化最小
C.30 ℃时,100 g丙的饱和溶液中,溶质的质量为36.3 g
D.分别将50 ℃时甲、乙的饱和溶液降温至T ℃,两种溶液中溶质的质量分数相等
11.如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是( )
A.t1℃时,等质量的甲、丙溶液中所含溶质的质量分数为丙>甲
B.t2℃时,20 g丙溶解于50 g水中能形成70 g溶液
C.分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙
D.若要将组成在N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
12.两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二(X、Y的溶解度曲线图)判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2 ℃降温到t1 ℃,溶质的质量分数变大
D.t3 ℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
二、填空题(每空2分,共38分)
13.分别指出下列溶液中的溶质和溶剂,用相关物质的化学式填空:
(1)浓硫酸中的溶质是________。
(2)石灰水中的溶质是________。
(3)35%的酒精溶液中溶质是____________,溶剂是____________。
(4)铁与稀硫酸恰好完全反应后的溶液中,溶质是________,溶剂是________。
14.硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答:
温度/℃ 20 40 60 80 100
硝酸钾 31.6 63.9 110 169 246
氯化钠 36.0 36.6 37.3 38.4 39.8
(1)60 ℃时硝酸钾的溶解度是__ __g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是__ __。
(3)20 ℃时,将硝酸钾和氯化钠两种固体各36 g 分别加入盛有100 g水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是__ __。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解,溶液变为饱和溶液,则溶液中溶质的质量分数__ __(填“变大”“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80 ℃,则A、B中溶质的质量__ __(填“一定”或“不一定”)相等。
15.下表是KNO3 、NaCl在不同温度下的溶解度:
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
KNO3/g 13.3 20.9 32 45.8 64 85.5 110 138 169 202 246
NaCl/g 35.7 35.8 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8
(1)以上两种物质的溶解度受温度变化影响较小的是________。
(2)30 ℃时,KNO3 的溶解度是________g。
(3)KNO3 溶液中含有少量NaCl时,可通过________________的方法提纯KNO3。
(4)对(3)析出的晶体和剩余溶液描述正确的是________(填写编号)。
Ⅰ.剩余溶液一定是KNO3的饱和溶液
Ⅱ.剩余溶液一定是NaCl溶液
Ⅲ.上述方法可以将两者完全分离
Ⅳ.析出的晶体中一定只含有KNO3
16.已知甲物质的溶解度与温度的关系如下表所示:
温度/℃ 10 20 30 40
溶解度/g 10.0 18.0 36.0 56.0
按如图步骤进行操作:
(1)甲属于_________ (填“易”或“可”)溶性物质,它的溶解度随温度的升高而增大 。
(2)在A~E的溶液中,属于不饱和溶液的是___________ (填字母,下同),与B溶液的溶质质量分数相同的是___________ 。
(3)要使E中未溶的甲物质全部溶解,至少需要加入30 ℃的水________ g。
三、实验探究题(每空2分,共20分)
17.下列是“粗盐中难溶性杂质的去除”的实验操作示意图:
(1)仪器a的名称: ________。
(2)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是_______________________。
(3)操作B中还需用到的仪器是____________________。
(4)操作C中,倒入液体时液面要低于滤纸边缘,主要是为了防止______(填序号)。
A. 过滤速度慢
B. 滤纸破损
C. 不溶性杂质未经过滤就进入滤液
(5)操作C完成后滤液中还含有少量的氯化钙,写出除去氯化钙的化学方程式: _________________________________________________________________。
(6)图中部分操作有错误,其中会导致精盐产率明显偏低的操作编号是________,说明引起产率偏低的原因__________________。
18.根据下面实验报告填空:
探究目的: 。
实验用品:药匙、烧杯、玻璃棒、温度计、氢氧化钠固体、水。
操作过程如下图所示:
(1)图示③中的操作存在一处错误,应改正为: 。
(2)图示③中错误操作改正后,上述实验能否达到实验目的?为什么?
、
四、综合应用题(共6分)
19. 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如右图所示。试计算:
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液中溶质的质量分数。
参考答案
一、选择题
1-6BCDBBD 7-12BCBDDD
二、填空题
13. (1)H2SO4 (2)Ca(OH)2 (3)C2H5OH H2O (4)FeSO4 H2O
14. (1)110 (2)降温结晶 (3)①硝酸钾 ②不变 ③一定
15. (1)NaCl (2)45. 8 (3)降温结晶(或冷却热饱和溶液) (4)Ⅰ
15. (1)易 (2)C、D A (3)50
三、实验探究题
17. (1)铁架台
(2)防止药品腐蚀托盘, 使称量更准确
(3)胶头滴管
(4)C
(5)Na2CO3+CaCl2===CaCO3↓+2NaCl
(6)D D中未用玻璃棒搅拌, 造成液滴飞溅, 精盐的产率偏低
18. 探究目的:物质溶解时,溶液的温度有何变化?
(1)用玻璃棒搅拌至全部溶解
(2)不能 应先测量水在溶解前的温度。
四、综合应用题
19. 解:设锌质量为x,H2SO4质量为y,ZnSO4质量为z
Zn + H2SO4══ ZnSO4 + H2↑
65 98 161 2
x y z 0.1g
65:2=X:0.1g x=3.25g
65:98=y:0.1g y=4.9g
65:161=z:0.1g z=8.05g
(1)即黄铜中Cu的质量分数为×100%=66.7%
(2) 4.9g / 9.8% =50g
(3) ×100%=15.1%
同课章节目录
