江苏省常州市教育学会2021-2022学年高一上学期期末学业水平监测化学试题(Word版含答案)
文档属性
| 名称 | 江苏省常州市教育学会2021-2022学年高一上学期期末学业水平监测化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 761.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-31 00:00:00 | ||
图片预览



文档简介
常州市教育学会2021-2022学年高一上学期期末学业水平监测
化学试题
2022年1月
注意事项:
1.本试卷分为选择题和非选择题两部分,满分为100分,考试时间为75分钟.
2.答题前请将学校、班级、学号、姓名填涂在答题卡密封线内;答案书写在答题卡规定区域内,在草稿纸、试卷上答题无效;考试结束后仅交答题卡.
可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Cl-35.5 Cu-64 Zn-65 Ba-137
一、单项选择题:共15小题,每题3分,共45分.每题只有一个选项符合题意.
1.造纸是我国古代四大发明之一,碱液蒸煮制浆法是在蒸煮原料时往浆水中加入草木灰(住要成分为)和石灰水,成浆效果更佳.其中与发生的反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.下列含硫物质属于非电解质的是( )
A.S B. C. D.
3.下列物质间的转化不能通过一步化学反应实现的是( )
A. B. C. D.
4.下列物质转化过程中不涉及氧化还原反应的是( )
A.硫铁矿 B.硫酸型酸雨
C.海带(含) D.胆矾
5.下列实验设计能达到目的的是( )
A.用酒精作萃取剂萃取碘水中的碘 B.用饱和食盐水除去氯气中的
C.用湿润的蓝色石蕊试纸检验 D.将通入溶液验证其漂白性
6.钠遇水立即发生剧烈反应:,实验室将钠保存在煤油中.下列表示反应中相关微粒的化学用语正确的是( )
A.中子数为12的钠原子: B.的结构式:
C.的电子式: D.的空间填充模型:
7.室温下,下列各组离子在指定溶液中能大量共存的是( )
A.溶液:、、、
B.溶液:、、、
C.溶液:、、、
D.溶液:、、、
8.下列物质的性质与用途不具有对应关系的是( )
A.氧化镁熔点高,可用作耐高温材料
B.氢氧化铁胶体的胶粒具有吸附性,可用于净水
C.硫酸钡不溶于水,可用作检查肠胃的内服药剂
D.常温下铁遇浓硫酸会钝化,可用铁罐储运浓疏酸
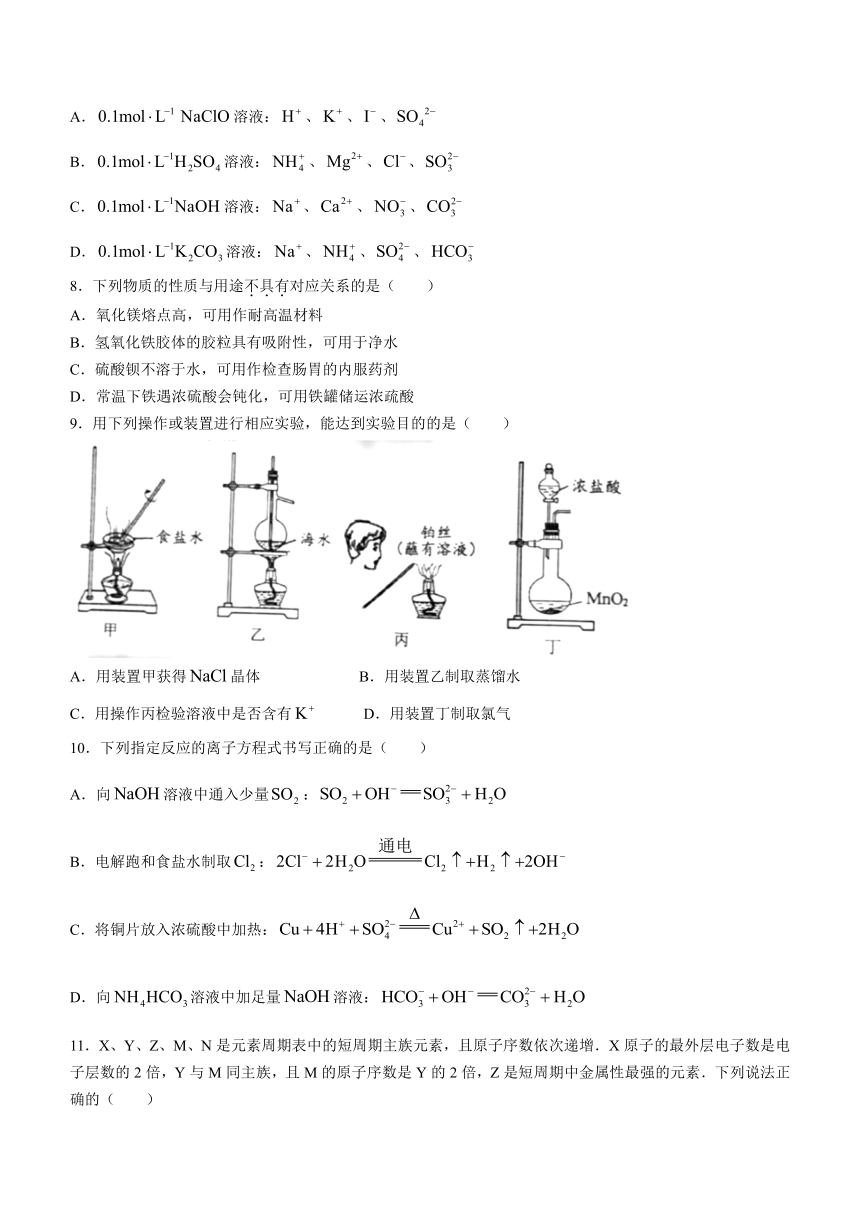
9.用下列操作或装置进行相应实验,能达到实验目的的是( )
A.用装置甲获得晶体 B.用装置乙制取蒸馏水
C.用操作丙检验溶液中是否含有 D.用装置丁制取氯气
10.下列指定反应的离子方程式书写正确的是( )
A.向溶液中通入少量:
B.电解跑和食盐水制取:
C.将铜片放入浓硫酸中加热:
D.向溶液中加足量溶液:
11.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.X原子的最外层电子数是电子层数的2倍,Y与M同主族,且M的原子序数是Y的2倍,Z是短周期中金属性最强的元素.下列说法正确的( )
A,简单离子的半径: B.简单气态氢化物的热稳定性:
C.最高价氧化物对应水化物的酸性: D.固态转变为气态,需克服分子同作用力
12.类比的思维方法常用于预测物质的结构与性质,下列类比分析结果正确的是( )
A.条能在中剧烈燃烧,则也能与反应
B.丝在中燃烧生成,则粉和硫粉反应产物为
C.乙醇和二甲醚的分子组成均为,则两者的结构也完全相同
D.和都是双原子共价分子,则分子中均只有1对共用电子对
阅读下列资料,完成13~14题:大气污染物易溶于水,通常表现出较强的还原性,对人体的呼吸系统和中枢神经系统等均有毒性作用.认识和利用的性质可有效防治对环境的污染,并实现的综合利用.
13.实验室通过下列实验探究的性质.
实验 实验操作和现象
1 用充有的针筒吸入蒸馏水,用橡皮塞堵住针筒前端,充分振荡,针筒内几乎没有气体剩余
2 取实验1中的溶液,滴入几滴紫色石蕊试液,溶液显红色
3 取实验1中的溶液,加入的溶液,观察不到实验现象
4 取实验1中的溶液,通入气体,出现淡黄色浑浊
下列有关说法正确的是( )
A.实验1说明与水发生了化学反应
B.实验2中发生了以下过程:、
C.实验3中可能发生了反应
D.实验4说明水溶液具有还原性
14.某研究团队提出的烟气脱硫工艺流程如下,该流程中脱硫剂反复循环,可实现对烟气中的持续脱除.
已知:脱疏塔中发生的主要反应为、.
下列有关说法正确的是( )
A.脱硫塔中反应生成的S为还原产物
B.经冷凝器得到的几种单质、、和互为同分异构体
C.将和煤粉碎混合,再投入再生塔,有利于反应充分进行
D.再生塔中得到的X主要成分为
15.己知在热碱性溶液中,发生反应.在某温度下,用溶液吸收尾气,经测定,反应后混合溶液中和的物质的量均为,则反应消耗的物质的量为( )
A. B. C. D.
二、非选择题:共4题,共55分.
16.(14分)下图为元素周期表的一部分.
(1)在元素周期表中位于___________,其原子结构示意图为_________.
(2)在考古学中常用于测定生物死亡年代,它与、互称为__________.
(3)(结构式为)可作某些有机合成反应的催化剂,其所含化学键类型为___________.
(4)将N和两种元素的简单离子组成的化合物X投入水中,反应生成白色沉淀,并释放出.
①写出化合物X与水发生的化学反应方程式:__________.
②写出白色沉淀溶于盐酸的离子反应方程式:___________.
17.(10分)炼焦厂从煤焦油中提取酚类物质后产生的废水中主要含有硫酸钠、硫酸和油类物质,直接排放严重污染水源,一种从该废水中回收纯碱和硫铵的工业流程如下:
(1)光学显微镜下观察发现,该废水是水包油型乳化液.加入破乳化剂搅拌,可使油浮于水面,再经________(填操作名称),分离得到含的酸性溶液.
(2)将含的酸性溶液蒸发浓缩,冷却至室温.为了提高目标产品的回收率,应向浓缩液中先通足量___________(填“”或“”),再通足量___________(填“”或“”).
(3)写出滤渣经灼烧得到纯碱的化学方程式:____________.
(4)母液经多步结晶操作获得硫铵.硫铵的主要成分为________(填化学式).
(5)根据上述工业流程可推知:室温时,在硫酸钠、硫铵、碳酸氢钠和碳酸氢铵四种物质中,___________的溶解度最小.
18.(15分)高效灭菌消毒剂气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸.工业上通常先制成稳定性溶液贮存,再经酸活化处理后使用.以氯酸盐、过氧化氢和碳酸盐为主要原料制备稳定性溶液的流程如下:
(1)反应器中发生的主要反应为.
①该反应中是___________(填“氧化剂”、“还原剂”或“氧化剂和还原剂”).
②制备时向反应器中通入空气的作用是___________.
(2)反应器中的反应温度控制在左右为宜.
①工业上采用的加热方式为__________.
②当温度超过,的收率()随温度升高而减小,其原因可能是__________.
(3)吸收瓶中发生反应,获得稳定性溶液.
当有参加反应,转移的电子数为_______.
(4)以亚氯酸盐()为原料进行酸化是生产最简单的方法,其反应原理为,但该方法在实际生产中未得到广泛应用.与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是___________.
19.(16分)硫酸铜在水产养殖业中可用于防治多种鱼病,不同鱼类对硫酸铜浓度的适应性不同,在使用时需注意掌控用量.为测定某溶液的浓度,研究性学习小组设计了以下两个实验方案.
【方案Ⅰ】实验步骤:
(1)步骤②中检验固体是否洗涤干净选用的试剂为___________.
(2)步骤③灼烧时盛放药品的仪器是___________.
(3)步骤④称得固体质量为,则________.
(4)若步骤①将烧杯中的固液混合物转移入过滤器时未洗涤烧杯,则导致的测定值___________(填“偏高”、“偏低”或“无影响”).
【方案Ⅱ】实验步骤:
①按右图组装实验仪器(夹持装置略去);
②……
③在各仪器中加入相应的试剂;
④调整D、E两管中液面相平,读数并记录;
⑤将溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
⑥待体系恢复至室温,读数并记录.
(5)请补充实验步骤②:____________.
(6)己知实验条件下气体摩尔体积为.实验中使用的粉质量为,测得产生的气体体积为,求算溶液的物质的量浓度________(写出计算过程,结果用含m、V、的代数式表示,无需化简).
(7)方案Ⅱ测得的数值比方案Ⅰ大,其原因是__________.
常州市教育学会2021-2022学年高一上学期期末学业水平监测
化学参考答案
2022年1月
选择题(45分)
单项选择题:本题包括15小题,每小题3分,共计45分.每小题只有一个选项符合题意.
1.D 2.B 3.A 4.D 5.B 6.B 7.D 8.C 9.A 10.B 11.D 12.A 13.C 14.C 15.C
非选择题(55分)
16.(14分)
(1)第三(或3)周期第ⅧA族 (2分)
(2分)
(2)同位素 (2分)
(3)共价键(或极性共价键) (2分)
(4)① (2分)
② (3分)
17.(10分)
(1)分液 (2分)
(2) (1分) (1分)
(3) (2分)
(条件写“高温”亦给分,写“灼烧”暂给分)
(4) (2分)
(S)碳酸氢钠(或) (2分)
18.(15分)
(1)①还原剂 (2分)
②将生成的及时导出反应器,防止浓度太高发生分解爆炸 (3分)
(2)①水浴加热 (2分)
②温度升高,不稳定,发生分解;头温度升高,易分解;或温度升高,在酸性条件下还原能力增强,氯酸根可能会进一步被还原为 (3分)
(3)0.5 (2分)
(4)该方法原料中氯元素的利用率相对较低(或该方法所能达到的最大理论转化率只有80%,而氯酸盐法可达100%) (3分)
19.(16分)
(1)溶液(2分) (2)坩埚(2分) (3)0.40(2分) (4)偏低 (2分)
(5)检查装置的气密性(2分)
(6)根据
与酸反应的(1分)
锌的总量
与硫酸铜反应的
根据
则
(2分)
(7)实验⑥读数前未调整D、E两管液面齐平,测得氢气的体积偏小(3分)
使得与稀硫酸反应的质量减小,与反应的质量增大,则测得偏高(后面推理过程的描述暂不计分)
化学试题
2022年1月
注意事项:
1.本试卷分为选择题和非选择题两部分,满分为100分,考试时间为75分钟.
2.答题前请将学校、班级、学号、姓名填涂在答题卡密封线内;答案书写在答题卡规定区域内,在草稿纸、试卷上答题无效;考试结束后仅交答题卡.
可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Cl-35.5 Cu-64 Zn-65 Ba-137
一、单项选择题:共15小题,每题3分,共45分.每题只有一个选项符合题意.
1.造纸是我国古代四大发明之一,碱液蒸煮制浆法是在蒸煮原料时往浆水中加入草木灰(住要成分为)和石灰水,成浆效果更佳.其中与发生的反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.下列含硫物质属于非电解质的是( )
A.S B. C. D.
3.下列物质间的转化不能通过一步化学反应实现的是( )
A. B. C. D.
4.下列物质转化过程中不涉及氧化还原反应的是( )
A.硫铁矿 B.硫酸型酸雨
C.海带(含) D.胆矾
5.下列实验设计能达到目的的是( )
A.用酒精作萃取剂萃取碘水中的碘 B.用饱和食盐水除去氯气中的
C.用湿润的蓝色石蕊试纸检验 D.将通入溶液验证其漂白性
6.钠遇水立即发生剧烈反应:,实验室将钠保存在煤油中.下列表示反应中相关微粒的化学用语正确的是( )
A.中子数为12的钠原子: B.的结构式:
C.的电子式: D.的空间填充模型:
7.室温下,下列各组离子在指定溶液中能大量共存的是( )
A.溶液:、、、
B.溶液:、、、
C.溶液:、、、
D.溶液:、、、
8.下列物质的性质与用途不具有对应关系的是( )
A.氧化镁熔点高,可用作耐高温材料
B.氢氧化铁胶体的胶粒具有吸附性,可用于净水
C.硫酸钡不溶于水,可用作检查肠胃的内服药剂
D.常温下铁遇浓硫酸会钝化,可用铁罐储运浓疏酸
9.用下列操作或装置进行相应实验,能达到实验目的的是( )
A.用装置甲获得晶体 B.用装置乙制取蒸馏水
C.用操作丙检验溶液中是否含有 D.用装置丁制取氯气
10.下列指定反应的离子方程式书写正确的是( )
A.向溶液中通入少量:
B.电解跑和食盐水制取:
C.将铜片放入浓硫酸中加热:
D.向溶液中加足量溶液:
11.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.X原子的最外层电子数是电子层数的2倍,Y与M同主族,且M的原子序数是Y的2倍,Z是短周期中金属性最强的元素.下列说法正确的( )
A,简单离子的半径: B.简单气态氢化物的热稳定性:
C.最高价氧化物对应水化物的酸性: D.固态转变为气态,需克服分子同作用力
12.类比的思维方法常用于预测物质的结构与性质,下列类比分析结果正确的是( )
A.条能在中剧烈燃烧,则也能与反应
B.丝在中燃烧生成,则粉和硫粉反应产物为
C.乙醇和二甲醚的分子组成均为,则两者的结构也完全相同
D.和都是双原子共价分子,则分子中均只有1对共用电子对
阅读下列资料,完成13~14题:大气污染物易溶于水,通常表现出较强的还原性,对人体的呼吸系统和中枢神经系统等均有毒性作用.认识和利用的性质可有效防治对环境的污染,并实现的综合利用.
13.实验室通过下列实验探究的性质.
实验 实验操作和现象
1 用充有的针筒吸入蒸馏水,用橡皮塞堵住针筒前端,充分振荡,针筒内几乎没有气体剩余
2 取实验1中的溶液,滴入几滴紫色石蕊试液,溶液显红色
3 取实验1中的溶液,加入的溶液,观察不到实验现象
4 取实验1中的溶液,通入气体,出现淡黄色浑浊
下列有关说法正确的是( )
A.实验1说明与水发生了化学反应
B.实验2中发生了以下过程:、
C.实验3中可能发生了反应
D.实验4说明水溶液具有还原性
14.某研究团队提出的烟气脱硫工艺流程如下,该流程中脱硫剂反复循环,可实现对烟气中的持续脱除.
已知:脱疏塔中发生的主要反应为、.
下列有关说法正确的是( )
A.脱硫塔中反应生成的S为还原产物
B.经冷凝器得到的几种单质、、和互为同分异构体
C.将和煤粉碎混合,再投入再生塔,有利于反应充分进行
D.再生塔中得到的X主要成分为
15.己知在热碱性溶液中,发生反应.在某温度下,用溶液吸收尾气,经测定,反应后混合溶液中和的物质的量均为,则反应消耗的物质的量为( )
A. B. C. D.
二、非选择题:共4题,共55分.
16.(14分)下图为元素周期表的一部分.
(1)在元素周期表中位于___________,其原子结构示意图为_________.
(2)在考古学中常用于测定生物死亡年代,它与、互称为__________.
(3)(结构式为)可作某些有机合成反应的催化剂,其所含化学键类型为___________.
(4)将N和两种元素的简单离子组成的化合物X投入水中,反应生成白色沉淀,并释放出.
①写出化合物X与水发生的化学反应方程式:__________.
②写出白色沉淀溶于盐酸的离子反应方程式:___________.
17.(10分)炼焦厂从煤焦油中提取酚类物质后产生的废水中主要含有硫酸钠、硫酸和油类物质,直接排放严重污染水源,一种从该废水中回收纯碱和硫铵的工业流程如下:
(1)光学显微镜下观察发现,该废水是水包油型乳化液.加入破乳化剂搅拌,可使油浮于水面,再经________(填操作名称),分离得到含的酸性溶液.
(2)将含的酸性溶液蒸发浓缩,冷却至室温.为了提高目标产品的回收率,应向浓缩液中先通足量___________(填“”或“”),再通足量___________(填“”或“”).
(3)写出滤渣经灼烧得到纯碱的化学方程式:____________.
(4)母液经多步结晶操作获得硫铵.硫铵的主要成分为________(填化学式).
(5)根据上述工业流程可推知:室温时,在硫酸钠、硫铵、碳酸氢钠和碳酸氢铵四种物质中,___________的溶解度最小.
18.(15分)高效灭菌消毒剂气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸.工业上通常先制成稳定性溶液贮存,再经酸活化处理后使用.以氯酸盐、过氧化氢和碳酸盐为主要原料制备稳定性溶液的流程如下:
(1)反应器中发生的主要反应为.
①该反应中是___________(填“氧化剂”、“还原剂”或“氧化剂和还原剂”).
②制备时向反应器中通入空气的作用是___________.
(2)反应器中的反应温度控制在左右为宜.
①工业上采用的加热方式为__________.
②当温度超过,的收率()随温度升高而减小,其原因可能是__________.
(3)吸收瓶中发生反应,获得稳定性溶液.
当有参加反应,转移的电子数为_______.
(4)以亚氯酸盐()为原料进行酸化是生产最简单的方法,其反应原理为,但该方法在实际生产中未得到广泛应用.与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是___________.
19.(16分)硫酸铜在水产养殖业中可用于防治多种鱼病,不同鱼类对硫酸铜浓度的适应性不同,在使用时需注意掌控用量.为测定某溶液的浓度,研究性学习小组设计了以下两个实验方案.
【方案Ⅰ】实验步骤:
(1)步骤②中检验固体是否洗涤干净选用的试剂为___________.
(2)步骤③灼烧时盛放药品的仪器是___________.
(3)步骤④称得固体质量为,则________.
(4)若步骤①将烧杯中的固液混合物转移入过滤器时未洗涤烧杯,则导致的测定值___________(填“偏高”、“偏低”或“无影响”).
【方案Ⅱ】实验步骤:
①按右图组装实验仪器(夹持装置略去);
②……
③在各仪器中加入相应的试剂;
④调整D、E两管中液面相平,读数并记录;
⑤将溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
⑥待体系恢复至室温,读数并记录.
(5)请补充实验步骤②:____________.
(6)己知实验条件下气体摩尔体积为.实验中使用的粉质量为,测得产生的气体体积为,求算溶液的物质的量浓度________(写出计算过程,结果用含m、V、的代数式表示,无需化简).
(7)方案Ⅱ测得的数值比方案Ⅰ大,其原因是__________.
常州市教育学会2021-2022学年高一上学期期末学业水平监测
化学参考答案
2022年1月
选择题(45分)
单项选择题:本题包括15小题,每小题3分,共计45分.每小题只有一个选项符合题意.
1.D 2.B 3.A 4.D 5.B 6.B 7.D 8.C 9.A 10.B 11.D 12.A 13.C 14.C 15.C
非选择题(55分)
16.(14分)
(1)第三(或3)周期第ⅧA族 (2分)
(2分)
(2)同位素 (2分)
(3)共价键(或极性共价键) (2分)
(4)① (2分)
② (3分)
17.(10分)
(1)分液 (2分)
(2) (1分) (1分)
(3) (2分)
(条件写“高温”亦给分,写“灼烧”暂给分)
(4) (2分)
(S)碳酸氢钠(或) (2分)
18.(15分)
(1)①还原剂 (2分)
②将生成的及时导出反应器,防止浓度太高发生分解爆炸 (3分)
(2)①水浴加热 (2分)
②温度升高,不稳定,发生分解;头温度升高,易分解;或温度升高,在酸性条件下还原能力增强,氯酸根可能会进一步被还原为 (3分)
(3)0.5 (2分)
(4)该方法原料中氯元素的利用率相对较低(或该方法所能达到的最大理论转化率只有80%,而氯酸盐法可达100%) (3分)
19.(16分)
(1)溶液(2分) (2)坩埚(2分) (3)0.40(2分) (4)偏低 (2分)
(5)检查装置的气密性(2分)
(6)根据
与酸反应的(1分)
锌的总量
与硫酸铜反应的
根据
则
(2分)
(7)实验⑥读数前未调整D、E两管液面齐平,测得氢气的体积偏小(3分)
使得与稀硫酸反应的质量减小,与反应的质量增大,则测得偏高(后面推理过程的描述暂不计分)
同课章节目录
