高中化学苏教版(2019)必修第二册 专题七 氮与社会可持续发展-含氮化合物的合理使用 走进NO课件(24张ppt)
文档属性
| 名称 | 高中化学苏教版(2019)必修第二册 专题七 氮与社会可持续发展-含氮化合物的合理使用 走进NO课件(24张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 37.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-01 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
氮及其化合物
走进NO
NO的物理性质
NO是一种无色不溶于水的气体
观察与思考
乌普萨拉大学的研究人员发现,治疗2003年SARS疫情的一氧化氮(NO),同样适用于目前正在蔓延的COVID-19。一氧化氮(NO)是一种由人体自身产生的具有抗病毒特性的化合物。
——《氧化还原生物学》2020年10月4日
资料卡
N
O
NO为什么可以杀死新冠病毒?
Q1
1.捏住鼻子。
【实验1】
人体一氧化氮检测
操作指南
2.嘴对准呼气口,形成密闭环境。用嘴轻轻吸一口气(该吸入气体经过检测仪过滤)。
3.均匀呼气排空吸入气体。
4.保持均匀呼气使显示屏中人的头像始终在蓝色线条内6s以上。
人体内有NO吗?
Q2
感知NO的存在
环节一
环境中有NO吗?
淮安10月20日[21:00]空气质量报告
AQI:63,良
45.0 μg/m
细颗粒物
氮氧化物(NO、NO2)
一氧化碳
臭氧
粗颗粒物
二氧化硫
65.0 μg/m
7.0 μg/m
75.0 μg/m
0.0 μg/m
38.0 μg/m
Q3
认识
角度
原料
预测性质
环境中一氧化氮怎么产生的?
Q4
【实验2】
N2+O2
化学性质不活泼,常温下很难跟其他物质发生反应。
反应条件
高温、高能量。
N2性质
常温下很容易与氧气化合,生成二氧化氮。
二氧化氮是红棕色、刺激性气味的有毒气体。
检验NO
无色气体遇到氧气迅速变为红棕色。
NO性质
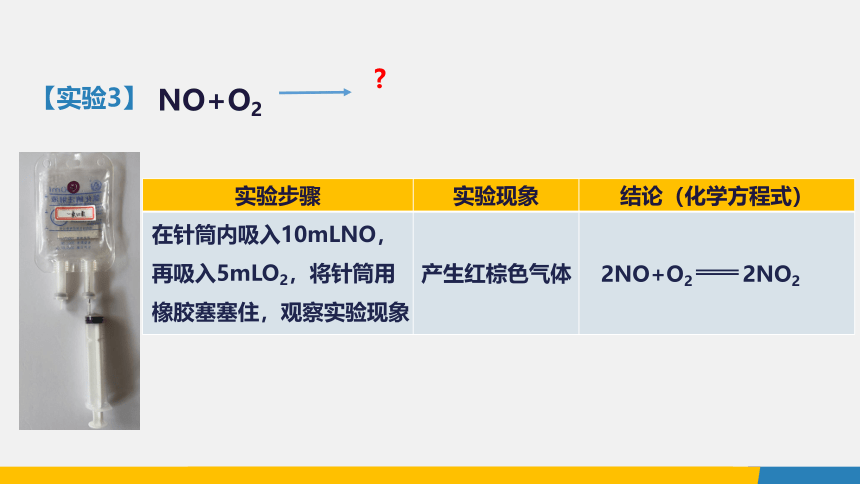
【实验3】
NO+O2
在针筒内吸入10mLNO,再吸入5mLO2,将针筒用橡胶塞塞住,观察实验现象
产生红棕色气体
2NO+O2 2NO2
实验步骤 实验现象 结论(化学方程式)
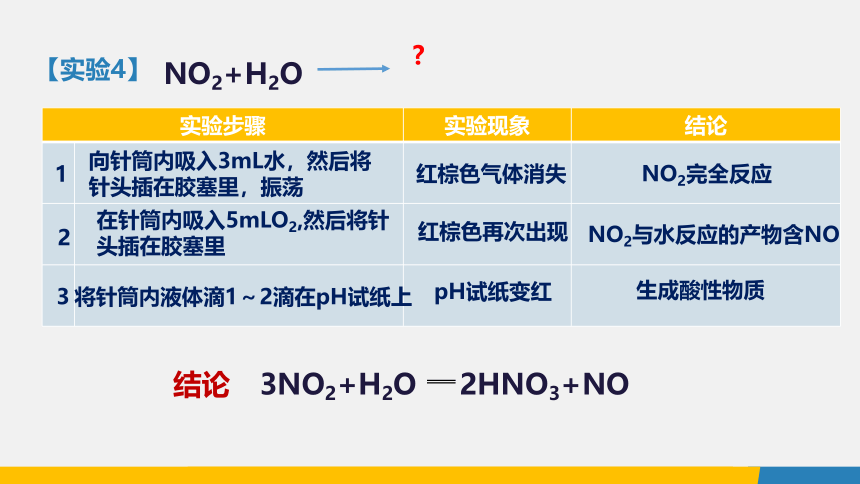
【实验4】
实验步骤 实验现象 结论
1
向针筒内吸入3mL水,然后将针头插在胶塞里,振荡
红棕色气体消失
NO2完全反应
将针筒内液体滴1~2滴在pH试纸上
pH试纸变红
生成酸性物质
2
3
在针筒内吸入5mLO2,然后将针头插在胶塞里
红棕色再次出现
NO2与水反应的产物含NO
NO2+H2O
3NO2+H2O 2HNO3+NO
结论
═
认识
角度
反应
原理
原料
预测性质
提出方案
实验验证
环境中一氧化氮怎么产生的?
Q4
NO
解决“物质转化类“问题的思维模型图
认识
角度
反应
原理
观察
现象
Yes
No
原料
预测性质
提出方案
实验验证
分析推理
方案错误
揭示本质
结论:
N2+O2 2NO
放电
环境中一氧化氮怎么产生的?
Q4
R-NH2
+ O2
酶
NO
R-NH2
-3
C
H
R
COOH
NH2
精氨酸(氨基酸中的一种)和氧气在
一氧化氮合酶的作用下生成一氧化氮。
伊格纳罗
穆拉德
【化学史话】
人体内的NO怎么产生的?
Q5
-3
小结
探究NO的产生
NO的产生:氮及其化合物的氧化或者还原。
NO
N2
NO2
R-NH2
氧化
还原
氧化
环节二
-3
0
+4
NO有什么作用?
NO对环境意义
NO
NO2
O2
H2O
HNO3
土壤
硝酸盐(氮肥)
【交流与讨论】NO在环境中会发生哪些反应?将转化为什么物质?
Q6
谚语“雷雨发庄稼”
氮循环
氮气
雷电
动物
植物
氨
铵盐
硝酸盐
根瘤菌
自然固氮
固氮:游离态的氮转化为化合态的氮
N2+3H2 2NH3
高温、高压
催化剂
1918年的诺贝尔化学奖
【思考】自然固氮无法满足人类生产和生活需要,如何人工固氮?
工业合成氨
【化学史话】
高温下煤燃烧
我国环境中的NO为何逐年升高?
08-12年我国一氧化氮排放量
资料卡
单位/亿公吨
交流与讨论
汽车尾气
NO浓度过高引发的环境问题
硝酸性酸雨
臭氧层空洞
光化学烟雾
如何应对NO过量引发的环境问题?
NO
氧化
还原
交流与讨论
交流与讨论
2
NO参与免疫反应、杀灭病毒。
NO到神经系统,提高记忆力。
4
3
NO到炎症处,消除炎症。
NO到血管中,扩张血管。
1
明星分子
如何看待NO?
体悟NO的价值
环节三
Q7
【反思与提升】
谈谈这节课你的收获
人与自然、社会和谐、可持续发展
化学
人
自然
社会
氮及其化合物
走进NO
NO的物理性质
NO是一种无色不溶于水的气体
观察与思考
乌普萨拉大学的研究人员发现,治疗2003年SARS疫情的一氧化氮(NO),同样适用于目前正在蔓延的COVID-19。一氧化氮(NO)是一种由人体自身产生的具有抗病毒特性的化合物。
——《氧化还原生物学》2020年10月4日
资料卡
N
O
NO为什么可以杀死新冠病毒?
Q1
1.捏住鼻子。
【实验1】
人体一氧化氮检测
操作指南
2.嘴对准呼气口,形成密闭环境。用嘴轻轻吸一口气(该吸入气体经过检测仪过滤)。
3.均匀呼气排空吸入气体。
4.保持均匀呼气使显示屏中人的头像始终在蓝色线条内6s以上。
人体内有NO吗?
Q2
感知NO的存在
环节一
环境中有NO吗?
淮安10月20日[21:00]空气质量报告
AQI:63,良
45.0 μg/m
细颗粒物
氮氧化物(NO、NO2)
一氧化碳
臭氧
粗颗粒物
二氧化硫
65.0 μg/m
7.0 μg/m
75.0 μg/m
0.0 μg/m
38.0 μg/m
Q3
认识
角度
原料
预测性质
环境中一氧化氮怎么产生的?
Q4
【实验2】
N2+O2
化学性质不活泼,常温下很难跟其他物质发生反应。
反应条件
高温、高能量。
N2性质
常温下很容易与氧气化合,生成二氧化氮。
二氧化氮是红棕色、刺激性气味的有毒气体。
检验NO
无色气体遇到氧气迅速变为红棕色。
NO性质
【实验3】
NO+O2
在针筒内吸入10mLNO,再吸入5mLO2,将针筒用橡胶塞塞住,观察实验现象
产生红棕色气体
2NO+O2 2NO2
实验步骤 实验现象 结论(化学方程式)
【实验4】
实验步骤 实验现象 结论
1
向针筒内吸入3mL水,然后将针头插在胶塞里,振荡
红棕色气体消失
NO2完全反应
将针筒内液体滴1~2滴在pH试纸上
pH试纸变红
生成酸性物质
2
3
在针筒内吸入5mLO2,然后将针头插在胶塞里
红棕色再次出现
NO2与水反应的产物含NO
NO2+H2O
3NO2+H2O 2HNO3+NO
结论
═
认识
角度
反应
原理
原料
预测性质
提出方案
实验验证
环境中一氧化氮怎么产生的?
Q4
NO
解决“物质转化类“问题的思维模型图
认识
角度
反应
原理
观察
现象
Yes
No
原料
预测性质
提出方案
实验验证
分析推理
方案错误
揭示本质
结论:
N2+O2 2NO
放电
环境中一氧化氮怎么产生的?
Q4
R-NH2
+ O2
酶
NO
R-NH2
-3
C
H
R
COOH
NH2
精氨酸(氨基酸中的一种)和氧气在
一氧化氮合酶的作用下生成一氧化氮。
伊格纳罗
穆拉德
【化学史话】
人体内的NO怎么产生的?
Q5
-3
小结
探究NO的产生
NO的产生:氮及其化合物的氧化或者还原。
NO
N2
NO2
R-NH2
氧化
还原
氧化
环节二
-3
0
+4
NO有什么作用?
NO对环境意义
NO
NO2
O2
H2O
HNO3
土壤
硝酸盐(氮肥)
【交流与讨论】NO在环境中会发生哪些反应?将转化为什么物质?
Q6
谚语“雷雨发庄稼”
氮循环
氮气
雷电
动物
植物
氨
铵盐
硝酸盐
根瘤菌
自然固氮
固氮:游离态的氮转化为化合态的氮
N2+3H2 2NH3
高温、高压
催化剂
1918年的诺贝尔化学奖
【思考】自然固氮无法满足人类生产和生活需要,如何人工固氮?
工业合成氨
【化学史话】
高温下煤燃烧
我国环境中的NO为何逐年升高?
08-12年我国一氧化氮排放量
资料卡
单位/亿公吨
交流与讨论
汽车尾气
NO浓度过高引发的环境问题
硝酸性酸雨
臭氧层空洞
光化学烟雾
如何应对NO过量引发的环境问题?
NO
氧化
还原
交流与讨论
交流与讨论
2
NO参与免疫反应、杀灭病毒。
NO到神经系统,提高记忆力。
4
3
NO到炎症处,消除炎症。
NO到血管中,扩张血管。
1
明星分子
如何看待NO?
体悟NO的价值
环节三
Q7
【反思与提升】
谈谈这节课你的收获
人与自然、社会和谐、可持续发展
化学
人
自然
社会
