第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元溶液单元测试训练卷-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 406.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-29 00:00:00 | ||
图片预览


文档简介
人教版九年级化学下册
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题3分,共36分)
1.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是( )
A.冰糖 B.味精
C.芝麻油 D.葡萄糖
2.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是( )
A.生石灰 B.氢氧化钠
C.氯化钠 D.硝酸铵
3.市场上有一种俗称“摇摇冰”的罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动使它们混合,罐内饮料温度就会降低。这种固体物质可能是( )
A.生石灰 B.烧碱
C.食盐 D.硝酸铵
4.乳化现象在生产和生活中很常见,下列常用的清洗方法中,用到乳化作用的是( )
A.用洗洁精除去盘子上的油污 B.用清水洗手
C.用洗衣粉洗去衣服上的泥渍 D.用盐酸除铁锈
5.下列关于“粗盐中难溶性杂质的去除”实验的说法中,错误的是( )
A.称量:用托盘天平称取5 g粗盐,用量筒量取10 mL水
B.溶解:将水倒入烧杯,逐渐加入粗盐,边加边用玻璃棒搅拌,至粗盐不再溶解为止
C.过滤:将烧杯内的所有物质全部倒入过滤器内,边倒边用玻璃棒搅拌
D.蒸发:将所得澄清滤液倒入蒸发皿,边加热边用玻璃棒搅拌,至较多晶体析出时停止加热
6.某同学用25 ℃的水溶解一定量的氯化钾,充分搅拌后发现杯底还有部分氯化钾固体没有溶解,然后该同学又用酒精灯加热至50 ℃(不考虑水分挥发),固体全部溶解。那么在加热前后,以下各量没有发生改变的是( )
A.氯化钾的溶解度 B.溶质的质量
C.溶剂的质量 D.溶质的质量分数
7.向100 g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
A.②中A的质量分数最大
B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液
D.①③④⑤中没有固体存在
8.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。下列关于海水晒盐原理的说法正确的是( )
A. 日晒风吹使海水中的氯化钠蒸发 B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发、晶体析出 D. 日晒风吹使氯化钠的溶解度变小
9.下列有关溶液的说法中正确的是( )
A. 常温下将100 mL饱和Ca(OH)2溶液加热至50 ℃,会使溶液由饱和溶液变为不饱和溶液
B. 从100 mL溶质质量分数为25%的硫酸溶液中取出10 mL,则取出的10 mL硫酸溶液的溶质质量分数仍为25%
C. 20 ℃时,50 g水中溶解了18 g NaCl,则20 ℃时 NaCl的溶解度为36 g
D. 将95 g KCl溶液蒸干得到5 g KCl固体,则原溶液中KCl的溶质质量分数为5%
10.在一定温度下,向一定量的氯化钠不饱和溶液中不断加氯化钠固体,并搅拌。在此过程中,加入氯化钠的质量(n)与溶液中溶质的质量分数(m)的变化关系如图所示,其中正确的是( )
A B C D
11.已知20 ℃时CuSO4的溶解度为32 g。20 ℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是( )
A.溶液中溶质质量分数的大小关系为丁>丙>甲
B.丙中溶液溶质与溶剂的质量比为8?25
C.丁溶液一定是饱和溶液
D.CuSO4 50 ℃时的溶解度比20 ℃时的大
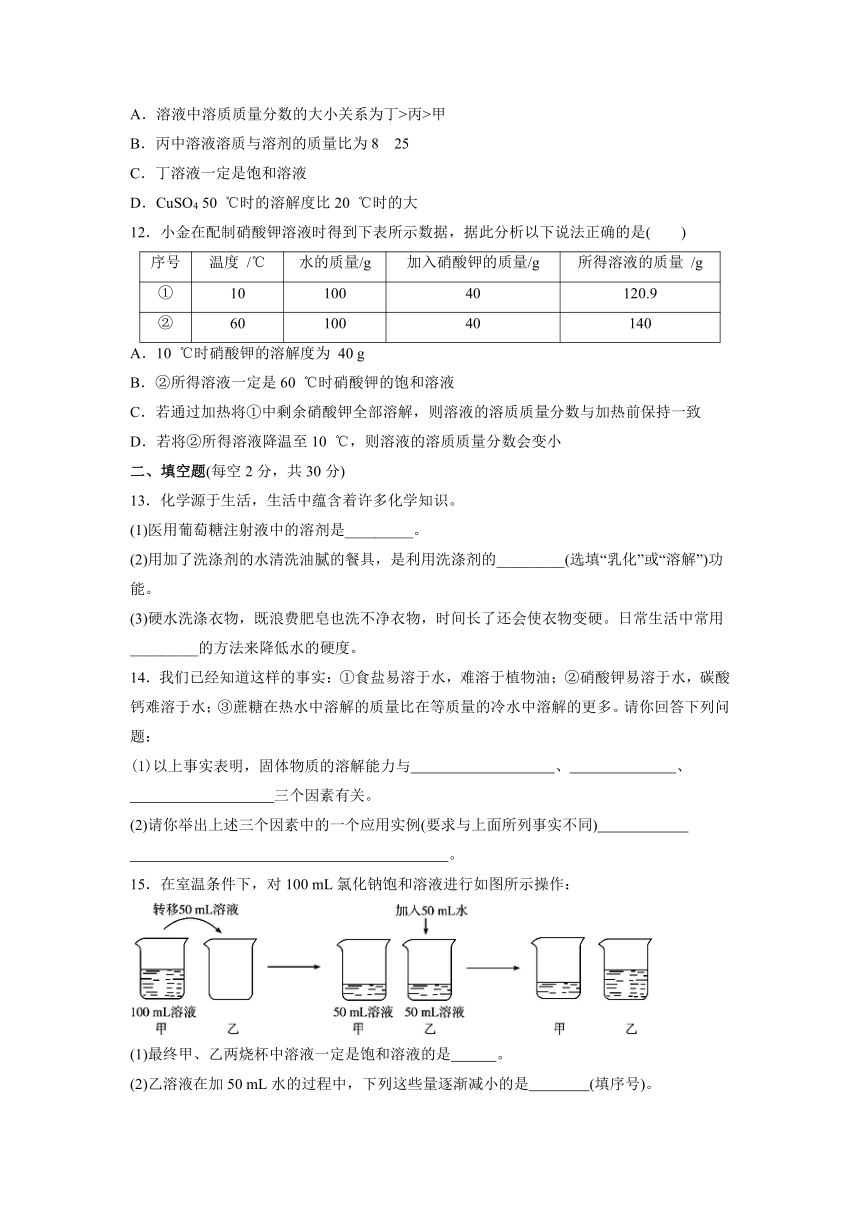
12.小金在配制硝酸钾溶液时得到下表所示数据,据此分析以下说法正确的是( )
序号 温度 /℃ 水的质量/g 加入硝酸钾的质量/g 所得溶液的质量 /g
① 10 100 40 120.9
② 60 100 40 140
A.10 ℃时硝酸钾的溶解度为 40 g
B.②所得溶液一定是60 ℃时硝酸钾的饱和溶液
C.若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致
D.若将②所得溶液降温至10 ℃,则溶液的溶质质量分数会变小
二、填空题(每空2分,共30分)
13.化学源于生活,生活中蕴含着许多化学知识。
(1)医用葡萄糖注射液中的溶剂是_________。
(2)用加了洗涤剂的水清洗油腻的餐具,是利用洗涤剂的_________(选填“乳化”或“溶解”)功能。
(3)硬水洗涤衣物,既浪费肥皂也洗不净衣物,时间长了还会使衣物变硬。日常生活中常用_________的方法来降低水的硬度。
14.我们已经知道这样的事实:①食盐易溶于水,难溶于植物油;②硝酸钾易溶于水,碳酸钙难溶于水;③蔗糖在热水中溶解的质量比在等质量的冷水中溶解的更多。请你回答下列问题:
(1)以上事实表明,固体物质的溶解能力与 、 、
三个因素有关。
(2)请你举出上述三个因素中的一个应用实例(要求与上面所列事实不同)
。
15.在室温条件下,对100 mL氯化钠饱和溶液进行如图所示操作:
(1)最终甲、乙两烧杯中溶液一定是饱和溶液的是 。
(2)乙溶液在加50 mL水的过程中,下列这些量逐渐减小的是 (填序号)。
①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
16.苯甲酸是一种食品防腐剂,它是一种片状晶体,在水中的溶解度如下表:
某同学为了提纯某一苯甲酸样品(其中含泥沙等难溶于水的杂质),进行了如下实验:
(1)取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 。
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
(3)将所得滤液 ,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体。
17. KNO3和KCl在不同温度时的溶解度(单位为 g)如下表所示。
请回答下列问题:
(1)20 ℃时,KCl的溶解度为_____g。
(2)依据上表数据,绘制KNO3和KCl的溶解度曲线如图1,图中能表示KNO3溶解度曲线的是____(填“m”或“n”)。
(3)由上表数据,可知KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是_____________。
三、实验探究题(每空2分,共22分)
18.小红在做饭时,发现很多因素都能影响食盐在水中溶解速率。
(1)从你能想到的因素中,写出其中两项,并预测此因素对食盐溶解速率的影响:
因素① ,你的预测 ;
因素② ,你的预测 ;
(2)从你所列因素中选出一个是_________,通过实验验证你的预测。你设计的实验方案是:
。
19.某实验小组利用图1所示仪器进行“配制溶质质量分数一定的氯化钠溶液”的实验:
(1)图1中仪器a的名称是__ __;按实验要求,图1中还缺少的玻璃仪器是__ __(填名称)。
(2)小婧按图2的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__ __;她称取的氯化钠实际质量为__ __g。
(3)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为__ __(水的密度为1 g/cm3)。
四、综合应用题(共12分)
20. 称取5.8 g某生铁样品放入94.6 g稀盐酸中,恰好完全反应(生铁样品中的杂质不溶于水也不与盐酸发生反应),产生0.2 g氢气。试计算反应后所得溶液中溶质的质量分数。
参考答案
一、选择题
1-6CDDACC 7-12DCBACD
二、填空题
13.水 乳化 煮沸
14.⑴溶剂性质 溶质性质 溶液温度 ⑵用汽油清洗衣服上的油污
15. (1)甲 (2)②④
16. (1)常温下苯甲酸溶解度很小 (2)减小过滤时苯甲酸的损失 (3)缓慢冷却至室温
17. (1)34.0 (2)m (3)34.0<x<37.0
三、实验探究题
18. (1) ①温度 温度越高,食盐溶解越快;
②是否搅拌 搅拌使食盐溶解更快
(2)温度 取两烧杯体积一样但温度不同的水,分别加入质量相同、颗粒大小一样的少量食盐,分别记录食盐完全溶解所需的时间。
19. (1)烧杯 玻璃棒
(2)称量时砝码放反了位置 12
(3)18%
四、综合应用题
20. 解:设5.8 g生铁样品中铁的质量为x,反应生成的FeCl2的质量为y。
Fe+2HCl===FeCl2+H2↑
56 127 2
x y 0.2 g
= x==5.6 g
= y==12.7 g
反应后所得FeCl2溶液中的溶质的质量分数为:×100%=12.7%
答:反应后所得FeCl2溶液中的溶质的质量分数为12.7%。
第九单元 溶液
单元测试训练卷
一、选择题(本题共12小题,每小题3分,共36分)
1.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是( )
A.冰糖 B.味精
C.芝麻油 D.葡萄糖
2.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是( )
A.生石灰 B.氢氧化钠
C.氯化钠 D.硝酸铵
3.市场上有一种俗称“摇摇冰”的罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动使它们混合,罐内饮料温度就会降低。这种固体物质可能是( )
A.生石灰 B.烧碱
C.食盐 D.硝酸铵
4.乳化现象在生产和生活中很常见,下列常用的清洗方法中,用到乳化作用的是( )
A.用洗洁精除去盘子上的油污 B.用清水洗手
C.用洗衣粉洗去衣服上的泥渍 D.用盐酸除铁锈
5.下列关于“粗盐中难溶性杂质的去除”实验的说法中,错误的是( )
A.称量:用托盘天平称取5 g粗盐,用量筒量取10 mL水
B.溶解:将水倒入烧杯,逐渐加入粗盐,边加边用玻璃棒搅拌,至粗盐不再溶解为止
C.过滤:将烧杯内的所有物质全部倒入过滤器内,边倒边用玻璃棒搅拌
D.蒸发:将所得澄清滤液倒入蒸发皿,边加热边用玻璃棒搅拌,至较多晶体析出时停止加热
6.某同学用25 ℃的水溶解一定量的氯化钾,充分搅拌后发现杯底还有部分氯化钾固体没有溶解,然后该同学又用酒精灯加热至50 ℃(不考虑水分挥发),固体全部溶解。那么在加热前后,以下各量没有发生改变的是( )
A.氯化钾的溶解度 B.溶质的质量
C.溶剂的质量 D.溶质的质量分数
7.向100 g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
A.②中A的质量分数最大
B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液
D.①③④⑤中没有固体存在
8.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。下列关于海水晒盐原理的说法正确的是( )
A. 日晒风吹使海水中的氯化钠蒸发 B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发、晶体析出 D. 日晒风吹使氯化钠的溶解度变小
9.下列有关溶液的说法中正确的是( )
A. 常温下将100 mL饱和Ca(OH)2溶液加热至50 ℃,会使溶液由饱和溶液变为不饱和溶液
B. 从100 mL溶质质量分数为25%的硫酸溶液中取出10 mL,则取出的10 mL硫酸溶液的溶质质量分数仍为25%
C. 20 ℃时,50 g水中溶解了18 g NaCl,则20 ℃时 NaCl的溶解度为36 g
D. 将95 g KCl溶液蒸干得到5 g KCl固体,则原溶液中KCl的溶质质量分数为5%
10.在一定温度下,向一定量的氯化钠不饱和溶液中不断加氯化钠固体,并搅拌。在此过程中,加入氯化钠的质量(n)与溶液中溶质的质量分数(m)的变化关系如图所示,其中正确的是( )
A B C D
11.已知20 ℃时CuSO4的溶解度为32 g。20 ℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是( )
A.溶液中溶质质量分数的大小关系为丁>丙>甲
B.丙中溶液溶质与溶剂的质量比为8?25
C.丁溶液一定是饱和溶液
D.CuSO4 50 ℃时的溶解度比20 ℃时的大
12.小金在配制硝酸钾溶液时得到下表所示数据,据此分析以下说法正确的是( )
序号 温度 /℃ 水的质量/g 加入硝酸钾的质量/g 所得溶液的质量 /g
① 10 100 40 120.9
② 60 100 40 140
A.10 ℃时硝酸钾的溶解度为 40 g
B.②所得溶液一定是60 ℃时硝酸钾的饱和溶液
C.若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致
D.若将②所得溶液降温至10 ℃,则溶液的溶质质量分数会变小
二、填空题(每空2分,共30分)
13.化学源于生活,生活中蕴含着许多化学知识。
(1)医用葡萄糖注射液中的溶剂是_________。
(2)用加了洗涤剂的水清洗油腻的餐具,是利用洗涤剂的_________(选填“乳化”或“溶解”)功能。
(3)硬水洗涤衣物,既浪费肥皂也洗不净衣物,时间长了还会使衣物变硬。日常生活中常用_________的方法来降低水的硬度。
14.我们已经知道这样的事实:①食盐易溶于水,难溶于植物油;②硝酸钾易溶于水,碳酸钙难溶于水;③蔗糖在热水中溶解的质量比在等质量的冷水中溶解的更多。请你回答下列问题:
(1)以上事实表明,固体物质的溶解能力与 、 、
三个因素有关。
(2)请你举出上述三个因素中的一个应用实例(要求与上面所列事实不同)
。
15.在室温条件下,对100 mL氯化钠饱和溶液进行如图所示操作:
(1)最终甲、乙两烧杯中溶液一定是饱和溶液的是 。
(2)乙溶液在加50 mL水的过程中,下列这些量逐渐减小的是 (填序号)。
①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
16.苯甲酸是一种食品防腐剂,它是一种片状晶体,在水中的溶解度如下表:
某同学为了提纯某一苯甲酸样品(其中含泥沙等难溶于水的杂质),进行了如下实验:
(1)取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 。
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
(3)将所得滤液 ,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体。
17. KNO3和KCl在不同温度时的溶解度(单位为 g)如下表所示。
请回答下列问题:
(1)20 ℃时,KCl的溶解度为_____g。
(2)依据上表数据,绘制KNO3和KCl的溶解度曲线如图1,图中能表示KNO3溶解度曲线的是____(填“m”或“n”)。
(3)由上表数据,可知KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是_____________。
三、实验探究题(每空2分,共22分)
18.小红在做饭时,发现很多因素都能影响食盐在水中溶解速率。
(1)从你能想到的因素中,写出其中两项,并预测此因素对食盐溶解速率的影响:
因素① ,你的预测 ;
因素② ,你的预测 ;
(2)从你所列因素中选出一个是_________,通过实验验证你的预测。你设计的实验方案是:
。
19.某实验小组利用图1所示仪器进行“配制溶质质量分数一定的氯化钠溶液”的实验:
(1)图1中仪器a的名称是__ __;按实验要求,图1中还缺少的玻璃仪器是__ __(填名称)。
(2)小婧按图2的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__ __;她称取的氯化钠实际质量为__ __g。
(3)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为__ __(水的密度为1 g/cm3)。
四、综合应用题(共12分)
20. 称取5.8 g某生铁样品放入94.6 g稀盐酸中,恰好完全反应(生铁样品中的杂质不溶于水也不与盐酸发生反应),产生0.2 g氢气。试计算反应后所得溶液中溶质的质量分数。
参考答案
一、选择题
1-6CDDACC 7-12DCBACD
二、填空题
13.水 乳化 煮沸
14.⑴溶剂性质 溶质性质 溶液温度 ⑵用汽油清洗衣服上的油污
15. (1)甲 (2)②④
16. (1)常温下苯甲酸溶解度很小 (2)减小过滤时苯甲酸的损失 (3)缓慢冷却至室温
17. (1)34.0 (2)m (3)34.0<x<37.0
三、实验探究题
18. (1) ①温度 温度越高,食盐溶解越快;
②是否搅拌 搅拌使食盐溶解更快
(2)温度 取两烧杯体积一样但温度不同的水,分别加入质量相同、颗粒大小一样的少量食盐,分别记录食盐完全溶解所需的时间。
19. (1)烧杯 玻璃棒
(2)称量时砝码放反了位置 12
(3)18%
四、综合应用题
20. 解:设5.8 g生铁样品中铁的质量为x,反应生成的FeCl2的质量为y。
Fe+2HCl===FeCl2+H2↑
56 127 2
x y 0.2 g
= x==5.6 g
= y==12.7 g
反应后所得FeCl2溶液中的溶质的质量分数为:×100%=12.7%
答:反应后所得FeCl2溶液中的溶质的质量分数为12.7%。
同课章节目录
