第九单元溶液-2021-2022学年九年级化学人教版下册 (1)(word版 含解析)
文档属性
| 名称 | 第九单元溶液-2021-2022学年九年级化学人教版下册 (1)(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 152.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-30 00:00:00 | ||
图片预览


文档简介
第九单元溶液2021_2022学年九年级化学(人教版)
一.选择题(共13小题)
1.下列操作会引起所配制的溶液溶质质量分数降低的是( )
A.用托盘天平称量6.2g食盐,误将砝码放在左盘并使用游码
B.称量时,两托盘分别垫上大小质量相同的纸
C.用量筒量水时,俯视凹液面的最低处
D.将配制好的溶液转移到试剂瓶时,不慎洒出
2.下列过程中,有一个去污原理与其他三个不同的是( )
A.用洗涤剂洗去餐具上的油脂
B.用汽油除去衣服上的油污
C.用酒精除去附着在试管内壁的碘
D.用热水洗去附着在烧杯底部的硝酸钾
3.衣服上沾有碘很难洗净.由下表分析,在家中除去碘污渍最好选用( )
溶质 溶剂
水 酒精 苯(一种有机物,有毒) 汽油
碘 微溶 可溶 易溶 易溶
A.水 B.苯 C.汽油 D.酒精
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2 叫做“干冰”,可用于制冷剂
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
5.下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )
A.面粉和水 B.酒精和水
C.植物油和汽油 D.碘和酒精
6.下列溶液中的溶剂不是水的是( )
A.碘酒 B.蔗糖水 C.盐酸 D.氯化钠溶液
7.铁与足量的稀硫酸完全反应后,最终得到的液体是( )
A.悬浊液 B.乳浊液 C.溶液 D.无法判断
8.生活中常用洗涤剂清洗油污,是因为它能将油污( )
A.乳化 B.分解 C.反应 D.溶解
9.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
10.下表是NaCl、KNO3 在不同温度时的溶解度
温度 10 20 30 40 50 60
溶解度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
据此数据,判断下列说法错误的是( )
A.KNO3 和NaCl 的溶解度曲线在20℃~30℃温度范围内会相交
B.在60℃时,KNO3 的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C.在20℃时,NaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D.从含有少量NaCl 的KNO3 饱和溶液中得到较多的KNO3 晶体,通常采用冷却热的饱和溶液法
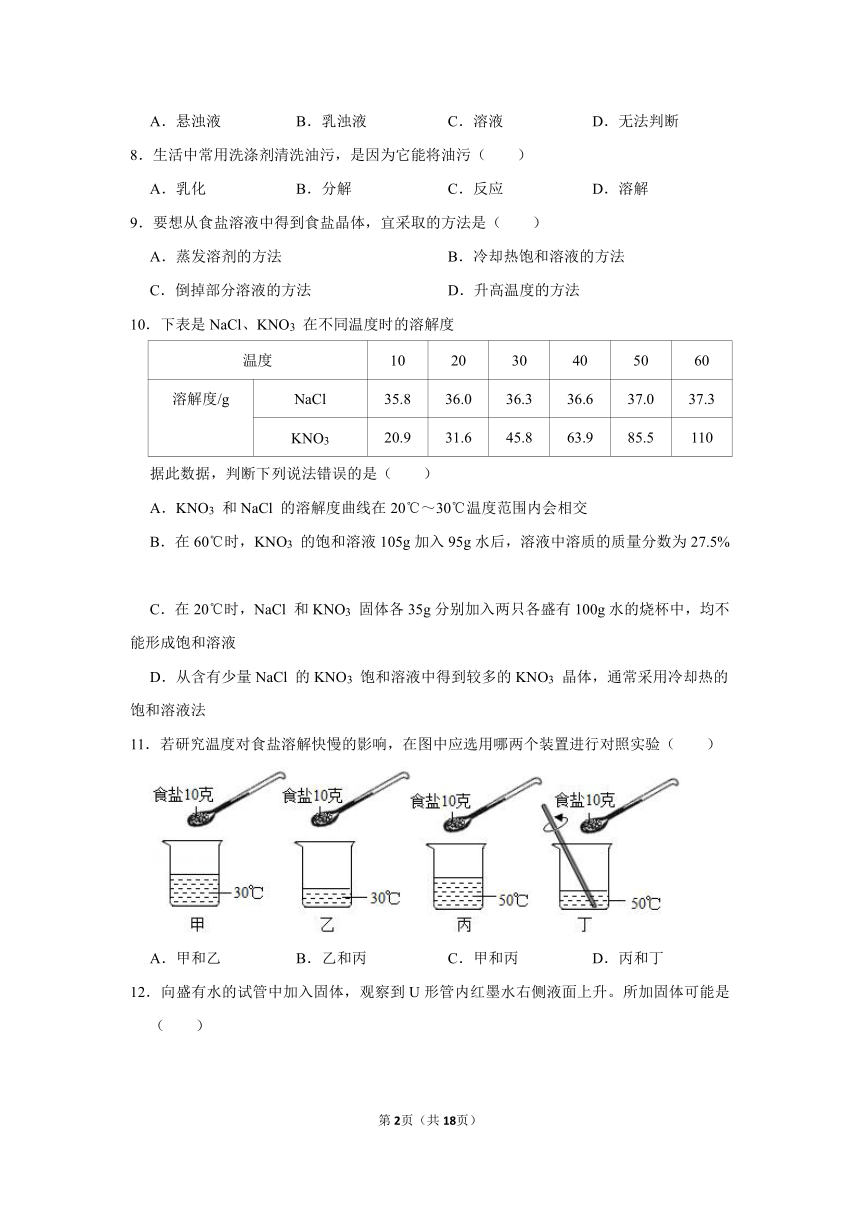
11.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
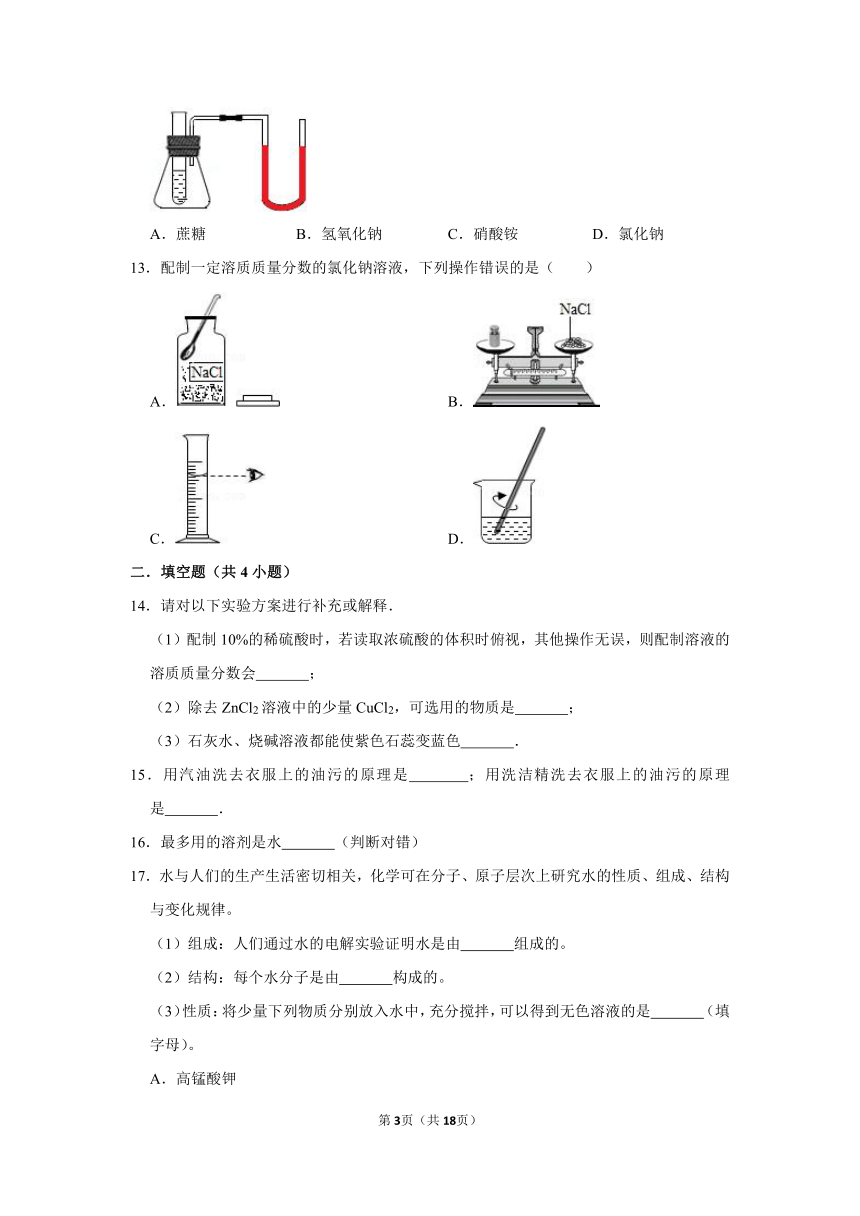
12.向盛有水的试管中加入固体,观察到U形管内红墨水右侧液面上升。所加固体可能是( )
A.蔗糖 B.氢氧化钠 C.硝酸铵 D.氯化钠
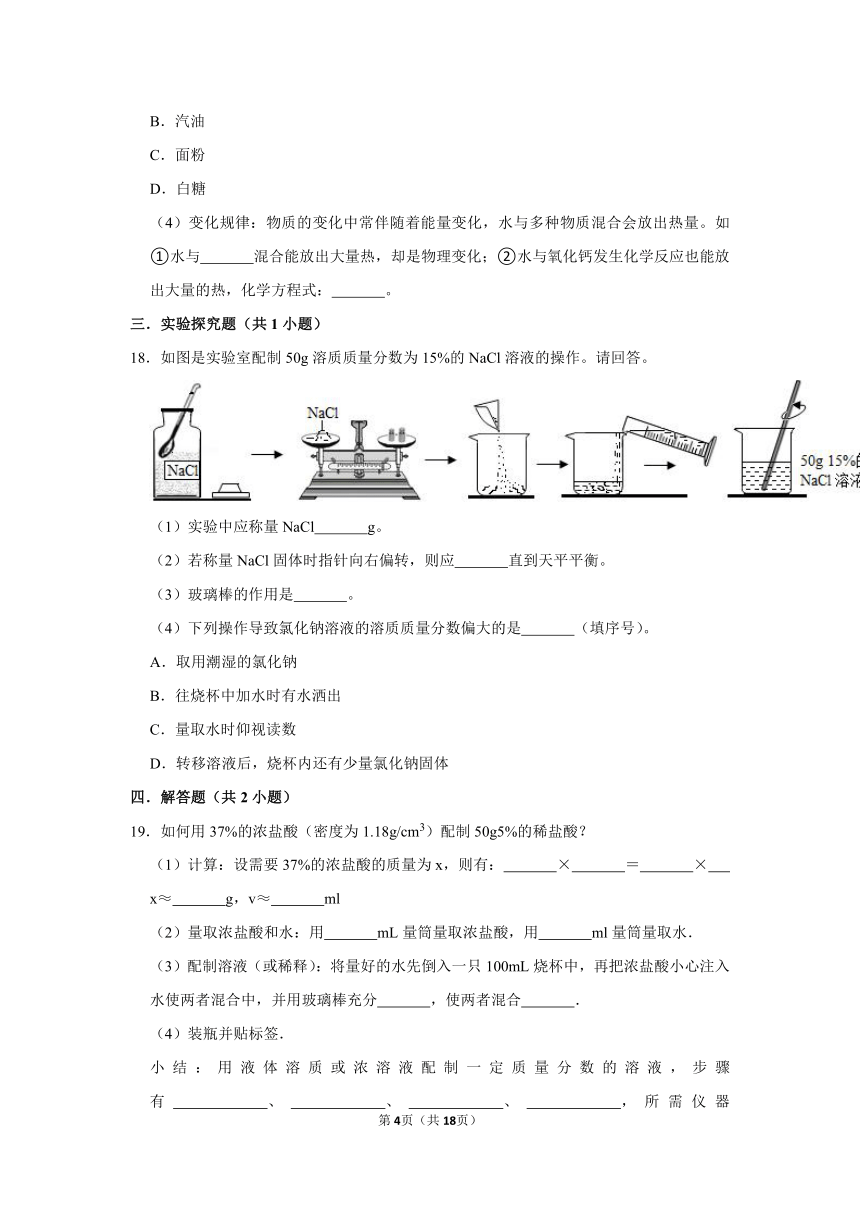
13.配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
A. B.
C. D.
二.填空题(共4小题)
14.请对以下实验方案进行补充或解释.
(1)配制10%的稀硫酸时,若读取浓硫酸的体积时俯视,其他操作无误,则配制溶液的溶质质量分数会 ;
(2)除去ZnCl2溶液中的少量CuCl2,可选用的物质是 ;
(3)石灰水、烧碱溶液都能使紫色石蕊变蓝色 .
15.用汽油洗去衣服上的油污的原理是 ;用洗洁精洗去衣服上的油污的原理是 .
16.最多用的溶剂是水 (判断对错)
17.水与人们的生产生活密切相关,化学可在分子、原子层次上研究水的性质、组成、结构与变化规律。
(1)组成:人们通过水的电解实验证明水是由 组成的。
(2)结构:每个水分子是由 构成的。
(3)性质:将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是 (填字母)。
A.高锰酸钾
B.汽油
C.面粉
D.白糖
(4)变化规律:物质的变化中常伴随着能量变化,水与多种物质混合会放出热量。如①水与 混合能放出大量热,却是物理变化;②水与氧化钙发生化学反应也能放出大量的热,化学方程式: 。
三.实验探究题(共1小题)
18.如图是实验室配制50g溶质质量分数为15%的NaCl溶液的操作。请回答。
(1)实验中应称量NaCl g。
(2)若称量NaCl固体时指针向右偏转,则应 直到天平平衡。
(3)玻璃棒的作用是 。
(4)下列操作导致氯化钠溶液的溶质质量分数偏大的是 (填序号)。
A.取用潮湿的氯化钠
B.往烧杯中加水时有水洒出
C.量取水时仰视读数
D.转移溶液后,烧杯内还有少量氯化钠固体
四.解答题(共2小题)
19.如何用37%的浓盐酸(密度为1.18g/cm3)配制50g5%的稀盐酸?
(1)计算:设需要37%的浓盐酸的质量为x,则有: × = ×
x≈ g,v≈ ml
(2)量取浓盐酸和水:用 mL量筒量取浓盐酸,用 ml量筒量取水.
(3)配制溶液(或稀释):将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分 ,使两者混合 .
(4)装瓶并贴标签.
小结:用液体溶质或浓溶液配制一定质量分数的溶液,步骤有 、 、 、 ,所需仪器有 、 、 、 、 .
20.将植物油放入汽油中看到的现象是 .
第九单元溶液2021_2022学年九年级化学(人教版)
参考答案与试题解析
一.选择题(共13小题)
1.下列操作会引起所配制的溶液溶质质量分数降低的是( )
A.用托盘天平称量6.2g食盐,误将砝码放在左盘并使用游码
B.称量时,两托盘分别垫上大小质量相同的纸
C.用量筒量水时,俯视凹液面的最低处
D.将配制好的溶液转移到试剂瓶时,不慎洒出
【分析】引起溶液中溶质的质量分数偏小,从两个方面考虑:①溶质少了(称量时左码右物并移动了游码、药品中含有杂质等)②水量多了(量水时仰视读数,烧杯中原来有水等).
【解答】解:
A、左码右物称量6.2g食盐,食盐的实际质量为5.8g,所以溶质少了,溶质质量分数就小了,故A正确;
B、称量时,两托盘分别垫上大小质量相同的纸,这是正确操作,不产生误差,故B错误;
C、俯视凹液面的最低处,会导致量水量少了,溶质质量分数偏大,故C错误;
D、由于溶液是均一的,将配制好的溶液转移到试剂瓶时,不慎洒出,溶质质量分数不变,故D错误。
故选:A。
【点评】通过回答本题知道了引起溶液中溶质的质量分数偏小的原因,主要从溶质和溶剂的质量两方面考虑.
2.下列过程中,有一个去污原理与其他三个不同的是( )
A.用洗涤剂洗去餐具上的油脂
B.用汽油除去衣服上的油污
C.用酒精除去附着在试管内壁的碘
D.用热水洗去附着在烧杯底部的硝酸钾
【分析】A、根据洗涤剂具有乳化作用,进行分析判断。
B、根据酒精能溶解碘,进行分析判断。
C、根据汽油能溶解油污,进行分析判断。
D、根据硝酸钾易溶于水,进行分析判断。
【解答】解:A、用洗涤剂洗去餐具上的油脂,是利用了洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴随水冲走,可洗去餐具上的油脂。
B、汽油能溶解油污,可用汽油除去衣服上的油污,利用的是溶解原理。
C、酒精能溶解碘,可用酒精除去附着在试管内壁的碘,利用的是溶解原理。
D、用热水洗去附着在烧杯底部的硝酸钾,利用的是溶解原理。
故A选项利用的去污原理与其他三个不同。
故选:A。
【点评】常见的洗涤原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污等发生化学反应,理解洗涤过程中利用的原理是解题的关键。
3.衣服上沾有碘很难洗净.由下表分析,在家中除去碘污渍最好选用( )
溶质 溶剂
水 酒精 苯(一种有机物,有毒) 汽油
碘 微溶 可溶 易溶 易溶
A.水 B.苯 C.汽油 D.酒精
【分析】根据碘在不同溶剂中的溶解性和各溶剂的性质,进行分析判断.
【解答】解:A、碘微溶于水,不能用水清洗来清除碘,故选项错误。
B、碘易溶于苯,但是苯有毒,故选项错误。
C、碘易溶于汽油,可用汽油快速除去碘渍,故选项正确。
D、碘可溶于酒精,能用于清洗碘,但是速度不是最快,故选项错误。
故选:C。
【点评】本题难度不大,理解溶解原理并能灵活运用是正确解答本题的关键.
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2 叫做“干冰”,可用于制冷剂
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
【分析】A、根据水是常见的溶剂,但不能溶解所有的物质分析判断;
B、根据一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析判断;
C、根据固体二氧化碳俗称干冰,易升华吸热判断;
D、根据磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁判断.
【解答】解:A、水是常见的溶剂,但不能溶解所有的物质,故A说法不正确;
B、一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力,造成生物体内缺氧,故B说法正确;
C、固体二氧化碳俗称干冰,易升华吸热,可用于制冷剂,故C说法正确;
D、磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁,故D说法正确。
故选:A。
【点评】本题考查了水、一氧化碳、二氧化碳的性质和铁矿石的主要成分,及他们的用途,综合性的考查,但难度不大.
5.下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )
A.面粉和水 B.酒精和水
C.植物油和汽油 D.碘和酒精
【分析】本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物。
【解答】解:A、面粉不溶于水,与水混合形成不均一、不稳定的悬浊液,故A正确;
B、酒精易溶于水,形成均一、稳定的混合物,属于溶液,故B错;
C、植物油溶于汽油,形成均一、稳定的混合物,属于溶液,故C错;
D、碘溶于酒精,形成均一、稳定的混合物,属于溶液,故D错。
故选:A。
【点评】应熟悉溶液是一种均一稳定的混合物,在不改变条件时,溶液的组成和浓度都不会发生变化,要与悬浊液和乳浊液区分。
6.下列溶液中的溶剂不是水的是( )
A.碘酒 B.蔗糖水 C.盐酸 D.氯化钠溶液
【分析】根据溶液中只要有水,水一定是溶剂回答本题.
【解答】解:A、碘酒是将碘溶解于酒精中,溶质是碘,溶剂是酒精,故A正确;
B、蔗糖水中溶质是蔗糖,溶剂是水,故B错;
C、盐酸中溶质是氯化氢气体,溶剂是水,故C错;
D、氯化钠溶液中溶质是氯化钠,溶剂是水,故D错。
故选:A。
【点评】固体、气体溶于液体时,固体、气体是溶质,液体是溶剂,溶液中只要有水,水一定是溶剂.
7.铁与足量的稀硫酸完全反应后,最终得到的液体是( )
A.悬浊液 B.乳浊液 C.溶液 D.无法判断
【分析】铁与稀硫酸反应生成硫酸亚铁和氢气,铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,据此进行分析判断.
【解答】解:A、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是悬浊液,故选项错误。
B、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是乳浊液,故选项错误。
C、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,故选项正确。
D、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是无法判断,故选项错误。
故选:C。
【点评】本题难度不大,掌握金属的化学性质、溶液的本质特征(均一性、稳定性、混合物)是解答本题的关键.
8.生活中常用洗涤剂清洗油污,是因为它能将油污( )
A.乳化 B.分解 C.反应 D.溶解
【分析】根据乳化原理来分析。
【解答】解:洗涤剂对油污有乳化作用,能将油污分解成小油滴,并随水流走,所以可用洗涤剂去除油污。
故选:A。
【点评】本题考查了洗涤剂的乳化作用以及应用,难度较小。
9.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
【分析】根据食盐的溶解度受温度的影响变化不大,进行分析解答.
【解答】解:A、食盐的溶解度受温度的影响变化不大,从食盐溶液中得到食盐晶体,可采用蒸发溶剂的方法,故选项正确。
B、食盐的溶解度受温度的影响变化不大,从食盐溶液中得到食盐晶体,可采用蒸发溶剂的方法,而不是冷却热饱和溶液的方法,故选项错误。
C、倒掉部分溶液的方法,不能从食盐溶液中得到食盐晶体,故选项错误。
D、食盐的溶解度受温度的影响变化不大,升高温度,不能从食盐溶液中得到食盐晶体,故选项错误。
故选:A。
【点评】本题难度不大,了解结晶的原理与方法(降温结晶、蒸发结晶)并能灵活运用是正确解答本题的关键.
10.下表是NaCl、KNO3 在不同温度时的溶解度
温度 10 20 30 40 50 60
溶解度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
据此数据,判断下列说法错误的是( )
A.KNO3 和NaCl 的溶解度曲线在20℃~30℃温度范围内会相交
B.在60℃时,KNO3 的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C.在20℃时,NaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D.从含有少量NaCl 的KNO3 饱和溶液中得到较多的KNO3 晶体,通常采用冷却热的饱和溶液法
【分析】根据表格提供的溶解度的数据结合饱和溶液的形成进行分析解答即可.
【解答】解:A、根据表格提供的数据可以发现,在20℃~30℃温度范围内硝酸钾和氯化钠存在溶解度相同的数值,故KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内会相交,正确;
B、在60℃时,硝酸钾的溶解度为110g,KNO3的饱和溶液105g,含有硝酸钾55g,加入95g水后,溶液中溶质的质量分数为,正确;
C、在20℃时,氯化钠的溶解度为36g,硝酸钾的溶解度为31.6g,gNaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,氯化钠不能形成饱和溶液,硝酸钾形成的是饱和溶液,错误;
D、硝酸钾的溶解度随温度的升高而变化很大,故含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热的饱和溶液的方法,正确;
故选:C。
【点评】掌握溶解度随温度变化的特点以及饱和溶液中结晶析出晶体的方法是正确解答本题的关键.
11.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
【分析】运用控制变量法来对影响溶解快慢的因素进行解答即可。
【解答】解:研究温度对食盐溶解快慢的影响,可选用甲与丙两个装置进行对照实验,
故选:C。
【点评】此题考查影响溶解快慢的因素,关键是运用控制变量法来对影响溶解快慢的因素解答。
12.向盛有水的试管中加入固体,观察到U形管内红墨水右侧液面上升。所加固体可能是( )
A.蔗糖 B.氢氧化钠 C.硝酸铵 D.氯化钠
【分析】根据物质溶于水时的吸热和放热现象进行分析,U形管右侧的液面明显上升,说明瓶内的气体压强增大;氢氧化钠溶于水时放热。
【解答】解:右边支管的红墨水液面上升,说明装置内气体压强增大,由于热胀冷缩的原理,可知物质溶于水放热,使瓶内气体膨胀,压强增大。
A、蔗糖加入水中温度没有明显的变化,错误;
B、氢氧化钠溶于水放出大量的热,正确;
C、硝酸铵溶于水温度降低。错误;
D、氯化钠加入水中温度没有明显的变化,错误。
故选:B。
【点评】本题考查了物质与水混合时能量的变化以及与压强结合的知识,完成此题,可以依据已有的知识进行.要求同学们熟记物质与水混合时能量的变化,以便灵活应用.
13.配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
A. B.
C. D.
【分析】根据配制溶质质量分数一定溶液的步骤中的注意事项考虑。
【解答】解:A、瓶塞倒放,用药匙取药品,故A操作正确;
B、应左物右码,故B操作错误;
C、视线与凹液面最低处保持水平,故C正确;
D、用玻璃棒搅拌溶解,故D操作正确。
由于该题选择错误的,故选:B。
【点评】要熟记配制溶液的注意事项,防止由于错误操作造成误差。
二.填空题(共4小题)
14.请对以下实验方案进行补充或解释.
(1)配制10%的稀硫酸时,若读取浓硫酸的体积时俯视,其他操作无误,则配制溶液的溶质质量分数会 偏小 ;
(2)除去ZnCl2溶液中的少量CuCl2,可选用的物质是 Zn粒 ;
(3)石灰水、烧碱溶液都能使紫色石蕊变蓝色 溶液中含有相同的OH﹣ .
【分析】(1)俯视意味着实际体积小于看到的体积,所以量取的浓硫酸的体积小.根据稀释前后溶质的质量不变即可判断.
(2)根据除杂的条件即可.
(3)根据酸碱指示剂的变色范围即可.
【解答】解:(1)俯视意味着实际体积小于看到的体积,所以量取的浓硫酸的体积偏小(或者溶质的质量偏小),又因为稀释前后溶质的质量不变,则最后溶液的浓度偏小,故答案为:偏小.
(2)除杂的条件是:①能除去杂质,②不能带入新的杂质,③不能和想要的物质反应.在金属活动性顺序表中,锌元素排在铜元素的前面,所以锌可以把铜从其盐中置换出来,即锌和氯化铜生成氯化锌和铜.故答案为:Zn粒.
(3)紫色石蕊试液遇到酸性溶液变红色,紫色石蕊试液遇到碱性溶液变蓝色.石灰水、烧碱溶液都是碱性溶液,所以都能使紫色石蕊试液变蓝色,故答案为:溶液中含有相同的OH﹣.
【点评】掌握除杂的条件和酸碱指示剂的变色范围,即除杂的条件是:①能除去杂质,②不能带入新的杂质,③不能和想要的物质反应;紫色石蕊试液遇到酸性溶液变红色,紫色石蕊试液遇到碱性溶液变蓝色.
15.用汽油洗去衣服上的油污的原理是 油污可以溶解在汽油里 ;用洗洁精洗去衣服上的油污的原理是 洗洁精具有乳化作用 .
【分析】根据常见的溶解现象和乳化作用进行分析解答;洗洁精、洗衣粉等这样的能使乳浊液变成稳定的混合物的物质称为乳化剂,乳化剂所起的作用称为乳化作用.
【解答】解:汽油能洗去衣服上的油污是因为油污易溶于汽油,利用的是溶解原理;
洗洁精中含有乳化剂,有乳化作用,能将大的油滴分散成细小的油滴,而能够随水流走.
故答案为:油污可以溶解在汽油里;洗洁精具有乳化作用.
【点评】常见的洗涤原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污等发生化学反应,理解洗涤过程中利用的原理是解题的关键.
16.最多用的溶剂是水 √ (判断对错)
【分析】根据常见的溶剂有水、汽油、酒精等,进行分析解答。
【解答】解:常见的溶剂有水、汽油、酒精等,最多用的溶剂是水,故正确;
答案:√。
【点评】本题难度不大,了解常见的溶剂的种类(水、汽油、酒精等)是正确解答本题的关键。
17.水与人们的生产生活密切相关,化学可在分子、原子层次上研究水的性质、组成、结构与变化规律。
(1)组成:人们通过水的电解实验证明水是由 氢元素和氧元素 组成的。
(2)结构:每个水分子是由 2个氢原子和1个氧原子 构成的。
(3)性质:将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是 D (填字母)。
A.高锰酸钾
B.汽油
C.面粉
D.白糖
(4)变化规律:物质的变化中常伴随着能量变化,水与多种物质混合会放出热量。如①水与 氢氧化钠固体(或浓硫酸) 混合能放出大量热,却是物理变化;②水与氧化钙发生化学反应也能放出大量的热,化学方程式: CaO+H2O=Ca(OH)2 。
【分析】(1)根据水的电解实验分析;
(2)根据水分子的微观结构分析;
(3)根据物质的溶解性以及溶液的颜色来分析;
(4)根据变化中能量变化分析。
【解答】解:(1)水通电生成氢气和氧气,通过该实验可以得出的结论是水是由氢氧两种元素组成的;
(2)由水分子的微观结构示意图可知,每个水分子是由2个氢原子和1个氧原子构成的;
(3)A.高锰酸钾溶于水,溶液为紫红色,故错误;
B.汽油难溶于水,不能形成溶液,故错误;
C.面粉难溶于水,不能形成溶液,故错误;
D.白糖溶于水,溶液为无色,故正确。
故填:D;
(4)①氢氧化钠固体或浓硫酸溶于水属于物理变化,溶解过程中会放出大量的热;
②水与氧化钙发生化学反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2 。
故答案为:(1)氢元素和氧元素;
(2)2个氢原子和1个氧原子;
(3)D;
(4)①氢氧化钠固体(或浓硫酸);
②CaO+H2O=Ca(OH)2 。
【点评】本题考查的知识点较多,掌握溶液的形成、水的电解、化学方程式的写法等是解题的关键。
三.实验探究题(共1小题)
18.如图是实验室配制50g溶质质量分数为15%的NaCl溶液的操作。请回答。
(1)实验中应称量NaCl 7.5 g。
(2)若称量NaCl固体时指针向右偏转,则应 添加氯化钠直到天平平衡 直到天平平衡。
(3)玻璃棒的作用是 搅拌,加速氯化钠固体的溶解 。
(4)下列操作导致氯化钠溶液的溶质质量分数偏大的是 B (填序号)。
A.取用潮湿的氯化钠
B.往烧杯中加水时有水洒出
C.量取水时仰视读数
D.转移溶液后,烧杯内还有少量氯化钠固体
【分析】(1)依据题中数据分析;
(2)依据天平指针向右偏转分析;
(3)依据玻璃棒的作用分析;
(4)依据选项信息分析。
【解答】解:(1)称量氯化钠的质量为50g×15%=7.5g;
(2)天平指针向右偏转,说明砝码重,则应加氯化钠直到天平平衡;
(3)溶液配制过程中,玻璃棒的作用是搅拌,加速氯化钠固体的溶解;
(4)A.称量时,取用潮湿的氯化钠,称取的氯化钠质量偏小,溶质质量分数偏小,故错误;
B.往烧杯中加水时有水洒出,溶剂质量偏少,溶质质量分数偏大,故正确。
C.量取水时仰视读数,水的实际体积偏大,溶质质量分数偏小,故错误;
D.将称量好的氯化钠转移倒入烧杯时,转移后烧杯内还有少量固体,溶质质量偏小,导致溶质的质量分数偏小,故错误。
故选:B。
故答案为:(1)7.5;
(2)添加氯化钠直到天平平衡;
(3)搅拌,加速氯化钠固体的溶解;
(4)B。
【点评】此题主要考查一定溶质质量分数溶液的配制,难度不大,学生易于完成。
四.解答题(共2小题)
19.如何用37%的浓盐酸(密度为1.18g/cm3)配制50g5%的稀盐酸?
(1)计算:设需要37%的浓盐酸的质量为x,则有: 50g × 5% = x × 37%
x≈ 6.8 g,v≈ 5.7 ml
(2)量取浓盐酸和水:用 10 mL量筒量取浓盐酸,用 50 ml量筒量取水.
(3)配制溶液(或稀释):将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分 搅拌 ,使两者混合 均匀 .
(4)装瓶并贴标签.
小结:用液体溶质或浓溶液配制一定质量分数的溶液,步骤有 计算 、 量取 、 溶解 、 装瓶 ,所需仪器有 量筒 、 滴管 、 烧杯 、 玻璃棒 、 试剂瓶 .
【分析】(1)溶液稀释前后,溶质质量不变;
(2)选择量筒时,量筒的量程应该大于或大于量取的液体体积,还应该和量取的液体体积最接近;
(3)烧杯是常用的配制溶液的容器;
(4)根据配制稀盐酸的过程可以判断实验步骤和相应的仪器.
【解答】解:(1)设需要37%的浓盐酸的质量为x,
根据题意有:50g×5%=x×37%,
x=6.8g,
6.8g盐酸的体积为:6.8g÷1.18g/mL=5.7mL,
故填:50g;5%;x;37%;6.8;5.7.
(2)需要水的体积为:(50g﹣1.18g/cm3×5.7mL)÷1g/mL=43.3mL,
因此应该用10mL的量筒量取5.7mL浓盐酸,用50mL量筒量取43.3mL水.
故填:10;50.
(3)将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分搅拌,使两者混合均匀.
故填:搅拌;均匀.
(4)用液体溶质或浓溶液配制一定质量分数的溶液,步骤有计算、量取、溶解、装瓶;
所需仪器有量筒、滴管、烧杯、玻璃棒、试剂瓶.
故填:计算、量取、溶解、装瓶;量筒、滴管、烧杯、玻璃棒、试剂瓶.
【点评】本题主要考查了配制溶液的过程,同时考查了计算能力,要注意掌握.
20.将植物油放入汽油中看到的现象是 均匀混合在一起 .
【分析】根据已有的知识进行分析解答,植物油溶于汽油,据此解答.
【解答】解:植物油溶于汽油,形成植物油的汽油溶液,因此是均匀混合在一起,故填:均匀混合在一起.
【点评】本题考查了溶解的知识,完成此题,可以依据已有的知识进行.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/29 20:55:19;用户:15877047552;邮箱:15877047552;学号:38945411第1页(共3页)
一.选择题(共13小题)
1.下列操作会引起所配制的溶液溶质质量分数降低的是( )
A.用托盘天平称量6.2g食盐,误将砝码放在左盘并使用游码
B.称量时,两托盘分别垫上大小质量相同的纸
C.用量筒量水时,俯视凹液面的最低处
D.将配制好的溶液转移到试剂瓶时,不慎洒出
2.下列过程中,有一个去污原理与其他三个不同的是( )
A.用洗涤剂洗去餐具上的油脂
B.用汽油除去衣服上的油污
C.用酒精除去附着在试管内壁的碘
D.用热水洗去附着在烧杯底部的硝酸钾
3.衣服上沾有碘很难洗净.由下表分析,在家中除去碘污渍最好选用( )
溶质 溶剂
水 酒精 苯(一种有机物,有毒) 汽油
碘 微溶 可溶 易溶 易溶
A.水 B.苯 C.汽油 D.酒精
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2 叫做“干冰”,可用于制冷剂
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
5.下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )
A.面粉和水 B.酒精和水
C.植物油和汽油 D.碘和酒精
6.下列溶液中的溶剂不是水的是( )
A.碘酒 B.蔗糖水 C.盐酸 D.氯化钠溶液
7.铁与足量的稀硫酸完全反应后,最终得到的液体是( )
A.悬浊液 B.乳浊液 C.溶液 D.无法判断
8.生活中常用洗涤剂清洗油污,是因为它能将油污( )
A.乳化 B.分解 C.反应 D.溶解
9.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
10.下表是NaCl、KNO3 在不同温度时的溶解度
温度 10 20 30 40 50 60
溶解度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
据此数据,判断下列说法错误的是( )
A.KNO3 和NaCl 的溶解度曲线在20℃~30℃温度范围内会相交
B.在60℃时,KNO3 的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C.在20℃时,NaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D.从含有少量NaCl 的KNO3 饱和溶液中得到较多的KNO3 晶体,通常采用冷却热的饱和溶液法
11.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
12.向盛有水的试管中加入固体,观察到U形管内红墨水右侧液面上升。所加固体可能是( )
A.蔗糖 B.氢氧化钠 C.硝酸铵 D.氯化钠
13.配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
A. B.
C. D.
二.填空题(共4小题)
14.请对以下实验方案进行补充或解释.
(1)配制10%的稀硫酸时,若读取浓硫酸的体积时俯视,其他操作无误,则配制溶液的溶质质量分数会 ;
(2)除去ZnCl2溶液中的少量CuCl2,可选用的物质是 ;
(3)石灰水、烧碱溶液都能使紫色石蕊变蓝色 .
15.用汽油洗去衣服上的油污的原理是 ;用洗洁精洗去衣服上的油污的原理是 .
16.最多用的溶剂是水 (判断对错)
17.水与人们的生产生活密切相关,化学可在分子、原子层次上研究水的性质、组成、结构与变化规律。
(1)组成:人们通过水的电解实验证明水是由 组成的。
(2)结构:每个水分子是由 构成的。
(3)性质:将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是 (填字母)。
A.高锰酸钾
B.汽油
C.面粉
D.白糖
(4)变化规律:物质的变化中常伴随着能量变化,水与多种物质混合会放出热量。如①水与 混合能放出大量热,却是物理变化;②水与氧化钙发生化学反应也能放出大量的热,化学方程式: 。
三.实验探究题(共1小题)
18.如图是实验室配制50g溶质质量分数为15%的NaCl溶液的操作。请回答。
(1)实验中应称量NaCl g。
(2)若称量NaCl固体时指针向右偏转,则应 直到天平平衡。
(3)玻璃棒的作用是 。
(4)下列操作导致氯化钠溶液的溶质质量分数偏大的是 (填序号)。
A.取用潮湿的氯化钠
B.往烧杯中加水时有水洒出
C.量取水时仰视读数
D.转移溶液后,烧杯内还有少量氯化钠固体
四.解答题(共2小题)
19.如何用37%的浓盐酸(密度为1.18g/cm3)配制50g5%的稀盐酸?
(1)计算:设需要37%的浓盐酸的质量为x,则有: × = ×
x≈ g,v≈ ml
(2)量取浓盐酸和水:用 mL量筒量取浓盐酸,用 ml量筒量取水.
(3)配制溶液(或稀释):将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分 ,使两者混合 .
(4)装瓶并贴标签.
小结:用液体溶质或浓溶液配制一定质量分数的溶液,步骤有 、 、 、 ,所需仪器有 、 、 、 、 .
20.将植物油放入汽油中看到的现象是 .
第九单元溶液2021_2022学年九年级化学(人教版)
参考答案与试题解析
一.选择题(共13小题)
1.下列操作会引起所配制的溶液溶质质量分数降低的是( )
A.用托盘天平称量6.2g食盐,误将砝码放在左盘并使用游码
B.称量时,两托盘分别垫上大小质量相同的纸
C.用量筒量水时,俯视凹液面的最低处
D.将配制好的溶液转移到试剂瓶时,不慎洒出
【分析】引起溶液中溶质的质量分数偏小,从两个方面考虑:①溶质少了(称量时左码右物并移动了游码、药品中含有杂质等)②水量多了(量水时仰视读数,烧杯中原来有水等).
【解答】解:
A、左码右物称量6.2g食盐,食盐的实际质量为5.8g,所以溶质少了,溶质质量分数就小了,故A正确;
B、称量时,两托盘分别垫上大小质量相同的纸,这是正确操作,不产生误差,故B错误;
C、俯视凹液面的最低处,会导致量水量少了,溶质质量分数偏大,故C错误;
D、由于溶液是均一的,将配制好的溶液转移到试剂瓶时,不慎洒出,溶质质量分数不变,故D错误。
故选:A。
【点评】通过回答本题知道了引起溶液中溶质的质量分数偏小的原因,主要从溶质和溶剂的质量两方面考虑.
2.下列过程中,有一个去污原理与其他三个不同的是( )
A.用洗涤剂洗去餐具上的油脂
B.用汽油除去衣服上的油污
C.用酒精除去附着在试管内壁的碘
D.用热水洗去附着在烧杯底部的硝酸钾
【分析】A、根据洗涤剂具有乳化作用,进行分析判断。
B、根据酒精能溶解碘,进行分析判断。
C、根据汽油能溶解油污,进行分析判断。
D、根据硝酸钾易溶于水,进行分析判断。
【解答】解:A、用洗涤剂洗去餐具上的油脂,是利用了洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴随水冲走,可洗去餐具上的油脂。
B、汽油能溶解油污,可用汽油除去衣服上的油污,利用的是溶解原理。
C、酒精能溶解碘,可用酒精除去附着在试管内壁的碘,利用的是溶解原理。
D、用热水洗去附着在烧杯底部的硝酸钾,利用的是溶解原理。
故A选项利用的去污原理与其他三个不同。
故选:A。
【点评】常见的洗涤原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污等发生化学反应,理解洗涤过程中利用的原理是解题的关键。
3.衣服上沾有碘很难洗净.由下表分析,在家中除去碘污渍最好选用( )
溶质 溶剂
水 酒精 苯(一种有机物,有毒) 汽油
碘 微溶 可溶 易溶 易溶
A.水 B.苯 C.汽油 D.酒精
【分析】根据碘在不同溶剂中的溶解性和各溶剂的性质,进行分析判断.
【解答】解:A、碘微溶于水,不能用水清洗来清除碘,故选项错误。
B、碘易溶于苯,但是苯有毒,故选项错误。
C、碘易溶于汽油,可用汽油快速除去碘渍,故选项正确。
D、碘可溶于酒精,能用于清洗碘,但是速度不是最快,故选项错误。
故选:C。
【点评】本题难度不大,理解溶解原理并能灵活运用是正确解答本题的关键.
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2 叫做“干冰”,可用于制冷剂
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
【分析】A、根据水是常见的溶剂,但不能溶解所有的物质分析判断;
B、根据一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析判断;
C、根据固体二氧化碳俗称干冰,易升华吸热判断;
D、根据磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁判断.
【解答】解:A、水是常见的溶剂,但不能溶解所有的物质,故A说法不正确;
B、一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力,造成生物体内缺氧,故B说法正确;
C、固体二氧化碳俗称干冰,易升华吸热,可用于制冷剂,故C说法正确;
D、磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁,故D说法正确。
故选:A。
【点评】本题考查了水、一氧化碳、二氧化碳的性质和铁矿石的主要成分,及他们的用途,综合性的考查,但难度不大.
5.下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )
A.面粉和水 B.酒精和水
C.植物油和汽油 D.碘和酒精
【分析】本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物。
【解答】解:A、面粉不溶于水,与水混合形成不均一、不稳定的悬浊液,故A正确;
B、酒精易溶于水,形成均一、稳定的混合物,属于溶液,故B错;
C、植物油溶于汽油,形成均一、稳定的混合物,属于溶液,故C错;
D、碘溶于酒精,形成均一、稳定的混合物,属于溶液,故D错。
故选:A。
【点评】应熟悉溶液是一种均一稳定的混合物,在不改变条件时,溶液的组成和浓度都不会发生变化,要与悬浊液和乳浊液区分。
6.下列溶液中的溶剂不是水的是( )
A.碘酒 B.蔗糖水 C.盐酸 D.氯化钠溶液
【分析】根据溶液中只要有水,水一定是溶剂回答本题.
【解答】解:A、碘酒是将碘溶解于酒精中,溶质是碘,溶剂是酒精,故A正确;
B、蔗糖水中溶质是蔗糖,溶剂是水,故B错;
C、盐酸中溶质是氯化氢气体,溶剂是水,故C错;
D、氯化钠溶液中溶质是氯化钠,溶剂是水,故D错。
故选:A。
【点评】固体、气体溶于液体时,固体、气体是溶质,液体是溶剂,溶液中只要有水,水一定是溶剂.
7.铁与足量的稀硫酸完全反应后,最终得到的液体是( )
A.悬浊液 B.乳浊液 C.溶液 D.无法判断
【分析】铁与稀硫酸反应生成硫酸亚铁和氢气,铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,据此进行分析判断.
【解答】解:A、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是悬浊液,故选项错误。
B、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是乳浊液,故选项错误。
C、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,故选项正确。
D、铁与足量的稀硫酸完全反应后,最终得到的液体是硫酸亚铁和稀硫酸的混合溶液,不是无法判断,故选项错误。
故选:C。
【点评】本题难度不大,掌握金属的化学性质、溶液的本质特征(均一性、稳定性、混合物)是解答本题的关键.
8.生活中常用洗涤剂清洗油污,是因为它能将油污( )
A.乳化 B.分解 C.反应 D.溶解
【分析】根据乳化原理来分析。
【解答】解:洗涤剂对油污有乳化作用,能将油污分解成小油滴,并随水流走,所以可用洗涤剂去除油污。
故选:A。
【点评】本题考查了洗涤剂的乳化作用以及应用,难度较小。
9.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
【分析】根据食盐的溶解度受温度的影响变化不大,进行分析解答.
【解答】解:A、食盐的溶解度受温度的影响变化不大,从食盐溶液中得到食盐晶体,可采用蒸发溶剂的方法,故选项正确。
B、食盐的溶解度受温度的影响变化不大,从食盐溶液中得到食盐晶体,可采用蒸发溶剂的方法,而不是冷却热饱和溶液的方法,故选项错误。
C、倒掉部分溶液的方法,不能从食盐溶液中得到食盐晶体,故选项错误。
D、食盐的溶解度受温度的影响变化不大,升高温度,不能从食盐溶液中得到食盐晶体,故选项错误。
故选:A。
【点评】本题难度不大,了解结晶的原理与方法(降温结晶、蒸发结晶)并能灵活运用是正确解答本题的关键.
10.下表是NaCl、KNO3 在不同温度时的溶解度
温度 10 20 30 40 50 60
溶解度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
据此数据,判断下列说法错误的是( )
A.KNO3 和NaCl 的溶解度曲线在20℃~30℃温度范围内会相交
B.在60℃时,KNO3 的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C.在20℃时,NaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D.从含有少量NaCl 的KNO3 饱和溶液中得到较多的KNO3 晶体,通常采用冷却热的饱和溶液法
【分析】根据表格提供的溶解度的数据结合饱和溶液的形成进行分析解答即可.
【解答】解:A、根据表格提供的数据可以发现,在20℃~30℃温度范围内硝酸钾和氯化钠存在溶解度相同的数值,故KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内会相交,正确;
B、在60℃时,硝酸钾的溶解度为110g,KNO3的饱和溶液105g,含有硝酸钾55g,加入95g水后,溶液中溶质的质量分数为,正确;
C、在20℃时,氯化钠的溶解度为36g,硝酸钾的溶解度为31.6g,gNaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,氯化钠不能形成饱和溶液,硝酸钾形成的是饱和溶液,错误;
D、硝酸钾的溶解度随温度的升高而变化很大,故含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热的饱和溶液的方法,正确;
故选:C。
【点评】掌握溶解度随温度变化的特点以及饱和溶液中结晶析出晶体的方法是正确解答本题的关键.
11.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
【分析】运用控制变量法来对影响溶解快慢的因素进行解答即可。
【解答】解:研究温度对食盐溶解快慢的影响,可选用甲与丙两个装置进行对照实验,
故选:C。
【点评】此题考查影响溶解快慢的因素,关键是运用控制变量法来对影响溶解快慢的因素解答。
12.向盛有水的试管中加入固体,观察到U形管内红墨水右侧液面上升。所加固体可能是( )
A.蔗糖 B.氢氧化钠 C.硝酸铵 D.氯化钠
【分析】根据物质溶于水时的吸热和放热现象进行分析,U形管右侧的液面明显上升,说明瓶内的气体压强增大;氢氧化钠溶于水时放热。
【解答】解:右边支管的红墨水液面上升,说明装置内气体压强增大,由于热胀冷缩的原理,可知物质溶于水放热,使瓶内气体膨胀,压强增大。
A、蔗糖加入水中温度没有明显的变化,错误;
B、氢氧化钠溶于水放出大量的热,正确;
C、硝酸铵溶于水温度降低。错误;
D、氯化钠加入水中温度没有明显的变化,错误。
故选:B。
【点评】本题考查了物质与水混合时能量的变化以及与压强结合的知识,完成此题,可以依据已有的知识进行.要求同学们熟记物质与水混合时能量的变化,以便灵活应用.
13.配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
A. B.
C. D.
【分析】根据配制溶质质量分数一定溶液的步骤中的注意事项考虑。
【解答】解:A、瓶塞倒放,用药匙取药品,故A操作正确;
B、应左物右码,故B操作错误;
C、视线与凹液面最低处保持水平,故C正确;
D、用玻璃棒搅拌溶解,故D操作正确。
由于该题选择错误的,故选:B。
【点评】要熟记配制溶液的注意事项,防止由于错误操作造成误差。
二.填空题(共4小题)
14.请对以下实验方案进行补充或解释.
(1)配制10%的稀硫酸时,若读取浓硫酸的体积时俯视,其他操作无误,则配制溶液的溶质质量分数会 偏小 ;
(2)除去ZnCl2溶液中的少量CuCl2,可选用的物质是 Zn粒 ;
(3)石灰水、烧碱溶液都能使紫色石蕊变蓝色 溶液中含有相同的OH﹣ .
【分析】(1)俯视意味着实际体积小于看到的体积,所以量取的浓硫酸的体积小.根据稀释前后溶质的质量不变即可判断.
(2)根据除杂的条件即可.
(3)根据酸碱指示剂的变色范围即可.
【解答】解:(1)俯视意味着实际体积小于看到的体积,所以量取的浓硫酸的体积偏小(或者溶质的质量偏小),又因为稀释前后溶质的质量不变,则最后溶液的浓度偏小,故答案为:偏小.
(2)除杂的条件是:①能除去杂质,②不能带入新的杂质,③不能和想要的物质反应.在金属活动性顺序表中,锌元素排在铜元素的前面,所以锌可以把铜从其盐中置换出来,即锌和氯化铜生成氯化锌和铜.故答案为:Zn粒.
(3)紫色石蕊试液遇到酸性溶液变红色,紫色石蕊试液遇到碱性溶液变蓝色.石灰水、烧碱溶液都是碱性溶液,所以都能使紫色石蕊试液变蓝色,故答案为:溶液中含有相同的OH﹣.
【点评】掌握除杂的条件和酸碱指示剂的变色范围,即除杂的条件是:①能除去杂质,②不能带入新的杂质,③不能和想要的物质反应;紫色石蕊试液遇到酸性溶液变红色,紫色石蕊试液遇到碱性溶液变蓝色.
15.用汽油洗去衣服上的油污的原理是 油污可以溶解在汽油里 ;用洗洁精洗去衣服上的油污的原理是 洗洁精具有乳化作用 .
【分析】根据常见的溶解现象和乳化作用进行分析解答;洗洁精、洗衣粉等这样的能使乳浊液变成稳定的混合物的物质称为乳化剂,乳化剂所起的作用称为乳化作用.
【解答】解:汽油能洗去衣服上的油污是因为油污易溶于汽油,利用的是溶解原理;
洗洁精中含有乳化剂,有乳化作用,能将大的油滴分散成细小的油滴,而能够随水流走.
故答案为:油污可以溶解在汽油里;洗洁精具有乳化作用.
【点评】常见的洗涤原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污等发生化学反应,理解洗涤过程中利用的原理是解题的关键.
16.最多用的溶剂是水 √ (判断对错)
【分析】根据常见的溶剂有水、汽油、酒精等,进行分析解答。
【解答】解:常见的溶剂有水、汽油、酒精等,最多用的溶剂是水,故正确;
答案:√。
【点评】本题难度不大,了解常见的溶剂的种类(水、汽油、酒精等)是正确解答本题的关键。
17.水与人们的生产生活密切相关,化学可在分子、原子层次上研究水的性质、组成、结构与变化规律。
(1)组成:人们通过水的电解实验证明水是由 氢元素和氧元素 组成的。
(2)结构:每个水分子是由 2个氢原子和1个氧原子 构成的。
(3)性质:将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是 D (填字母)。
A.高锰酸钾
B.汽油
C.面粉
D.白糖
(4)变化规律:物质的变化中常伴随着能量变化,水与多种物质混合会放出热量。如①水与 氢氧化钠固体(或浓硫酸) 混合能放出大量热,却是物理变化;②水与氧化钙发生化学反应也能放出大量的热,化学方程式: CaO+H2O=Ca(OH)2 。
【分析】(1)根据水的电解实验分析;
(2)根据水分子的微观结构分析;
(3)根据物质的溶解性以及溶液的颜色来分析;
(4)根据变化中能量变化分析。
【解答】解:(1)水通电生成氢气和氧气,通过该实验可以得出的结论是水是由氢氧两种元素组成的;
(2)由水分子的微观结构示意图可知,每个水分子是由2个氢原子和1个氧原子构成的;
(3)A.高锰酸钾溶于水,溶液为紫红色,故错误;
B.汽油难溶于水,不能形成溶液,故错误;
C.面粉难溶于水,不能形成溶液,故错误;
D.白糖溶于水,溶液为无色,故正确。
故填:D;
(4)①氢氧化钠固体或浓硫酸溶于水属于物理变化,溶解过程中会放出大量的热;
②水与氧化钙发生化学反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2 。
故答案为:(1)氢元素和氧元素;
(2)2个氢原子和1个氧原子;
(3)D;
(4)①氢氧化钠固体(或浓硫酸);
②CaO+H2O=Ca(OH)2 。
【点评】本题考查的知识点较多,掌握溶液的形成、水的电解、化学方程式的写法等是解题的关键。
三.实验探究题(共1小题)
18.如图是实验室配制50g溶质质量分数为15%的NaCl溶液的操作。请回答。
(1)实验中应称量NaCl 7.5 g。
(2)若称量NaCl固体时指针向右偏转,则应 添加氯化钠直到天平平衡 直到天平平衡。
(3)玻璃棒的作用是 搅拌,加速氯化钠固体的溶解 。
(4)下列操作导致氯化钠溶液的溶质质量分数偏大的是 B (填序号)。
A.取用潮湿的氯化钠
B.往烧杯中加水时有水洒出
C.量取水时仰视读数
D.转移溶液后,烧杯内还有少量氯化钠固体
【分析】(1)依据题中数据分析;
(2)依据天平指针向右偏转分析;
(3)依据玻璃棒的作用分析;
(4)依据选项信息分析。
【解答】解:(1)称量氯化钠的质量为50g×15%=7.5g;
(2)天平指针向右偏转,说明砝码重,则应加氯化钠直到天平平衡;
(3)溶液配制过程中,玻璃棒的作用是搅拌,加速氯化钠固体的溶解;
(4)A.称量时,取用潮湿的氯化钠,称取的氯化钠质量偏小,溶质质量分数偏小,故错误;
B.往烧杯中加水时有水洒出,溶剂质量偏少,溶质质量分数偏大,故正确。
C.量取水时仰视读数,水的实际体积偏大,溶质质量分数偏小,故错误;
D.将称量好的氯化钠转移倒入烧杯时,转移后烧杯内还有少量固体,溶质质量偏小,导致溶质的质量分数偏小,故错误。
故选:B。
故答案为:(1)7.5;
(2)添加氯化钠直到天平平衡;
(3)搅拌,加速氯化钠固体的溶解;
(4)B。
【点评】此题主要考查一定溶质质量分数溶液的配制,难度不大,学生易于完成。
四.解答题(共2小题)
19.如何用37%的浓盐酸(密度为1.18g/cm3)配制50g5%的稀盐酸?
(1)计算:设需要37%的浓盐酸的质量为x,则有: 50g × 5% = x × 37%
x≈ 6.8 g,v≈ 5.7 ml
(2)量取浓盐酸和水:用 10 mL量筒量取浓盐酸,用 50 ml量筒量取水.
(3)配制溶液(或稀释):将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分 搅拌 ,使两者混合 均匀 .
(4)装瓶并贴标签.
小结:用液体溶质或浓溶液配制一定质量分数的溶液,步骤有 计算 、 量取 、 溶解 、 装瓶 ,所需仪器有 量筒 、 滴管 、 烧杯 、 玻璃棒 、 试剂瓶 .
【分析】(1)溶液稀释前后,溶质质量不变;
(2)选择量筒时,量筒的量程应该大于或大于量取的液体体积,还应该和量取的液体体积最接近;
(3)烧杯是常用的配制溶液的容器;
(4)根据配制稀盐酸的过程可以判断实验步骤和相应的仪器.
【解答】解:(1)设需要37%的浓盐酸的质量为x,
根据题意有:50g×5%=x×37%,
x=6.8g,
6.8g盐酸的体积为:6.8g÷1.18g/mL=5.7mL,
故填:50g;5%;x;37%;6.8;5.7.
(2)需要水的体积为:(50g﹣1.18g/cm3×5.7mL)÷1g/mL=43.3mL,
因此应该用10mL的量筒量取5.7mL浓盐酸,用50mL量筒量取43.3mL水.
故填:10;50.
(3)将量好的水先倒入一只100mL烧杯中,再把浓盐酸小心注入水使两者混合中,并用玻璃棒充分搅拌,使两者混合均匀.
故填:搅拌;均匀.
(4)用液体溶质或浓溶液配制一定质量分数的溶液,步骤有计算、量取、溶解、装瓶;
所需仪器有量筒、滴管、烧杯、玻璃棒、试剂瓶.
故填:计算、量取、溶解、装瓶;量筒、滴管、烧杯、玻璃棒、试剂瓶.
【点评】本题主要考查了配制溶液的过程,同时考查了计算能力,要注意掌握.
20.将植物油放入汽油中看到的现象是 均匀混合在一起 .
【分析】根据已有的知识进行分析解答,植物油溶于汽油,据此解答.
【解答】解:植物油溶于汽油,形成植物油的汽油溶液,因此是均匀混合在一起,故填:均匀混合在一起.
【点评】本题考查了溶解的知识,完成此题,可以依据已有的知识进行.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/29 20:55:19;用户:15877047552;邮箱:15877047552;学号:38945411第1页(共3页)
同课章节目录
