第九单元溶液单元测试卷-2021-2022学年九年级化学人教版下册(word版 含解析)
文档属性
| 名称 | 第九单元溶液单元测试卷-2021-2022学年九年级化学人教版下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 143.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-30 00:00:00 | ||
图片预览



文档简介
第九单元溶液2021_2022学年九年级化学同步练习(人教版)
一.选择题(共13小题)
1.在配制75g质量分数为10%的NaCl溶液过程中,某同学进行了下列操作:①用量筒量取水时俯视读数;②把量筒中的水转移到配制溶液的烧杯中时有少许洒出;③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡;④配制溶液的烧杯用少量蒸馏水润洗.以下叙述正确的是( )
A.以上操作除④外都有错误
B.以上操作会使所配溶液的溶质质量分数偏大的只有①
C.以上操作可能使所配溶液的溶质质量分数偏小的只有④
D.以上操作可能会使所配溶液的溶质质量分数偏大或偏小的是③
2.下列现象中,不属于溶解现象的是( )
A.把食盐投入水中 B.把植物油注入汽油中
C.把泥土投入到水中 D.把品红投入到水中
3.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是( )
A.水 B.酒精 C.汽油 D.苯
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2叫做“干冰”,可用于人工降雨
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
5.厨房是家庭中的小小实验室,厨房中有①面粉②豆油③纯碱④料酒⑤味精⑥胡椒面⑦面酱⑧食醋⑨食盐⑩白砂糖等,把它们分别放入适量水中,充分搅拌能够得到溶液的是( )
A.①③⑤⑥⑧⑨⑩ B.③④⑤⑧⑨⑩ C.②③⑦⑧⑨⑩ D.③④⑥⑧⑨⑩
6.下列各组物质混合形成的溶液中,前者是溶剂,后者是溶质的一组是( )
A.糖、水 B.硫酸铜、水
C.酒精、碘 D.氢氧化钠、水
7.锌与足量的盐酸反应后的液体和少量二氧化碳通入澄清石灰水后的液体分别是( )
A.乳浊液、溶液 B.溶液、乳浊液
C.悬浊液、乳浊液 D.溶液、悬浊液
8.各种洗涤剂广泛进入人们的生活,下列所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣
D.用沐浴露洗澡
9.海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度变小
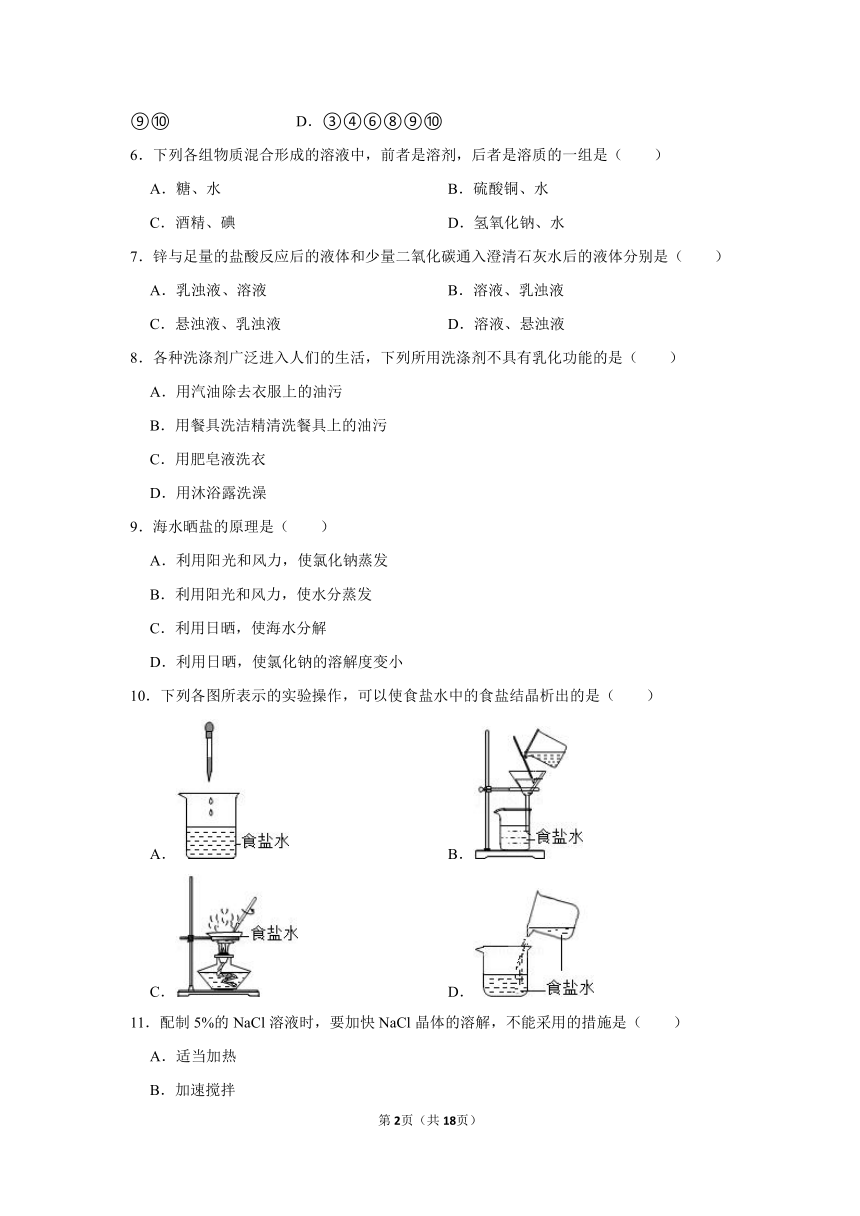
10.下列各图所表示的实验操作,可以使食盐水中的食盐结晶析出的是( )
A. B.
C. D.
11.配制5%的NaCl溶液时,要加快NaCl晶体的溶解,不能采用的措施是( )
A.适当加热
B.加速搅拌
C.选用颗粒较小的NaCl晶体
D.降低温度
12.下列物质能对啤酒起冰镇作用的是( )
A.木炭 B.氯化钠 C.氢氧化钠 D.硝酸铵
13.要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是( )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中
二.填空题(共4小题)
14.实验室配制溶液时,有以下操作:
①溶解 ②称量 ③计算 ④装瓶存放,贴上标签.
回答下列问题:
(1)现欲配制50g 5%氯化钠溶液,操作步骤为 (填序号).
(2)溶解操作中需要的仪器有 、 .
(3)量取蒸馏水时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 (填“<”或“>”)5%.
15.汽油能洗去衣服上的油污,这是由于汽油能 油污,形成 .用加了洗涤剂的水也能洗去油污,这是由于洗涤剂能 油污,形成 ,两者去污的原理 (填“相同”或“不同”)
16.溶液一定是某种溶质与水组成的 .
17.水是人类宝贵的自然资源,与人类的生产、生活密切相关.
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是 .
A.蔗糖 B.纯碱 C.食盐 D.花生油
(2)“节约用水,从我做起”.请你写出一种生活中节约用水的做法 .
(3)为了保护水质,下列做法合理的是 .
A.随意丢弃废旧电池 B.生活污水经处理达标后排放
C.农业上合理使用农药、化肥 D.工业“三废”未经处理任意排放
(4)通过电解水实验,可以知道水是由 组成.
(5)生活中降低水的硬度的常用方法是 .
(6)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号) .
三.实验探究题(共1小题)
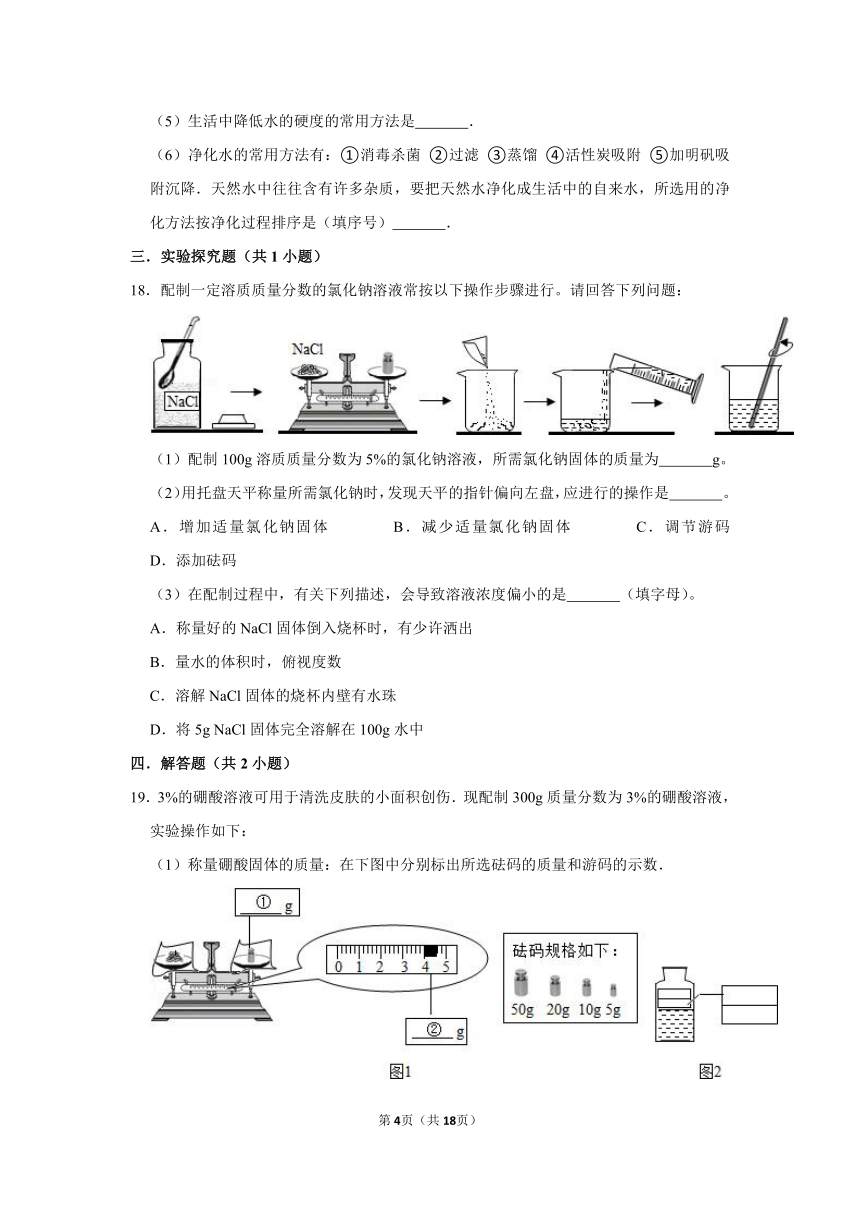
18.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
四.解答题(共2小题)
19.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
20.汽油可以溶解油渍,这是根据汽油中的 与油污相解离;若只是因为汽油是有机溶液,那么此油渍可不可以被其他油类溶液所溶解?
第九单元溶液2021_2022学年九年级化学同步练习(人教版)
参考答案与试题解析
一.选择题(共13小题)
1.在配制75g质量分数为10%的NaCl溶液过程中,某同学进行了下列操作:①用量筒量取水时俯视读数;②把量筒中的水转移到配制溶液的烧杯中时有少许洒出;③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡;④配制溶液的烧杯用少量蒸馏水润洗.以下叙述正确的是( )
A.以上操作除④外都有错误
B.以上操作会使所配溶液的溶质质量分数偏大的只有①
C.以上操作可能使所配溶液的溶质质量分数偏小的只有④
D.以上操作可能会使所配溶液的溶质质量分数偏大或偏小的是③
【分析】抓住导致配制溶液时所出现误差的根本原因:溶质量或多或少、溶剂量或多或少,分析各项操作对溶质、溶剂量所造成的影响解答即可.
【解答】解:①用量筒量取水时俯视读数,读数大于所量水的实际体积,使量取水的体积偏小,所配制氯化钠溶液的质量分数偏大;
②把量筒中的水转移到配制溶液的烧杯中时有少许洒出,使溶解时所加水的体积偏小,所配制氯化钠溶液的质量分数偏大;
③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡,会使氯化钠的质量偏大或偏小,所配制氯化钠溶液的质量分数也会随着偏大或偏小;
④配制溶液的烧杯用蒸馏水润洗,水的体积因此而偏大,所配制氯化钠溶液的质量分数偏小;
综合推断,故选D
【点评】用量筒量取液体时,仰视读数偏小,俯视读数偏大;天平称量时左盘放砝码而右盘放药品,药品的质量为砝码与游码的质量差.
2.下列现象中,不属于溶解现象的是( )
A.把食盐投入水中 B.把植物油注入汽油中
C.把泥土投入到水中 D.把品红投入到水中
【分析】根据溶解的概念去解答.(一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液,这一过程叫溶解.)
【解答】解:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液,这一过程叫溶解。
ABD中涉及到的溶质都会溶于溶剂中,所以形成的都是溶液,这三个过程都叫溶解,但C中泥土不溶于水中,得到的不是溶液,而是悬浊液。
故选:C。
【点评】植物油不会溶于水,它分散到水中形成的是乳浊液,但它会溶于汽油中,它溶于汽油中得到的是溶液.
3.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是( )
A.水 B.酒精 C.汽油 D.苯
【分析】根据碘在不同溶剂中的溶解性和各溶剂的性质来判断。
【解答】解:A、碘不溶于水,不能用水清洗来清除碘,故A错误;
B、碘能溶解于酒精,能用于清洗碘,但是速度不是最快,故B错误;
C、碘易溶于汽油,可用汽油快速除去碘污,且汽油具有很强的挥发性,快速挥发掉,故C正确;
D、碘可溶于苯,但是苯挥发有毒,故D错误。
故选:C。
【点评】本题考查了物质的溶解性,完成此题,可以依据表格提供的信息进行。
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2叫做“干冰”,可用于人工降雨
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
【分析】A、根据水是常见的溶剂,但不能溶解所有的物质分析判断;
B、根据一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析判断;
C、根据固体二氧化碳俗称干冰,易升华可用于人工降雨判断;
D、根据磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁判断.
【解答】解:A、水是常见的溶剂,但不能溶解所有的物质,A说法不正确;
B、一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析,B说法正确;
C、固体二氧化碳俗称干冰,易升华可用于人工降雨,C说法正确;
D、磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁,D说法正确;
故选:A。
【点评】本题考查了水、一氧化碳、二氧化碳的性质和铁矿石的主要成分,及他们的用途,综合性的考查,但难度不大.
5.厨房是家庭中的小小实验室,厨房中有①面粉②豆油③纯碱④料酒⑤味精⑥胡椒面⑦面酱⑧食醋⑨食盐⑩白砂糖等,把它们分别放入适量水中,充分搅拌能够得到溶液的是( )
A.①③⑤⑥⑧⑨⑩ B.③④⑤⑧⑨⑩ C.②③⑦⑧⑨⑩ D.③④⑥⑧⑨⑩
【分析】溶液是均一、稳定的混合物;溶液的本质特征是均一性、稳定性,属于混合物;据此分析判断.
【解答】解:面粉、胡椒面、面酱不溶于水,放入水中形成不均一、不稳定的混合物,属于悬浊液;
豆油不溶于水,放入水中形成不均一、不稳定的混合物,属于乳浊液;
纯碱、食盐、料酒、白砂糖、食醋等易溶于水,形成均一、稳定的混合物,均属于溶液。
故选:B。
【点评】本题难度不大,掌握溶液的本质特征、各种物质的水溶性方面的知识是正确解题的关键.
6.下列各组物质混合形成的溶液中,前者是溶剂,后者是溶质的一组是( )
A.糖、水 B.硫酸铜、水
C.酒精、碘 D.氢氧化钠、水
【分析】根据溶剂和溶质的判定方法分析.
【解答】解:溶液中只要有水,水为溶剂,故ABD中溶剂均为水,即后者为溶剂;C中酒精为液体,作为溶剂,碘为固体,作为溶质。
故选:C。
【点评】熟练掌握溶剂和溶质的判定方法是解答本题的关键.
7.锌与足量的盐酸反应后的液体和少量二氧化碳通入澄清石灰水后的液体分别是( )
A.乳浊液、溶液 B.溶液、乳浊液
C.悬浊液、乳浊液 D.溶液、悬浊液
【分析】锌与足量的盐酸反应后的液体是生成的氯化锌溶液;二氧化碳和氢氧化钙反应能生成不溶于水的碳酸钙,碳酸钙悬浮在液体中形成悬浊液.
【解答】解:
锌与足量的盐酸反应后的液体是生成的氯化锌溶于水形成的均一的、稳定的混合物,属于溶液;将少量二氧化碳气体通入足量的澄清石灰水后,二氧化碳和氢氧化钙反应能生成不溶于水的碳酸钙,碳酸钙悬浮在液体中形成悬浊液。
故选:D。
【点评】被分散的物质在另一种物质中是可溶的,二者混合后才会形成溶液;不溶于液体的固体悬浮在液体中形成的混合物属于悬浊液.
8.各种洗涤剂广泛进入人们的生活,下列所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣
D.用沐浴露洗澡
【分析】洗涤油污的原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污发生化学反应.
【解答】解:A、汽油是良好的有机溶剂,可以溶解油污,用汽油除去衣服上的油污,利用的是溶解原理,所以错误。
B、洗洁精是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
C、肥皂是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
D、沐浴露是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
故选:A。
【点评】洗涤油污的原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污发生化学反应,理解洗涤油污时利用的原理是解题的关键.
9.海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度变小
【分析】由于食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用蒸发溶剂的方法.
【解答】解:由于食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用蒸发溶剂的方法。故选:B。
【点评】该题主要考查了结晶的方法和溶解度之间的关系.
10.下列各图所表示的实验操作,可以使食盐水中的食盐结晶析出的是( )
A. B.
C. D.
【分析】结晶的方法主要有①降温②蒸发溶剂的方法,不同物质结晶的方法不同,食盐的溶解度随温度变化不明显,故只能采用蒸发溶剂的方法
【解答】解:A、是加水稀释的过程与析出晶体无关,故A错误
B、过滤是分离固体与液体的方法,与晶体析出无关,故B错误
C、蒸发是减少溶剂的过程,能使溶液析出溶质,故C正确
D、增加溶液的量与析出溶质无关,故D错误
故选:C。
【点评】此题是对溶液溶质析出的考查,对晶体析出的知识训练有一定帮助。
11.配制5%的NaCl溶液时,要加快NaCl晶体的溶解,不能采用的措施是( )
A.适当加热
B.加速搅拌
C.选用颗粒较小的NaCl晶体
D.降低温度
【分析】加快固体溶解的方法很多,只要能改变固体与水的接触机会就能改变固体的溶解速率.利用化学知识及生活中的一些常识解决此题.
【解答】解:A、适当加热可以增加分子的运动速度,加快溶解,正确;
B、搅拌可以改变固体周围的饱和状态,加速溶解,正确;
C、粉碎固体,选用颗粒较小的NaCl晶体,能够增加溶剂和固体的接触面积,可以加速溶解,正确;
D、降低温度可以减慢分子的运动速度,溶解减慢,错误。
故选:D。
【点评】熟记改变固体在水中溶解速率的影响因素:搅拌、温度、固体颗粒大小.知道它们的具体影响效果.
12.下列物质能对啤酒起冰镇作用的是( )
A.木炭 B.氯化钠 C.氢氧化钠 D.硝酸铵
【分析】根据常见物质溶于水的吸热与放热现象、溶液温度的变化情况进行分析解答即可.
【解答】解:A、木炭不溶于水,不能对啤酒起到冰镇作用,故选项错误;
B、氯化钠溶于水温度变化不大,不能对啤酒起到冰镇作用,故选项错误;
C、氢氧化钠溶于水放出大量的热,温度升高,不能对啤酒起到冰镇作用,故选项错误;
D、硝酸铵固体溶于水吸热,温度降低,能对啤酒起到冰镇作用,故选项正确。
故选:D。
【点评】本题难度不大,掌握常见物质溶于水的吸热与放热现象、温度变化情况是正确解答本题的关键.
13.要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是( )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中
【分析】配制溶液时,称取的溶质质量的多少或量取水的多少,都将直接影响溶液的配制结果;分析操作能否正确称量配制所需要的溶质和溶剂量,判断操作是否影响配制溶液的质量分数.
【解答】解:A、游码没有回到零位就开始称量,使所称得食盐质量偏大,所配制的溶液质量分数偏高;
B、只在称量食盐的托盘垫上了干净的纸,忽略了纸的质量而使所称量的氯化钠质量偏低,配制的溶液质量分数偏小;
C、所用烧杯不干燥,有少量水,此时水的质量变大,所配制溶液的质量分数偏小;
D、溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中,此操作对溶质质量、溶剂质量已无影响,只是不符合操作规范。所以,对所配制溶液的质量分数没有影响。
故选:D。
【点评】固体药品与液体药品混合时,先把固体药品放入容器,然后再倒入液体.
二.填空题(共4小题)
14.实验室配制溶液时,有以下操作:
①溶解 ②称量 ③计算 ④装瓶存放,贴上标签.
回答下列问题:
(1)现欲配制50g 5%氯化钠溶液,操作步骤为 ③②①④ (填序号).
(2)溶解操作中需要的仪器有 玻璃棒 、 烧杯 .
(3)量取蒸馏水时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 < (填“<”或“>”)5%.
【分析】(1)根据配制溶质质量分数一定的溶液的基本步骤考虑;
(2)根据配制溶质质量分数一定的溶液的步骤推出需要的仪器,玻璃棒的作用要根据使用方法考虑;
(3)量筒量取液体,读数要规范,视线要与液体凹液面的最低处相平,仰视、俯视都会导致读数错误.
【解答】解:(1)配制溶质质量分数一定的溶液的基本步骤:计算、称量、溶解、装瓶存放.所以顺序为③②①④;
(2)溶解的操作中要用到的玻璃仪器有:玻璃棒、烧杯,玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
(3)在量取定体积液体时,若仰视读数,则会导致实际液体体积比所需体积大,溶剂质量偏大,溶液质量偏大,溶质的质量分数偏小.
故答案为:(1)③②①④;
(2)玻璃棒;烧杯;
(3)<.
【点评】此题考查配制一定溶质质量分数的溶液,解决此类问题应明确步骤,注意量筒、托盘天平的规范使用,明确错误操作引起的不良后果.
15.汽油能洗去衣服上的油污,这是由于汽油能 溶解 油污,形成 溶液 .用加了洗涤剂的水也能洗去油污,这是由于洗涤剂能 乳化 油污,形成 乳浊液 ,两者去污的原理 不同 (填“相同”或“不同”)
【分析】利用相似相溶原理可知,有机物能溶解在有机物中;洗涤剂去污是乳化作用的结果等知识解决.
【解答】解:汽油不能溶于水,但能溶于有机溶剂中,洗涤剂不能使油污溶解但能起到乳化作用从而去污,两者的去污原理不同.
故答案为:溶解;溶液;乳化;乳浊液;不同
【点评】此题是对油污去除原理的探讨,通过类比的方式可加深对这一问题的认识.
16.溶液一定是某种溶质与水组成的 混合物 .
【分析】根据溶液是由溶质与水组成的混合物来分析解答;
【解答】解:溶液是由溶质与水组成的混合物;
答案:混合物;
【点评】解答本题关键是要知道溶液的特点,知道溶质的种类,常见的溶剂是水,但溶剂不一定是水.
17.水是人类宝贵的自然资源,与人类的生产、生活密切相关.
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是 D .
A.蔗糖 B.纯碱 C.食盐 D.花生油
(2)“节约用水,从我做起”.请你写出一种生活中节约用水的做法 淘米水浇花 .
(3)为了保护水质,下列做法合理的是 BC .
A.随意丢弃废旧电池 B.生活污水经处理达标后排放
C.农业上合理使用农药、化肥 D.工业“三废”未经处理任意排放
(4)通过电解水实验,可以知道水是由 氢、氧元素 组成.
(5)生活中降低水的硬度的常用方法是 煮沸 .
(6)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号) ⑤②④① .
【分析】(1)根据溶液的特征分析判断;
(2)根据生活中节约用水的措施进行解答;
(3)根据保护水资源考虑;
(4)根据质量守恒定律来分析解答;
(5)根据硬水软化法考虑;
(6)根据净水的知识进行分析,除杂时可以采用先除去易除的杂质,再除去难除的杂质的顺序.水中含有的不溶性固体大颗粒杂质可以通过沉降除去,不溶性小颗粒固体杂质可以通过过滤除去,投药消毒可以除去细菌微生物.
【解答】解:(1)食盐、纯碱和蔗糖都能溶于水,形成溶液,而植物油不能溶于水,不能形成溶液;故填:C;
(2)生活中节约用水的措施有:随手关闭水龙头、淘米水浇花等;
(3)生活污水经处理达标后排放、农业上合理使用农药、化肥都可保护水质;
(4)电解水生成氢气和氧气,氢气是由氢元素组成的,氧气是由氧元素组成的,根据质量守恒定律可知,水是由氢元素和氧元素组成的;
(5)生活中降低水的硬度的常用方法是煮沸;
(6)加明矾吸附是把水中小颗粒泥尘聚集成大的,以利于沉降;不溶性小颗粒固体杂质可以通过过滤除去;投药消毒可以除去细菌微生物,故要将混有泥沙的天然水净化成生活用的自来水,将所选用的方法按净化过程排序是:⑤加明矾吸附沉降→②过滤→④活性炭层吸附→①消毒杀菌.
故答案为:(1)D;(2)淘米水浇花;(3)BC;(4)氢、氧元素;(5)煮沸;(6)⑤②④①.
【点评】熟练掌握水的性质,熟知水的净化过程,溶液的特征,硬水和软水的区别、水的电解实验等,才能灵活分析解答.
三.实验探究题(共1小题)
18.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 5 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 B 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 ACD (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
【分析】(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量。
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品。
(3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl。
(3)A、称量好的NaCl固体倒入烧杯时,有少许洒出,溶质偏少,则使溶质质量分数偏小,故选项正确。
B、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项不正确。
C、溶解NaCl固体的烧杯内壁有水珠,多取了水,则使溶质质量分数偏小,故选项正确。
D、将5g NaCl固体完全溶解在100g水中,溶液质量大于100g,溶质质量分数偏小,故选项正确。
故答案为:(1)5,95,100;(2)B;(3)ACD。
【点评】本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键。
四.解答题(共2小题)
19.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 291 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 烧杯、玻璃棒 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
【分析】(1)根据溶质质量=溶液质量×溶质的质量分数,计算出所需硼酸固体的质量,进而确定所选砝码的质量和游码的示数.
(2)溶剂质量=溶液质量﹣溶质质量,据此进行分析解答.
(3)根据溶解操作所需的仪器,进行分析判断.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制300g质量分数为3%的硼酸溶液,所需硼酸固体的质量为300g×3%=9g;选用5g的砝码,游码拨到4g处即可.
(2)溶剂质量=溶液质量﹣溶质质量,则所需水的质量=300g﹣9g=291g(合291mL).
(3)溶解用到的玻璃仪器是烧杯、玻璃棒.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,图2的标签中填上相应的内容是硼酸溶液,3%.
故答案为:(1)5g;4g;(2)291;(3)烧杯、玻璃棒;(4)硼酸溶液,3%.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
20.汽油可以溶解油渍,这是根据汽油中的 汽油分子 与油污相解离;若只是因为汽油是有机溶液,那么此油渍可不可以被其他油类溶液所溶解?
【分析】根据汽油和油污都是有机物,油污可以溶于汽油,且汽油极易挥发,将油污带走,当将油污除去后,残留在衣服上的汽油可以全部挥发.进行解答;
【解答】解:汽油和油污都是有机物,油污可以溶于汽油,且汽油极易挥发,将油污带走,当将油污除去后,残留在衣服上的汽油可以全部挥发.此油渍可不一定被其他油类溶液所溶解.
答案:汽油分子;不一定.
【点评】本题主要考查学生对乳化现象及去污原理的理解和掌握.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/29 20:46:50;用户:15877047552;邮箱:15877047552;学号:38945411第1页(共3页)
一.选择题(共13小题)
1.在配制75g质量分数为10%的NaCl溶液过程中,某同学进行了下列操作:①用量筒量取水时俯视读数;②把量筒中的水转移到配制溶液的烧杯中时有少许洒出;③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡;④配制溶液的烧杯用少量蒸馏水润洗.以下叙述正确的是( )
A.以上操作除④外都有错误
B.以上操作会使所配溶液的溶质质量分数偏大的只有①
C.以上操作可能使所配溶液的溶质质量分数偏小的只有④
D.以上操作可能会使所配溶液的溶质质量分数偏大或偏小的是③
2.下列现象中,不属于溶解现象的是( )
A.把食盐投入水中 B.把植物油注入汽油中
C.把泥土投入到水中 D.把品红投入到水中
3.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是( )
A.水 B.酒精 C.汽油 D.苯
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2叫做“干冰”,可用于人工降雨
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
5.厨房是家庭中的小小实验室,厨房中有①面粉②豆油③纯碱④料酒⑤味精⑥胡椒面⑦面酱⑧食醋⑨食盐⑩白砂糖等,把它们分别放入适量水中,充分搅拌能够得到溶液的是( )
A.①③⑤⑥⑧⑨⑩ B.③④⑤⑧⑨⑩ C.②③⑦⑧⑨⑩ D.③④⑥⑧⑨⑩
6.下列各组物质混合形成的溶液中,前者是溶剂,后者是溶质的一组是( )
A.糖、水 B.硫酸铜、水
C.酒精、碘 D.氢氧化钠、水
7.锌与足量的盐酸反应后的液体和少量二氧化碳通入澄清石灰水后的液体分别是( )
A.乳浊液、溶液 B.溶液、乳浊液
C.悬浊液、乳浊液 D.溶液、悬浊液
8.各种洗涤剂广泛进入人们的生活,下列所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣
D.用沐浴露洗澡
9.海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度变小
10.下列各图所表示的实验操作,可以使食盐水中的食盐结晶析出的是( )
A. B.
C. D.
11.配制5%的NaCl溶液时,要加快NaCl晶体的溶解,不能采用的措施是( )
A.适当加热
B.加速搅拌
C.选用颗粒较小的NaCl晶体
D.降低温度
12.下列物质能对啤酒起冰镇作用的是( )
A.木炭 B.氯化钠 C.氢氧化钠 D.硝酸铵
13.要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是( )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中
二.填空题(共4小题)
14.实验室配制溶液时,有以下操作:
①溶解 ②称量 ③计算 ④装瓶存放,贴上标签.
回答下列问题:
(1)现欲配制50g 5%氯化钠溶液,操作步骤为 (填序号).
(2)溶解操作中需要的仪器有 、 .
(3)量取蒸馏水时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 (填“<”或“>”)5%.
15.汽油能洗去衣服上的油污,这是由于汽油能 油污,形成 .用加了洗涤剂的水也能洗去油污,这是由于洗涤剂能 油污,形成 ,两者去污的原理 (填“相同”或“不同”)
16.溶液一定是某种溶质与水组成的 .
17.水是人类宝贵的自然资源,与人类的生产、生活密切相关.
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是 .
A.蔗糖 B.纯碱 C.食盐 D.花生油
(2)“节约用水,从我做起”.请你写出一种生活中节约用水的做法 .
(3)为了保护水质,下列做法合理的是 .
A.随意丢弃废旧电池 B.生活污水经处理达标后排放
C.农业上合理使用农药、化肥 D.工业“三废”未经处理任意排放
(4)通过电解水实验,可以知道水是由 组成.
(5)生活中降低水的硬度的常用方法是 .
(6)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号) .
三.实验探究题(共1小题)
18.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
四.解答题(共2小题)
19.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
20.汽油可以溶解油渍,这是根据汽油中的 与油污相解离;若只是因为汽油是有机溶液,那么此油渍可不可以被其他油类溶液所溶解?
第九单元溶液2021_2022学年九年级化学同步练习(人教版)
参考答案与试题解析
一.选择题(共13小题)
1.在配制75g质量分数为10%的NaCl溶液过程中,某同学进行了下列操作:①用量筒量取水时俯视读数;②把量筒中的水转移到配制溶液的烧杯中时有少许洒出;③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡;④配制溶液的烧杯用少量蒸馏水润洗.以下叙述正确的是( )
A.以上操作除④外都有错误
B.以上操作会使所配溶液的溶质质量分数偏大的只有①
C.以上操作可能使所配溶液的溶质质量分数偏小的只有④
D.以上操作可能会使所配溶液的溶质质量分数偏大或偏小的是③
【分析】抓住导致配制溶液时所出现误差的根本原因:溶质量或多或少、溶剂量或多或少,分析各项操作对溶质、溶剂量所造成的影响解答即可.
【解答】解:①用量筒量取水时俯视读数,读数大于所量水的实际体积,使量取水的体积偏小,所配制氯化钠溶液的质量分数偏大;
②把量筒中的水转移到配制溶液的烧杯中时有少许洒出,使溶解时所加水的体积偏小,所配制氯化钠溶液的质量分数偏大;
③在托盘天平的右盘放入砝码并移动游码到合适位置,左盘放入氯化钠后移动游码至天平平衡,会使氯化钠的质量偏大或偏小,所配制氯化钠溶液的质量分数也会随着偏大或偏小;
④配制溶液的烧杯用蒸馏水润洗,水的体积因此而偏大,所配制氯化钠溶液的质量分数偏小;
综合推断,故选D
【点评】用量筒量取液体时,仰视读数偏小,俯视读数偏大;天平称量时左盘放砝码而右盘放药品,药品的质量为砝码与游码的质量差.
2.下列现象中,不属于溶解现象的是( )
A.把食盐投入水中 B.把植物油注入汽油中
C.把泥土投入到水中 D.把品红投入到水中
【分析】根据溶解的概念去解答.(一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液,这一过程叫溶解.)
【解答】解:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液,这一过程叫溶解。
ABD中涉及到的溶质都会溶于溶剂中,所以形成的都是溶液,这三个过程都叫溶解,但C中泥土不溶于水中,得到的不是溶液,而是悬浊液。
故选:C。
【点评】植物油不会溶于水,它分散到水中形成的是乳浊液,但它会溶于汽油中,它溶于汽油中得到的是溶液.
3.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是( )
A.水 B.酒精 C.汽油 D.苯
【分析】根据碘在不同溶剂中的溶解性和各溶剂的性质来判断。
【解答】解:A、碘不溶于水,不能用水清洗来清除碘,故A错误;
B、碘能溶解于酒精,能用于清洗碘,但是速度不是最快,故B错误;
C、碘易溶于汽油,可用汽油快速除去碘污,且汽油具有很强的挥发性,快速挥发掉,故C正确;
D、碘可溶于苯,但是苯挥发有毒,故D错误。
故选:C。
【点评】本题考查了物质的溶解性,完成此题,可以依据表格提供的信息进行。
4.下列关于常见氧化物的叙述,不正确的是( )
A.H2O是最常用的溶剂,能溶解所有的物质
B.CO极易与血液中的血红蛋白结合,造成生物体内缺氧
C.固态CO2叫做“干冰”,可用于人工降雨
D.磁铁矿的主要成分是Fe3O4,有磁性,可用于炼铁
【分析】A、根据水是常见的溶剂,但不能溶解所有的物质分析判断;
B、根据一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析判断;
C、根据固体二氧化碳俗称干冰,易升华可用于人工降雨判断;
D、根据磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁判断.
【解答】解:A、水是常见的溶剂,但不能溶解所有的物质,A说法不正确;
B、一氧化碳易与血液中的血红蛋白结合,从而使血液失去运输氧的能力分析,B说法正确;
C、固体二氧化碳俗称干冰,易升华可用于人工降雨,C说法正确;
D、磁铁矿的主要成分是Fe3O4,有磁性,可用炼铁,D说法正确;
故选:A。
【点评】本题考查了水、一氧化碳、二氧化碳的性质和铁矿石的主要成分,及他们的用途,综合性的考查,但难度不大.
5.厨房是家庭中的小小实验室,厨房中有①面粉②豆油③纯碱④料酒⑤味精⑥胡椒面⑦面酱⑧食醋⑨食盐⑩白砂糖等,把它们分别放入适量水中,充分搅拌能够得到溶液的是( )
A.①③⑤⑥⑧⑨⑩ B.③④⑤⑧⑨⑩ C.②③⑦⑧⑨⑩ D.③④⑥⑧⑨⑩
【分析】溶液是均一、稳定的混合物;溶液的本质特征是均一性、稳定性,属于混合物;据此分析判断.
【解答】解:面粉、胡椒面、面酱不溶于水,放入水中形成不均一、不稳定的混合物,属于悬浊液;
豆油不溶于水,放入水中形成不均一、不稳定的混合物,属于乳浊液;
纯碱、食盐、料酒、白砂糖、食醋等易溶于水,形成均一、稳定的混合物,均属于溶液。
故选:B。
【点评】本题难度不大,掌握溶液的本质特征、各种物质的水溶性方面的知识是正确解题的关键.
6.下列各组物质混合形成的溶液中,前者是溶剂,后者是溶质的一组是( )
A.糖、水 B.硫酸铜、水
C.酒精、碘 D.氢氧化钠、水
【分析】根据溶剂和溶质的判定方法分析.
【解答】解:溶液中只要有水,水为溶剂,故ABD中溶剂均为水,即后者为溶剂;C中酒精为液体,作为溶剂,碘为固体,作为溶质。
故选:C。
【点评】熟练掌握溶剂和溶质的判定方法是解答本题的关键.
7.锌与足量的盐酸反应后的液体和少量二氧化碳通入澄清石灰水后的液体分别是( )
A.乳浊液、溶液 B.溶液、乳浊液
C.悬浊液、乳浊液 D.溶液、悬浊液
【分析】锌与足量的盐酸反应后的液体是生成的氯化锌溶液;二氧化碳和氢氧化钙反应能生成不溶于水的碳酸钙,碳酸钙悬浮在液体中形成悬浊液.
【解答】解:
锌与足量的盐酸反应后的液体是生成的氯化锌溶于水形成的均一的、稳定的混合物,属于溶液;将少量二氧化碳气体通入足量的澄清石灰水后,二氧化碳和氢氧化钙反应能生成不溶于水的碳酸钙,碳酸钙悬浮在液体中形成悬浊液。
故选:D。
【点评】被分散的物质在另一种物质中是可溶的,二者混合后才会形成溶液;不溶于液体的固体悬浮在液体中形成的混合物属于悬浊液.
8.各种洗涤剂广泛进入人们的生活,下列所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣
D.用沐浴露洗澡
【分析】洗涤油污的原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污发生化学反应.
【解答】解:A、汽油是良好的有机溶剂,可以溶解油污,用汽油除去衣服上的油污,利用的是溶解原理,所以错误。
B、洗洁精是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
C、肥皂是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
D、沐浴露是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,所以正确。
故选:A。
【点评】洗涤油污的原理有三种,一是利用乳化作用,二是利用溶解原理,三是利用物质与油污发生化学反应,理解洗涤油污时利用的原理是解题的关键.
9.海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度变小
【分析】由于食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用蒸发溶剂的方法.
【解答】解:由于食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用蒸发溶剂的方法。故选:B。
【点评】该题主要考查了结晶的方法和溶解度之间的关系.
10.下列各图所表示的实验操作,可以使食盐水中的食盐结晶析出的是( )
A. B.
C. D.
【分析】结晶的方法主要有①降温②蒸发溶剂的方法,不同物质结晶的方法不同,食盐的溶解度随温度变化不明显,故只能采用蒸发溶剂的方法
【解答】解:A、是加水稀释的过程与析出晶体无关,故A错误
B、过滤是分离固体与液体的方法,与晶体析出无关,故B错误
C、蒸发是减少溶剂的过程,能使溶液析出溶质,故C正确
D、增加溶液的量与析出溶质无关,故D错误
故选:C。
【点评】此题是对溶液溶质析出的考查,对晶体析出的知识训练有一定帮助。
11.配制5%的NaCl溶液时,要加快NaCl晶体的溶解,不能采用的措施是( )
A.适当加热
B.加速搅拌
C.选用颗粒较小的NaCl晶体
D.降低温度
【分析】加快固体溶解的方法很多,只要能改变固体与水的接触机会就能改变固体的溶解速率.利用化学知识及生活中的一些常识解决此题.
【解答】解:A、适当加热可以增加分子的运动速度,加快溶解,正确;
B、搅拌可以改变固体周围的饱和状态,加速溶解,正确;
C、粉碎固体,选用颗粒较小的NaCl晶体,能够增加溶剂和固体的接触面积,可以加速溶解,正确;
D、降低温度可以减慢分子的运动速度,溶解减慢,错误。
故选:D。
【点评】熟记改变固体在水中溶解速率的影响因素:搅拌、温度、固体颗粒大小.知道它们的具体影响效果.
12.下列物质能对啤酒起冰镇作用的是( )
A.木炭 B.氯化钠 C.氢氧化钠 D.硝酸铵
【分析】根据常见物质溶于水的吸热与放热现象、溶液温度的变化情况进行分析解答即可.
【解答】解:A、木炭不溶于水,不能对啤酒起到冰镇作用,故选项错误;
B、氯化钠溶于水温度变化不大,不能对啤酒起到冰镇作用,故选项错误;
C、氢氧化钠溶于水放出大量的热,温度升高,不能对啤酒起到冰镇作用,故选项错误;
D、硝酸铵固体溶于水吸热,温度降低,能对啤酒起到冰镇作用,故选项正确。
故选:D。
【点评】本题难度不大,掌握常见物质溶于水的吸热与放热现象、温度变化情况是正确解答本题的关键.
13.要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是( )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中
【分析】配制溶液时,称取的溶质质量的多少或量取水的多少,都将直接影响溶液的配制结果;分析操作能否正确称量配制所需要的溶质和溶剂量,判断操作是否影响配制溶液的质量分数.
【解答】解:A、游码没有回到零位就开始称量,使所称得食盐质量偏大,所配制的溶液质量分数偏高;
B、只在称量食盐的托盘垫上了干净的纸,忽略了纸的质量而使所称量的氯化钠质量偏低,配制的溶液质量分数偏小;
C、所用烧杯不干燥,有少量水,此时水的质量变大,所配制溶液的质量分数偏小;
D、溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中,此操作对溶质质量、溶剂质量已无影响,只是不符合操作规范。所以,对所配制溶液的质量分数没有影响。
故选:D。
【点评】固体药品与液体药品混合时,先把固体药品放入容器,然后再倒入液体.
二.填空题(共4小题)
14.实验室配制溶液时,有以下操作:
①溶解 ②称量 ③计算 ④装瓶存放,贴上标签.
回答下列问题:
(1)现欲配制50g 5%氯化钠溶液,操作步骤为 ③②①④ (填序号).
(2)溶解操作中需要的仪器有 玻璃棒 、 烧杯 .
(3)量取蒸馏水时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 < (填“<”或“>”)5%.
【分析】(1)根据配制溶质质量分数一定的溶液的基本步骤考虑;
(2)根据配制溶质质量分数一定的溶液的步骤推出需要的仪器,玻璃棒的作用要根据使用方法考虑;
(3)量筒量取液体,读数要规范,视线要与液体凹液面的最低处相平,仰视、俯视都会导致读数错误.
【解答】解:(1)配制溶质质量分数一定的溶液的基本步骤:计算、称量、溶解、装瓶存放.所以顺序为③②①④;
(2)溶解的操作中要用到的玻璃仪器有:玻璃棒、烧杯,玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
(3)在量取定体积液体时,若仰视读数,则会导致实际液体体积比所需体积大,溶剂质量偏大,溶液质量偏大,溶质的质量分数偏小.
故答案为:(1)③②①④;
(2)玻璃棒;烧杯;
(3)<.
【点评】此题考查配制一定溶质质量分数的溶液,解决此类问题应明确步骤,注意量筒、托盘天平的规范使用,明确错误操作引起的不良后果.
15.汽油能洗去衣服上的油污,这是由于汽油能 溶解 油污,形成 溶液 .用加了洗涤剂的水也能洗去油污,这是由于洗涤剂能 乳化 油污,形成 乳浊液 ,两者去污的原理 不同 (填“相同”或“不同”)
【分析】利用相似相溶原理可知,有机物能溶解在有机物中;洗涤剂去污是乳化作用的结果等知识解决.
【解答】解:汽油不能溶于水,但能溶于有机溶剂中,洗涤剂不能使油污溶解但能起到乳化作用从而去污,两者的去污原理不同.
故答案为:溶解;溶液;乳化;乳浊液;不同
【点评】此题是对油污去除原理的探讨,通过类比的方式可加深对这一问题的认识.
16.溶液一定是某种溶质与水组成的 混合物 .
【分析】根据溶液是由溶质与水组成的混合物来分析解答;
【解答】解:溶液是由溶质与水组成的混合物;
答案:混合物;
【点评】解答本题关键是要知道溶液的特点,知道溶质的种类,常见的溶剂是水,但溶剂不一定是水.
17.水是人类宝贵的自然资源,与人类的生产、生活密切相关.
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是 D .
A.蔗糖 B.纯碱 C.食盐 D.花生油
(2)“节约用水,从我做起”.请你写出一种生活中节约用水的做法 淘米水浇花 .
(3)为了保护水质,下列做法合理的是 BC .
A.随意丢弃废旧电池 B.生活污水经处理达标后排放
C.农业上合理使用农药、化肥 D.工业“三废”未经处理任意排放
(4)通过电解水实验,可以知道水是由 氢、氧元素 组成.
(5)生活中降低水的硬度的常用方法是 煮沸 .
(6)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号) ⑤②④① .
【分析】(1)根据溶液的特征分析判断;
(2)根据生活中节约用水的措施进行解答;
(3)根据保护水资源考虑;
(4)根据质量守恒定律来分析解答;
(5)根据硬水软化法考虑;
(6)根据净水的知识进行分析,除杂时可以采用先除去易除的杂质,再除去难除的杂质的顺序.水中含有的不溶性固体大颗粒杂质可以通过沉降除去,不溶性小颗粒固体杂质可以通过过滤除去,投药消毒可以除去细菌微生物.
【解答】解:(1)食盐、纯碱和蔗糖都能溶于水,形成溶液,而植物油不能溶于水,不能形成溶液;故填:C;
(2)生活中节约用水的措施有:随手关闭水龙头、淘米水浇花等;
(3)生活污水经处理达标后排放、农业上合理使用农药、化肥都可保护水质;
(4)电解水生成氢气和氧气,氢气是由氢元素组成的,氧气是由氧元素组成的,根据质量守恒定律可知,水是由氢元素和氧元素组成的;
(5)生活中降低水的硬度的常用方法是煮沸;
(6)加明矾吸附是把水中小颗粒泥尘聚集成大的,以利于沉降;不溶性小颗粒固体杂质可以通过过滤除去;投药消毒可以除去细菌微生物,故要将混有泥沙的天然水净化成生活用的自来水,将所选用的方法按净化过程排序是:⑤加明矾吸附沉降→②过滤→④活性炭层吸附→①消毒杀菌.
故答案为:(1)D;(2)淘米水浇花;(3)BC;(4)氢、氧元素;(5)煮沸;(6)⑤②④①.
【点评】熟练掌握水的性质,熟知水的净化过程,溶液的特征,硬水和软水的区别、水的电解实验等,才能灵活分析解答.
三.实验探究题(共1小题)
18.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 5 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 B 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 ACD (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
【分析】(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量。
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品。
(3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl。
(3)A、称量好的NaCl固体倒入烧杯时,有少许洒出,溶质偏少,则使溶质质量分数偏小,故选项正确。
B、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项不正确。
C、溶解NaCl固体的烧杯内壁有水珠,多取了水,则使溶质质量分数偏小,故选项正确。
D、将5g NaCl固体完全溶解在100g水中,溶液质量大于100g,溶质质量分数偏小,故选项正确。
故答案为:(1)5,95,100;(2)B;(3)ACD。
【点评】本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键。
四.解答题(共2小题)
19.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 291 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 烧杯、玻璃棒 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
【分析】(1)根据溶质质量=溶液质量×溶质的质量分数,计算出所需硼酸固体的质量,进而确定所选砝码的质量和游码的示数.
(2)溶剂质量=溶液质量﹣溶质质量,据此进行分析解答.
(3)根据溶解操作所需的仪器,进行分析判断.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制300g质量分数为3%的硼酸溶液,所需硼酸固体的质量为300g×3%=9g;选用5g的砝码,游码拨到4g处即可.
(2)溶剂质量=溶液质量﹣溶质质量,则所需水的质量=300g﹣9g=291g(合291mL).
(3)溶解用到的玻璃仪器是烧杯、玻璃棒.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,图2的标签中填上相应的内容是硼酸溶液,3%.
故答案为:(1)5g;4g;(2)291;(3)烧杯、玻璃棒;(4)硼酸溶液,3%.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
20.汽油可以溶解油渍,这是根据汽油中的 汽油分子 与油污相解离;若只是因为汽油是有机溶液,那么此油渍可不可以被其他油类溶液所溶解?
【分析】根据汽油和油污都是有机物,油污可以溶于汽油,且汽油极易挥发,将油污带走,当将油污除去后,残留在衣服上的汽油可以全部挥发.进行解答;
【解答】解:汽油和油污都是有机物,油污可以溶于汽油,且汽油极易挥发,将油污带走,当将油污除去后,残留在衣服上的汽油可以全部挥发.此油渍可不一定被其他油类溶液所溶解.
答案:汽油分子;不一定.
【点评】本题主要考查学生对乳化现象及去污原理的理解和掌握.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/29 20:46:50;用户:15877047552;邮箱:15877047552;学号:38945411第1页(共3页)
同课章节目录
