第三章 物质的转化和元素的循环 单元练习(含答案)
文档属性
| 名称 | 第三章 物质的转化和元素的循环 单元练习(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 116.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-01-30 00:00:00 | ||
图片预览



文档简介
第3章 物质的转化和元素的循环
一、选择题
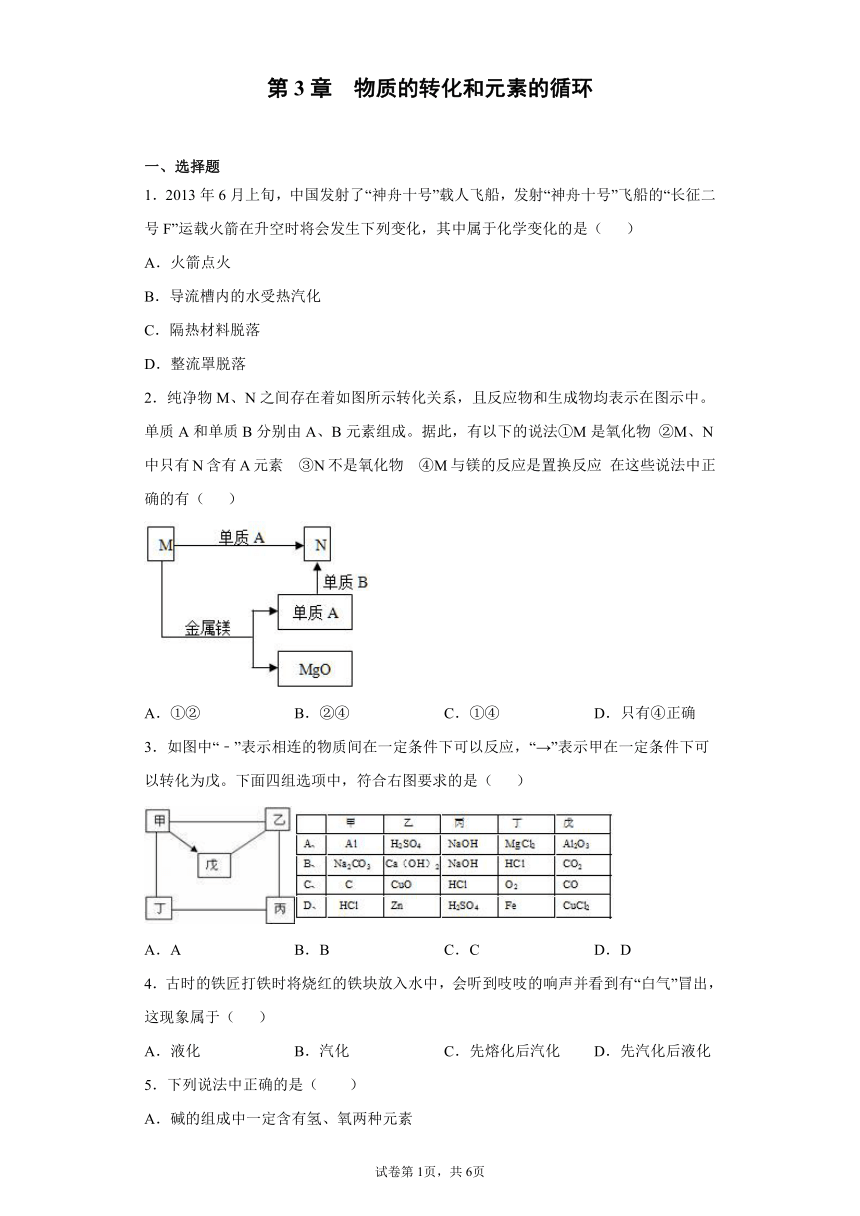
1.2013年6月上旬,中国发射了“神舟十号”载人飞船,发射“神舟十号”飞船的“长征二号F”运载火箭在升空时将会发生下列变化,其中属于化学变化的是( )
A.火箭点火
B.导流槽内的水受热汽化
C.隔热材料脱落
D.整流罩脱落
2.纯净物M、N之间存在着如图所示转化关系,且反应物和生成物均表示在图示中。单质A和单质B分别由A、B元素组成。据此,有以下的说法①M是氧化物 ②M、N中只有N含有A元素 ③N不是氧化物 ④M与镁的反应是置换反应 在这些说法中正确的有( )
A.①② B.②④ C.①④ D.只有④正确
3.如图中“﹣”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊。下面四组选项中,符合右图要求的是( )
A.A B.B C.C D.D
4.古时的铁匠打铁时将烧红的铁块放入水中,会听到吱吱的响声并看到有“白气”冒出,这现象属于( )
A.液化 B.汽化 C.先熔化后汽化 D.先汽化后液化
5.下列说法中正确的是( )
A.碱的组成中一定含有氢、氧两种元素
B.金属都可以与盐酸反应生成盐和氢气
C.铁与氧气反应一定生成四氧化三铁
D.含有金属元素和氧元素的化合物一定是金属氧化物
6.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
7.下列事例中,属于产生氧气的途径的是
A.打开窗户通风
B.使用空气清新剂
C.夜晚在屋内放置绿色植物
D.阳光良好的原始森林
8.下列变化中,前者属于物理变化,后者属于化学变化的一组是( )
①用砂纸打磨除锈、活性炭吸附色素
②金属铝表面生成氧化膜,空气液化
③酒精溶于水,二氧化碳通往石灰水
④白色硫酸铜粉末加水变蓝,石蜡熔化
⑤二氧化碳低温受压凝固成干冰,冰融化成水
⑥汽油挥发,汽油燃烧
A.①③ B.③⑥ C.④⑤ D.⑤⑥
9.相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( )
A.Na2O B.NaOH C.CuSO4·5H2O D.H2SO4
10.下列物质露置于空气中,因发生化学变化而使质量减小的是( )
A.浓硫酸 B.烧碱 C.浓盐酸 D.双氧水
11.自然界中有几千万种含碳物质,并循环转化。下列说法正确的是
A.人的生命活动离不开碳循环
B.森林的减少对碳的循环没有影响
C.金刚石中碳原子间没有间隔
D.地下的煤中碳原子是静止不动的
12.现有10克CuO和ZnO的混合物,下列实验方案,不能确定CuO质量分数的是( )
A.将混合物与足量H2充分反应,冷却后测出剩余固体质量
B.将混合物与足量CO充分反应,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值
C.将混合物完全溶于稀H2SO4,加入足量铁粉,充分反应后,过滤、洗涤、干燥,测出剩余固体质量
D.将混合物完全溶于稀H2SO4,加入足量NaOH溶液,过滤、洗涤、干燥,测出剩余固体质量
二、填空题
13.有下列物质的变化或物质的性质:① 蔗糖能溶于水;②滴水成冰;③氢气燃烧;④镁可以燃烧;⑤鸡蛋发臭;⑥玻璃破碎;⑦酒精易挥发;⑧铁在潮湿环境中容易生锈。
其中,属于化学变化的是________________;属于物理性质的是_______________。
14.空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
(1)X是空气中含量最多的气体,其分子式为_____。
(2)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为_____。
(3)①天然气的主要成分是CH4,点燃CH4之前应_____。8g CH4完全燃烧消耗32g O2,生成a g CO2和18g H2O,则a=_____。
②由CH4在该流程中的作用表明:化学反应中发生物质变化的同时也会伴随有_____变化(选填“能量”或“原子个数”)。
(4)尿素属于_____(选填“氮肥”“磷肥”或“钾肥”);写出NH3合成尿素的化学反应方程式:_____。
15.碳和部分碳的化合物间转化关系如图所示。
(1)物质X的化学式为_____。
(2)在物质的分类中CO属于_____。
A 酸 B 碱 C 盐 D 氧化物
(3)写出图中转化关系中属于化合反应的一个化学方程式:_____。
16.实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数己模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克.
(1)在过滤操作中使用的玻璃仪器有:烧杯、____________和玻璃棒.
(2)样品中氯化钾的质量分数为多少?______________(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?______________
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值.造成这种结果的原因可能是___________.(选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
17.A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是_____。
(2)若C是锌,A和B都属于酸,写出D可能的化学式:_____(物质类别不同的两种即可)。
18.低碳是指较低(更低)的温室气体(二氧化碳为主)排放。低碳生活,就是低能量、低消耗的生活方式。上海世博会是第一个正式提出“低碳”理念的世博会,也是第一个“无烟世博会”。
(1)煤炭、石油和天然气的燃烧与人的呼吸一样,会消耗大气中的_________,并释放出____气体。(填化学式)
(2)一公顷树林,每天能吸收150~500千克的二氧化碳,并释放出60~400千克的氧气,这是依靠植物的____________作用。因此,绿色植物的这种作用有利于维持生物圈中的____________平衡。
(3)在日常生活中,你应如何响应“低碳”的生活方式?___________(举出一例即可)。
三、简答题
19.科学家尝试通过多种途径减少的排放,或将转化为有用的物质。其中一种途径是利用溶液来“捕捉”,并将储存或利用,反应流程如图所示。
(1)反应分离室中分离物质的操作是___________。
(2)上述反应流程中,可循环利用的物质___________。(填化学式)
(3)若反应分离室中有溶质质量分数为10.6%的溶液100千克。求完全反应后,理论上可生成的质量___________(要求根据化学方程式计算)。
四、探究题
20.科学课上,老师告诉学生能发生复分解反应的两种盐通常是可溶的。有通常就有例外,能否找到某些可溶性盐和难溶性盐发生复分解反应的证据呢?科学兴趣小组进行了探究
(查阅资料)①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减少的方向进行
②了解到某些难溶性盐的溶解能力和颜色,其中AgI是一种难溶于水的黄色沉淀。
(实验取证)取一支试管,加入少量AgNO3溶液,再加入过量NaCl溶液,有白色沉淀生成.再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀
(分析讨论)(1)为什么要加入过量的NaCl溶液?请说明理由________
(2)写出加入少量KI溶液后发生反应的化学方程式________
(3)该反应能发生的原因是AgI在水中的溶解能力________AgCl(选填大于、等于或小于)
(得出结论)某些可溶性盐和难溶性盐之间能发生复分解反应.
试卷第2页,共2页
试卷第1页,共1页
参考答案
1.A
2.C
3.D
4.D
5.A
6.B
7.D
8.B
9.A
10.D
11.A
12.C
13.③⑤ ①⑦
14.N2 CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验甲烷的纯度 22 能量 氮肥 CO2+2NH3CO(NH2)2+H2O
15.CO2 D C+O2CO2(合理答案均可)
16.漏斗 74.5% 12.65g BC
17.Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(合理即可) Na2CO3、CuO、NaOH(或其他碳酸盐、金属氧化物、碱的化学式)三种中的任意两种
18.O2 CO2 光合 碳 氧 节约纸张(或随手关灯等)
19.过滤 NaOH和CaO 设生成碳酸钙的质量为x,
x=10kg,
答:生成碳酸钙的质量为10kg。
20.使银离子全部沉淀 KI+AgCl=AgI↓+KCl 小于 答案第1页,共2页
答案第1页,共2页
一、选择题
1.2013年6月上旬,中国发射了“神舟十号”载人飞船,发射“神舟十号”飞船的“长征二号F”运载火箭在升空时将会发生下列变化,其中属于化学变化的是( )
A.火箭点火
B.导流槽内的水受热汽化
C.隔热材料脱落
D.整流罩脱落
2.纯净物M、N之间存在着如图所示转化关系,且反应物和生成物均表示在图示中。单质A和单质B分别由A、B元素组成。据此,有以下的说法①M是氧化物 ②M、N中只有N含有A元素 ③N不是氧化物 ④M与镁的反应是置换反应 在这些说法中正确的有( )
A.①② B.②④ C.①④ D.只有④正确
3.如图中“﹣”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊。下面四组选项中,符合右图要求的是( )
A.A B.B C.C D.D
4.古时的铁匠打铁时将烧红的铁块放入水中,会听到吱吱的响声并看到有“白气”冒出,这现象属于( )
A.液化 B.汽化 C.先熔化后汽化 D.先汽化后液化
5.下列说法中正确的是( )
A.碱的组成中一定含有氢、氧两种元素
B.金属都可以与盐酸反应生成盐和氢气
C.铁与氧气反应一定生成四氧化三铁
D.含有金属元素和氧元素的化合物一定是金属氧化物
6.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
7.下列事例中,属于产生氧气的途径的是
A.打开窗户通风
B.使用空气清新剂
C.夜晚在屋内放置绿色植物
D.阳光良好的原始森林
8.下列变化中,前者属于物理变化,后者属于化学变化的一组是( )
①用砂纸打磨除锈、活性炭吸附色素
②金属铝表面生成氧化膜,空气液化
③酒精溶于水,二氧化碳通往石灰水
④白色硫酸铜粉末加水变蓝,石蜡熔化
⑤二氧化碳低温受压凝固成干冰,冰融化成水
⑥汽油挥发,汽油燃烧
A.①③ B.③⑥ C.④⑤ D.⑤⑥
9.相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( )
A.Na2O B.NaOH C.CuSO4·5H2O D.H2SO4
10.下列物质露置于空气中,因发生化学变化而使质量减小的是( )
A.浓硫酸 B.烧碱 C.浓盐酸 D.双氧水
11.自然界中有几千万种含碳物质,并循环转化。下列说法正确的是
A.人的生命活动离不开碳循环
B.森林的减少对碳的循环没有影响
C.金刚石中碳原子间没有间隔
D.地下的煤中碳原子是静止不动的
12.现有10克CuO和ZnO的混合物,下列实验方案,不能确定CuO质量分数的是( )
A.将混合物与足量H2充分反应,冷却后测出剩余固体质量
B.将混合物与足量CO充分反应,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值
C.将混合物完全溶于稀H2SO4,加入足量铁粉,充分反应后,过滤、洗涤、干燥,测出剩余固体质量
D.将混合物完全溶于稀H2SO4,加入足量NaOH溶液,过滤、洗涤、干燥,测出剩余固体质量
二、填空题
13.有下列物质的变化或物质的性质:① 蔗糖能溶于水;②滴水成冰;③氢气燃烧;④镁可以燃烧;⑤鸡蛋发臭;⑥玻璃破碎;⑦酒精易挥发;⑧铁在潮湿环境中容易生锈。
其中,属于化学变化的是________________;属于物理性质的是_______________。
14.空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
(1)X是空气中含量最多的气体,其分子式为_____。
(2)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为_____。
(3)①天然气的主要成分是CH4,点燃CH4之前应_____。8g CH4完全燃烧消耗32g O2,生成a g CO2和18g H2O,则a=_____。
②由CH4在该流程中的作用表明:化学反应中发生物质变化的同时也会伴随有_____变化(选填“能量”或“原子个数”)。
(4)尿素属于_____(选填“氮肥”“磷肥”或“钾肥”);写出NH3合成尿素的化学反应方程式:_____。
15.碳和部分碳的化合物间转化关系如图所示。
(1)物质X的化学式为_____。
(2)在物质的分类中CO属于_____。
A 酸 B 碱 C 盐 D 氧化物
(3)写出图中转化关系中属于化合反应的一个化学方程式:_____。
16.实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数己模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克.
(1)在过滤操作中使用的玻璃仪器有:烧杯、____________和玻璃棒.
(2)样品中氯化钾的质量分数为多少?______________(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?______________
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值.造成这种结果的原因可能是___________.(选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
17.A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是_____。
(2)若C是锌,A和B都属于酸,写出D可能的化学式:_____(物质类别不同的两种即可)。
18.低碳是指较低(更低)的温室气体(二氧化碳为主)排放。低碳生活,就是低能量、低消耗的生活方式。上海世博会是第一个正式提出“低碳”理念的世博会,也是第一个“无烟世博会”。
(1)煤炭、石油和天然气的燃烧与人的呼吸一样,会消耗大气中的_________,并释放出____气体。(填化学式)
(2)一公顷树林,每天能吸收150~500千克的二氧化碳,并释放出60~400千克的氧气,这是依靠植物的____________作用。因此,绿色植物的这种作用有利于维持生物圈中的____________平衡。
(3)在日常生活中,你应如何响应“低碳”的生活方式?___________(举出一例即可)。
三、简答题
19.科学家尝试通过多种途径减少的排放,或将转化为有用的物质。其中一种途径是利用溶液来“捕捉”,并将储存或利用,反应流程如图所示。
(1)反应分离室中分离物质的操作是___________。
(2)上述反应流程中,可循环利用的物质___________。(填化学式)
(3)若反应分离室中有溶质质量分数为10.6%的溶液100千克。求完全反应后,理论上可生成的质量___________(要求根据化学方程式计算)。
四、探究题
20.科学课上,老师告诉学生能发生复分解反应的两种盐通常是可溶的。有通常就有例外,能否找到某些可溶性盐和难溶性盐发生复分解反应的证据呢?科学兴趣小组进行了探究
(查阅资料)①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减少的方向进行
②了解到某些难溶性盐的溶解能力和颜色,其中AgI是一种难溶于水的黄色沉淀。
(实验取证)取一支试管,加入少量AgNO3溶液,再加入过量NaCl溶液,有白色沉淀生成.再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀
(分析讨论)(1)为什么要加入过量的NaCl溶液?请说明理由________
(2)写出加入少量KI溶液后发生反应的化学方程式________
(3)该反应能发生的原因是AgI在水中的溶解能力________AgCl(选填大于、等于或小于)
(得出结论)某些可溶性盐和难溶性盐之间能发生复分解反应.
试卷第2页,共2页
试卷第1页,共1页
参考答案
1.A
2.C
3.D
4.D
5.A
6.B
7.D
8.B
9.A
10.D
11.A
12.C
13.③⑤ ①⑦
14.N2 CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验甲烷的纯度 22 能量 氮肥 CO2+2NH3CO(NH2)2+H2O
15.CO2 D C+O2CO2(合理答案均可)
16.漏斗 74.5% 12.65g BC
17.Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(合理即可) Na2CO3、CuO、NaOH(或其他碳酸盐、金属氧化物、碱的化学式)三种中的任意两种
18.O2 CO2 光合 碳 氧 节约纸张(或随手关灯等)
19.过滤 NaOH和CaO 设生成碳酸钙的质量为x,
x=10kg,
答:生成碳酸钙的质量为10kg。
20.使银离子全部沉淀 KI+AgCl=AgI↓+KCl 小于 答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
