3.3纯净物组成的表示方法-2021-2022学年九年级化学仁爱版上册(word版 含解析)
文档属性
| 名称 | 3.3纯净物组成的表示方法-2021-2022学年九年级化学仁爱版上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 147.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-01 00:00:00 | ||
图片预览




文档简介
3.3纯净物组成的表示方法
一、选择题(共16题)
1.下列说法正确的是
A.H2O2、H2CO3中均含有氢分子
B.KClO3、KCl 中氯元素的化合价均为-1价
C.Na+、Mg2+、Al3+原子核外电子数均为10
D.CO2和CO均由碳元素和氧元素组成,且元素的质量比相同
2.当前,在食品生产经营中违法添加非食用物质和滥用食品添加剂已成为影响中国食品安全的突出问题。如一些不法生猪饲养户为使商品猪多长瘦肉,在饲料中非法添加“瘦肉精”(化学式为C12H18Cl2N2O),对消费者身体造成了极大危害。下列有关说法正确的是
A.“瘦肉精”是由有机物C12H18,单质Cl2和氧化物N2O组成的混合物
B.“瘦肉精”由五种元素组成
C.“瘦肉精”由35个原子构成
D.“瘦肉精”中碳元素和氢元素的质量比为2 :3
3.酚酞是一种常用的化学试剂,其化学式是C20H14O4,下列关于酚酞的说法错误的是
A.酚酞由三种元素组成,属于化合物
B.酚酞分子中碳、氧原子个数比为5:1
C.酚酞中的碳元素和氧元素的质量之比为15:4
D.酚酞的原子质量为318
4.下列含氮化合物中,氮元素的化合价最低的是
A.NO B.NO2 C.NH3 D.HNO3
5.下列关于乙醇(C2H5OH)的说法正确的是
A.乙醇是一种氧化物 B.乙醇中碳、氢元素的质量比为2∶5
C.乙醇中含有9个原子 D.乙醇由碳、氢、氧三种元素组成
6.表示一种元素,又能表示该元素的一个原子,还能表示一种单质的是
A.H2O B.CO C.N2 D.Na
7.下列化学用语书写正确的是
A.3个氮分子:N3
B.3个一氧化氮分子:3NO
C.5个铁离子:5Fe2+
D.氧化镁中镁元素的化合价为+2价:
8.月幔中含橄榄石( Mg2SiO4),其中硅元素的化合价是
A.-3 B.+3 C.+4 D.-4
9.人体在代谢酒精的过程中,会产生一种中间产物乙醛(CH3CHO),如果不能及时将乙醛转化,则会影响身体健康。有关乙醛的说法正确的是( )
A.乙醛由二种元素组成
B.乙醛中碳元素的质量分数最大
C.乙醛属于一种氧化物
D.乙醛中碳和氢的元素个数比为l:2
10.已知硫的氧化物元素质量比为2:3,则硫的化合价为( )
A.-2 B.+4 C.+5 D.+6
11.在新冠疫情防控过程中,75%的乙醇溶液是常见的医用消毒剂。下列有关乙醇(C2H6O)的说法正确的是
A.乙醇的相对分子质量为46g
B.乙醇由2个碳原子、6个氢原子和1个氧原子构成
C.75%的乙醇溶液中氧元素的质量分数为34.8%
D.等质量甲烷比等质量乙醇完全燃烧后CO2排放量高
12.一种新型催化剂,可将二氧化碳高效清洁地转化成液体燃料,反应的微观示意图如下。有关该反应的说法正确的是
A.该反应是分解反应
B.反应物和生成物中共有两种氧化物
C.生成物的符号是H2C2O
D.有利于缓解全球变暖
13.维生素是人体必需的营养素之一,关于维生素C(化学式C6H8O6)的说法中,错误的是
A.维生素C是化合物
B.维生素C是由C、H、O三种元素组成
C.维生素C中氢元素的质量分数最小
D.维生素C的相对分子质量为176g
14.生活中我们经常用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(C17H35COONa)。下列有关说法正确的是
A.硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.硬脂酸钠分子是由碳、氢、氧、钠四种元素组成
C.硬脂酸钠中氢、氧原子的个数比为35:2
D.硬脂酸钠中碳、氧元素的质量比为9:1
15.某氮的氧化物中,氮、氧元素的质量比为7:16,则氮元素的化合价是
A.+4价 B.+3价 C.+2价 D.+1价
16.2016年初美洲、非洲等国家相继出现寨卡病毒。寨卡病毒主要是通过人接触蚊虫而感染。使用驱蚊剂是一种很好的驱蚊方法。某驱蚊剂的主要成分为丙烯菊酯,化学式为C19H26O3。下列相关说法正确的是( )
A.丙烯菊酯由48个原子构成 B.丙烯菊酯分子由碳、氢、氧三种元素组成
C.丙烯菊酯为有机物 D.丙烯菊酯中氢元素的质量分数最大
二、综合题(共5题)
17.小明同学去油车水库进行社会实践活动,用瓶装了一些水库里的水,带回实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水。实验流程如下:
请回答:
(1)操作①的名称是 _________ ,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 __________ (填写字母)。
a漏斗内液面高于滤纸的边缘 b漏斗内的滤纸有破损
c漏斗尖端未靠在烧杯内壁 d用玻璃棒引流
(2)利用如图所示装置进行操作②,除去一些异味和色素,待净化的水应该从 _________ 端通入(选填字母“a”或“b”)。
(3)在制得蒸馏水前常一般加入消毒剂。常用的消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。求:
①高铁酸钠中铁元素的化合价为 ______________ ;
②83g高铁酸钠中含钠元素的质量为 _________ g。
18.(1)下图是氢分子和氧分子运动的示意图。
①上图中,能比较得出“温度越高,分子运动速率越快”这一结论的两幅图片是_______(填字母)。
②比较图A、B可知,影响分子运动速率的因素除温度外,还与________有关。
(2)我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度。
①TiO2中Ti的化合价为__________。氧气与二氧化钛(TiO2)两种物质中都含有______(填“氧元素”或“氧分子”);
②萘胺中C、N元素的质量比为________(最简整数比);
③_______克的萘胺中含氮元素的质量为5.6克?(写出详细的计算过程)
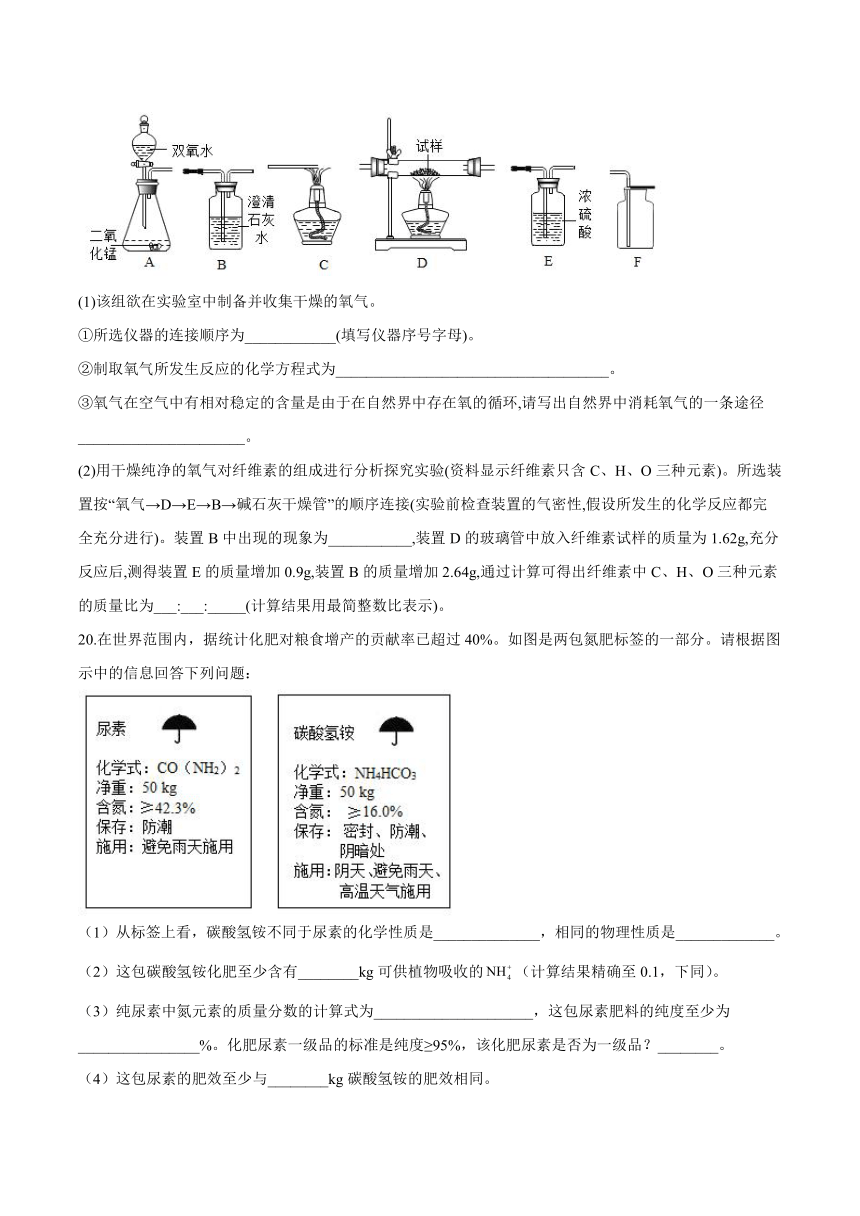
19.如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各实验,回答下列问题:
(1)该组欲在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为____________(填写仪器序号字母)。
②制取氧气所发生反应的化学方程式为____________________________________。
③氧气在空气中有相对稳定的含量是由于在自然界中存在氧的循环,请写出自然界中消耗氧气的一条途径______________________。
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按“氧气→D→E→B→碱石灰干燥管”的顺序连接(实验前检查装置的气密性,假设所发生的化学反应都完全充分进行)。装置B中出现的现象为___________,装置D的玻璃管中放入纤维素试样的质量为1.62g,充分反应后,测得装置E的质量增加0.9g,装置B的质量增加2.64g,通过计算可得出纤维素中C、H、O三种元素的质量比为___:___:_____(计算结果用最简整数比表示)。
20.在世界范围内,据统计化肥对粮食增产的贡献率已超过40%。如图是两包氮肥标签的一部分。请根据图示中的信息回答下列问题:
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是______________,相同的物理性质是_____________。
(2)这包碳酸氢铵化肥至少含有________kg可供植物吸收的(计算结果精确至0.1,下同)。
(3)纯尿素中氮元素的质量分数的计算式为_____________________,这包尿素肥料的纯度至少为________________%。化肥尿素一级品的标准是纯度≥95%,该化肥尿素是否为一级品?________。
(4)这包尿素的肥效至少与________kg碳酸氢铵的肥效相同。
(5)1吨纯净氮肥的市场价格如下:1080元、330元。这包尿素的价格为________元,用这个价格的钱采购碳铵,购得的氮肥含氮元素最多的是________。
21.淀粉类食物是人类饮食的重要组成之一。淀粉[化学式为(C6H10O5)n](n的取值从几万到几十万)在人体中被分解生成葡萄糖(化学式为C6H12O6)参与细胞代谢。
(1)淀粉由_____种元素组成,分子中的氢、氧原子个数比为_____。
(2)已知1mol(mol,摩尔,表示物质的量,是一种单位)葡萄糖的质量是180g,则90g葡萄糖的物质的量是_____mol。
(3)列式计算葡萄糖中含量最多的元素质量分数_____。
参考答案
1.C
【详解】
A、分子由原子构成,H2O2、H2CO3中均含有氢原子,不符合题意;
B、KClO3中氯元素的化合价均为+5价, KCl 中氯元素的化合价均为-1价,不符合题意;
C、Na原子核外电子数为11,失去一个电子得到的Na+原子核外电子数为10;Mg原子核外电子数为12,失去2个电子得到的Mg2+原子核外电子数为10;Al原子核外电子数为13,失去3个电子得到的Al3+原子核外电子数为10,符合题意;
D、CO2 中碳氧元素的质量比=12:32;CO中碳氧元素的质量比=12:16,不符合题意;故选C。
2.B
【详解】
A、“瘦肉精”不是由有机物C12H18,单质Cl2和氧化物N2O组成的混合物,而是由碳元素、氢元素、氯元素、氮元素和氧元素组成的纯净物,故错误;
B、由“瘦肉精”(化学式为C12H18Cl2N2O)可知,“瘦肉精”由五种元素组成,故正确;
C、由“瘦肉精”(化学式为C12H18Cl2N2O)可知,1个“瘦肉精”分子由35个原子构成,故错误;
D、“瘦肉精”中碳元素和氢元素的质量比为:12×12:1×18=8:1,故错误。
故选B。
3.D
【解析】
试题分析:A选项酚酞是由碳、氢、氧三种元素组成的纯净物,属于化合物,故选项说法正确. B选项1个酚酞分子中含有20个碳原子、4个氧原子,则酚酞分子中碳、氧原子个数比为20:4=5:1,故选项说法正确. C选项酚酞中的碳元素和氧元素的质量之比为(12×20):(16×4)=15:4,故选项说法正确. D选项酚酞的相对分子质量为12×20+1×14+16×4=318,而不是酚酞的相对原子质量是318,故选项说法错误.故选D.
4.C
【详解】
A、氧元素显﹣2价,设NO中氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)=0,则x=+2价。
B、氧元素显﹣2价,设NO2中氮元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(﹣2)×2=0,则y=+4价。
C、氢元素显+1价,设NH3中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:z+(+1)×3=0,则z=﹣3价。
D、氢元素显+1价,氧元素显﹣2价,设HNO3中氮元素的化合价是w,根据在化合物中正负化合价代数和为零,可得:(+1)+w+(﹣2)×3=0,则w=+5价。故氮元素的化合价最低的是C。故选C。
5.D
【详解】
A、氧化物是氧元素与另一种元素组成的化合物,而乙醇由三种元素组成,不属于氧化物,选项错误;
B、乙醇中碳、氢元素的质量比=(12×2):(1×6)=4:1,选项错误;
C、由化学式可知,1个乙醇分子中含有2+6+1=9个原子,选项错误;
D、由化学式可知,乙醇由碳、氢、氧三种元素组成,选项正确。
故选D。
6.D
【解析】
试题分析:A选项表示水这种物质,不能表示元素;B选项表示一氧化碳这种物质不能表示元素;C选项为氮气的化学式不能表示元素;D选项为金属钠的元素符号,既可以表示元素、又可以表示1个原子、还可以表示钠单质;故答案选择D
7.B
【详解】
A、分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故3个氮分子表示为:3N2,不符合题意;
B、分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故3个一氧化氮分子表示为:3NO,符合题意;
C、离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故5个铁离子表示为:5Fe3+,不符合题意;
D、元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面。故氧化镁中镁元素的化合价为+2价,表示为:,不符合题意。
故选B。
8.C
【详解】
Mg2SiO4中镁元素显+2价,氧元素显-2价,设硅元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:(+2)×2+x+(-2)×4=0,x=+4。
故选C。
9.B
【详解】
A、乙醛(CH3CHO)是碳氢氧三种元素组成的,而不是由两种元素组成,选项错误;
B、乙醛(CH3CHO)中碳氢氧三种元素的质量比为(12×2):(1×4):16=6:1:4,所以碳元素质量分数最大,选项正确;
C、乙醛(CH3CHO)是碳氢氧三种元素组成的,而氧化物只能是由两种元素组成,所以乙醛(CH3CHO)不是氧化物,选项错误;
D、乙醛(CH3CHO)碳氢原子个数比为2:4=1:2,但不是元素个数,选项错误,故选B。
10.D
【详解】
某种硫的氧化物中,硫元素与氧元素的质量比为2:3,则该氧化物的分子中硫原子和氧原子的个数比= ,则该氧化物的化学式为SO3:氧元素显-2价,设:硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×3-0,则x=+6价。故选D。
11.D
【详解】
A、乙醇的相对分子质量为:24+6+16=46,单位是“1”,通常省略,选项A不正确;
B、乙醇是由乙醇分子构成的,每个乙醇分子由2个碳原子、6个氢原子、1个氧原子构成,选项B不正确;
C、乙醇中氧元素的质量分数为,但乙醇溶液中含有水,水中含有氧元素,75%的乙醇溶液中氧元素的质量分数大于34.8%,选项C不正确;
D、甲烷的化学式为CH4,乙醇的化学式为C2H6O,甲烷中碳元素的质量分数为:,乙醇中碳元素的质量分数为:,甲烷含碳量比乙醇含碳量高,等质量的碳转化成的二氧化碳质量相等,故等质量甲烷比等质量乙醇完全燃烧后CO2排放量高,选项D正确。
故选D。
12.D
【详解】
A、根据反应的微观示意图,反应物是两种:CO2和H2,生成物是一种:CH2O2,符合化合反应的定义,是化合反应,选项A不正确;
B、根据反应的微观示意图,反应物是CO2和H2,生成物是CH2O2,只有CO2一种氧化物,选项B不正确;
C、根据反应的微观示意图,生成物的化学式是CH2O2,选项C不正确;
D、因为反应中将二氧化碳转化为CH2O2,减少了CO2的排放,可以减轻温室效应,有利于缓解全球变暖,选项D正确。故选D。
13.D
【详解】
A、维生素C是由C、H、O三种元素组成的纯净物,属于化合物,不符合题意;
B、由化学式可知,维生素C是由C、H、O三种元素组成,不符合题意;
C、维生素C中C、H、O元素的质量比为:(12×6):8:(16×6)=9:1:12,故氢元素的质量分数最小,不符合题意;
D、维生素C的相对分子质量为:12×6+8+16×6=176,相对分子质量是一个比值,单位为“1”,常省略不写,符合题意。
故选D。
14.C
【详解】
A、硬脂酸钠是由硬脂酸钠分子构成的,每个硬脂酸钠分子是由18个碳原子、35个氢原子、2个氧原子和1个钠原子构成的。选项A错误;
B、硬脂酸钠分子是由碳原子、氢原子、氧原子和钠原子构成的,硬脂酸钠是由碳、氢、氧、钠四种元素组成的。选项B错误;
C、由硬脂酸钠的化学式可知,在硬脂酸钠中氢、氧原子个数比为35:2。选项C正确;
D.硬脂酸钠中碳元素和氧元素的质量比为(12×18):(16×2)=27:4。选项D错误。
故选:C。
15.A
【解析】
试题分析:由某种氮的氧化物中,氮元素与氧元素的质量比为7:16,可以确定其化合物的化学式,进而由在化合物中正负化合价代数和为零,进行分析解答即可.
解:某种氮的氧化物中,氮元素与氧元素的质量比为7:16,则该氧化物中氮原子和氧原子的个数比为:=1:2,故其氧化物的化学式为:NO2.
氧元素显﹣2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)×2=0,则x=+4价.
故选A.
16.C
【解析】A、一个丙烯菊酯分子由48个原子构成,错误B、由丙烯菊酯(化学式:C19H26O3)的化学式可知,丙烯菊酯分子由碳、氢、氧三种元素构成,错误;C、丙烯菊酯是含有碳元素的化合物,属于有机物,正确;D、丙烯菊酯中碳、氢、氧三种元素的质量比为(12×19):(1×26):(16×3)=114:13:24,丙烯菊酯中氢元素的质量分数最小,错误。故选C。
17.过滤 ab b +6 23
【详解】
(1)操作①是将固体和液体分离的操作,故填写:过滤;
若经过过滤后,所得液体C中仍有浑浊,其原因可能是:漏斗内液面高于滤纸的边缘和漏斗内的滤纸有破损,故填写:ab;
(2)除去一些异味和色素,待净化的水最好从下端进入,这样净化的效果会更好,故填写:b;
(3)高铁酸钠中钠的化合价为+1,氧的化合价为-2,根据化合物中,正负化合价为零的原则,若假设高铁酸钠中铁的化合价为x,则(-2)ⅹ4+(+1)ⅹ2+x=0,x=+6,故填写:+6;
83g高铁酸钠中含钠元素的质量为:83gⅹ=23g,故填写:23。
18.BC 分子种类/分子大小/分子质量 +4 氧元素 60∶7 57.2g
【详解】
(1) ①BC是同种分子在不同温度下的运动速率不同,故在A、B和C中,能比较得出“温度越高,分子运动速度越快”的是BC;②由AB可知,温度相同,分子不同,运动速率不同,故影响分子运动速率的因素除温度外,还与分子种类(分子大小、分子质量)有关;(2) ①TiO2中氧元素是-2价,根据正负化合价的代数和为零的原则,因此Ti的化合价为+4价;物质是由元素组成的,氧气与二氧化钛(TiO2)中都含有氧元素;②根据“萘胺”(C10H9N),萘胺中C、N元素的质量比:1012:14=60∶7;③设:需要萘胺的为:X,则:
X100%=5.6g,X=57.2g。
19.AEF 呼吸作用 澄清石灰水变浑浊 36 5 40
【详解】
(1)
①所选仪器的连接顺序为:通过A制取氧气,通过E干燥氧气,通过F收集氧气。
故填:AEF。
②过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为:。
③自然界中消耗氧气的一条途径是呼吸作用,呼吸作用过程中消耗氧气,生成二氧化碳等物质。
故填:呼吸作用。
(2)纤维素与氧气在加热时反应生成二氧化碳和水,通过E浓硫酸干燥后进入装置B,B中澄清石灰水遇到二氧化碳要变浑浊;
测得装置E的质量增加0.9g,说明生成了0.9g水,装置B的质量增加2.64g,说明生成了2.64g二氧化碳;
0.9g水中氢元素质量为:;
2.64g二氧化碳中碳元素质量为:2.64g×=0.72g;
水中的氢元素、二氧化碳中的碳元素都来自于纤维素,故纤维素中碳元素质量是0.72g,氢元素质量是0.1g,纤维素只有三种元素,所以其中氧元素质量就等于纤维素质量减去氢和碳元素的质量,即:1.62g-0.72g-0.1=0.8g,
纤维素中C、H、O三种元素的质量比为:0.72g:0.1g:0.8g=36:5:40,
故填:36;5;40。
20.受热易分解 易溶于水 10.3 (合理均可) 90.6% 否 132.1 48.9 碳酸氢铵
【详解】
(1)由表可知,碳酸氢铵受热易分解。易溶于水。
(2)50kg的肥料中氮元素的质量为:50kg×16%=8kg,50kg的肥料中的碳酸氢铵的质量为:8kg÷ ≈45.14kg,45.14kg的碳酸氢铵中的质量为:45.14kg×≈10.3kg。
(3)尿素中氮元素的质量分数的计算式为;50kg的尿素中氮元素的质量最低为:50kg×42.3%=21.15kg。含氮元素21.15kg的纯尿素的质量为:21.15kg÷≈45.32kg。故这包尿素的纯度为:×100%≈90.6%。90.6%小于95%,故不是一等品。
(4)这包尿素中的氮元素的质量为21.15kg,含有21.15kg的氮元素的碳酸氢铵的质量为:21.15kg÷≈119.3kg。该碳酸氢铵中碳酸氢铵的纯度为:45.14kg÷50kg×100%=90.28%,119.3kg÷90.28%=132.1kg。
(5)50kg尿素的价格为:1080元÷1000×50×90.6%≈48.9元。用48.9元钱可以购买尿素的质量为:50kg,其中含有氮元素的质量为21.15kg,可以购买碳酸氢铵的质量 为:48.9÷330×1000≈148.2(kg),148.2kg的碳酸氢铵中含有氮元素的质量为:148.2kg×16%≈23.7kg,故购买的碳酸氢铵含氮元素多。
3; 2:1; 0.5; 53.3%。
【详解】
(1)淀粉中含有碳、氢、氧三种元素,其中氢氧原子个数比为:12:6=2:1,故答案为3;淀粉[化学式为(C6H10O5)n]中 氢氧原子个数比为:12:6=2:1,故答案为2:1;
(2)1mol葡萄糖的质量是180g,则90g葡萄糖的物质的量是,故答案为0.5;
(3)葡萄糖中碳、氢、氧三种元素的质量比为:(12×6):(1×12):(16×6)=6:1:8,故氧元素的质量分数最大,其质量分数为:,故答案为53.3%。
一、选择题(共16题)
1.下列说法正确的是
A.H2O2、H2CO3中均含有氢分子
B.KClO3、KCl 中氯元素的化合价均为-1价
C.Na+、Mg2+、Al3+原子核外电子数均为10
D.CO2和CO均由碳元素和氧元素组成,且元素的质量比相同
2.当前,在食品生产经营中违法添加非食用物质和滥用食品添加剂已成为影响中国食品安全的突出问题。如一些不法生猪饲养户为使商品猪多长瘦肉,在饲料中非法添加“瘦肉精”(化学式为C12H18Cl2N2O),对消费者身体造成了极大危害。下列有关说法正确的是
A.“瘦肉精”是由有机物C12H18,单质Cl2和氧化物N2O组成的混合物
B.“瘦肉精”由五种元素组成
C.“瘦肉精”由35个原子构成
D.“瘦肉精”中碳元素和氢元素的质量比为2 :3
3.酚酞是一种常用的化学试剂,其化学式是C20H14O4,下列关于酚酞的说法错误的是
A.酚酞由三种元素组成,属于化合物
B.酚酞分子中碳、氧原子个数比为5:1
C.酚酞中的碳元素和氧元素的质量之比为15:4
D.酚酞的原子质量为318
4.下列含氮化合物中,氮元素的化合价最低的是
A.NO B.NO2 C.NH3 D.HNO3
5.下列关于乙醇(C2H5OH)的说法正确的是
A.乙醇是一种氧化物 B.乙醇中碳、氢元素的质量比为2∶5
C.乙醇中含有9个原子 D.乙醇由碳、氢、氧三种元素组成
6.表示一种元素,又能表示该元素的一个原子,还能表示一种单质的是
A.H2O B.CO C.N2 D.Na
7.下列化学用语书写正确的是
A.3个氮分子:N3
B.3个一氧化氮分子:3NO
C.5个铁离子:5Fe2+
D.氧化镁中镁元素的化合价为+2价:
8.月幔中含橄榄石( Mg2SiO4),其中硅元素的化合价是
A.-3 B.+3 C.+4 D.-4
9.人体在代谢酒精的过程中,会产生一种中间产物乙醛(CH3CHO),如果不能及时将乙醛转化,则会影响身体健康。有关乙醛的说法正确的是( )
A.乙醛由二种元素组成
B.乙醛中碳元素的质量分数最大
C.乙醛属于一种氧化物
D.乙醛中碳和氢的元素个数比为l:2
10.已知硫的氧化物元素质量比为2:3,则硫的化合价为( )
A.-2 B.+4 C.+5 D.+6
11.在新冠疫情防控过程中,75%的乙醇溶液是常见的医用消毒剂。下列有关乙醇(C2H6O)的说法正确的是
A.乙醇的相对分子质量为46g
B.乙醇由2个碳原子、6个氢原子和1个氧原子构成
C.75%的乙醇溶液中氧元素的质量分数为34.8%
D.等质量甲烷比等质量乙醇完全燃烧后CO2排放量高
12.一种新型催化剂,可将二氧化碳高效清洁地转化成液体燃料,反应的微观示意图如下。有关该反应的说法正确的是
A.该反应是分解反应
B.反应物和生成物中共有两种氧化物
C.生成物的符号是H2C2O
D.有利于缓解全球变暖
13.维生素是人体必需的营养素之一,关于维生素C(化学式C6H8O6)的说法中,错误的是
A.维生素C是化合物
B.维生素C是由C、H、O三种元素组成
C.维生素C中氢元素的质量分数最小
D.维生素C的相对分子质量为176g
14.生活中我们经常用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(C17H35COONa)。下列有关说法正确的是
A.硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.硬脂酸钠分子是由碳、氢、氧、钠四种元素组成
C.硬脂酸钠中氢、氧原子的个数比为35:2
D.硬脂酸钠中碳、氧元素的质量比为9:1
15.某氮的氧化物中,氮、氧元素的质量比为7:16,则氮元素的化合价是
A.+4价 B.+3价 C.+2价 D.+1价
16.2016年初美洲、非洲等国家相继出现寨卡病毒。寨卡病毒主要是通过人接触蚊虫而感染。使用驱蚊剂是一种很好的驱蚊方法。某驱蚊剂的主要成分为丙烯菊酯,化学式为C19H26O3。下列相关说法正确的是( )
A.丙烯菊酯由48个原子构成 B.丙烯菊酯分子由碳、氢、氧三种元素组成
C.丙烯菊酯为有机物 D.丙烯菊酯中氢元素的质量分数最大
二、综合题(共5题)
17.小明同学去油车水库进行社会实践活动,用瓶装了一些水库里的水,带回实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水。实验流程如下:
请回答:
(1)操作①的名称是 _________ ,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 __________ (填写字母)。
a漏斗内液面高于滤纸的边缘 b漏斗内的滤纸有破损
c漏斗尖端未靠在烧杯内壁 d用玻璃棒引流
(2)利用如图所示装置进行操作②,除去一些异味和色素,待净化的水应该从 _________ 端通入(选填字母“a”或“b”)。
(3)在制得蒸馏水前常一般加入消毒剂。常用的消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。求:
①高铁酸钠中铁元素的化合价为 ______________ ;
②83g高铁酸钠中含钠元素的质量为 _________ g。
18.(1)下图是氢分子和氧分子运动的示意图。
①上图中,能比较得出“温度越高,分子运动速率越快”这一结论的两幅图片是_______(填字母)。
②比较图A、B可知,影响分子运动速率的因素除温度外,还与________有关。
(2)我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度。
①TiO2中Ti的化合价为__________。氧气与二氧化钛(TiO2)两种物质中都含有______(填“氧元素”或“氧分子”);
②萘胺中C、N元素的质量比为________(最简整数比);
③_______克的萘胺中含氮元素的质量为5.6克?(写出详细的计算过程)
19.如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各实验,回答下列问题:
(1)该组欲在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为____________(填写仪器序号字母)。
②制取氧气所发生反应的化学方程式为____________________________________。
③氧气在空气中有相对稳定的含量是由于在自然界中存在氧的循环,请写出自然界中消耗氧气的一条途径______________________。
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按“氧气→D→E→B→碱石灰干燥管”的顺序连接(实验前检查装置的气密性,假设所发生的化学反应都完全充分进行)。装置B中出现的现象为___________,装置D的玻璃管中放入纤维素试样的质量为1.62g,充分反应后,测得装置E的质量增加0.9g,装置B的质量增加2.64g,通过计算可得出纤维素中C、H、O三种元素的质量比为___:___:_____(计算结果用最简整数比表示)。
20.在世界范围内,据统计化肥对粮食增产的贡献率已超过40%。如图是两包氮肥标签的一部分。请根据图示中的信息回答下列问题:
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是______________,相同的物理性质是_____________。
(2)这包碳酸氢铵化肥至少含有________kg可供植物吸收的(计算结果精确至0.1,下同)。
(3)纯尿素中氮元素的质量分数的计算式为_____________________,这包尿素肥料的纯度至少为________________%。化肥尿素一级品的标准是纯度≥95%,该化肥尿素是否为一级品?________。
(4)这包尿素的肥效至少与________kg碳酸氢铵的肥效相同。
(5)1吨纯净氮肥的市场价格如下:1080元、330元。这包尿素的价格为________元,用这个价格的钱采购碳铵,购得的氮肥含氮元素最多的是________。
21.淀粉类食物是人类饮食的重要组成之一。淀粉[化学式为(C6H10O5)n](n的取值从几万到几十万)在人体中被分解生成葡萄糖(化学式为C6H12O6)参与细胞代谢。
(1)淀粉由_____种元素组成,分子中的氢、氧原子个数比为_____。
(2)已知1mol(mol,摩尔,表示物质的量,是一种单位)葡萄糖的质量是180g,则90g葡萄糖的物质的量是_____mol。
(3)列式计算葡萄糖中含量最多的元素质量分数_____。
参考答案
1.C
【详解】
A、分子由原子构成,H2O2、H2CO3中均含有氢原子,不符合题意;
B、KClO3中氯元素的化合价均为+5价, KCl 中氯元素的化合价均为-1价,不符合题意;
C、Na原子核外电子数为11,失去一个电子得到的Na+原子核外电子数为10;Mg原子核外电子数为12,失去2个电子得到的Mg2+原子核外电子数为10;Al原子核外电子数为13,失去3个电子得到的Al3+原子核外电子数为10,符合题意;
D、CO2 中碳氧元素的质量比=12:32;CO中碳氧元素的质量比=12:16,不符合题意;故选C。
2.B
【详解】
A、“瘦肉精”不是由有机物C12H18,单质Cl2和氧化物N2O组成的混合物,而是由碳元素、氢元素、氯元素、氮元素和氧元素组成的纯净物,故错误;
B、由“瘦肉精”(化学式为C12H18Cl2N2O)可知,“瘦肉精”由五种元素组成,故正确;
C、由“瘦肉精”(化学式为C12H18Cl2N2O)可知,1个“瘦肉精”分子由35个原子构成,故错误;
D、“瘦肉精”中碳元素和氢元素的质量比为:12×12:1×18=8:1,故错误。
故选B。
3.D
【解析】
试题分析:A选项酚酞是由碳、氢、氧三种元素组成的纯净物,属于化合物,故选项说法正确. B选项1个酚酞分子中含有20个碳原子、4个氧原子,则酚酞分子中碳、氧原子个数比为20:4=5:1,故选项说法正确. C选项酚酞中的碳元素和氧元素的质量之比为(12×20):(16×4)=15:4,故选项说法正确. D选项酚酞的相对分子质量为12×20+1×14+16×4=318,而不是酚酞的相对原子质量是318,故选项说法错误.故选D.
4.C
【详解】
A、氧元素显﹣2价,设NO中氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)=0,则x=+2价。
B、氧元素显﹣2价,设NO2中氮元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(﹣2)×2=0,则y=+4价。
C、氢元素显+1价,设NH3中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:z+(+1)×3=0,则z=﹣3价。
D、氢元素显+1价,氧元素显﹣2价,设HNO3中氮元素的化合价是w,根据在化合物中正负化合价代数和为零,可得:(+1)+w+(﹣2)×3=0,则w=+5价。故氮元素的化合价最低的是C。故选C。
5.D
【详解】
A、氧化物是氧元素与另一种元素组成的化合物,而乙醇由三种元素组成,不属于氧化物,选项错误;
B、乙醇中碳、氢元素的质量比=(12×2):(1×6)=4:1,选项错误;
C、由化学式可知,1个乙醇分子中含有2+6+1=9个原子,选项错误;
D、由化学式可知,乙醇由碳、氢、氧三种元素组成,选项正确。
故选D。
6.D
【解析】
试题分析:A选项表示水这种物质,不能表示元素;B选项表示一氧化碳这种物质不能表示元素;C选项为氮气的化学式不能表示元素;D选项为金属钠的元素符号,既可以表示元素、又可以表示1个原子、还可以表示钠单质;故答案选择D
7.B
【详解】
A、分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故3个氮分子表示为:3N2,不符合题意;
B、分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故3个一氧化氮分子表示为:3NO,符合题意;
C、离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故5个铁离子表示为:5Fe3+,不符合题意;
D、元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面。故氧化镁中镁元素的化合价为+2价,表示为:,不符合题意。
故选B。
8.C
【详解】
Mg2SiO4中镁元素显+2价,氧元素显-2价,设硅元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:(+2)×2+x+(-2)×4=0,x=+4。
故选C。
9.B
【详解】
A、乙醛(CH3CHO)是碳氢氧三种元素组成的,而不是由两种元素组成,选项错误;
B、乙醛(CH3CHO)中碳氢氧三种元素的质量比为(12×2):(1×4):16=6:1:4,所以碳元素质量分数最大,选项正确;
C、乙醛(CH3CHO)是碳氢氧三种元素组成的,而氧化物只能是由两种元素组成,所以乙醛(CH3CHO)不是氧化物,选项错误;
D、乙醛(CH3CHO)碳氢原子个数比为2:4=1:2,但不是元素个数,选项错误,故选B。
10.D
【详解】
某种硫的氧化物中,硫元素与氧元素的质量比为2:3,则该氧化物的分子中硫原子和氧原子的个数比= ,则该氧化物的化学式为SO3:氧元素显-2价,设:硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×3-0,则x=+6价。故选D。
11.D
【详解】
A、乙醇的相对分子质量为:24+6+16=46,单位是“1”,通常省略,选项A不正确;
B、乙醇是由乙醇分子构成的,每个乙醇分子由2个碳原子、6个氢原子、1个氧原子构成,选项B不正确;
C、乙醇中氧元素的质量分数为,但乙醇溶液中含有水,水中含有氧元素,75%的乙醇溶液中氧元素的质量分数大于34.8%,选项C不正确;
D、甲烷的化学式为CH4,乙醇的化学式为C2H6O,甲烷中碳元素的质量分数为:,乙醇中碳元素的质量分数为:,甲烷含碳量比乙醇含碳量高,等质量的碳转化成的二氧化碳质量相等,故等质量甲烷比等质量乙醇完全燃烧后CO2排放量高,选项D正确。
故选D。
12.D
【详解】
A、根据反应的微观示意图,反应物是两种:CO2和H2,生成物是一种:CH2O2,符合化合反应的定义,是化合反应,选项A不正确;
B、根据反应的微观示意图,反应物是CO2和H2,生成物是CH2O2,只有CO2一种氧化物,选项B不正确;
C、根据反应的微观示意图,生成物的化学式是CH2O2,选项C不正确;
D、因为反应中将二氧化碳转化为CH2O2,减少了CO2的排放,可以减轻温室效应,有利于缓解全球变暖,选项D正确。故选D。
13.D
【详解】
A、维生素C是由C、H、O三种元素组成的纯净物,属于化合物,不符合题意;
B、由化学式可知,维生素C是由C、H、O三种元素组成,不符合题意;
C、维生素C中C、H、O元素的质量比为:(12×6):8:(16×6)=9:1:12,故氢元素的质量分数最小,不符合题意;
D、维生素C的相对分子质量为:12×6+8+16×6=176,相对分子质量是一个比值,单位为“1”,常省略不写,符合题意。
故选D。
14.C
【详解】
A、硬脂酸钠是由硬脂酸钠分子构成的,每个硬脂酸钠分子是由18个碳原子、35个氢原子、2个氧原子和1个钠原子构成的。选项A错误;
B、硬脂酸钠分子是由碳原子、氢原子、氧原子和钠原子构成的,硬脂酸钠是由碳、氢、氧、钠四种元素组成的。选项B错误;
C、由硬脂酸钠的化学式可知,在硬脂酸钠中氢、氧原子个数比为35:2。选项C正确;
D.硬脂酸钠中碳元素和氧元素的质量比为(12×18):(16×2)=27:4。选项D错误。
故选:C。
15.A
【解析】
试题分析:由某种氮的氧化物中,氮元素与氧元素的质量比为7:16,可以确定其化合物的化学式,进而由在化合物中正负化合价代数和为零,进行分析解答即可.
解:某种氮的氧化物中,氮元素与氧元素的质量比为7:16,则该氧化物中氮原子和氧原子的个数比为:=1:2,故其氧化物的化学式为:NO2.
氧元素显﹣2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)×2=0,则x=+4价.
故选A.
16.C
【解析】A、一个丙烯菊酯分子由48个原子构成,错误B、由丙烯菊酯(化学式:C19H26O3)的化学式可知,丙烯菊酯分子由碳、氢、氧三种元素构成,错误;C、丙烯菊酯是含有碳元素的化合物,属于有机物,正确;D、丙烯菊酯中碳、氢、氧三种元素的质量比为(12×19):(1×26):(16×3)=114:13:24,丙烯菊酯中氢元素的质量分数最小,错误。故选C。
17.过滤 ab b +6 23
【详解】
(1)操作①是将固体和液体分离的操作,故填写:过滤;
若经过过滤后,所得液体C中仍有浑浊,其原因可能是:漏斗内液面高于滤纸的边缘和漏斗内的滤纸有破损,故填写:ab;
(2)除去一些异味和色素,待净化的水最好从下端进入,这样净化的效果会更好,故填写:b;
(3)高铁酸钠中钠的化合价为+1,氧的化合价为-2,根据化合物中,正负化合价为零的原则,若假设高铁酸钠中铁的化合价为x,则(-2)ⅹ4+(+1)ⅹ2+x=0,x=+6,故填写:+6;
83g高铁酸钠中含钠元素的质量为:83gⅹ=23g,故填写:23。
18.BC 分子种类/分子大小/分子质量 +4 氧元素 60∶7 57.2g
【详解】
(1) ①BC是同种分子在不同温度下的运动速率不同,故在A、B和C中,能比较得出“温度越高,分子运动速度越快”的是BC;②由AB可知,温度相同,分子不同,运动速率不同,故影响分子运动速率的因素除温度外,还与分子种类(分子大小、分子质量)有关;(2) ①TiO2中氧元素是-2价,根据正负化合价的代数和为零的原则,因此Ti的化合价为+4价;物质是由元素组成的,氧气与二氧化钛(TiO2)中都含有氧元素;②根据“萘胺”(C10H9N),萘胺中C、N元素的质量比:1012:14=60∶7;③设:需要萘胺的为:X,则:
X100%=5.6g,X=57.2g。
19.AEF 呼吸作用 澄清石灰水变浑浊 36 5 40
【详解】
(1)
①所选仪器的连接顺序为:通过A制取氧气,通过E干燥氧气,通过F收集氧气。
故填:AEF。
②过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为:。
③自然界中消耗氧气的一条途径是呼吸作用,呼吸作用过程中消耗氧气,生成二氧化碳等物质。
故填:呼吸作用。
(2)纤维素与氧气在加热时反应生成二氧化碳和水,通过E浓硫酸干燥后进入装置B,B中澄清石灰水遇到二氧化碳要变浑浊;
测得装置E的质量增加0.9g,说明生成了0.9g水,装置B的质量增加2.64g,说明生成了2.64g二氧化碳;
0.9g水中氢元素质量为:;
2.64g二氧化碳中碳元素质量为:2.64g×=0.72g;
水中的氢元素、二氧化碳中的碳元素都来自于纤维素,故纤维素中碳元素质量是0.72g,氢元素质量是0.1g,纤维素只有三种元素,所以其中氧元素质量就等于纤维素质量减去氢和碳元素的质量,即:1.62g-0.72g-0.1=0.8g,
纤维素中C、H、O三种元素的质量比为:0.72g:0.1g:0.8g=36:5:40,
故填:36;5;40。
20.受热易分解 易溶于水 10.3 (合理均可) 90.6% 否 132.1 48.9 碳酸氢铵
【详解】
(1)由表可知,碳酸氢铵受热易分解。易溶于水。
(2)50kg的肥料中氮元素的质量为:50kg×16%=8kg,50kg的肥料中的碳酸氢铵的质量为:8kg÷ ≈45.14kg,45.14kg的碳酸氢铵中的质量为:45.14kg×≈10.3kg。
(3)尿素中氮元素的质量分数的计算式为;50kg的尿素中氮元素的质量最低为:50kg×42.3%=21.15kg。含氮元素21.15kg的纯尿素的质量为:21.15kg÷≈45.32kg。故这包尿素的纯度为:×100%≈90.6%。90.6%小于95%,故不是一等品。
(4)这包尿素中的氮元素的质量为21.15kg,含有21.15kg的氮元素的碳酸氢铵的质量为:21.15kg÷≈119.3kg。该碳酸氢铵中碳酸氢铵的纯度为:45.14kg÷50kg×100%=90.28%,119.3kg÷90.28%=132.1kg。
(5)50kg尿素的价格为:1080元÷1000×50×90.6%≈48.9元。用48.9元钱可以购买尿素的质量为:50kg,其中含有氮元素的质量为21.15kg,可以购买碳酸氢铵的质量 为:48.9÷330×1000≈148.2(kg),148.2kg的碳酸氢铵中含有氮元素的质量为:148.2kg×16%≈23.7kg,故购买的碳酸氢铵含氮元素多。
3; 2:1; 0.5; 53.3%。
【详解】
(1)淀粉中含有碳、氢、氧三种元素,其中氢氧原子个数比为:12:6=2:1,故答案为3;淀粉[化学式为(C6H10O5)n]中 氢氧原子个数比为:12:6=2:1,故答案为2:1;
(2)1mol葡萄糖的质量是180g,则90g葡萄糖的物质的量是,故答案为0.5;
(3)葡萄糖中碳、氢、氧三种元素的质量比为:(12×6):(1×12):(16×6)=6:1:8,故氧元素的质量分数最大,其质量分数为:,故答案为53.3%。
同课章节目录
- 专题一 走进化学殿堂
- 单元1 化学使生活更美好
- 单元2 如何学习化学
- 专题二 空气和水
- 单元1 多组分的空气
- 单元2 氧气
- 单元3 自然界的水
- 专题三 物质的构成
- 单元1 构成物质的微粒
- 单元2 组成物质的元素
- 单元3 纯净物组成的表示方法
- 专题四 燃料与燃烧
- 单元1 燃烧与灭火
- 单元2 碳及其化合物
- 单元3 化石燃料的利用
- 专题五 化学变化及其表示
- 单元1 化学变化是有条件的
- 单元2 质量守恒定律
- 单元3 化学方程式
- 专题六 物质的溶解
- 单元1 物质的溶解过程
- 单元2 物质的溶解性
- 单元3 物质的溶解性的改变
- 学生实验
- 实验1 实验基本操作
- 实验2 氧气的实验室制取与性质
- 实验3 燃烧的条件
- 实验4 二氧化碳的实验室制取与性质
- 实验5 一定浓度溶液的配置
