第九单元课题3 溶液的浓度综合训练—2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 第九单元课题3 溶液的浓度综合训练—2021-2022学年九年级化学人教版下册(word版有答案) |  | |
| 格式 | docx | ||
| 文件大小 | 166.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-02 23:36:56 | ||
图片预览

文档简介
2021-2022学年人教版初三化学下册第九单元课题3 溶液的浓度 综合训练
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
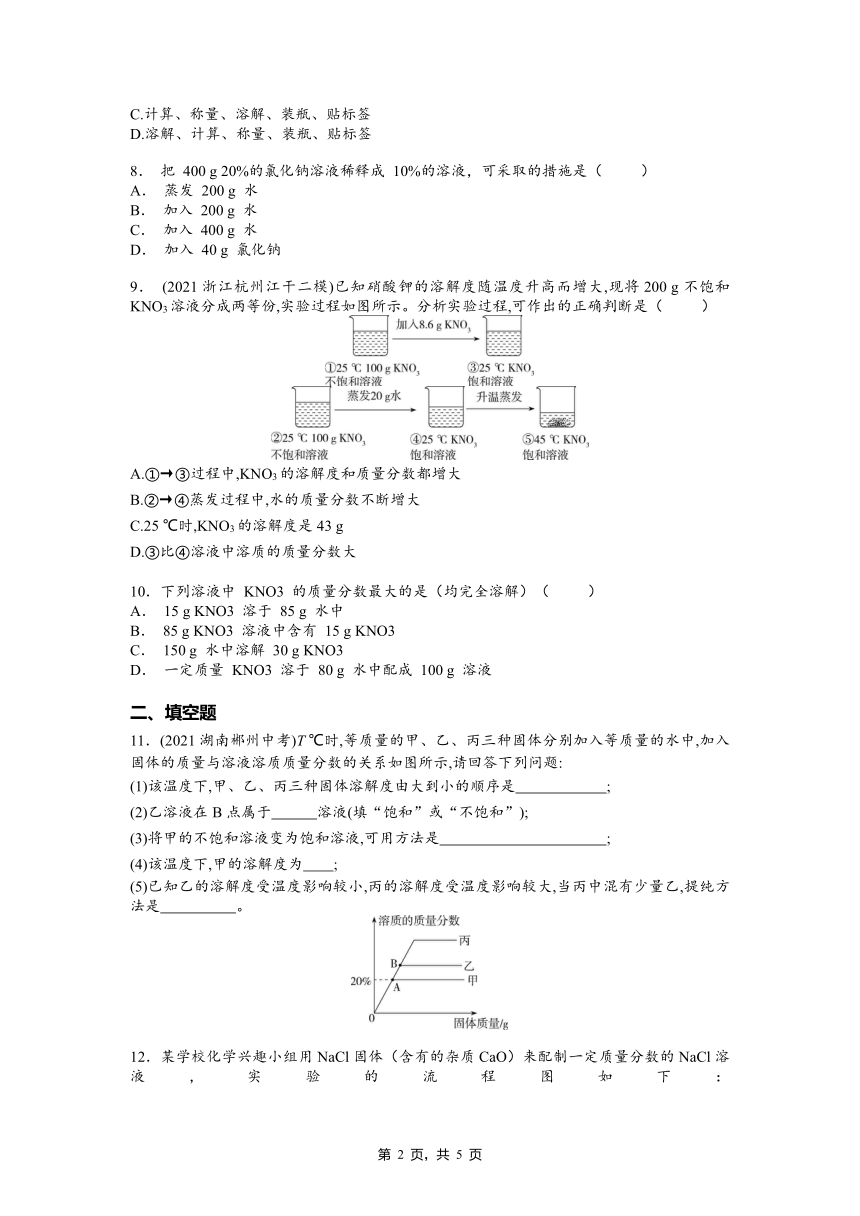
1. 如图是配制100g溶质质量分数为5%的氯化钠溶液的操作过程.以下说法错误的是( )
A.该实验操作顺序为③②④⑤①
B.称量时如果发现指针偏向右边,应向左盘添加氯化钠
C.配制该溶液需要称取5g氯化钠,量取100mL水
D操作①中玻璃棒的作用是搅拌,加速溶解
2. (2021·岳阳一模)如要将100 g溶质质量分数为20%的氯化钠溶液稀释成溶质质量分数为10%的氯化钠溶液,需加入水的质量为( )
A.50 g B.90 g
C.100 g D.200 g
3. 小兰同学配制50 g 5%的氯化钠溶液,取水时他是俯视读数的,这位同学配得的溶液质量分数( )
A.等于5% B.大于5%
C.小于5% D.无法判断
4. 向200 g溶质质量分数为10%的蔗糖溶液中加200 g水,搅拌后把所得溶液倒掉一半,剩余的溶液溶质质量分数为( )
A.10% B.5%
C.2.5% D.20%
5. 如图是某同体物质的溶解度曲线。则t2℃时,该物质的饱和溶液中溶质的质量分数为( )
A.20% B.l6.7%
C.30% D.23.1%
6. 将 40 g 98%的浓 H2SO4 配制成20% 的稀 H2SO4,需加水的质量为( )
A. 196 g B. 156 g C. 155.2 g D. 8.16 g
7. 要配制一定质量分数的氢氧化钠溶液,正确的操作步骤是( )
A.称量、溶解、计算、装瓶、贴标签
B.称量、计算、溶解、装瓶、贴标签
C.计算、称量、溶解、装瓶、贴标签
D.溶解、计算、称量、装瓶、贴标签
8. 把 400 g 20%的氯化钠溶液稀释成 10%的溶液,可采取的措施是( )
A. 蒸发 200 g 水
B. 加入 200 g 水
C. 加入 400 g 水
D. 加入 40 g 氯化钠
9. (2021浙江杭州江干二模)已知硝酸钾的溶解度随温度升高而增大,现将200 g不饱和KNO3溶液分成两等份,实验过程如图所示。分析实验过程,可作出的正确判断是( )
A.①→③过程中,KNO3的溶解度和质量分数都增大
B.②→④蒸发过程中,水的质量分数不断增大
C.25 ℃时,KNO3的溶解度是43 g
D.③比④溶液中溶质的质量分数大
10.下列溶液中 KNO3 的质量分数最大的是(均完全溶解)( )
A. 15 g KNO3 溶于 85 g 水中
B. 85 g KNO3 溶液中含有 15 g KNO3
C. 150 g 水中溶解 30 g KNO3
D. 一定质量 KNO3 溶于 80 g 水中配成 100 g 溶液
二、填空题
11.(2021湖南郴州中考)T ℃时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
(1)该温度下,甲、乙、丙三种固体溶解度由大到小的顺序是 ;
(2)乙溶液在B点属于 溶液(填“饱和”或“不饱和”);
(3)将甲的不饱和溶液变为饱和溶液,可用方法是 ;
(4)该温度下,甲的溶解度为 ;
(5)已知乙的溶解度受温度影响较小,丙的溶解度受温度影响较大,当丙中混有少量乙,提纯方法是 。
12.某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下:
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为________。
(2)操作2的名称是________,在溶液A中加入过量碳酸钠的目的是________。
(3)若要配制100 g质量分数为5.5%的氯化钠溶液,除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是________,其作用是________。
(4)如果配制后溶液溶质的质量分数低于5.5%,你认为可能的原因是________。(任写一个)
13.用5%的KNO3溶液配制150g溶质质量分数为2%的硝酸钾营养液,需要加水的质量是________g;用量筒量取水时,若读数时仰视,则导致配制溶液的质量分数________(天“偏大”或“偏小”);玻璃棒在配制过程中的作用是________。
14.(2021吉林长春二模)硝酸钾、氯化钾的溶解度曲线如图甲所示,回答下列问题:
甲
乙
(1)t1 ℃时硝酸钾的溶解度 氯化钾的溶解度(填“>”“<”或“=”);
(2)t2 ℃时,将60 g 氯化钾放入 g水中,完全溶解后,可得到恰好饱和的溶液;
(3)如图乙是有关硝酸钾溶液的实验操作及变化情况,下列说法正确的是 ;
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.若将等温度等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.若将等温度等质量的硝酸钾和氯化钾的饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
(4)用40%的硝酸钾溶液配制100 g 10%的硝酸钾溶液,需要加入水的体积是 。
15.溶解性是指________。物质的溶解性主要与________、________和________等因素有关。其中________被称为影响物质溶解性的外部因素;而________和________被称为影响溶解性的内部因素。
三、计算题
16.某化学活动小组需要用溶质质量分数为19.6%的稀硫酸和锌粒反应来制取氢气,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将50 g浓硫酸配制成所需的稀硫酸,需要水的质量为多少?
(2)取上述配制好的稀硫酸100 g与20 g铜锌合金恰好完全反应。求参加反应的锌的质量分数和反应生成的氢气质量?(反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑)
17.(2021云南昆明二模)将150 g稀盐酸分三次加入一定质量的铜锌合金中,所加入的稀盐酸与产生气体的质量关系如图所示,请分析计算:
(1)实验结束时,产生的氢气质量为 g。
(2)计算所用稀盐酸的溶质质量分数。(计算结果精确到0.1%)
2021-2022学年人教版初三化学下册第九单元课题3 溶液的浓度 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 C C B B D B C C C D
二、填空题
11. (1)丙>乙>甲 (2)饱和 (3)加入甲物质或蒸发溶剂 (4)25 g (5)降温结晶
12.(1)Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)过滤 充分除尽溶液中的氢氧化钙
(3)玻璃棒 搅拌加快食盐溶解速率
(4)用量筒量取水时错误,如取水时仰视读数、烧杯中有水
13.90 偏小 搅拌,使溶液混合均匀
14. (1)= (2)150 (3)ABD (4)75 mL
15.物质在溶剂里的溶解能力 溶质的性质 溶剂的性质 温度 温度 溶质的性质 溶剂的性质
三、计算题
16.(1)解:设需要加水的质量为x。
50g×98%=( 50g-x)×19.6% x=200 g
(2)解:设参加反应的锌的质量为y,生成氢气质量为m。
参加反应的硫酸质量=100g×19.6%=19.6克
Zn + H2SO4====ZnSO4 + H2↑
65 98 2
y 19.6 g m
65/98=y/19.6g y=13 g
98/2=19.6g/m m=0.4 g
所以参加反应的锌的质量分数=13 g/20 g*100%=65%
答:参加反应的锌的质量分数为65%,反应生成的氢气质量为0.4 g。
17. (1)0.4
(2)解:设100 g稀盐酸中溶质的质量为x。
Zn+2HClZnCl2+H2↑
73 2
x 0.4 g
= x=14.6 g
则所用稀盐酸的溶质质量分数为×100%=14.6%
答:所用稀盐酸的溶质质量分数为14.6%。
第 1 页,共 3 页
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
1. 如图是配制100g溶质质量分数为5%的氯化钠溶液的操作过程.以下说法错误的是( )
A.该实验操作顺序为③②④⑤①
B.称量时如果发现指针偏向右边,应向左盘添加氯化钠
C.配制该溶液需要称取5g氯化钠,量取100mL水
D操作①中玻璃棒的作用是搅拌,加速溶解
2. (2021·岳阳一模)如要将100 g溶质质量分数为20%的氯化钠溶液稀释成溶质质量分数为10%的氯化钠溶液,需加入水的质量为( )
A.50 g B.90 g
C.100 g D.200 g
3. 小兰同学配制50 g 5%的氯化钠溶液,取水时他是俯视读数的,这位同学配得的溶液质量分数( )
A.等于5% B.大于5%
C.小于5% D.无法判断
4. 向200 g溶质质量分数为10%的蔗糖溶液中加200 g水,搅拌后把所得溶液倒掉一半,剩余的溶液溶质质量分数为( )
A.10% B.5%
C.2.5% D.20%
5. 如图是某同体物质的溶解度曲线。则t2℃时,该物质的饱和溶液中溶质的质量分数为( )
A.20% B.l6.7%
C.30% D.23.1%
6. 将 40 g 98%的浓 H2SO4 配制成20% 的稀 H2SO4,需加水的质量为( )
A. 196 g B. 156 g C. 155.2 g D. 8.16 g
7. 要配制一定质量分数的氢氧化钠溶液,正确的操作步骤是( )
A.称量、溶解、计算、装瓶、贴标签
B.称量、计算、溶解、装瓶、贴标签
C.计算、称量、溶解、装瓶、贴标签
D.溶解、计算、称量、装瓶、贴标签
8. 把 400 g 20%的氯化钠溶液稀释成 10%的溶液,可采取的措施是( )
A. 蒸发 200 g 水
B. 加入 200 g 水
C. 加入 400 g 水
D. 加入 40 g 氯化钠
9. (2021浙江杭州江干二模)已知硝酸钾的溶解度随温度升高而增大,现将200 g不饱和KNO3溶液分成两等份,实验过程如图所示。分析实验过程,可作出的正确判断是( )
A.①→③过程中,KNO3的溶解度和质量分数都增大
B.②→④蒸发过程中,水的质量分数不断增大
C.25 ℃时,KNO3的溶解度是43 g
D.③比④溶液中溶质的质量分数大
10.下列溶液中 KNO3 的质量分数最大的是(均完全溶解)( )
A. 15 g KNO3 溶于 85 g 水中
B. 85 g KNO3 溶液中含有 15 g KNO3
C. 150 g 水中溶解 30 g KNO3
D. 一定质量 KNO3 溶于 80 g 水中配成 100 g 溶液
二、填空题
11.(2021湖南郴州中考)T ℃时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
(1)该温度下,甲、乙、丙三种固体溶解度由大到小的顺序是 ;
(2)乙溶液在B点属于 溶液(填“饱和”或“不饱和”);
(3)将甲的不饱和溶液变为饱和溶液,可用方法是 ;
(4)该温度下,甲的溶解度为 ;
(5)已知乙的溶解度受温度影响较小,丙的溶解度受温度影响较大,当丙中混有少量乙,提纯方法是 。
12.某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下:
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为________。
(2)操作2的名称是________,在溶液A中加入过量碳酸钠的目的是________。
(3)若要配制100 g质量分数为5.5%的氯化钠溶液,除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是________,其作用是________。
(4)如果配制后溶液溶质的质量分数低于5.5%,你认为可能的原因是________。(任写一个)
13.用5%的KNO3溶液配制150g溶质质量分数为2%的硝酸钾营养液,需要加水的质量是________g;用量筒量取水时,若读数时仰视,则导致配制溶液的质量分数________(天“偏大”或“偏小”);玻璃棒在配制过程中的作用是________。
14.(2021吉林长春二模)硝酸钾、氯化钾的溶解度曲线如图甲所示,回答下列问题:
甲
乙
(1)t1 ℃时硝酸钾的溶解度 氯化钾的溶解度(填“>”“<”或“=”);
(2)t2 ℃时,将60 g 氯化钾放入 g水中,完全溶解后,可得到恰好饱和的溶液;
(3)如图乙是有关硝酸钾溶液的实验操作及变化情况,下列说法正确的是 ;
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.若将等温度等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.若将等温度等质量的硝酸钾和氯化钾的饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
(4)用40%的硝酸钾溶液配制100 g 10%的硝酸钾溶液,需要加入水的体积是 。
15.溶解性是指________。物质的溶解性主要与________、________和________等因素有关。其中________被称为影响物质溶解性的外部因素;而________和________被称为影响溶解性的内部因素。
三、计算题
16.某化学活动小组需要用溶质质量分数为19.6%的稀硫酸和锌粒反应来制取氢气,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将50 g浓硫酸配制成所需的稀硫酸,需要水的质量为多少?
(2)取上述配制好的稀硫酸100 g与20 g铜锌合金恰好完全反应。求参加反应的锌的质量分数和反应生成的氢气质量?(反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑)
17.(2021云南昆明二模)将150 g稀盐酸分三次加入一定质量的铜锌合金中,所加入的稀盐酸与产生气体的质量关系如图所示,请分析计算:
(1)实验结束时,产生的氢气质量为 g。
(2)计算所用稀盐酸的溶质质量分数。(计算结果精确到0.1%)
2021-2022学年人教版初三化学下册第九单元课题3 溶液的浓度 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 C C B B D B C C C D
二、填空题
11. (1)丙>乙>甲 (2)饱和 (3)加入甲物质或蒸发溶剂 (4)25 g (5)降温结晶
12.(1)Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)过滤 充分除尽溶液中的氢氧化钙
(3)玻璃棒 搅拌加快食盐溶解速率
(4)用量筒量取水时错误,如取水时仰视读数、烧杯中有水
13.90 偏小 搅拌,使溶液混合均匀
14. (1)= (2)150 (3)ABD (4)75 mL
15.物质在溶剂里的溶解能力 溶质的性质 溶剂的性质 温度 温度 溶质的性质 溶剂的性质
三、计算题
16.(1)解:设需要加水的质量为x。
50g×98%=( 50g-x)×19.6% x=200 g
(2)解:设参加反应的锌的质量为y,生成氢气质量为m。
参加反应的硫酸质量=100g×19.6%=19.6克
Zn + H2SO4====ZnSO4 + H2↑
65 98 2
y 19.6 g m
65/98=y/19.6g y=13 g
98/2=19.6g/m m=0.4 g
所以参加反应的锌的质量分数=13 g/20 g*100%=65%
答:参加反应的锌的质量分数为65%,反应生成的氢气质量为0.4 g。
17. (1)0.4
(2)解:设100 g稀盐酸中溶质的质量为x。
Zn+2HClZnCl2+H2↑
73 2
x 0.4 g
= x=14.6 g
则所用稀盐酸的溶质质量分数为×100%=14.6%
答:所用稀盐酸的溶质质量分数为14.6%。
第 1 页,共 3 页
同课章节目录
