10.1金属与合金同步练习—2021_2022学年九年级化学京改版(2013)下册(word版 含解析)
文档属性
| 名称 | 10.1金属与合金同步练习—2021_2022学年九年级化学京改版(2013)下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 306.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-05 00:00:00 | ||
图片预览




文档简介
10.1金属与合金
一、选择题(共16题)
1.下列物质属于纯净物的是
A.石油 B.合金 C.煤 D.水银
2.相同条件下,下列金属中,导电性最好的是( )
A.铜 B.银 C.铝 D.钨
3.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:,下列说法错误的是
A.X的化学式是CO2 B.生成气体中可能含有一氧化碳
C.该不锈钢中还含有铁和碳 D.该不锈钢合金的硬度小于纯铁
4.下列有关事实的相关解释,错误的是
A.生铁和钢的机械性能不同—一含碳量不同
B.铁原子和铁离子化学性质不同—一最外层电子数不同
C.水和过氧化氢的化学性质不同—一组成元素种类不同
D.金刚石和石墨的硬度不同—一碳原子的空间排列方式不同
5.锌铬黄(ZnCrO4)可用于制防锈涂料,下列有关锌铬黄的说法正确的是
A.该物质是氧化物 B.其中铬元素的化合价为+6
C.含有一种金属元素 D.锌铬黄属于合金
6.哈尔滨地铁1号线是哈尔滨地铁“十线一环”规划中第一条动工的地铁,全长27.3公里,设25座车站,下列说法不正确的是( )
A.地铁车辆的外部装饰上,以冰的颜色为主色,以雪花点缀,与城市环境相融合
B.地铁运行时是电能转化为机械能
C.车体材料为铝合金,具有密度小、抗腐蚀等优点
D.铺设地铁的钢轨用的是不锈钢
7.芜湖工业发展迅速,奇瑞汽车、海螺集团、新兴铸管、鑫科材料等企业在国内外已具有一定影响,这些企业的以下产品中,不含金属材料的是
A.汽车 B.水泥 C.钢管 D.铜缆
8.下列有关金属性质的比较,正确的是 。
A.导电性:银>铜
B.密度:铁>铅
C.熔点:锡>钨
D.硬度:铅>铬
9.下列有关合金的说法中,错误的是( )
A.钢是一种化合物 B.黄铜的硬度比纯铜的硬度大
C.生铁是一种铁的合金 D.焊锡的熔点比纯锡的熔点低
10.下列物质性质或现象描述错误的是( )
A.合金的硬度比组成它们的纯金属的硬度小 B.消防队员用水降低可燃物的温度来灭火
C.极易与血红蛋白结合的有毒气体是一氧化碳 D.硫在氧气中燃烧产生明亮的蓝紫色火焰
11.下列有关物质性质和用途的说法错误的是( )
A.氮气化学性质稳定,可作保护气
B.生石灰能吸收水分,可作食品干燥剂
C.金刚石硬度大,可作钻探机钻头
D.武德合金熔点高,可用作保险丝
12.按一定的特点或规律对物质进行分类是学习化学的重要方法之一。下列各组物质分类不正确的是( )
A.合金:不锈钢、铜片、保险丝 B.单质:C60、金刚石、水银
C.可燃物:天然气、酒精、一氧化碳 D.清洁能源:太阳能、氢能、风能
13.归纳法是一种重要的学习方法,可将零碎的知识系统化,下列归纳都正确的是
A.化学与生活 B.化学与材料
1、制糖工业中利用活性炭脱色制白糖 2、衣服上的油污用洗涤剂和汽油都能除去,其去污原理是一样的 1、涤纶衣服的优点是吸湿透气性好 2、Fe2O3、CuO属于合金
C.化学与安全 D.化学与环保
1、点燃可燃性气体前,一定要验纯 2、煤矿井中一定要通风,严禁烟火 1、为防止温室效应推广使用脱硫煤 2、废旧电池可以随手丢弃
A.A B.B C.C D.D
14.物质的性质决定了用途,下列物质的用途仅与其物理性质有关的是
A.二氧化碳用于灭火 B.木炭用作燃料
C.铜用作导线 D.稀有气体作保护气
15.中华古代文化蕴含着丰富的化学知识,下面理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即钢)柔锡柔,合两柔则刚 合金的熔点比组成它的纯金属高
D 一尺之棰,日取其半,万世不竭 蕴含着物质无限可分的思想
A.A B.B C.C D.D
16.南京大学课题组研制出ZnGa2O4催化材料,实现将CO2转化为碳氢化合物燃料。下列有关ZnGa2O4的说法正确的是
A.属于金属材料 B.含有2个氧分子
C.对碳循环利用有积极意义 D.Ga、O元素质量比为1:2
二、综合题(共6题)
17.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属为例,请你参与其中回答相关问题:
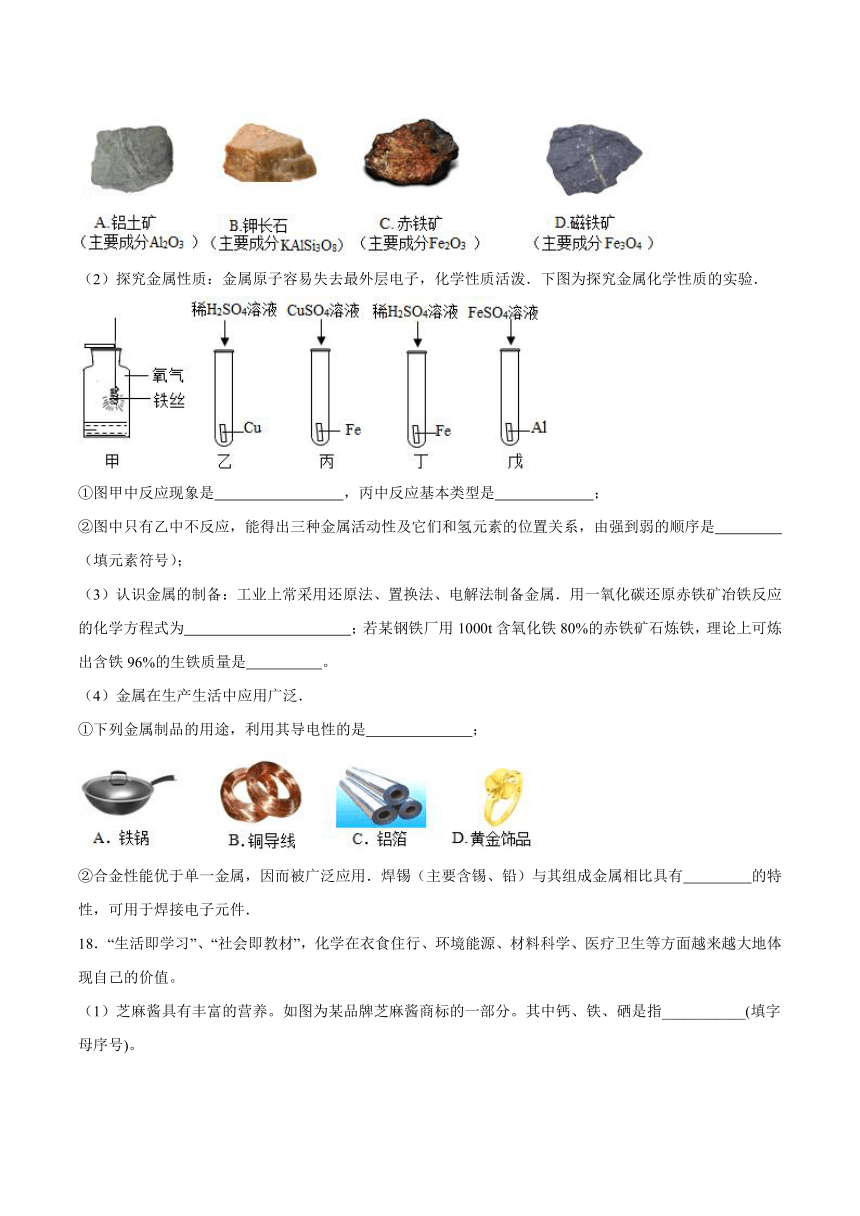
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是 (填字母序号,下同);
(2)探究金属性质:金属原子容易失去最外层电子,化学性质活泼.下图为探究金属化学性质的实验.
①图甲中反应现象是 ,丙中反应基本类型是 ;
②图中只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,由强到弱的顺序是 (填元素符号);
(3)认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.用一氧化碳还原赤铁矿冶铁反应的化学方程式为 ;若某钢铁厂用1000t含氧化铁80%的赤铁矿石炼铁,理论上可炼出含铁96%的生铁质量是 。
(4)金属在生产生活中应用广泛.
①下列金属制品的用途,利用其导电性的是 ;
②合金性能优于单一金属,因而被广泛应用.焊锡(主要含锡、铅)与其组成金属相比具有 的特性,可用于焊接电子元件.
18.“生活即学习”、“社会即教材”,化学在衣食住行、环境能源、材料科学、医疗卫生等方面越来越大地体现自己的价值。
(1)芝麻酱具有丰富的营养。如图为某品牌芝麻酱商标的一部分。其中钙、铁、硒是指___________(填字母序号)。
A.分子 B.原子 C.单质 D.元素
(2)废电池中铅、镉、汞等重金属对土壤和水源的污染非常严重,小芳从废干电池中回收有关物质并进行探究。
①她将上图电池中各物质进行分类,其中可回收的金属材料是___________。(写一例即可)
②提取二氧化锰:除去二氧化锰中的少量碳粉(少量碳粉与二氧化锰不反应),可采用的方法是___________。
(3)制备高纯硅和二氧化硅主要工艺流程如下图所示。
(Ⅰ)反应①的化学方程式为:,从氧化还原反应角度分析,C发生了___________反应。
(Ⅱ)用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为___________。
19.对金属材料的研究,在人类发展的历史长河中骑着非常重要的作用。
(1)金属的应用
①用铁锅炒菜主要利用铁具有良好的_________性。
②做门窗常用铝合金而不用纯铝,是因为_________。
(2)金属的获得。
一定条件下,金属化合物与一些具有还原性的物质发生反应。
化学兴趣小组的同学模仿工业高炉炼铁原理,在如图1所示装置中用CO还原CuO制取金属Cu。
①装置中气球的作用是_________。
②实验开始前,需要先通过一段时间CO,然后开始加热,先通CO的目的是_________,当观察到_________现象,说明CO与CuO已经发生反应。澄清石灰水的作用是_________(用化学方程式表示)。
③为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图2所示(该图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同),据图回答下列问题:
a.400℃时,反应的固体产物中含有Cu和_________。
b.500℃时,该反应的化学方程式为_________。
c.用CO还原CuO制取纯净的Cu,反应温度至少要控制在_________℃以上。
20.2017年5月,国产大飞机C919成功进行首次试飞.请回答下列问题:
(1)图1中标示的材料中,属于有机合成材料的是 _____ ;
(2)飞机机身大量使用了铝合金材料.铝合金具有硬度大、密度小和 _____ 等优点;
(3)以金红石(主要成分是TiO2)为原料生产钛的流程如图2:其中“反应I”需要在高温条件下进行,反应的化学方程式为 _____ ;“反应II”中使用氩气的目的是 _____ ,该反应的基本反应类型属于 _____ 反应;
(4)现代民用飞机上使用的氧气发生器以氯酸钠为产氧剂,氯酸钠(NaClO3)中氯元素的化合价为 _____ ;
(5)C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能使燃油消耗减少16%.使用高密度空气的原因是 _____ .
21.依据所学知识回答问题
(1)网购、高铁、共享单车和打码支付被称为中国“新四大发明”。
①网购离不开光纤宽带。光纤的主要成分是SiO2,其中Si的化合价是_______。
②高铁车体的外壳由铝合金制成,用铝合金制作外壳的优点是_______(答一条)。
③共享单车的轮胎为实体轮胎,而普通自行车的轮胎在夏天易爆胎请用分子观点解释“夏天易爆胎”的原因_______。
④许多商品的二维码印在PVC不干胶贴纸上,PVC(化学式(C2H3C1)n)中碳、氢元素的质量比是_。
(2)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如下:
(其中,表示钠原子,表示氯原子, 表示氧原子)请回答题:
①A物质中氯元素的化合价为_______。
②D物质的名称是_______。
③该反应的化学方程式是_______。
22.已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.D
【详解】
A、石油中含有多种碳氢化合物,是混合物;
B、合金是金属中加热融合其它金属或非金属形成的具有金属特性的混合物;
C、煤中含有多种成分,是混合物;
D、水银是汞的俗称,是由一种物质组成的,是纯净物。
故选:D。
2.B
【详解】
导电、导热性最好的金属是银。
故选B。
3.D
【详解】
A、根据,反应前碳原子为1个,Ni原子为2个,氧原子为2个,反应后Ni原子为2个,则X为CO2,故选项说法正确。
B、碳过量时,二氧化碳能与碳在高温下反应生成一氧化碳,气体产物中可能有CO,故选项说法正确。
C、钢中含有碳,该不锈钢中还含有铁和碳,故选项说法正确。
D、一般合金的硬度大于其组成中纯金属的硬度,因此该不锈钢的硬度大于纯铁,故选项说法错误。
故选:D。
4.C
【详解】
A、生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁和钢的机械性能不同是因为含碳量不同,A正确,不符合题意;
B、最外层电子数不同,化学性质不同,铁原子和铁离子化学性质不同也是这个原因,B正确,不符合题意;
C、水(H2O)和过氧化氢(H2O2)都是由氢、氧元素组成的,二者化学性质不同是因为分子构成不同,不同种分子化学性质不同,C错误,符合题意;
D、金刚石和石墨的硬度不同是因为碳原子的空间排列方式不同,D正确,不符合题意;
故选:C。
5.B
【详解】
A、锌铬黄(化学式为ZnCrO4)是由锌、铬、氧三种元素组成的化合物,不属于氧化物,故A错误;
B、锌元素显+2,氧元素显-2,设:铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可知锌铬黄(化学式为ZnCrO4)中铭元素的化合价:(+2)+x+(-2)×4=0,则x=+6,故B正确;
C、根据锌铬黄(ZnCrO4)化学式可知,锌铬黄含有锌和铬两种金属元素,故C错误;
D、根据锌铬黄(ZnCrO4)化学式可知,锌铬黄属于化合物,不属于合金,故D错误。故选B。
6.D
【详解】
A、地铁车辆的外部装饰上,以冰的颜色为主色,以雪花点缀,与城市环境相融合,故A正确;
B、地铁列车是电力牵引的电动列车,其动力是电能,运行时是电能转化为机械能,故B正确;
C、车体材料为铝合金,具有密度小、抗腐蚀等优点,故C正确;
D、地铺设地铁的钢轨一般是用高锰钢,不是不锈钢,故D不正确。故选D。
7.B
【详解】
A、汽车、钢管、铜缆都含有金属材料,而水泥属于无机非金属材料;
故选B.
8.A
【详解】
A、导电性:银>铜;故选项正确;
B、密度:铁<铅;故选项错误;
C、熔点:锡<钨;故选项错误;
D、硬度:铅<铬;故选项错误;
故选:A。
9.A
【详解】
A.钢是铁合金,属于混合物,错误;
B.黄铜是铜合金,其硬度大于纯铜,正确;
C.生铁是铁合金,正确;
D.焊锡是锡合金,其熔点比纯锡的低,正确。故选A。
10.A
【详解】
A、合金的硬度比组成它们的纯金属的硬度大,选项错误;B、消防队员用水降低可燃物的温度,使温度降到可燃物着火点以下达到灭火的目的,选项正确;C、一氧化碳与血红蛋白结合的能力非常强,导致氧气无法再与血红蛋白结合,最终缺氧而亡,选项正确;D、硫在氧气中燃烧产生明亮的蓝紫色火焰,选项正确。故本题选A。
11.D
【详解】
A、氮气的化学性质稳定,可用作保护气,此选项正确;
B、生石灰能吸收水分,可作食品干燥剂,此选项正确;
C、金刚石硬度很大,可作钻探机钻头,此选项正确;
D、武德合金熔点低,可用作保险丝,此选项错误。 故选D。
12.A
【详解】
A. 不锈钢是铁的合金,铜片是金属单质,保险丝是一种合金,此选项错误;
B. 由同种元素组成的纯净物是单质,C60、金刚石的是碳的单质,水银是汞的俗称,是一种单质,此选项正确;
C. 天然气、酒精、一氧化碳都具有可燃性,是可燃物,此选项正确;
D. 太阳能、氢能、风能无污染,是清洁能源,此选项正确。故选A。
13.C
【详解】
A、制糖工业中可以利用活性炭脱色制白糖;洗涤剂对油污有乳化作用,汽油能溶解油污,所以衣服上的油污用洗涤剂和汽油都能除去,但去污原理是不一样的,故选项错误;
B、涤纶衣服的优点是耐磨、有弹性,但吸湿透气性差;合金属于混合物,而Fe2O3、CuO是纯净物,不属于合金,故选项错误;
C、点燃可燃性气体前,一定要验纯,以防气体不纯点燃时发生爆炸;煤矿井中存在着可燃性气体,一定要通风,严禁烟火,以防发生爆炸,故选项正确;
D、脱硫煤燃烧也会生成大量的二氧化碳气体,所以推广使用脱硫煤不能防止温室效应;废旧电池中含有有毒的重金属,所以废旧电池随手丢弃会造成土壤污染和水体污染,故选项错误。
故选C
14.C
【详解】
A. 二氧化碳用于灭火,利用不可燃、不助燃的化学性质和密度比空气的大的物理性质,选项错误;
B. 木炭用作燃料利用了木条能燃烧的化学性质,选项错误;
C. 铜用作导线利用了铜有良好的导电性的物理性质,选项正确;
D. 稀有气体作保护气利用了氮气的化学性质稳定,选项错误。故选C。
15.C
【详解】
A物理变化和化学变化的根本区别在于是否有新物质生成,如果有新物质生成,则属于化学变化; 反之,则是物理变化。露从今夜白,描述的是水的状态的变化,是物理变化。B、“墟里烟”描述的是物质燃烧,是化学变化;C、金(即钢)柔锡柔,合两柔则刚 说明合金的硬度比组成它的纯金属大;D、宏观物质是由微观粒子构成,因此物质可以分成构成物质的微粒。即无限可分。选C
16.C
【解析】A、金属材料包括纯金属及它们的合金,ZnGa2O4属于化合物,错误;B、一个ZnGa2O4分子中含有4个氧原子,错误;C、ZnGa2O4作催化剂,将CO2转化为碳氢化合物,对碳循环利用有积极意义,正确;D、ZnGa2O4中Ga、O元素质量比为(70×2):(16×4)=35:16,错误。故选C。
17.(1)ACD;
(2)① 剧烈燃烧,火星四溅,生成黑色固体 , 置换反应;② Al Fe H Cu ;
(3)化学方程式 略 ;生铁质量是 583t (此空2分)。
(4)①B ;②熔点低.
【详解】
试题分析:(1)由二种元素组成其中一种元素是氧元素的化合物为氧化物,因此由其主要成分的化学式可得Al2O3、Fe2O3、Fe3O4属于氧化物,因此选ACD;
(2) ① 铁丝在氧气中剧烈燃烧,火星四溅,生成黑色固体 ,丙为Fe + CuSO4 ="=" FeSO4 + Cu,一种单质和一种化合物反应生成另一种单质和化合物,属于置换反应 ;②活动性强的能将活动性弱的置换出来,因此乙不反应可得H>Cu,丙能反应可得Fe>Cu;丁能反应可得Fe>H;戊能反应可得Al>Fe,综合可得Al>Fe>H>Cu;
(3) 为一氧化碳还原氧化铁3CO+ Fe2O32Fe + 3CO2;设理论上可以炼出含铁96%的生铁的质量为x.
Fe2O3+3CO2Fe+3CO2
160 112
1000t×80% 96%x
160/112=1000t×80%/96%x,x=583t
答:理论上可以炼出含铁96%的生铁的质量为583t.
(4)①作导线是利用其导电性,因此选B;②焊锡是利用合金的熔点比成分金属低
18.
(1)D
(2) 铜或锌 在空气中加热
(3) 氧化
【解析】
(1)
芝麻酱中的钙、铁、硒不是以单质、分子、原子等形式存在的,而是指元素,因此图中钙、铁、硒是指元素,故选D;
(2)
二氧化锰是由锰、氧两种元素组成的化合物,属于氧化物.塑料膜是人工合成的含有有机物的材料,锌、铜属于金属材料,故其中可回收的金属材料是铜和锌,故填:铜或锌;在空气中加热使碳与空气中的氧气反应生成二氧化碳,可以除去二氧化锰中的碳,故填:在空气中加热
(3)
反应①中的C被氧化为CO,C发生了氧化反应,故填:氧化;根据质量守恒定律,化学反应前后,元素种类不变,且这种物质是此工艺流程中可循环使用的物质,那么推断这种物质是氯气,因此反应的化学方程式为:。
19.导热 铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好 收集一氧化碳,尾气处理 排净装置内空气,防止发生爆炸 黑色固体变为红色,澄清石灰水变浑浊 Ca(OH)2+CO2=CaCO3↓+H2O CuO、Cu2O CO+CuOCu+CO2 500
【详解】
(1)①用铁锅炒菜主要利用铁具有良好的导热性,故填:导热。
②做门窗常用铝合金而不用纯铝,是因为铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好,故填:铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好。
(2)①装置中气球的作用是收集一氧化碳,尾气处理,故填:收集一氧化碳,尾气处理。
②实验开始前,需要先通过一段时间CO,然后开始加热,先通CO的目的是排净装置内空气,防止发生爆炸,当观察到黑色固体变为红色,澄清石灰水变浑浊现象,说明CO与CuO已经发生反应。澄清石灰水的作用是检验二氧化碳,发生的反应Ca(OH)2+CO2=CaCO3↓+H2O,故填:排净装置内空气,防止发生爆炸;排净装置内空气,防止发生爆炸;Ca(OH)2+CO2=CaCO3↓+H2O。
③a、由图可知,400℃时,反应的固体产物中含有Cu和CuO、Cu2O,故填:CuO、Cu2O。
b、由图可知,500℃时,该反应固体全部为Cu,化学方程式为CO+CuOCu+CO2,故填:CO+CuOCu+CO2。
c、由图可知500℃时,该反应固体全部为Cu,用CO还原CuO制取纯净的Cu,反应温度至少要控制在500℃以上,故填:500。
20.合成橡胶 抗腐蚀性好 TiO2+2C+2Cl2TiCl4+2CO 作保护气防止金属氧化 置换反应 +5 提供足够的氧气,使燃油燃烧更充分
【详解】
(1)图中标示的材料中,合成橡胶属于有机合成材料;故填:合成橡胶;
(2)合金与组成它的成分相比较,一般情况下是密度小、硬度大、抗腐蚀性好,故答案为抗腐蚀性好;
(3)在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体是一氧化碳,反应的化学方程式为:TiO2+2C+2Cl2TiCl4+2CO; Mg容易被氧气氧化,使用氩气防止镁被氧化;在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,属于置换反应;故答案为TiO2+2C+2Cl2TiCl4+2CO;作保护气防止金属氧化;置换反应;
(4)设NaClO3中氯元素的化合价为x,由于钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合价的代数和为零可得(+1)+x+(-2×3)=0,解得x=+5,故答案为+5;
(5)高密度空气能使航空煤油更充分燃烧的微观原因是高密度空气中的氧分子与煤油分子接触更充分,使燃油燃烧更充分;故答案为供足够的氧气,使燃油燃烧更充分。
21.
(1) +4 密度小 温度升高,分子间的间隔变大,体积膨胀 8:1
(2) +3 二氧化氯
【分析】
(1)
根据各元素的化合价的代数和为零,SiO2中氧元素的化合价为-2价,所以Si的化合价是+4价;
铝合金具有密度小,机械强度大 、抗腐蚀性强等优点;
夏天易爆胎”的原因是温度升高,分子运动剧烈,分子间的间隙增大,气体的体积膨胀;
PVC【化学式(C2H3C1)n】中碳、氢元素的质量比是
故填:+4;密度小;温度升高,分子间的间隔变大,体积膨胀;8:1
(2)
由微观示意图可知该反应方程式为:,所以A为NaClO2中钠元素的化合价为+1价,氧元素的化合价为-2价,根据元素的化合价的代数和为零,所以物质中氯元素的化合价为+3价;
D为ClO2,名称为二氧化氯;
该反应的化学方程式是:
故填:+3;二氧化氯;
22.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
一、选择题(共16题)
1.下列物质属于纯净物的是
A.石油 B.合金 C.煤 D.水银
2.相同条件下,下列金属中,导电性最好的是( )
A.铜 B.银 C.铝 D.钨
3.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:,下列说法错误的是
A.X的化学式是CO2 B.生成气体中可能含有一氧化碳
C.该不锈钢中还含有铁和碳 D.该不锈钢合金的硬度小于纯铁
4.下列有关事实的相关解释,错误的是
A.生铁和钢的机械性能不同—一含碳量不同
B.铁原子和铁离子化学性质不同—一最外层电子数不同
C.水和过氧化氢的化学性质不同—一组成元素种类不同
D.金刚石和石墨的硬度不同—一碳原子的空间排列方式不同
5.锌铬黄(ZnCrO4)可用于制防锈涂料,下列有关锌铬黄的说法正确的是
A.该物质是氧化物 B.其中铬元素的化合价为+6
C.含有一种金属元素 D.锌铬黄属于合金
6.哈尔滨地铁1号线是哈尔滨地铁“十线一环”规划中第一条动工的地铁,全长27.3公里,设25座车站,下列说法不正确的是( )
A.地铁车辆的外部装饰上,以冰的颜色为主色,以雪花点缀,与城市环境相融合
B.地铁运行时是电能转化为机械能
C.车体材料为铝合金,具有密度小、抗腐蚀等优点
D.铺设地铁的钢轨用的是不锈钢
7.芜湖工业发展迅速,奇瑞汽车、海螺集团、新兴铸管、鑫科材料等企业在国内外已具有一定影响,这些企业的以下产品中,不含金属材料的是
A.汽车 B.水泥 C.钢管 D.铜缆
8.下列有关金属性质的比较,正确的是 。
A.导电性:银>铜
B.密度:铁>铅
C.熔点:锡>钨
D.硬度:铅>铬
9.下列有关合金的说法中,错误的是( )
A.钢是一种化合物 B.黄铜的硬度比纯铜的硬度大
C.生铁是一种铁的合金 D.焊锡的熔点比纯锡的熔点低
10.下列物质性质或现象描述错误的是( )
A.合金的硬度比组成它们的纯金属的硬度小 B.消防队员用水降低可燃物的温度来灭火
C.极易与血红蛋白结合的有毒气体是一氧化碳 D.硫在氧气中燃烧产生明亮的蓝紫色火焰
11.下列有关物质性质和用途的说法错误的是( )
A.氮气化学性质稳定,可作保护气
B.生石灰能吸收水分,可作食品干燥剂
C.金刚石硬度大,可作钻探机钻头
D.武德合金熔点高,可用作保险丝
12.按一定的特点或规律对物质进行分类是学习化学的重要方法之一。下列各组物质分类不正确的是( )
A.合金:不锈钢、铜片、保险丝 B.单质:C60、金刚石、水银
C.可燃物:天然气、酒精、一氧化碳 D.清洁能源:太阳能、氢能、风能
13.归纳法是一种重要的学习方法,可将零碎的知识系统化,下列归纳都正确的是
A.化学与生活 B.化学与材料
1、制糖工业中利用活性炭脱色制白糖 2、衣服上的油污用洗涤剂和汽油都能除去,其去污原理是一样的 1、涤纶衣服的优点是吸湿透气性好 2、Fe2O3、CuO属于合金
C.化学与安全 D.化学与环保
1、点燃可燃性气体前,一定要验纯 2、煤矿井中一定要通风,严禁烟火 1、为防止温室效应推广使用脱硫煤 2、废旧电池可以随手丢弃
A.A B.B C.C D.D
14.物质的性质决定了用途,下列物质的用途仅与其物理性质有关的是
A.二氧化碳用于灭火 B.木炭用作燃料
C.铜用作导线 D.稀有气体作保护气
15.中华古代文化蕴含着丰富的化学知识,下面理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即钢)柔锡柔,合两柔则刚 合金的熔点比组成它的纯金属高
D 一尺之棰,日取其半,万世不竭 蕴含着物质无限可分的思想
A.A B.B C.C D.D
16.南京大学课题组研制出ZnGa2O4催化材料,实现将CO2转化为碳氢化合物燃料。下列有关ZnGa2O4的说法正确的是
A.属于金属材料 B.含有2个氧分子
C.对碳循环利用有积极意义 D.Ga、O元素质量比为1:2
二、综合题(共6题)
17.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是 (填字母序号,下同);
(2)探究金属性质:金属原子容易失去最外层电子,化学性质活泼.下图为探究金属化学性质的实验.
①图甲中反应现象是 ,丙中反应基本类型是 ;
②图中只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,由强到弱的顺序是 (填元素符号);
(3)认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.用一氧化碳还原赤铁矿冶铁反应的化学方程式为 ;若某钢铁厂用1000t含氧化铁80%的赤铁矿石炼铁,理论上可炼出含铁96%的生铁质量是 。
(4)金属在生产生活中应用广泛.
①下列金属制品的用途,利用其导电性的是 ;
②合金性能优于单一金属,因而被广泛应用.焊锡(主要含锡、铅)与其组成金属相比具有 的特性,可用于焊接电子元件.
18.“生活即学习”、“社会即教材”,化学在衣食住行、环境能源、材料科学、医疗卫生等方面越来越大地体现自己的价值。
(1)芝麻酱具有丰富的营养。如图为某品牌芝麻酱商标的一部分。其中钙、铁、硒是指___________(填字母序号)。
A.分子 B.原子 C.单质 D.元素
(2)废电池中铅、镉、汞等重金属对土壤和水源的污染非常严重,小芳从废干电池中回收有关物质并进行探究。
①她将上图电池中各物质进行分类,其中可回收的金属材料是___________。(写一例即可)
②提取二氧化锰:除去二氧化锰中的少量碳粉(少量碳粉与二氧化锰不反应),可采用的方法是___________。
(3)制备高纯硅和二氧化硅主要工艺流程如下图所示。
(Ⅰ)反应①的化学方程式为:,从氧化还原反应角度分析,C发生了___________反应。
(Ⅱ)用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为___________。
19.对金属材料的研究,在人类发展的历史长河中骑着非常重要的作用。
(1)金属的应用
①用铁锅炒菜主要利用铁具有良好的_________性。
②做门窗常用铝合金而不用纯铝,是因为_________。
(2)金属的获得。
一定条件下,金属化合物与一些具有还原性的物质发生反应。
化学兴趣小组的同学模仿工业高炉炼铁原理,在如图1所示装置中用CO还原CuO制取金属Cu。
①装置中气球的作用是_________。
②实验开始前,需要先通过一段时间CO,然后开始加热,先通CO的目的是_________,当观察到_________现象,说明CO与CuO已经发生反应。澄清石灰水的作用是_________(用化学方程式表示)。
③为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图2所示(该图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同),据图回答下列问题:
a.400℃时,反应的固体产物中含有Cu和_________。
b.500℃时,该反应的化学方程式为_________。
c.用CO还原CuO制取纯净的Cu,反应温度至少要控制在_________℃以上。
20.2017年5月,国产大飞机C919成功进行首次试飞.请回答下列问题:
(1)图1中标示的材料中,属于有机合成材料的是 _____ ;
(2)飞机机身大量使用了铝合金材料.铝合金具有硬度大、密度小和 _____ 等优点;
(3)以金红石(主要成分是TiO2)为原料生产钛的流程如图2:其中“反应I”需要在高温条件下进行,反应的化学方程式为 _____ ;“反应II”中使用氩气的目的是 _____ ,该反应的基本反应类型属于 _____ 反应;
(4)现代民用飞机上使用的氧气发生器以氯酸钠为产氧剂,氯酸钠(NaClO3)中氯元素的化合价为 _____ ;
(5)C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能使燃油消耗减少16%.使用高密度空气的原因是 _____ .
21.依据所学知识回答问题
(1)网购、高铁、共享单车和打码支付被称为中国“新四大发明”。
①网购离不开光纤宽带。光纤的主要成分是SiO2,其中Si的化合价是_______。
②高铁车体的外壳由铝合金制成,用铝合金制作外壳的优点是_______(答一条)。
③共享单车的轮胎为实体轮胎,而普通自行车的轮胎在夏天易爆胎请用分子观点解释“夏天易爆胎”的原因_______。
④许多商品的二维码印在PVC不干胶贴纸上,PVC(化学式(C2H3C1)n)中碳、氢元素的质量比是_。
(2)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如下:
(其中,表示钠原子,表示氯原子, 表示氧原子)请回答题:
①A物质中氯元素的化合价为_______。
②D物质的名称是_______。
③该反应的化学方程式是_______。
22.已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.D
【详解】
A、石油中含有多种碳氢化合物,是混合物;
B、合金是金属中加热融合其它金属或非金属形成的具有金属特性的混合物;
C、煤中含有多种成分,是混合物;
D、水银是汞的俗称,是由一种物质组成的,是纯净物。
故选:D。
2.B
【详解】
导电、导热性最好的金属是银。
故选B。
3.D
【详解】
A、根据,反应前碳原子为1个,Ni原子为2个,氧原子为2个,反应后Ni原子为2个,则X为CO2,故选项说法正确。
B、碳过量时,二氧化碳能与碳在高温下反应生成一氧化碳,气体产物中可能有CO,故选项说法正确。
C、钢中含有碳,该不锈钢中还含有铁和碳,故选项说法正确。
D、一般合金的硬度大于其组成中纯金属的硬度,因此该不锈钢的硬度大于纯铁,故选项说法错误。
故选:D。
4.C
【详解】
A、生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁和钢的机械性能不同是因为含碳量不同,A正确,不符合题意;
B、最外层电子数不同,化学性质不同,铁原子和铁离子化学性质不同也是这个原因,B正确,不符合题意;
C、水(H2O)和过氧化氢(H2O2)都是由氢、氧元素组成的,二者化学性质不同是因为分子构成不同,不同种分子化学性质不同,C错误,符合题意;
D、金刚石和石墨的硬度不同是因为碳原子的空间排列方式不同,D正确,不符合题意;
故选:C。
5.B
【详解】
A、锌铬黄(化学式为ZnCrO4)是由锌、铬、氧三种元素组成的化合物,不属于氧化物,故A错误;
B、锌元素显+2,氧元素显-2,设:铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可知锌铬黄(化学式为ZnCrO4)中铭元素的化合价:(+2)+x+(-2)×4=0,则x=+6,故B正确;
C、根据锌铬黄(ZnCrO4)化学式可知,锌铬黄含有锌和铬两种金属元素,故C错误;
D、根据锌铬黄(ZnCrO4)化学式可知,锌铬黄属于化合物,不属于合金,故D错误。故选B。
6.D
【详解】
A、地铁车辆的外部装饰上,以冰的颜色为主色,以雪花点缀,与城市环境相融合,故A正确;
B、地铁列车是电力牵引的电动列车,其动力是电能,运行时是电能转化为机械能,故B正确;
C、车体材料为铝合金,具有密度小、抗腐蚀等优点,故C正确;
D、地铺设地铁的钢轨一般是用高锰钢,不是不锈钢,故D不正确。故选D。
7.B
【详解】
A、汽车、钢管、铜缆都含有金属材料,而水泥属于无机非金属材料;
故选B.
8.A
【详解】
A、导电性:银>铜;故选项正确;
B、密度:铁<铅;故选项错误;
C、熔点:锡<钨;故选项错误;
D、硬度:铅<铬;故选项错误;
故选:A。
9.A
【详解】
A.钢是铁合金,属于混合物,错误;
B.黄铜是铜合金,其硬度大于纯铜,正确;
C.生铁是铁合金,正确;
D.焊锡是锡合金,其熔点比纯锡的低,正确。故选A。
10.A
【详解】
A、合金的硬度比组成它们的纯金属的硬度大,选项错误;B、消防队员用水降低可燃物的温度,使温度降到可燃物着火点以下达到灭火的目的,选项正确;C、一氧化碳与血红蛋白结合的能力非常强,导致氧气无法再与血红蛋白结合,最终缺氧而亡,选项正确;D、硫在氧气中燃烧产生明亮的蓝紫色火焰,选项正确。故本题选A。
11.D
【详解】
A、氮气的化学性质稳定,可用作保护气,此选项正确;
B、生石灰能吸收水分,可作食品干燥剂,此选项正确;
C、金刚石硬度很大,可作钻探机钻头,此选项正确;
D、武德合金熔点低,可用作保险丝,此选项错误。 故选D。
12.A
【详解】
A. 不锈钢是铁的合金,铜片是金属单质,保险丝是一种合金,此选项错误;
B. 由同种元素组成的纯净物是单质,C60、金刚石的是碳的单质,水银是汞的俗称,是一种单质,此选项正确;
C. 天然气、酒精、一氧化碳都具有可燃性,是可燃物,此选项正确;
D. 太阳能、氢能、风能无污染,是清洁能源,此选项正确。故选A。
13.C
【详解】
A、制糖工业中可以利用活性炭脱色制白糖;洗涤剂对油污有乳化作用,汽油能溶解油污,所以衣服上的油污用洗涤剂和汽油都能除去,但去污原理是不一样的,故选项错误;
B、涤纶衣服的优点是耐磨、有弹性,但吸湿透气性差;合金属于混合物,而Fe2O3、CuO是纯净物,不属于合金,故选项错误;
C、点燃可燃性气体前,一定要验纯,以防气体不纯点燃时发生爆炸;煤矿井中存在着可燃性气体,一定要通风,严禁烟火,以防发生爆炸,故选项正确;
D、脱硫煤燃烧也会生成大量的二氧化碳气体,所以推广使用脱硫煤不能防止温室效应;废旧电池中含有有毒的重金属,所以废旧电池随手丢弃会造成土壤污染和水体污染,故选项错误。
故选C
14.C
【详解】
A. 二氧化碳用于灭火,利用不可燃、不助燃的化学性质和密度比空气的大的物理性质,选项错误;
B. 木炭用作燃料利用了木条能燃烧的化学性质,选项错误;
C. 铜用作导线利用了铜有良好的导电性的物理性质,选项正确;
D. 稀有气体作保护气利用了氮气的化学性质稳定,选项错误。故选C。
15.C
【详解】
A物理变化和化学变化的根本区别在于是否有新物质生成,如果有新物质生成,则属于化学变化; 反之,则是物理变化。露从今夜白,描述的是水的状态的变化,是物理变化。B、“墟里烟”描述的是物质燃烧,是化学变化;C、金(即钢)柔锡柔,合两柔则刚 说明合金的硬度比组成它的纯金属大;D、宏观物质是由微观粒子构成,因此物质可以分成构成物质的微粒。即无限可分。选C
16.C
【解析】A、金属材料包括纯金属及它们的合金,ZnGa2O4属于化合物,错误;B、一个ZnGa2O4分子中含有4个氧原子,错误;C、ZnGa2O4作催化剂,将CO2转化为碳氢化合物,对碳循环利用有积极意义,正确;D、ZnGa2O4中Ga、O元素质量比为(70×2):(16×4)=35:16,错误。故选C。
17.(1)ACD;
(2)① 剧烈燃烧,火星四溅,生成黑色固体 , 置换反应;② Al Fe H Cu ;
(3)化学方程式 略 ;生铁质量是 583t (此空2分)。
(4)①B ;②熔点低.
【详解】
试题分析:(1)由二种元素组成其中一种元素是氧元素的化合物为氧化物,因此由其主要成分的化学式可得Al2O3、Fe2O3、Fe3O4属于氧化物,因此选ACD;
(2) ① 铁丝在氧气中剧烈燃烧,火星四溅,生成黑色固体 ,丙为Fe + CuSO4 ="=" FeSO4 + Cu,一种单质和一种化合物反应生成另一种单质和化合物,属于置换反应 ;②活动性强的能将活动性弱的置换出来,因此乙不反应可得H>Cu,丙能反应可得Fe>Cu;丁能反应可得Fe>H;戊能反应可得Al>Fe,综合可得Al>Fe>H>Cu;
(3) 为一氧化碳还原氧化铁3CO+ Fe2O32Fe + 3CO2;设理论上可以炼出含铁96%的生铁的质量为x.
Fe2O3+3CO2Fe+3CO2
160 112
1000t×80% 96%x
160/112=1000t×80%/96%x,x=583t
答:理论上可以炼出含铁96%的生铁的质量为583t.
(4)①作导线是利用其导电性,因此选B;②焊锡是利用合金的熔点比成分金属低
18.
(1)D
(2) 铜或锌 在空气中加热
(3) 氧化
【解析】
(1)
芝麻酱中的钙、铁、硒不是以单质、分子、原子等形式存在的,而是指元素,因此图中钙、铁、硒是指元素,故选D;
(2)
二氧化锰是由锰、氧两种元素组成的化合物,属于氧化物.塑料膜是人工合成的含有有机物的材料,锌、铜属于金属材料,故其中可回收的金属材料是铜和锌,故填:铜或锌;在空气中加热使碳与空气中的氧气反应生成二氧化碳,可以除去二氧化锰中的碳,故填:在空气中加热
(3)
反应①中的C被氧化为CO,C发生了氧化反应,故填:氧化;根据质量守恒定律,化学反应前后,元素种类不变,且这种物质是此工艺流程中可循环使用的物质,那么推断这种物质是氯气,因此反应的化学方程式为:。
19.导热 铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好 收集一氧化碳,尾气处理 排净装置内空气,防止发生爆炸 黑色固体变为红色,澄清石灰水变浑浊 Ca(OH)2+CO2=CaCO3↓+H2O CuO、Cu2O CO+CuOCu+CO2 500
【详解】
(1)①用铁锅炒菜主要利用铁具有良好的导热性,故填:导热。
②做门窗常用铝合金而不用纯铝,是因为铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好,故填:铝合金相较于纯铝,强度大,硬度大,耐腐蚀性好。
(2)①装置中气球的作用是收集一氧化碳,尾气处理,故填:收集一氧化碳,尾气处理。
②实验开始前,需要先通过一段时间CO,然后开始加热,先通CO的目的是排净装置内空气,防止发生爆炸,当观察到黑色固体变为红色,澄清石灰水变浑浊现象,说明CO与CuO已经发生反应。澄清石灰水的作用是检验二氧化碳,发生的反应Ca(OH)2+CO2=CaCO3↓+H2O,故填:排净装置内空气,防止发生爆炸;排净装置内空气,防止发生爆炸;Ca(OH)2+CO2=CaCO3↓+H2O。
③a、由图可知,400℃时,反应的固体产物中含有Cu和CuO、Cu2O,故填:CuO、Cu2O。
b、由图可知,500℃时,该反应固体全部为Cu,化学方程式为CO+CuOCu+CO2,故填:CO+CuOCu+CO2。
c、由图可知500℃时,该反应固体全部为Cu,用CO还原CuO制取纯净的Cu,反应温度至少要控制在500℃以上,故填:500。
20.合成橡胶 抗腐蚀性好 TiO2+2C+2Cl2TiCl4+2CO 作保护气防止金属氧化 置换反应 +5 提供足够的氧气,使燃油燃烧更充分
【详解】
(1)图中标示的材料中,合成橡胶属于有机合成材料;故填:合成橡胶;
(2)合金与组成它的成分相比较,一般情况下是密度小、硬度大、抗腐蚀性好,故答案为抗腐蚀性好;
(3)在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体是一氧化碳,反应的化学方程式为:TiO2+2C+2Cl2TiCl4+2CO; Mg容易被氧气氧化,使用氩气防止镁被氧化;在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,属于置换反应;故答案为TiO2+2C+2Cl2TiCl4+2CO;作保护气防止金属氧化;置换反应;
(4)设NaClO3中氯元素的化合价为x,由于钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合价的代数和为零可得(+1)+x+(-2×3)=0,解得x=+5,故答案为+5;
(5)高密度空气能使航空煤油更充分燃烧的微观原因是高密度空气中的氧分子与煤油分子接触更充分,使燃油燃烧更充分;故答案为供足够的氧气,使燃油燃烧更充分。
21.
(1) +4 密度小 温度升高,分子间的间隔变大,体积膨胀 8:1
(2) +3 二氧化氯
【分析】
(1)
根据各元素的化合价的代数和为零,SiO2中氧元素的化合价为-2价,所以Si的化合价是+4价;
铝合金具有密度小,机械强度大 、抗腐蚀性强等优点;
夏天易爆胎”的原因是温度升高,分子运动剧烈,分子间的间隙增大,气体的体积膨胀;
PVC【化学式(C2H3C1)n】中碳、氢元素的质量比是
故填:+4;密度小;温度升高,分子间的间隔变大,体积膨胀;8:1
(2)
由微观示意图可知该反应方程式为:,所以A为NaClO2中钠元素的化合价为+1价,氧元素的化合价为-2价,根据元素的化合价的代数和为零,所以物质中氯元素的化合价为+3价;
D为ClO2,名称为二氧化氯;
该反应的化学方程式是:
故填:+3;二氧化氯;
22.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
