13.2化学合成材料同步练习—2021_2022学年九年级化学京改版(2013)下册(word版 含解析)
文档属性
| 名称 | 13.2化学合成材料同步练习—2021_2022学年九年级化学京改版(2013)下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 336.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-05 00:00:00 | ||
图片预览


文档简介
13.2化学合成材料
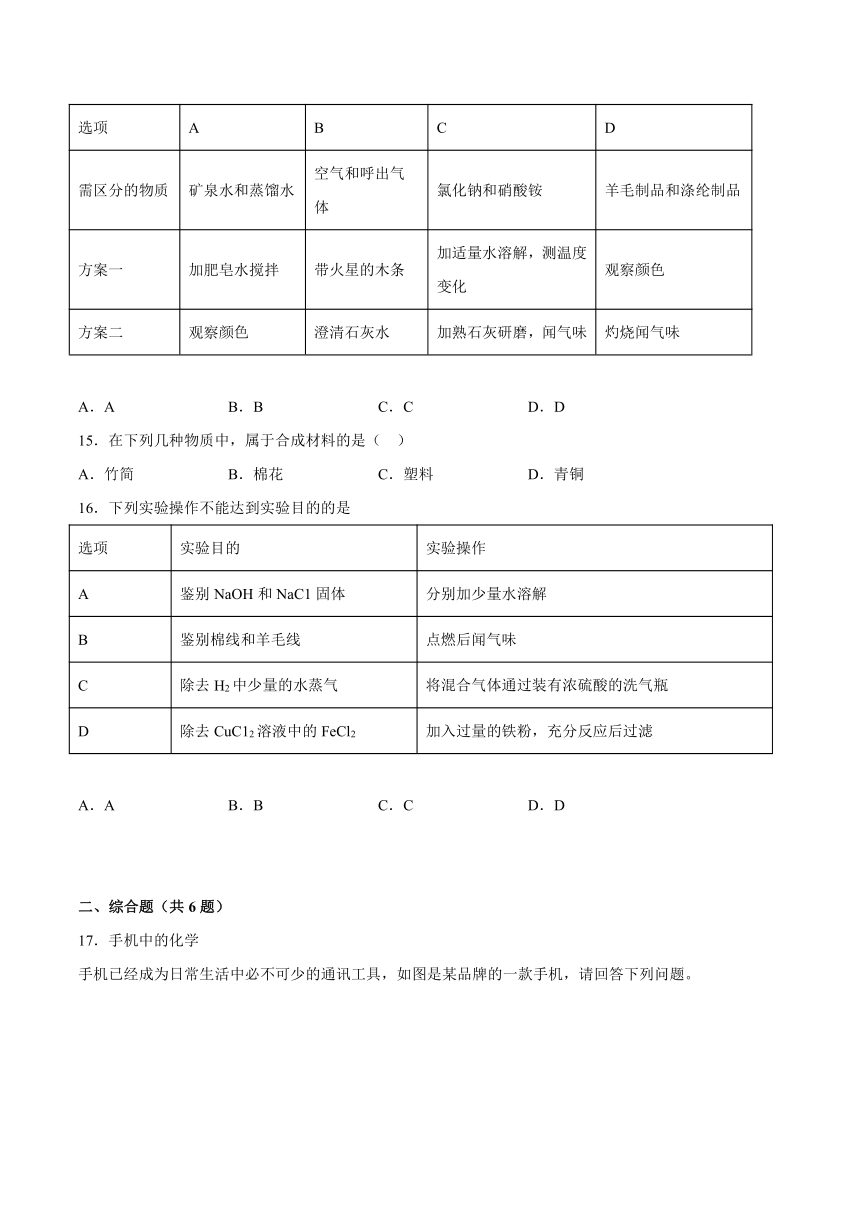
一、选择题(共16题)
1.汽车是常用的交通工具。下列某汽车部件所使用的材料中,属于无机非金属材料的是
A.方向盘包裹材料一塑料
B.发动机绝缘层一陶瓷
C.门窗防水密封圈一合成橡胶
D.底盘一合金钢
2.下列对“化学与生活”的认识中错误的是
A.使用加入铁强化剂的酱油有助于防治缺铁性贫血
B.喝豆浆能补充蛋白质
C.维生素在人体中需要量很少,它不属于人体的营养素
D.制作插座的塑料具有热固性
3.下列图标中,属于我国制定的塑料包装制品回收标志的是( )
A. B. C. D.
4.下列叙述正确的是
A.凡电离时能够产生氢氧根离子的一类化合物都称为碱
B.燃烧都是剧烈的发热发光的化合反应
C.催化剂在化学反应前后,其质量和化学性质都不发生变化
D.白色污染的消除办法是将废弃的塑料就地焚烧
5.下列材料中,属于有机合成材料的是( )
A.尼龙 B.棉花 C.羊绒 D.蚕丝
6.分类观是化学学习的一种重要观点。以下物质的分类正确的是
A.合金:生铁、锌
B.氧化物:四氧化三铁、碳酸钙
C.合成材料:合成纤维、合成橡胶
D.复合肥:硝酸钾、尿素
7.下列做法正确的是
A.用燃烧的方法区分纯羊毛毛线和腈纶毛线
B.将自来水通过活性炭,得到无色透明的纯净水
C.稀释浓硫酸时,将水缓慢倒入浓硫酸中,并不断搅拌
D.不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上稀盐酸
8.材料是社会文明进步的重要标志,下列属于复合材料的是
A.棉花 B.玻璃钢 C.武德合金 D.氮化硼陶瓷
9.下列生活用品所含的主要材料,属于有机合成材料的是( )
A.纯棉毛巾 B.塑料垃圾袋 C.玻璃啤酒瓶 D.铝质饮料罐
10.在生活中,下列做法正确的是
A.霉变大米清洗后食用
B.炒菜时食盐放多了可以用食醋中和
C.用合成纤维做内衣比用天然纤维做内衣穿着更舒适
D.炒菜时油锅中的油不慎着火,可用锅盖或加青菜灭火
11.为了加快城市建设,近两年来我市对多条路桥进行统一规划和改造,下列有关说法正确的是
A.建造路桥需要大量的钢筋混凝土,这些合成材料的使用,让人类摆脱了依赖利用天然材料的历史
B.施工中使用的挖掘机铲斗由韧性好、抗腐蚀性能好的锰钢制成
C.改造路段设置的防护栏大多都喷有“油漆”,其目的主要是为了美观
D.路基修建时用于路面的排水设施会用到PVC管,主要成分是聚氯乙烯
12.有关生活中的下列描述,正确的是( )
A.用洗洁精溶解油污
B.食用甲醛溶液浸泡过的海鲜
C.家中天然气泄漏时立即在房间内拨打 119
D.用灼烧、闻气味的方法区别羊毛纤维和合成纤维维
13.下列关于物质的分类表述正确的是
A.单质:C60、水银、生铁 B.化合物:小苏打、冰水、氯酸钾
C.钠盐:纯碱、氯化钠、烧碱 D.合成材料:塑料、橡胶、合金
14.区分下列各组物质的两种方法都正确的是
选项 A B C D
需区分的物质 矿泉水和蒸馏水 空气和呼出气体 氯化钠和硝酸铵 羊毛制品和涤纶制品
方案一 加肥皂水搅拌 带火星的木条 加适量水溶解,测温度变化 观察颜色
方案二 观察颜色 澄清石灰水 加熟石灰研磨,闻气味 灼烧闻气味
A.A B.B C.C D.D
15.在下列几种物质中,属于合成材料的是( )
A.竹简 B.棉花 C.塑料 D.青铜
16.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 鉴别NaOH和NaC1固体 分别加少量水溶解
B 鉴别棉线和羊毛线 点燃后闻气味
C 除去H2中少量的水蒸气 将混合气体通过装有浓硫酸的洗气瓶
D 除去CuC12溶液中的FeCl2 加入过量的铁粉,充分反应后过滤
A.A B.B C.C D.D
二、综合题(共6题)
17.手机中的化学
手机已经成为日常生活中必不可少的通讯工具,如图是某品牌的一款手机,请回答下列问题。
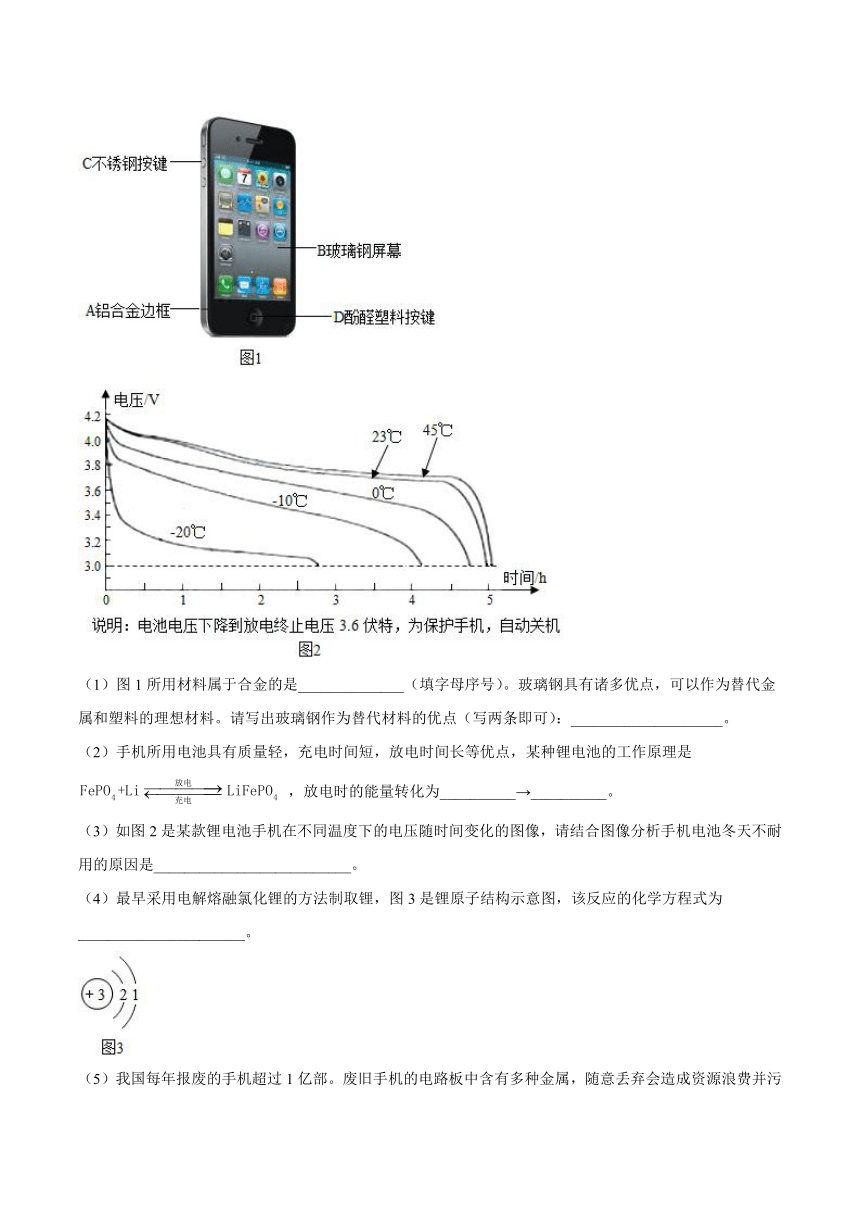
(1)图1所用材料属于合金的是______________(填字母序号)。玻璃钢具有诸多优点,可以作为替代金属和塑料的理想材料。请写出玻璃钢作为替代材料的优点(写两条即可):____________________。
(2)手机所用电池具有质量轻,充电时间短,放电时间长等优点,某种锂电池的工作原理是 ,放电时的能量转化为__________→__________。
(3)如图2是某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机电池冬天不耐用的原因是__________________________。
(4)最早采用电解熔融氯化锂的方法制取锂,图3是锂原子结构示意图,该反应的化学方程式为______________________。
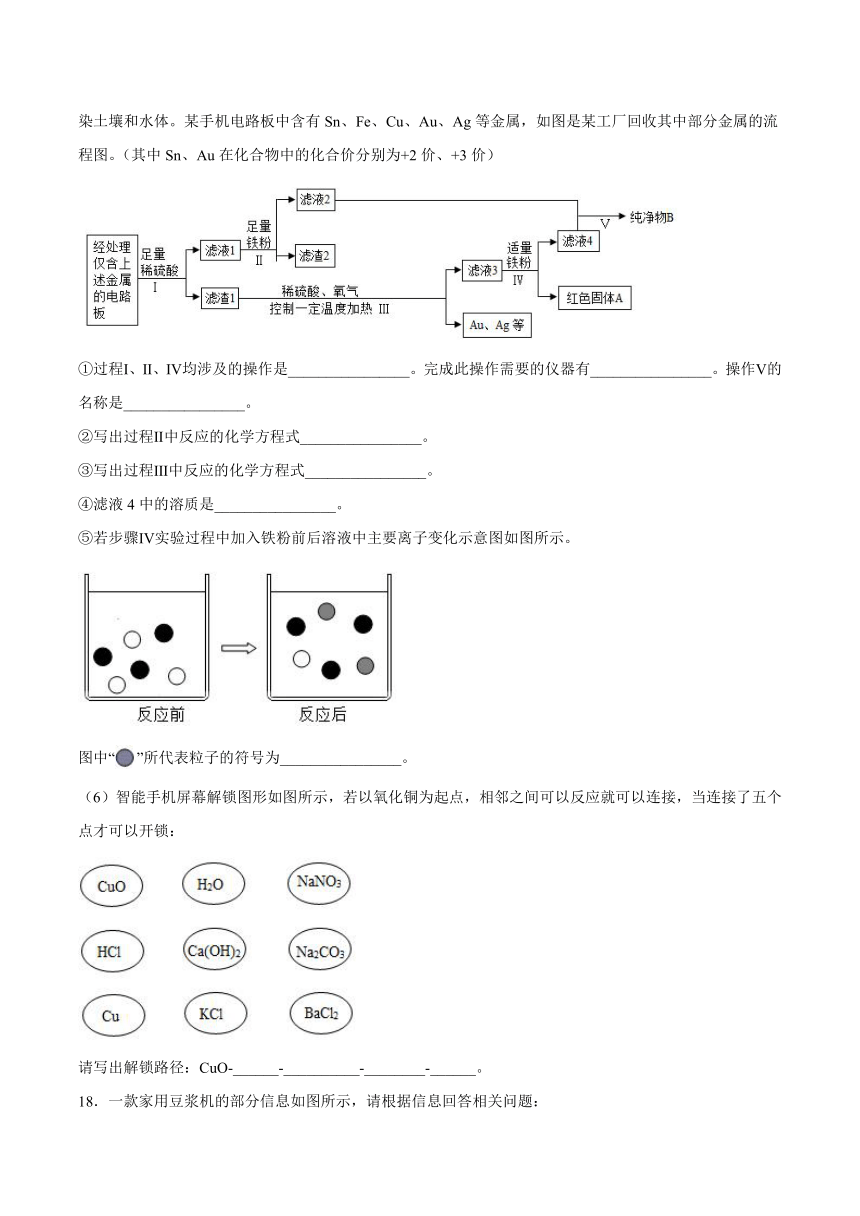
(5)我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有Sn、Fe、Cu、Au、Ag等金属,如图是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
①过程Ⅰ、Ⅱ、Ⅳ均涉及的操作是________________。完成此操作需要的仪器有________________。操作Ⅴ的名称是________________。
②写出过程Ⅱ中反应的化学方程式________________。
③写出过程Ⅲ中反应的化学方程式________________。
④滤液4中的溶质是________________。
⑤若步骤Ⅳ实验过程中加入铁粉前后溶液中主要离子变化示意图如图所示。
图中“”所代表粒子的符号为________________。
(6)智能手机屏幕解锁图形如图所示,若以氧化铜为起点,相邻之间可以反应就可以连接,当连接了五个点才可以开锁:
请写出解锁路径:CuO-______-__________-________-______。
18.一款家用豆浆机的部分信息如图所示,请根据信息回答相关问题:
(1)豆浆机各部件中,属于金属材料的是_________(填序号,一种即可,下同),属于有机合成材料的是___________。电源插头使用铜质插脚是利用了铜的__________性。
(2)豆浆机长时间使用后,内壁会有一层水垢,可以用厨房常用的食醋来除去。其原理是食醋中的醋酸(HAc)会与水垢中的碳酸钙发生复分解反应,请写出反应的化学方程式:______________________________________。
(3)从传统的磨制豆浆到使用豆浆机,你从中体会到化学与生活的关系是______。
19.日常生活、社会发展与化学密切相关。
Ⅰ.(1)有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入 __ (填序号)不足而引起的。
①维生素 ②油脂 ③蛋白质
(2)“××糕点”主要营养成分如图所示。请根据该表回答。
①所含营养素中属于无机盐的是 ___ (写化学式)。
②其中提供能量的营养素有蛋白质、 ___ 、糖类。
③食用300g该糕点,为人体提供钙元素的质量是 ____ mg
(3)直接参与人体新陈代谢活动的糖类是 __ (用化学式表示),自然界产生该物质过程的名称叫 ___ 。
Ⅱ.(1)生铁和钢都是铁的合金,从组成上看,二者性能不同的原因是 ___ ;
(2)厨房中的下列物品所使用的主要材料属于无机材料的是 ___ ;
A 陶瓷碗 B 不锈钢炊具 C 橡胶手套 D 铜质水龙头
(3)某录音录带磁粉中含有化学组成相当于CoFe2O4的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,则铁元素的化合价为 ____ ;
(4)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,其中的化合反应是 ___ (用化学方程式表示);
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则滤液中一定不含有的物质是 ___ 。
20.化学是造福人类的科学,请利用所学知识回答下列问题。
(1)新型材料有着广泛的应用。
应用 “蛟龙”号深潜器 “神舟”五号宇航员航天服 新型水处理剂
用到的材料 特种钢 高强度涤纶 纳米铁粉
①上述材料中属于有机合成材料的是______。
②纳米铁粉能吸附废水中的某些污染物,被吸附后的废水经沉降、过滤可去除污染物。
下列物质也能因吸附而具有净水作用的是______(填字母)
a.生石灰 b.活性炭 c.纯碱
(2)溶液与人们的生产生活密切相关,图1为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
②某同学按图2所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是______(填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______。(结果精确到0.1%)
21.华裔科学家高锟因提出“以高纯度的石英玻璃制造光纤”,获得2009年诺贝尔奖。从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料。回答问题:
(1)地壳里各种元素的含量(质量分数)如图所示,其中表示Si元素的含量为_____。
(2)根据元素周期表可知,原子序数为6的碳原子和原子序数为14的硅原子最外层电子数均为4。常温下,硅的化学性质______(填“活泼”或“不活泼”)。
(3)制备硅半导体材料必须先得到高纯硅,工业上以石英砂(主要成分SiO2)制取高纯度石英玻璃的生产原理如下。请回答:
①已知反应①的另一产物是有毒气体,其化学式为____,此副产物的用途是_______。
②已知反应②为化合反应,该反应的化学方程式为________________。
③反应③的化学方程式为SiCl4+O2SiO2+2Cl2,该反应的基本类型为______。
④将反应③中的氧气换成氢气,可制得生产计算机芯片的高纯硅,则另一产物的化学式为_____。
22.金属及其化合物与我们的生活生产息息相关,其中铁及其化合物的使用最为广泛。
一、金属的广泛应用
(1)人体因摄入铁元素不足而易导致的疾病是________;
(2)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到__________(填字母)
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
二、钢铁的冶炼和探究
(3)联合钢铁工业的基本生产流程示意如下:
①写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:__________。
②生铁和钢的最大区别是:______________。
③某赤铁矿石中含Fe2O380%,用3000 t这种矿石,可炼出含杂质4%的生铁质量是多少________?(请写出计算过程)
(4)甲组同学取24gFe2O3粉末设计了如图1所示的实验装置测定一氧化碳与氧化铁反应后的固体产物。已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。
如果实验成功,请回答下列问题:
①写出A中玻璃管内反应的实验现象_________。
②实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是________。
③B、C装置的作用是_________(填字母序号)
a 收集二氧化碳 b 检验二氧化碳 c 收集一氧化碳
(5)查阅资料得知CO与氧化铁反应,在不同的温度下,氧化铁因失氧程度不同而生成其他铁的氧化物(或铁单质)和CO2。乙组同学采集了用某种热分析仪记录的CO与氧化铁反应的有关数据,并得到固体质量与反应温度的关系曲线,如图2所示。根据相关信息,回答如下问题:
①图中D点对应的物质化学式为________;
②写出400℃~500℃发生的化学方程式________ 。
参考答案
1.B
【详解】
A、塑料属于合成材料,不符合题意;
B、陶瓷属于无机非金属材料,符合题意;
C、合成橡胶属于合成材料,不符合题意;
D、合金钢属于金属材料,不符合题意。
故选B。
2.C
【详解】
缺铁元素易得缺铁性贫血,所以A正确;豆浆富含植物性蛋白质,B正确;塑料具有热塑性和热固性,D正确;人体的营养素包括维生素,C错误。
3.B
【详解】
A、该图标是节水标记,不符合题意;
B、该图标是塑料回收标记,符合题意;
C、该图标是可燃物标识,不符合题意;
D、该图标是不可回收物标识,不符合题意。故选B。
4.C
【解析】
试题分析:电离时产生的阴离子只有氢氧根离子的一类化合物都称为碱;燃烧都是剧烈的发热发光的化学反应不一定是化合反应,比如甲烷的燃烧等;催化剂在化学反应前后,其质量和化学性质都不发生变化;白色污染的消除办法是将废弃的塑料集中处理,尽量少用塑料袋。故选C.
5.A
【详解】
有机合成材料必须具备三个条件,一是有机物,二是人工合成,三是高分子化合物.棉花、羊绒、蚕丝都属于天然有机材料,不属于合成材料;尼龙是有机合成材料.故选A。
6.C
【详解】
A、锌不是合金,是纯金属,故选项错误;
B、氧化物是含有两种元素且其中一种是氧元素的化合物;碳酸钙中含有三种元素,不是氧化物,故选项错误;
C、合成纤维、合成橡胶都属于合成材料,故选项正确;
D、复合肥是含有氮磷钾中至少两种营养元素的肥料,尿素属于氮肥,不是复合肥,故选项错误。故选C。
7.A
【解析】
试题分析:A、羊毛的主要成分是蛋白质,燃烧会有烧焦羽毛的味道,所以可用燃烧的方法区分纯羊毛毛线和腈纶毛线,故A正确;B、活性炭具有吸附性,只能吸附水中有颜色或有异味的物质,但不能除掉可溶性杂质,故B错误;C、浓硫酸稀释时放热,稀释浓硫酸时,将浓硫酸缓慢倒入水中,并不断搅拌,故C错误;D、盐酸具有强烈的腐蚀性,所以不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上硼酸,故D错误,使用答案选A。
8.B
【详解】
A、棉花属于天然有机高分子材料,故A不正确;
B、玻璃钢是指用玻璃纤维增强塑料得到的复合材料,故B正确;
C、武德合金属于金属材料,故C不正确;
D、氮化硼陶瓷属于无机非金属材料,故D不正确。故选B。
9.B
【详解】
A、纯棉毛巾属于天然有机材料,故不符合题意;
B、塑料垃圾袋属于有机合成材料,故符合题意;
C、玻璃啤酒瓶属于无机材料,故不符合题意;
D、铝质饮料罐属于金属材料,故不符合题意。
故选B。
10.D
【详解】
A、霉变大米清洗后,不能除去有毒物质,不能食用,做法错误;B、食盐是盐,显中性,食醋是酸,不是发生中和反应,做法错误;C、天然纤维吸水性和透气性好,用合成纤维做内衣比用天然纤维做内衣穿着差,做法错误;D、油锅中的有不慎着火,盖锅盖或者加青菜灭火是隔绝氧气或者降低温度到着火点以下,做法正确。故选D。
11.D
【详解】
A、钢筋混凝土属于复合材料,故A说法错误;
B、施工过程中使用的挖掘机的铲斗可以选用韧性好、硬度大的锰钢,但锰钢的抗腐蚀不强,故B说法错误;
C、改造路段设置的防护栏大多都喷有“油漆”,其目的主要是为了防止金属生锈,故C说法错误;
D、路基修建时用于路面的排水设施会用到PVC管,主要成分是聚氯乙烯,故D说法正确。
故选:D。
12.D
【详解】
A、洗洁精具有乳化作用,可洗去餐具上的油污,而不是溶解油污,故A选项说法错误;
B、甲醛有毒,能破坏人体蛋白质的结构,使蛋白质变性,食用会对人体健康造成危害,故B选项说法错误;
C、天然气具有可燃性,与空气混合后的气体遇明火、静电、电火花或加热易发生爆炸,在房间内拨打电话会产生电火花,故C选项说法错误;
D、区别羊毛纤维和合成纤维可用灼烧的方法,羊毛纤维的成分是蛋白质,灼烧会有烧焦羽毛的气味,而合成纤维维没有,故D选项说法正确。故选D。
13.B
【详解】
由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;由两种元素组成,且其中一种是氧的化合物叫氧化物。由金属或铵根和酸根组成的化合物叫盐。A. 单质:C60、水银,生铁 是铁的 合金,是混合物; B. 化合物:小苏打、冰水、氯酸钾都是化合物;C. 钠盐:纯碱、氯化钠,烧碱即氢氧化钠,是碱; D. 合成材料:塑料、合成橡胶、合成纤维;合金是金属材料;选B
14.C
【详解】
A、需区分的物质矿泉水和蒸馏水,方案一加肥皂水搅拌可行,看泡沫多少;方案二观察颜色不可行,两者都是无色,故错误;
B、空气和呼出气体用澄清石灰水可行,因为呼出气体含有二氧化碳较多,能使澄清石灰水变浑浊;带火星的木条不可行,因为两者都能使带火星的木条熄灭,故错误;
C、鉴别氯化钠和硝酸铵,加适量水溶解,测温度变化,降温的是硝酸铵,温度不变的是氯化钠,可行;加熟石灰研磨,闻气味也可行,硝酸铵与熟石灰反应会有刺激性气味的气体生成,氯化钠就无,故正确;
D、鉴别羊毛制品和涤纶制品灼烧闻气味可行,有烧焦羽毛气味的是羊毛;观察颜色则不可行,两者的颜色可能相同,故错误。
故选C。
15.C
【详解】
A.竹筒是由竹子这种天然材料制成的;
B.棉花属于天然材料;
C.塑料属于三大合成材料之一;
D.青铜属于合金,属于金属材料。
故选C。
16.D
【详解】
A、NaOH溶于水放出大量的热,使溶液的温度升高,氯化钠溶液溶于水温度几乎无变化可以鉴别,故选项实验操作能达到实验目的,不符合题意;
B、羊毛线的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,棉线燃烧产生烧纸的气味,可用燃烧法区别,故选项实验操作能达到实验目的,不符合题意;
C、浓硫酸具有吸水性,且不与氢气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项实验操作能达到实验目的,不符合题意;
D、加入过量铁粉会把溶液中的铜离子全部置换出来,氯化铜溶液被消耗,故选项实验操作不能达到实验目的,符合题意。
故选D。
17.AC 硬度大、密度小 化学能 电能 冬天温度低,温度越低,电压下降到放电终止电压的时间越短 过滤 烧杯、漏斗、带铁圈的铁架台、玻璃棒 蒸发结晶 、、 硫酸亚铁 Fe2+ HCl Ca(OH)2 Na2CO3 BaCl2
【详解】
(1)合金是指金属和金属或非金属熔合在一起具有金属特性的物质,不锈钢和铝合金都属于合金,故填:AC;玻璃钢具有硬度大、密度小的特点,故填:硬度大,密度小;
(2)锂电池放点过程中是化学能转化为电能,故填:化学能;电能;
(3)手机电池冬天不耐用的原因是冬天温度低,温度越低,电压下降到放电终止电压的时间越短;
(4)氯化锂通电生成锂和氯气,锂原子最外层只有一个电子,在反应中易失去最外层电子,形成一个带1个单位正电荷的锂离子,则氯化锂的化学式LiCl,该反应的化学方程式为;
(5)①过程Ⅰ、Ⅱ、Ⅳ都是分离难溶性固体与液体的方法,属于过滤操作,过滤操作中用到的仪器有烧杯、漏斗、带铁圈的铁架台、玻璃棒;操作V是实现溶液转化为晶体的过程,该操作属于蒸发结晶;
②加入稀硫酸后,Sn和Fe能与稀硫酸发生反应,而Cu、Au和Ag不能与稀硫酸发生反应,成为滤渣,滤液Ⅰ中含有的主要成分为硫酸铜和硫酸锡,因为铁的金属活动性比铜和锡强,因此铁能和硫酸锡发生置换反应,同时还发生了铁和硫酸的反应,反应的化学方程式为:
、;
③滤渣Ⅰ中有铜、金和银,铜能够和稀硫酸,氧气,在加热的条件下反应生成硫酸铜,该反应的化学方程式:;
④根据工艺流程图可知滤液4和滤液2的主要成分一直,滤液2主要成分为硫酸亚铁,滤液4的主要成分是硫酸亚铁,
⑤步骤Ⅳ实验过程中加入铁粉是指硫酸铜和铁反应生成硫酸亚铁和铜,图中“”所代表粒子的符号为Fe2+;
(6)氧化铜和盐酸反应生成氯化铜和水,盐酸和氢氧化钙反应生成氯化钙和水,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,所以解锁路径:CuO- HCl - Ca(OH)2- Na2CO3- BaCl2。
18.②或③; ① 导电性 2HAc+CaCO3=CaAc2+H2O+CO2↑ 化学的发展促进材料的变革,使日常生活更加方便(合理即可)
【详解】
(1)金属材料包括纯金属和合金,所以②③属于金属材料;有机合成材料包括塑料、合成橡胶和合成纤维,所以①属于有机合成材料;(2)铜具有优良的导电性,可用铜质材料制作电源插头的插脚;(2)醋酸(HAc)与水垢中的碳酸钙发生复分解反应生成醋酸钙、水和二氧化碳,化学方程式为:2HAc+CaCO3=CaAc2+H2O+CO2↑;(3)从传统的磨制豆浆到使用豆浆机,体会到化学与生活的关系是:化学的发展促进材料的变革,使日常生活更加方便。
19.① CaCO3 油脂 480 C6H12O6 光合作用 含碳量不同 A +3 CaO+H2O= Ca(OH)2 CuSO4、H2SO4
【详解】
(1) 蔬菜、水果中含有较多的维生素,则不爱吃蔬菜、水果,影响生长发育,主要是由于摄入①不足而引起的。
(2) ①盐是由金属阳离子或铵根离子和酸根离子构成的化合物,故所含营养素中属于无机盐的是。
②其中提供能量的营养素有蛋白质、油脂、糖类。
③食用300g该糕点,为人体提供钙元素的质量是
。
(3)直接参与人体新陈代谢活动的糖类是葡萄糖,化学式为,植物利用二氧化碳和水进行光合作用生成葡萄糖和氧气,故自然界产生该物质过程的名称叫光合作用。
Ⅱ、(1)生铁和钢都是铁的合金,从组成上看,二者性能不同的原因是含碳量不同。
(2) A、陶瓷碗属于无机非金属材料,故A正确;
B、不锈钢炊具,属于金属材料,故B不正确;
C、橡胶手套,属于合成材料,故C不正确;
D、铜质水龙头,属于金属材料,故D不正确。故选A。
(3)某录音录带磁粉中含有化学组成相当于的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,如果钴元素的化合价为+2价,设铁元素的化合价为x,则,;如果钴元素的化合价为+3价,则,,不是铁元素的化合价,故铁元素的化合价为+3价。
(4)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,其中的发生的反应是氧化钙和水反应生成氢氧化钙,硫酸铜和氢氧化钙反应生成氢氧化铜和硫酸钙,故化合反应是。
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则溶液中至少含有铁,滤渣中含有铁,则滤液中一定不含有的物质 。
20.高强度涤纶 b 丙>乙>甲 B 33.3%
【详解】
(1)①特种钢和纳米铁粉属于金属材料;高强度涤纶属于有机合成材料;
②活性炭具有疏松多孔结构,具有吸附性,具有净水作用;
(2)①由溶解度曲线可知,在t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是:丙>乙>甲;
②t2℃时甲物质的溶解度是28g,即100g水中最多可以溶解28g甲物质,所以B溶液是饱和溶液;t3℃时甲物质的溶解度是50g,在C溶液中含有溶质的质量是42g,是不饱和溶液;
③t3℃时甲物质的溶解度是50g,50g水中最多可以溶解25g甲物质,所得溶液溶质的质量分数=33.3%。
21.26.30% 不活泼 CO 用于冶金工业或气体燃料 Si+2Cl2SiCl4 置换反应 HCl
【详解】
(1)因为硅元素在地壳里含量是第二位。所以,硅的含量为26.30%;故填:26.30%;
(2)由于碳元素的化学性质不活泼,而硅元素的最外层电子数与碳相同,则其化学性质也应较稳定,故常温下硅的化学性质不活泼;故填:不活泼;
(3)①二氧化硅和碳反应生成有毒气体,根据反应中元素种类不变,可确定该产物为一氧化碳,一氧化碳具有还原性和可燃性,所以可用于冶金工业或气体燃料;故填:CO;用于冶金工业或气体燃料;
②反应②为两种物质生成一种物质的化合反应,所以是硅和氯气反应生成四氯化硅,反应的化学方程式为Si+2Cl2 SiCl4;故填:Si+2Cl2 SiCl4;
(3)反应③的化学方程式为SiCl4+O2SiO2+2Cl2,该反应是单质与化合物生成单质与化合物的置换反应。故填:置换反应;
(4)反应物为氢气和四氯化硅生成物有硅,根据反应中元素种类不变,可确定另一元素中含有氢、氯元素,所以则另一产物的化学式为HCl;故填:HCl。
22.贫血 B 含碳量不同 1750t 红色固体变为黑色 排尽装置内空气,避免发生爆炸 bc Fe
【详解】
一、(1)人体因摄入铁元素不足而易导致的疾病是贫血;
(2)A、铁与铬、镍等金属熔合可形成“不锈钢”属于合金,涉及合金;
B、不涉及无机非金属材料;
C、聚乙烯纤维属于合成材料,涉及合成材料;
D、耐酸防护服材料由合金、聚乙烯纤维组成,属于复合材料,涉及复合材料;
故填:B。
二、(3)①赤铁矿为原料在高温下与一氧化碳反应制取铁,高温条件下,氧化铁与一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:。
②生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁和钢的主要区别是含碳量不同。
③设可炼出含杂质4%的生铁质量是x,则
解得x= 1750t;
答:可炼出含杂质4%的生铁质量是1750t。
(4)①A中玻璃管内,高温条件下,红色氧化铁与一氧化碳反应生成黑色的铁和二氧化碳,反应的实验现象为红色固体变为黑色。
②一氧化碳为可燃性气体,不纯时点燃或受热会发生爆炸,实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是排尽装置内空气,避免发生爆炸。
③B装置中二氧化碳先与氢氧化钠反应,生成碳酸钠和水,而碳酸钠与氢氧化钙可以发生复分解反应,生成碳酸钙白色沉淀和氢氧化钠,一氧化碳不被吸收、也不被排出,收集在B中,故B、C装置的作用是检验二氧化碳、收集一氧化碳;
故填:bc。
(5)①图中D点时剩余固体为16.8g,24g氧化铁中铁元素质量为,D点对应的物质为铁,化学式为Fe;
②24g氧化铁中氧元素质量为,400℃时氧化铁恰好开始反应,500℃时固体质量减少24g-23.2g=0.8g,则剩余氧元素质量为7.2g-0.8g=6.4g,此时氧化物中铁与氧原子个数比为,即500℃时的产物为四氧化三铁,故400℃~500℃发生的化学方程式为。
一、选择题(共16题)
1.汽车是常用的交通工具。下列某汽车部件所使用的材料中,属于无机非金属材料的是
A.方向盘包裹材料一塑料
B.发动机绝缘层一陶瓷
C.门窗防水密封圈一合成橡胶
D.底盘一合金钢
2.下列对“化学与生活”的认识中错误的是
A.使用加入铁强化剂的酱油有助于防治缺铁性贫血
B.喝豆浆能补充蛋白质
C.维生素在人体中需要量很少,它不属于人体的营养素
D.制作插座的塑料具有热固性
3.下列图标中,属于我国制定的塑料包装制品回收标志的是( )
A. B. C. D.
4.下列叙述正确的是
A.凡电离时能够产生氢氧根离子的一类化合物都称为碱
B.燃烧都是剧烈的发热发光的化合反应
C.催化剂在化学反应前后,其质量和化学性质都不发生变化
D.白色污染的消除办法是将废弃的塑料就地焚烧
5.下列材料中,属于有机合成材料的是( )
A.尼龙 B.棉花 C.羊绒 D.蚕丝
6.分类观是化学学习的一种重要观点。以下物质的分类正确的是
A.合金:生铁、锌
B.氧化物:四氧化三铁、碳酸钙
C.合成材料:合成纤维、合成橡胶
D.复合肥:硝酸钾、尿素
7.下列做法正确的是
A.用燃烧的方法区分纯羊毛毛线和腈纶毛线
B.将自来水通过活性炭,得到无色透明的纯净水
C.稀释浓硫酸时,将水缓慢倒入浓硫酸中,并不断搅拌
D.不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上稀盐酸
8.材料是社会文明进步的重要标志,下列属于复合材料的是
A.棉花 B.玻璃钢 C.武德合金 D.氮化硼陶瓷
9.下列生活用品所含的主要材料,属于有机合成材料的是( )
A.纯棉毛巾 B.塑料垃圾袋 C.玻璃啤酒瓶 D.铝质饮料罐
10.在生活中,下列做法正确的是
A.霉变大米清洗后食用
B.炒菜时食盐放多了可以用食醋中和
C.用合成纤维做内衣比用天然纤维做内衣穿着更舒适
D.炒菜时油锅中的油不慎着火,可用锅盖或加青菜灭火
11.为了加快城市建设,近两年来我市对多条路桥进行统一规划和改造,下列有关说法正确的是
A.建造路桥需要大量的钢筋混凝土,这些合成材料的使用,让人类摆脱了依赖利用天然材料的历史
B.施工中使用的挖掘机铲斗由韧性好、抗腐蚀性能好的锰钢制成
C.改造路段设置的防护栏大多都喷有“油漆”,其目的主要是为了美观
D.路基修建时用于路面的排水设施会用到PVC管,主要成分是聚氯乙烯
12.有关生活中的下列描述,正确的是( )
A.用洗洁精溶解油污
B.食用甲醛溶液浸泡过的海鲜
C.家中天然气泄漏时立即在房间内拨打 119
D.用灼烧、闻气味的方法区别羊毛纤维和合成纤维维
13.下列关于物质的分类表述正确的是
A.单质:C60、水银、生铁 B.化合物:小苏打、冰水、氯酸钾
C.钠盐:纯碱、氯化钠、烧碱 D.合成材料:塑料、橡胶、合金
14.区分下列各组物质的两种方法都正确的是
选项 A B C D
需区分的物质 矿泉水和蒸馏水 空气和呼出气体 氯化钠和硝酸铵 羊毛制品和涤纶制品
方案一 加肥皂水搅拌 带火星的木条 加适量水溶解,测温度变化 观察颜色
方案二 观察颜色 澄清石灰水 加熟石灰研磨,闻气味 灼烧闻气味
A.A B.B C.C D.D
15.在下列几种物质中,属于合成材料的是( )
A.竹简 B.棉花 C.塑料 D.青铜
16.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 鉴别NaOH和NaC1固体 分别加少量水溶解
B 鉴别棉线和羊毛线 点燃后闻气味
C 除去H2中少量的水蒸气 将混合气体通过装有浓硫酸的洗气瓶
D 除去CuC12溶液中的FeCl2 加入过量的铁粉,充分反应后过滤
A.A B.B C.C D.D
二、综合题(共6题)
17.手机中的化学
手机已经成为日常生活中必不可少的通讯工具,如图是某品牌的一款手机,请回答下列问题。
(1)图1所用材料属于合金的是______________(填字母序号)。玻璃钢具有诸多优点,可以作为替代金属和塑料的理想材料。请写出玻璃钢作为替代材料的优点(写两条即可):____________________。
(2)手机所用电池具有质量轻,充电时间短,放电时间长等优点,某种锂电池的工作原理是 ,放电时的能量转化为__________→__________。
(3)如图2是某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机电池冬天不耐用的原因是__________________________。
(4)最早采用电解熔融氯化锂的方法制取锂,图3是锂原子结构示意图,该反应的化学方程式为______________________。
(5)我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有Sn、Fe、Cu、Au、Ag等金属,如图是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
①过程Ⅰ、Ⅱ、Ⅳ均涉及的操作是________________。完成此操作需要的仪器有________________。操作Ⅴ的名称是________________。
②写出过程Ⅱ中反应的化学方程式________________。
③写出过程Ⅲ中反应的化学方程式________________。
④滤液4中的溶质是________________。
⑤若步骤Ⅳ实验过程中加入铁粉前后溶液中主要离子变化示意图如图所示。
图中“”所代表粒子的符号为________________。
(6)智能手机屏幕解锁图形如图所示,若以氧化铜为起点,相邻之间可以反应就可以连接,当连接了五个点才可以开锁:
请写出解锁路径:CuO-______-__________-________-______。
18.一款家用豆浆机的部分信息如图所示,请根据信息回答相关问题:
(1)豆浆机各部件中,属于金属材料的是_________(填序号,一种即可,下同),属于有机合成材料的是___________。电源插头使用铜质插脚是利用了铜的__________性。
(2)豆浆机长时间使用后,内壁会有一层水垢,可以用厨房常用的食醋来除去。其原理是食醋中的醋酸(HAc)会与水垢中的碳酸钙发生复分解反应,请写出反应的化学方程式:______________________________________。
(3)从传统的磨制豆浆到使用豆浆机,你从中体会到化学与生活的关系是______。
19.日常生活、社会发展与化学密切相关。
Ⅰ.(1)有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入 __ (填序号)不足而引起的。
①维生素 ②油脂 ③蛋白质
(2)“××糕点”主要营养成分如图所示。请根据该表回答。
①所含营养素中属于无机盐的是 ___ (写化学式)。
②其中提供能量的营养素有蛋白质、 ___ 、糖类。
③食用300g该糕点,为人体提供钙元素的质量是 ____ mg
(3)直接参与人体新陈代谢活动的糖类是 __ (用化学式表示),自然界产生该物质过程的名称叫 ___ 。
Ⅱ.(1)生铁和钢都是铁的合金,从组成上看,二者性能不同的原因是 ___ ;
(2)厨房中的下列物品所使用的主要材料属于无机材料的是 ___ ;
A 陶瓷碗 B 不锈钢炊具 C 橡胶手套 D 铜质水龙头
(3)某录音录带磁粉中含有化学组成相当于CoFe2O4的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,则铁元素的化合价为 ____ ;
(4)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,其中的化合反应是 ___ (用化学方程式表示);
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则滤液中一定不含有的物质是 ___ 。
20.化学是造福人类的科学,请利用所学知识回答下列问题。
(1)新型材料有着广泛的应用。
应用 “蛟龙”号深潜器 “神舟”五号宇航员航天服 新型水处理剂
用到的材料 特种钢 高强度涤纶 纳米铁粉
①上述材料中属于有机合成材料的是______。
②纳米铁粉能吸附废水中的某些污染物,被吸附后的废水经沉降、过滤可去除污染物。
下列物质也能因吸附而具有净水作用的是______(填字母)
a.生石灰 b.活性炭 c.纯碱
(2)溶液与人们的生产生活密切相关,图1为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
②某同学按图2所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是______(填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______。(结果精确到0.1%)
21.华裔科学家高锟因提出“以高纯度的石英玻璃制造光纤”,获得2009年诺贝尔奖。从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料。回答问题:
(1)地壳里各种元素的含量(质量分数)如图所示,其中表示Si元素的含量为_____。
(2)根据元素周期表可知,原子序数为6的碳原子和原子序数为14的硅原子最外层电子数均为4。常温下,硅的化学性质______(填“活泼”或“不活泼”)。
(3)制备硅半导体材料必须先得到高纯硅,工业上以石英砂(主要成分SiO2)制取高纯度石英玻璃的生产原理如下。请回答:
①已知反应①的另一产物是有毒气体,其化学式为____,此副产物的用途是_______。
②已知反应②为化合反应,该反应的化学方程式为________________。
③反应③的化学方程式为SiCl4+O2SiO2+2Cl2,该反应的基本类型为______。
④将反应③中的氧气换成氢气,可制得生产计算机芯片的高纯硅,则另一产物的化学式为_____。
22.金属及其化合物与我们的生活生产息息相关,其中铁及其化合物的使用最为广泛。
一、金属的广泛应用
(1)人体因摄入铁元素不足而易导致的疾病是________;
(2)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到__________(填字母)
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
二、钢铁的冶炼和探究
(3)联合钢铁工业的基本生产流程示意如下:
①写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:__________。
②生铁和钢的最大区别是:______________。
③某赤铁矿石中含Fe2O380%,用3000 t这种矿石,可炼出含杂质4%的生铁质量是多少________?(请写出计算过程)
(4)甲组同学取24gFe2O3粉末设计了如图1所示的实验装置测定一氧化碳与氧化铁反应后的固体产物。已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。
如果实验成功,请回答下列问题:
①写出A中玻璃管内反应的实验现象_________。
②实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是________。
③B、C装置的作用是_________(填字母序号)
a 收集二氧化碳 b 检验二氧化碳 c 收集一氧化碳
(5)查阅资料得知CO与氧化铁反应,在不同的温度下,氧化铁因失氧程度不同而生成其他铁的氧化物(或铁单质)和CO2。乙组同学采集了用某种热分析仪记录的CO与氧化铁反应的有关数据,并得到固体质量与反应温度的关系曲线,如图2所示。根据相关信息,回答如下问题:
①图中D点对应的物质化学式为________;
②写出400℃~500℃发生的化学方程式________ 。
参考答案
1.B
【详解】
A、塑料属于合成材料,不符合题意;
B、陶瓷属于无机非金属材料,符合题意;
C、合成橡胶属于合成材料,不符合题意;
D、合金钢属于金属材料,不符合题意。
故选B。
2.C
【详解】
缺铁元素易得缺铁性贫血,所以A正确;豆浆富含植物性蛋白质,B正确;塑料具有热塑性和热固性,D正确;人体的营养素包括维生素,C错误。
3.B
【详解】
A、该图标是节水标记,不符合题意;
B、该图标是塑料回收标记,符合题意;
C、该图标是可燃物标识,不符合题意;
D、该图标是不可回收物标识,不符合题意。故选B。
4.C
【解析】
试题分析:电离时产生的阴离子只有氢氧根离子的一类化合物都称为碱;燃烧都是剧烈的发热发光的化学反应不一定是化合反应,比如甲烷的燃烧等;催化剂在化学反应前后,其质量和化学性质都不发生变化;白色污染的消除办法是将废弃的塑料集中处理,尽量少用塑料袋。故选C.
5.A
【详解】
有机合成材料必须具备三个条件,一是有机物,二是人工合成,三是高分子化合物.棉花、羊绒、蚕丝都属于天然有机材料,不属于合成材料;尼龙是有机合成材料.故选A。
6.C
【详解】
A、锌不是合金,是纯金属,故选项错误;
B、氧化物是含有两种元素且其中一种是氧元素的化合物;碳酸钙中含有三种元素,不是氧化物,故选项错误;
C、合成纤维、合成橡胶都属于合成材料,故选项正确;
D、复合肥是含有氮磷钾中至少两种营养元素的肥料,尿素属于氮肥,不是复合肥,故选项错误。故选C。
7.A
【解析】
试题分析:A、羊毛的主要成分是蛋白质,燃烧会有烧焦羽毛的味道,所以可用燃烧的方法区分纯羊毛毛线和腈纶毛线,故A正确;B、活性炭具有吸附性,只能吸附水中有颜色或有异味的物质,但不能除掉可溶性杂质,故B错误;C、浓硫酸稀释时放热,稀释浓硫酸时,将浓硫酸缓慢倒入水中,并不断搅拌,故C错误;D、盐酸具有强烈的腐蚀性,所以不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上硼酸,故D错误,使用答案选A。
8.B
【详解】
A、棉花属于天然有机高分子材料,故A不正确;
B、玻璃钢是指用玻璃纤维增强塑料得到的复合材料,故B正确;
C、武德合金属于金属材料,故C不正确;
D、氮化硼陶瓷属于无机非金属材料,故D不正确。故选B。
9.B
【详解】
A、纯棉毛巾属于天然有机材料,故不符合题意;
B、塑料垃圾袋属于有机合成材料,故符合题意;
C、玻璃啤酒瓶属于无机材料,故不符合题意;
D、铝质饮料罐属于金属材料,故不符合题意。
故选B。
10.D
【详解】
A、霉变大米清洗后,不能除去有毒物质,不能食用,做法错误;B、食盐是盐,显中性,食醋是酸,不是发生中和反应,做法错误;C、天然纤维吸水性和透气性好,用合成纤维做内衣比用天然纤维做内衣穿着差,做法错误;D、油锅中的有不慎着火,盖锅盖或者加青菜灭火是隔绝氧气或者降低温度到着火点以下,做法正确。故选D。
11.D
【详解】
A、钢筋混凝土属于复合材料,故A说法错误;
B、施工过程中使用的挖掘机的铲斗可以选用韧性好、硬度大的锰钢,但锰钢的抗腐蚀不强,故B说法错误;
C、改造路段设置的防护栏大多都喷有“油漆”,其目的主要是为了防止金属生锈,故C说法错误;
D、路基修建时用于路面的排水设施会用到PVC管,主要成分是聚氯乙烯,故D说法正确。
故选:D。
12.D
【详解】
A、洗洁精具有乳化作用,可洗去餐具上的油污,而不是溶解油污,故A选项说法错误;
B、甲醛有毒,能破坏人体蛋白质的结构,使蛋白质变性,食用会对人体健康造成危害,故B选项说法错误;
C、天然气具有可燃性,与空气混合后的气体遇明火、静电、电火花或加热易发生爆炸,在房间内拨打电话会产生电火花,故C选项说法错误;
D、区别羊毛纤维和合成纤维可用灼烧的方法,羊毛纤维的成分是蛋白质,灼烧会有烧焦羽毛的气味,而合成纤维维没有,故D选项说法正确。故选D。
13.B
【详解】
由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;由两种元素组成,且其中一种是氧的化合物叫氧化物。由金属或铵根和酸根组成的化合物叫盐。A. 单质:C60、水银,生铁 是铁的 合金,是混合物; B. 化合物:小苏打、冰水、氯酸钾都是化合物;C. 钠盐:纯碱、氯化钠,烧碱即氢氧化钠,是碱; D. 合成材料:塑料、合成橡胶、合成纤维;合金是金属材料;选B
14.C
【详解】
A、需区分的物质矿泉水和蒸馏水,方案一加肥皂水搅拌可行,看泡沫多少;方案二观察颜色不可行,两者都是无色,故错误;
B、空气和呼出气体用澄清石灰水可行,因为呼出气体含有二氧化碳较多,能使澄清石灰水变浑浊;带火星的木条不可行,因为两者都能使带火星的木条熄灭,故错误;
C、鉴别氯化钠和硝酸铵,加适量水溶解,测温度变化,降温的是硝酸铵,温度不变的是氯化钠,可行;加熟石灰研磨,闻气味也可行,硝酸铵与熟石灰反应会有刺激性气味的气体生成,氯化钠就无,故正确;
D、鉴别羊毛制品和涤纶制品灼烧闻气味可行,有烧焦羽毛气味的是羊毛;观察颜色则不可行,两者的颜色可能相同,故错误。
故选C。
15.C
【详解】
A.竹筒是由竹子这种天然材料制成的;
B.棉花属于天然材料;
C.塑料属于三大合成材料之一;
D.青铜属于合金,属于金属材料。
故选C。
16.D
【详解】
A、NaOH溶于水放出大量的热,使溶液的温度升高,氯化钠溶液溶于水温度几乎无变化可以鉴别,故选项实验操作能达到实验目的,不符合题意;
B、羊毛线的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,棉线燃烧产生烧纸的气味,可用燃烧法区别,故选项实验操作能达到实验目的,不符合题意;
C、浓硫酸具有吸水性,且不与氢气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项实验操作能达到实验目的,不符合题意;
D、加入过量铁粉会把溶液中的铜离子全部置换出来,氯化铜溶液被消耗,故选项实验操作不能达到实验目的,符合题意。
故选D。
17.AC 硬度大、密度小 化学能 电能 冬天温度低,温度越低,电压下降到放电终止电压的时间越短 过滤 烧杯、漏斗、带铁圈的铁架台、玻璃棒 蒸发结晶 、、 硫酸亚铁 Fe2+ HCl Ca(OH)2 Na2CO3 BaCl2
【详解】
(1)合金是指金属和金属或非金属熔合在一起具有金属特性的物质,不锈钢和铝合金都属于合金,故填:AC;玻璃钢具有硬度大、密度小的特点,故填:硬度大,密度小;
(2)锂电池放点过程中是化学能转化为电能,故填:化学能;电能;
(3)手机电池冬天不耐用的原因是冬天温度低,温度越低,电压下降到放电终止电压的时间越短;
(4)氯化锂通电生成锂和氯气,锂原子最外层只有一个电子,在反应中易失去最外层电子,形成一个带1个单位正电荷的锂离子,则氯化锂的化学式LiCl,该反应的化学方程式为;
(5)①过程Ⅰ、Ⅱ、Ⅳ都是分离难溶性固体与液体的方法,属于过滤操作,过滤操作中用到的仪器有烧杯、漏斗、带铁圈的铁架台、玻璃棒;操作V是实现溶液转化为晶体的过程,该操作属于蒸发结晶;
②加入稀硫酸后,Sn和Fe能与稀硫酸发生反应,而Cu、Au和Ag不能与稀硫酸发生反应,成为滤渣,滤液Ⅰ中含有的主要成分为硫酸铜和硫酸锡,因为铁的金属活动性比铜和锡强,因此铁能和硫酸锡发生置换反应,同时还发生了铁和硫酸的反应,反应的化学方程式为:
、;
③滤渣Ⅰ中有铜、金和银,铜能够和稀硫酸,氧气,在加热的条件下反应生成硫酸铜,该反应的化学方程式:;
④根据工艺流程图可知滤液4和滤液2的主要成分一直,滤液2主要成分为硫酸亚铁,滤液4的主要成分是硫酸亚铁,
⑤步骤Ⅳ实验过程中加入铁粉是指硫酸铜和铁反应生成硫酸亚铁和铜,图中“”所代表粒子的符号为Fe2+;
(6)氧化铜和盐酸反应生成氯化铜和水,盐酸和氢氧化钙反应生成氯化钙和水,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,所以解锁路径:CuO- HCl - Ca(OH)2- Na2CO3- BaCl2。
18.②或③; ① 导电性 2HAc+CaCO3=CaAc2+H2O+CO2↑ 化学的发展促进材料的变革,使日常生活更加方便(合理即可)
【详解】
(1)金属材料包括纯金属和合金,所以②③属于金属材料;有机合成材料包括塑料、合成橡胶和合成纤维,所以①属于有机合成材料;(2)铜具有优良的导电性,可用铜质材料制作电源插头的插脚;(2)醋酸(HAc)与水垢中的碳酸钙发生复分解反应生成醋酸钙、水和二氧化碳,化学方程式为:2HAc+CaCO3=CaAc2+H2O+CO2↑;(3)从传统的磨制豆浆到使用豆浆机,体会到化学与生活的关系是:化学的发展促进材料的变革,使日常生活更加方便。
19.① CaCO3 油脂 480 C6H12O6 光合作用 含碳量不同 A +3 CaO+H2O= Ca(OH)2 CuSO4、H2SO4
【详解】
(1) 蔬菜、水果中含有较多的维生素,则不爱吃蔬菜、水果,影响生长发育,主要是由于摄入①不足而引起的。
(2) ①盐是由金属阳离子或铵根离子和酸根离子构成的化合物,故所含营养素中属于无机盐的是。
②其中提供能量的营养素有蛋白质、油脂、糖类。
③食用300g该糕点,为人体提供钙元素的质量是
。
(3)直接参与人体新陈代谢活动的糖类是葡萄糖,化学式为,植物利用二氧化碳和水进行光合作用生成葡萄糖和氧气,故自然界产生该物质过程的名称叫光合作用。
Ⅱ、(1)生铁和钢都是铁的合金,从组成上看,二者性能不同的原因是含碳量不同。
(2) A、陶瓷碗属于无机非金属材料,故A正确;
B、不锈钢炊具,属于金属材料,故B不正确;
C、橡胶手套,属于合成材料,故C不正确;
D、铜质水龙头,属于金属材料,故D不正确。故选A。
(3)某录音录带磁粉中含有化学组成相当于的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,如果钴元素的化合价为+2价,设铁元素的化合价为x,则,;如果钴元素的化合价为+3价,则,,不是铁元素的化合价,故铁元素的化合价为+3价。
(4)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,其中的发生的反应是氧化钙和水反应生成氢氧化钙,硫酸铜和氢氧化钙反应生成氢氧化铜和硫酸钙,故化合反应是。
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则溶液中至少含有铁,滤渣中含有铁,则滤液中一定不含有的物质 。
20.高强度涤纶 b 丙>乙>甲 B 33.3%
【详解】
(1)①特种钢和纳米铁粉属于金属材料;高强度涤纶属于有机合成材料;
②活性炭具有疏松多孔结构,具有吸附性,具有净水作用;
(2)①由溶解度曲线可知,在t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是:丙>乙>甲;
②t2℃时甲物质的溶解度是28g,即100g水中最多可以溶解28g甲物质,所以B溶液是饱和溶液;t3℃时甲物质的溶解度是50g,在C溶液中含有溶质的质量是42g,是不饱和溶液;
③t3℃时甲物质的溶解度是50g,50g水中最多可以溶解25g甲物质,所得溶液溶质的质量分数=33.3%。
21.26.30% 不活泼 CO 用于冶金工业或气体燃料 Si+2Cl2SiCl4 置换反应 HCl
【详解】
(1)因为硅元素在地壳里含量是第二位。所以,硅的含量为26.30%;故填:26.30%;
(2)由于碳元素的化学性质不活泼,而硅元素的最外层电子数与碳相同,则其化学性质也应较稳定,故常温下硅的化学性质不活泼;故填:不活泼;
(3)①二氧化硅和碳反应生成有毒气体,根据反应中元素种类不变,可确定该产物为一氧化碳,一氧化碳具有还原性和可燃性,所以可用于冶金工业或气体燃料;故填:CO;用于冶金工业或气体燃料;
②反应②为两种物质生成一种物质的化合反应,所以是硅和氯气反应生成四氯化硅,反应的化学方程式为Si+2Cl2 SiCl4;故填:Si+2Cl2 SiCl4;
(3)反应③的化学方程式为SiCl4+O2SiO2+2Cl2,该反应是单质与化合物生成单质与化合物的置换反应。故填:置换反应;
(4)反应物为氢气和四氯化硅生成物有硅,根据反应中元素种类不变,可确定另一元素中含有氢、氯元素,所以则另一产物的化学式为HCl;故填:HCl。
22.贫血 B 含碳量不同 1750t 红色固体变为黑色 排尽装置内空气,避免发生爆炸 bc Fe
【详解】
一、(1)人体因摄入铁元素不足而易导致的疾病是贫血;
(2)A、铁与铬、镍等金属熔合可形成“不锈钢”属于合金,涉及合金;
B、不涉及无机非金属材料;
C、聚乙烯纤维属于合成材料,涉及合成材料;
D、耐酸防护服材料由合金、聚乙烯纤维组成,属于复合材料,涉及复合材料;
故填:B。
二、(3)①赤铁矿为原料在高温下与一氧化碳反应制取铁,高温条件下,氧化铁与一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:。
②生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁和钢的主要区别是含碳量不同。
③设可炼出含杂质4%的生铁质量是x,则
解得x= 1750t;
答:可炼出含杂质4%的生铁质量是1750t。
(4)①A中玻璃管内,高温条件下,红色氧化铁与一氧化碳反应生成黑色的铁和二氧化碳,反应的实验现象为红色固体变为黑色。
②一氧化碳为可燃性气体,不纯时点燃或受热会发生爆炸,实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是排尽装置内空气,避免发生爆炸。
③B装置中二氧化碳先与氢氧化钠反应,生成碳酸钠和水,而碳酸钠与氢氧化钙可以发生复分解反应,生成碳酸钙白色沉淀和氢氧化钠,一氧化碳不被吸收、也不被排出,收集在B中,故B、C装置的作用是检验二氧化碳、收集一氧化碳;
故填:bc。
(5)①图中D点时剩余固体为16.8g,24g氧化铁中铁元素质量为,D点对应的物质为铁,化学式为Fe;
②24g氧化铁中氧元素质量为,400℃时氧化铁恰好开始反应,500℃时固体质量减少24g-23.2g=0.8g,则剩余氧元素质量为7.2g-0.8g=6.4g,此时氧化物中铁与氧原子个数比为,即500℃时的产物为四氧化三铁,故400℃~500℃发生的化学方程式为。
