2021-2022学年人教版初三化学下册第十一单元课题1 生活中常见的盐 综合训练1(word版 含答案)
文档属性
| 名称 | 2021-2022学年人教版初三化学下册第十一单元课题1 生活中常见的盐 综合训练1(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 473.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-06 00:00:00 | ||
图片预览

文档简介
2021-2022学年人教版初三化学下册第十一单元课题1 生活中常见的盐 综合训练
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
1. 饮食店蒸馒头、炸油条常使用的是( )
A.火碱 B.小苏打 C.白醋 D.硫酸
2. (2021黑龙江龙东地区中考)下列各组离子在水中能大量共存,并形成无色透明溶液的是( )
A.Fe2+、Ag+、Cl-、N B.H+、N、N、C
C.K+、Ca2+、C、OH- D.Na+、Mg2+、Cl-、N
3. (2021山西太原万柏林一模)在一次课外兴趣实验中,同学们对NaHCO3的化学性质进行了探究,下列实验结论中,错误的是( )
A.实验①无色酚酞溶液变红,说明NaHCO3溶液呈碱性
B.实验②有气泡产生,实验③有白色沉淀生成,说明NaHCO3与酸和碱都能发生反应
C.实验④试管口有小水珠,说明NaHCO3固体受热易分解
D.以上实验操作都是规范的
4. (2021·济宁中考)下列化学方程式的书写和对反应类型的判断,都正确的是( )
A.2FeCl3+Fe===3FeCl2 化合反应
B.HgOHg+O2↑ 分解反应
C.CuO+COCu+CO2 置换反应
D.KCl+HNO3===KNO3+HCl 复分解反应
5. 下列物质之间的转化中,只有加入酸才能一步实现的是( )
A.CuO→CuCl2
B.Na2CO3→NaCl
C.Fe→FeSO4
D.CaCO3→CO2
6. (2021广东汕头潮阳模拟)如图所示流程是为了除去食盐水中的Na2SO4杂质。下列有关说法正确的是( )
混合溶液滤液NaCl溶液
A.X为BaCl2溶液 B.Y为K2CO3
C.Z可为稀硫酸 D.步骤③与④先后可对调
7. (2021·河南一模)下列各组物质能发生复分解反应且溶液质量变小的是( )
A.硝酸钾溶液和食盐水
B.氢氧化钠溶液和硫酸溶液
C.硫酸和氯化钡溶液
D.锌放入硝酸银溶液中
8. (2021·苏州一模)下列反应属于复分解反应的是( )
A.Zn与稀H2SO4反应
B.甲烷燃烧
C.加热碳酸氢铵
D.石灰石与稀盐酸反应
9. 小明想在鸡蛋壳(主要成分CaCO3)上腐蚀出一个“福”字(如图),送给奶奶作为生日礼物。下列溶液能帮他实现愿望的是( )
A.食盐水 B.白酒 C.蔗糖水 D.白醋
10.(2021·邵阳中考)含氢氧化铝的药物治疗胃酸过多的反应为Al(OH)3+3HCl===AlCl3+3H2O,该反应属于( )
A.化合反应 B.分解反应
C.复分解反应 D.置换反应
二、填空题
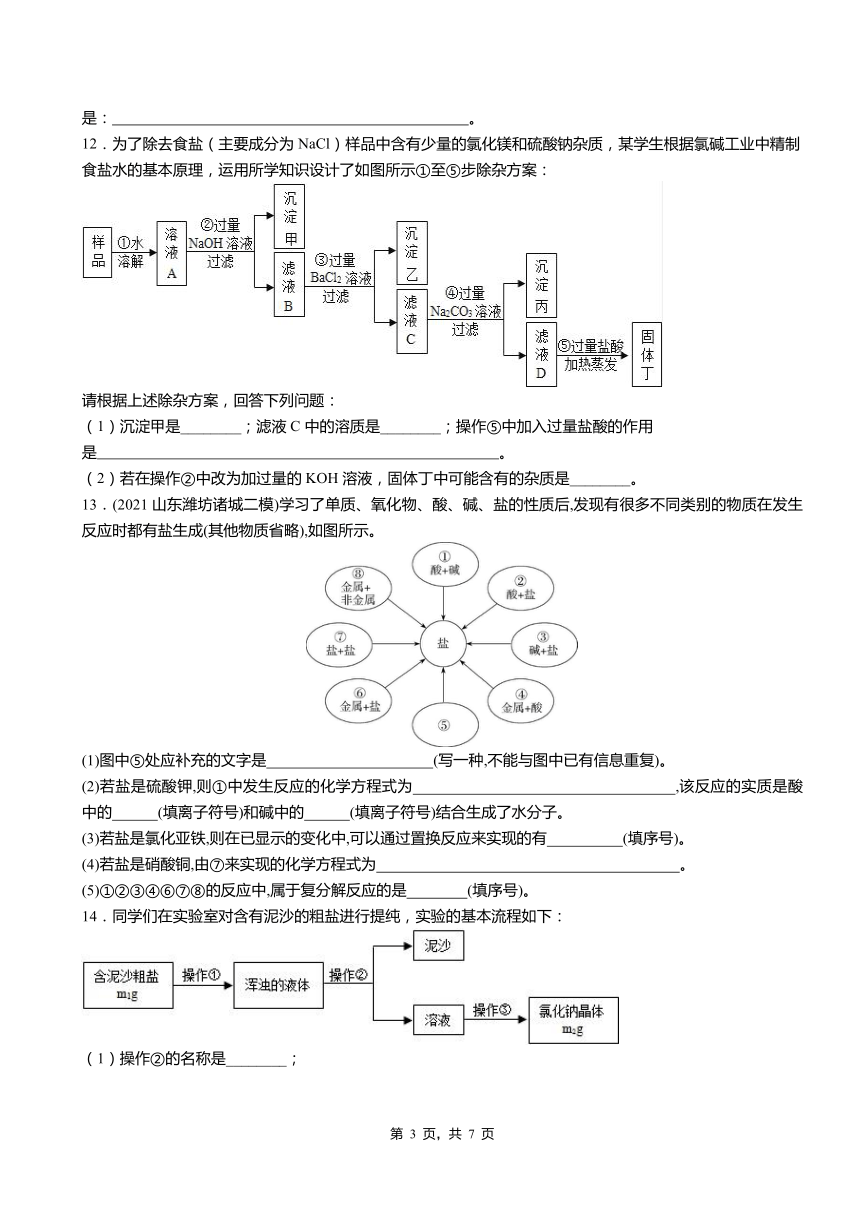
11.目前世界上60%的镁是从海水中提取的.海水提镁的主要流程如下:
(1)向海水中加入石灰乳的作用是________。
(2)从充分利用海洋化学资源、提高经济效益的角度,生产生石灰的主要原料来源于海洋中的贝壳,生石灰和水反应的化学方程式是
。
(3)操作A是________ ,加入的足量试剂a是 (填化学式)。
(4)已知MgCl2的溶解度随温度的升高而增大。下列各图是某MgCl2饱和溶液的浓度随温 度升高而变化的图象(不考虑溶剂的质量变化),其中正确的是________。
(5)海水提镁的过程中,将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁的原因是: 。
(6)试剂a具有刺激性气味,我们刚进实验室就能闻到这种气味,说明分子的性质是: 。
12.为了除去食盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如图所示①至⑤步除杂方案:
请根据上述除杂方案,回答下列问题:
(1)沉淀甲是________;滤液C中的溶质是________;操作⑤中加入过量盐酸的作用是 。
(2)若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是________。
13.(2021山东潍坊诸城二模)学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。
(1)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
(2)若盐是硫酸钾,则①中发生反应的化学方程式为 ,该反应的实质是酸中的 (填离子符号)和碱中的 (填离子符号)结合生成了水分子。
(3)若盐是氯化亚铁,则在已显示的变化中,可以通过置换反应来实现的有 (填序号)。
(4)若盐是硝酸铜,由⑦来实现的化学方程式为 。
(5)①②③④⑥⑦⑧的反应中,属于复分解反应的是 (填序号)。
14.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是________;
(2)操作①②③都要用到的一种玻璃仪器是________,在操作③中,使用这种玻璃仪器的目的是 。
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是________(只写一种原因)。
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号)。
a.称量氯化钠所用天平砝码沾有杂质;b.用量筒取水时俯视读数;c.用量筒取水时仰视读数;d.配制溶液的烧杯用蒸馏水润洗过。
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液________mL(结果保留小数点后一位)。
15.用符合要求的物质的字母填空。
A.稀盐酸 B.氢氧化钠 C.氯化钠 D.碳酸氢钠 E.硫酸铜
(1)可用于去除铁锈的是________;
(2)可用于治疗胃酸过多的是________;
(3)可用于游泳池杀菌消毒的是________。
三、实验探究题
16.(2021广西贺州中考)某化学兴趣小组在实验室探究碳酸钠溶液与稀盐酸的反应原理,请你一起完成实验探究。
实验一:在5 mL稀盐酸中逐滴加入碳酸钠溶液,边滴边振荡,直至滴完5 mL碳酸钠溶液。
现象:开始有气泡产生,一段时间后无气泡产生。写出碳酸钠与稀盐酸反应的化学方程式: 。在反应后的溶液中加入2滴酚酞溶液,溶液变红,则反应后溶液中的溶质是 。
实验二:在5 mL碳酸钠溶液中逐滴加入稀盐酸,边滴边振荡,直至滴完5 mL稀盐酸。
现象:整个实验过程无气泡产生。
【提出问题】用量相同的两种反应物,滴加顺序不同,现象为什么不一样呢
【查阅资料】碳酸钠溶液与盐酸反应:
1.盐酸过量时,反应生成NaCl、CO2和H2O;
2.盐酸不足时,产物是NaCl和NaHCO3。
【假设猜想】实验二结束后,试管中溶液的溶质有哪些
猜想1:NaCl、Na2CO3和NaHCO3
猜想2:
猜想3:NaCl
猜想4:NaCl和HCl
小明认为猜想3和4明显不合理,理由是 。
【实验探究】实验二结束后,将试管中溶液分成三等份,分别做下列三个实验。
序号 实验操作及实验现象 实验结论
实验1 加入硝酸银溶液,产生白色沉淀 再加入稀硝酸,沉淀不消失 溶液中含 (写离子符号)
实验2 加入 溶液,无沉淀产生 猜想1不成立
实验3 加入 ,有 产生 猜想2成立
【交流反思】用量相同的两种反应物,滴加顺序不同,现象和产物可能都不一样。
2021-2022学年人教版初三化学下册第十一单元课题1 生活中常见的盐 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 B D C A A A C D D C
二、填空题
11.使Mg2+形成Mg(OH)2沉淀 CaO+H2O═Ca(OH)2 过滤 HCl C 海水中氯化镁的含量很大,但镁离子浓度很低,该过程可以使镁离子富集,浓度高,且成本低 分子在永不停息地做无规律运动
12.氢氧化镁 氯化钠、氢氧化钠、氯化钡 除去滤液D中的NaOH和Na2CO3 氯化钾
13. (1)金属氧化物+酸(或某些非金属氧化物+碱) (2)2KOH+H2SO4K2SO4+2H2O H+ OH- (3)④⑥
(4)CuSO4+Ba(NO3)2BaSO4↓+Cu(NO3)2[或CuCl2+2AgNO3Cu(NO3)2+2AgCl↓] (5)①②③⑦
14.过滤 玻璃棒 防止液体外溅 蒸发溶液时液体外溅了一部分 ab 7.7
15.(1)A (2)D (3)E
三、实验探究题
16. 实验一:Na2CO3+2HCl2NaCl+H2O+CO2↑ Na2CO3、NaCl 实验二:【假设猜想】NaCl、NaHCO3 整个实验过程无气泡产生 【实验探究】Cl- 氯化钡(合理即可) 稀盐酸 气泡
第 1 页,共 3 页
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
1. 饮食店蒸馒头、炸油条常使用的是( )
A.火碱 B.小苏打 C.白醋 D.硫酸
2. (2021黑龙江龙东地区中考)下列各组离子在水中能大量共存,并形成无色透明溶液的是( )
A.Fe2+、Ag+、Cl-、N B.H+、N、N、C
C.K+、Ca2+、C、OH- D.Na+、Mg2+、Cl-、N
3. (2021山西太原万柏林一模)在一次课外兴趣实验中,同学们对NaHCO3的化学性质进行了探究,下列实验结论中,错误的是( )
A.实验①无色酚酞溶液变红,说明NaHCO3溶液呈碱性
B.实验②有气泡产生,实验③有白色沉淀生成,说明NaHCO3与酸和碱都能发生反应
C.实验④试管口有小水珠,说明NaHCO3固体受热易分解
D.以上实验操作都是规范的
4. (2021·济宁中考)下列化学方程式的书写和对反应类型的判断,都正确的是( )
A.2FeCl3+Fe===3FeCl2 化合反应
B.HgOHg+O2↑ 分解反应
C.CuO+COCu+CO2 置换反应
D.KCl+HNO3===KNO3+HCl 复分解反应
5. 下列物质之间的转化中,只有加入酸才能一步实现的是( )
A.CuO→CuCl2
B.Na2CO3→NaCl
C.Fe→FeSO4
D.CaCO3→CO2
6. (2021广东汕头潮阳模拟)如图所示流程是为了除去食盐水中的Na2SO4杂质。下列有关说法正确的是( )
混合溶液滤液NaCl溶液
A.X为BaCl2溶液 B.Y为K2CO3
C.Z可为稀硫酸 D.步骤③与④先后可对调
7. (2021·河南一模)下列各组物质能发生复分解反应且溶液质量变小的是( )
A.硝酸钾溶液和食盐水
B.氢氧化钠溶液和硫酸溶液
C.硫酸和氯化钡溶液
D.锌放入硝酸银溶液中
8. (2021·苏州一模)下列反应属于复分解反应的是( )
A.Zn与稀H2SO4反应
B.甲烷燃烧
C.加热碳酸氢铵
D.石灰石与稀盐酸反应
9. 小明想在鸡蛋壳(主要成分CaCO3)上腐蚀出一个“福”字(如图),送给奶奶作为生日礼物。下列溶液能帮他实现愿望的是( )
A.食盐水 B.白酒 C.蔗糖水 D.白醋
10.(2021·邵阳中考)含氢氧化铝的药物治疗胃酸过多的反应为Al(OH)3+3HCl===AlCl3+3H2O,该反应属于( )
A.化合反应 B.分解反应
C.复分解反应 D.置换反应
二、填空题
11.目前世界上60%的镁是从海水中提取的.海水提镁的主要流程如下:
(1)向海水中加入石灰乳的作用是________。
(2)从充分利用海洋化学资源、提高经济效益的角度,生产生石灰的主要原料来源于海洋中的贝壳,生石灰和水反应的化学方程式是
。
(3)操作A是________ ,加入的足量试剂a是 (填化学式)。
(4)已知MgCl2的溶解度随温度的升高而增大。下列各图是某MgCl2饱和溶液的浓度随温 度升高而变化的图象(不考虑溶剂的质量变化),其中正确的是________。
(5)海水提镁的过程中,将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁的原因是: 。
(6)试剂a具有刺激性气味,我们刚进实验室就能闻到这种气味,说明分子的性质是: 。
12.为了除去食盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如图所示①至⑤步除杂方案:
请根据上述除杂方案,回答下列问题:
(1)沉淀甲是________;滤液C中的溶质是________;操作⑤中加入过量盐酸的作用是 。
(2)若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是________。
13.(2021山东潍坊诸城二模)学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。
(1)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
(2)若盐是硫酸钾,则①中发生反应的化学方程式为 ,该反应的实质是酸中的 (填离子符号)和碱中的 (填离子符号)结合生成了水分子。
(3)若盐是氯化亚铁,则在已显示的变化中,可以通过置换反应来实现的有 (填序号)。
(4)若盐是硝酸铜,由⑦来实现的化学方程式为 。
(5)①②③④⑥⑦⑧的反应中,属于复分解反应的是 (填序号)。
14.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是________;
(2)操作①②③都要用到的一种玻璃仪器是________,在操作③中,使用这种玻璃仪器的目的是 。
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是________(只写一种原因)。
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号)。
a.称量氯化钠所用天平砝码沾有杂质;b.用量筒取水时俯视读数;c.用量筒取水时仰视读数;d.配制溶液的烧杯用蒸馏水润洗过。
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液________mL(结果保留小数点后一位)。
15.用符合要求的物质的字母填空。
A.稀盐酸 B.氢氧化钠 C.氯化钠 D.碳酸氢钠 E.硫酸铜
(1)可用于去除铁锈的是________;
(2)可用于治疗胃酸过多的是________;
(3)可用于游泳池杀菌消毒的是________。
三、实验探究题
16.(2021广西贺州中考)某化学兴趣小组在实验室探究碳酸钠溶液与稀盐酸的反应原理,请你一起完成实验探究。
实验一:在5 mL稀盐酸中逐滴加入碳酸钠溶液,边滴边振荡,直至滴完5 mL碳酸钠溶液。
现象:开始有气泡产生,一段时间后无气泡产生。写出碳酸钠与稀盐酸反应的化学方程式: 。在反应后的溶液中加入2滴酚酞溶液,溶液变红,则反应后溶液中的溶质是 。
实验二:在5 mL碳酸钠溶液中逐滴加入稀盐酸,边滴边振荡,直至滴完5 mL稀盐酸。
现象:整个实验过程无气泡产生。
【提出问题】用量相同的两种反应物,滴加顺序不同,现象为什么不一样呢
【查阅资料】碳酸钠溶液与盐酸反应:
1.盐酸过量时,反应生成NaCl、CO2和H2O;
2.盐酸不足时,产物是NaCl和NaHCO3。
【假设猜想】实验二结束后,试管中溶液的溶质有哪些
猜想1:NaCl、Na2CO3和NaHCO3
猜想2:
猜想3:NaCl
猜想4:NaCl和HCl
小明认为猜想3和4明显不合理,理由是 。
【实验探究】实验二结束后,将试管中溶液分成三等份,分别做下列三个实验。
序号 实验操作及实验现象 实验结论
实验1 加入硝酸银溶液,产生白色沉淀 再加入稀硝酸,沉淀不消失 溶液中含 (写离子符号)
实验2 加入 溶液,无沉淀产生 猜想1不成立
实验3 加入 ,有 产生 猜想2成立
【交流反思】用量相同的两种反应物,滴加顺序不同,现象和产物可能都不一样。
2021-2022学年人教版初三化学下册第十一单元课题1 生活中常见的盐 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 B D C A A A C D D C
二、填空题
11.使Mg2+形成Mg(OH)2沉淀 CaO+H2O═Ca(OH)2 过滤 HCl C 海水中氯化镁的含量很大,但镁离子浓度很低,该过程可以使镁离子富集,浓度高,且成本低 分子在永不停息地做无规律运动
12.氢氧化镁 氯化钠、氢氧化钠、氯化钡 除去滤液D中的NaOH和Na2CO3 氯化钾
13. (1)金属氧化物+酸(或某些非金属氧化物+碱) (2)2KOH+H2SO4K2SO4+2H2O H+ OH- (3)④⑥
(4)CuSO4+Ba(NO3)2BaSO4↓+Cu(NO3)2[或CuCl2+2AgNO3Cu(NO3)2+2AgCl↓] (5)①②③⑦
14.过滤 玻璃棒 防止液体外溅 蒸发溶液时液体外溅了一部分 ab 7.7
15.(1)A (2)D (3)E
三、实验探究题
16. 实验一:Na2CO3+2HCl2NaCl+H2O+CO2↑ Na2CO3、NaCl 实验二:【假设猜想】NaCl、NaHCO3 整个实验过程无气泡产生 【实验探究】Cl- 氯化钡(合理即可) 稀盐酸 气泡
第 1 页,共 3 页
同课章节目录
