2022年京改版九年级化学下册第10章金属检测题(word版有答案)
文档属性
| 名称 | 2022年京改版九年级化学下册第10章金属检测题(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 158.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-07 00:00:00 | ||
图片预览


文档简介
第10章《金属》检测题
一、单选题
1.将一定量铁粉置于AgNO3和Mg(NO3)2混合溶液中,充分反应完毕后,过滤所得滤液中一定含有的金属阳离子是
A.Fe3+、Mg2+ B.Mg2+ C.Fe2+、Mg2+ D.Fe2+、Mg2+、Ag+
2.中国诗词既蕴含人文思想,又焕发理性光辉。诗句“何意百炼钢,化为绕指柔”提到了古代将生铁煅烧捶打氧化变成钢的过程,下列化学解释不合理的是
A.生铁和钢是同种物质 B.煅打过程发生碳燃烧反应
C.钢的机械性能比生铁好 D.生铁和钢都是铁的合金
3.下列实验现象,描述正确的是
A.红热的铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.用火柴去点蜡烛刚熄灭时产生的白烟,蜡烛不能重新燃烧
C.将光亮的铁钉放入硫酸铜溶液中,铁钉表面变红
D.硫在空气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体
4.下列说法正确的是
A.黄铜的硬度比纯铜的硬度小 B.催化剂只能加快化学反应速率
C.活性炭吸附可降低水的硬度 D.溶液一定是混合物
5.向200.0gAgNO3溶液中加入mgAl和Cu的混合粉末,搅拌,充分反应后过滤、洗涤、干燥得到32.4g固体。向滤液中再次插入洁净光亮的细铜丝,铜丝表面产生银白色物质。下列说法正确的是
A.m的值可能为8.0 B.向过滤所得固体中加入稀盐酸可能会有气体生成
C.滤液的质量为167.6g D.原AgNO3溶液的溶质质量分数是25.5%
6.实验室现有硝酸银和硝酸铜的混合溶液,现要对其进行处理和回收。将过量的铁屑加入废液中,充分反应后过滤,得到滤液和滤渣。下列说法不正确的是
A.滤渣中一定有铁、铜、银 B.滤渣中一定有铜和银,可能含有铁
C.滤液中一定含有硝酸亚铁 D.滤液中一定没有硝酸铜和硝酸银
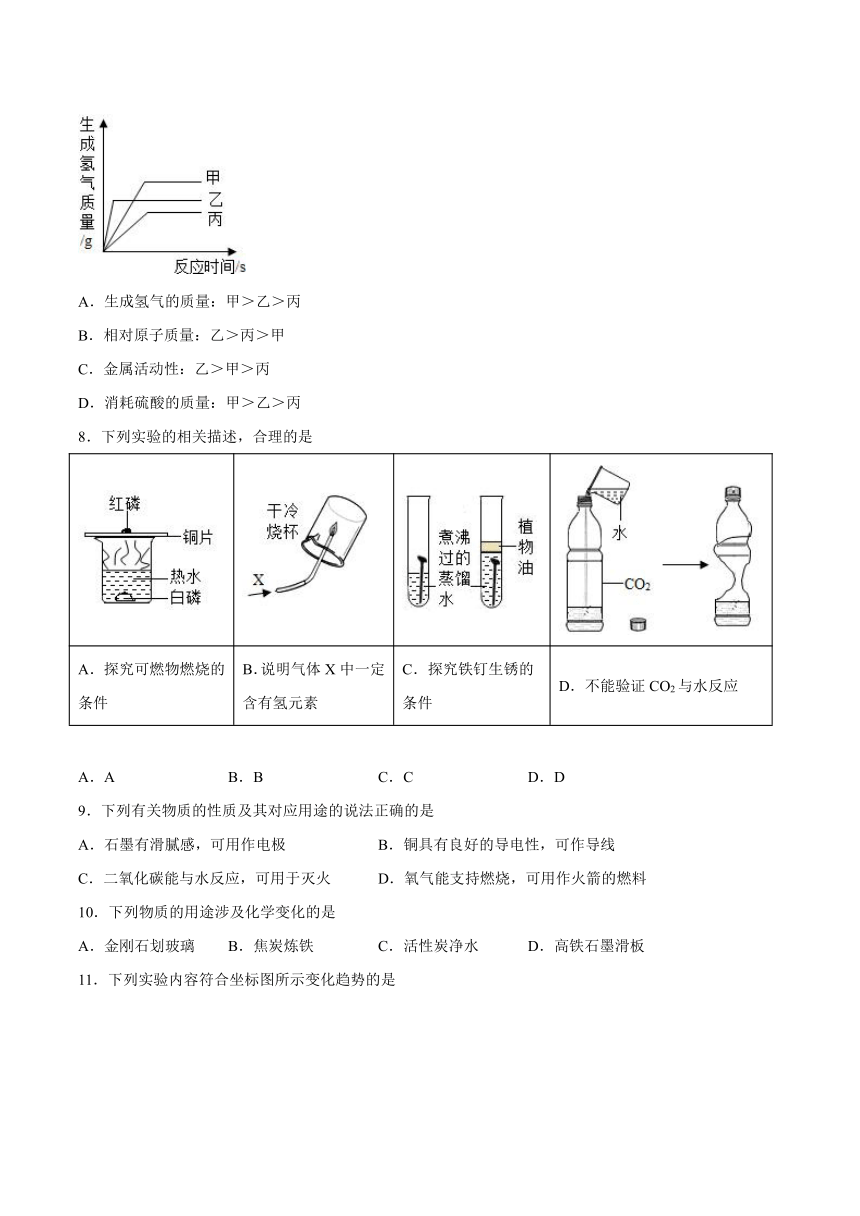
7.现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是
A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
8.下列实验的相关描述,合理的是
A.探究可燃物燃烧的条件 B.说明气体X中一定含有氢元素 C.探究铁钉生锈的条件 D.不能验证CO2与水反应
A.A B.B C.C D.D
9.下列有关物质的性质及其对应用途的说法正确的是
A.石墨有滑腻感,可用作电极 B.铜具有良好的导电性,可作导线
C.二氧化碳能与水反应,可用于灭火 D.氧气能支持燃烧,可用作火箭的燃料
10.下列物质的用途涉及化学变化的是
A.金刚石划玻璃 B.焦炭炼铁 C.活性炭净水 D.高铁石墨滑板
11.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
二、简答题
12.室温下足量镁片、铝片(已去除氧化膜)分别与40g溶质质量分数为7.3%的稀盐酸反应,用数据采集器测得装置内压强随时间的变化关系图(见如图)。
已知:相同温度下,装置内压强与产生气体的体积成正比。
(1)根据图乙可知,充分反应后产生氢气的质量:Mg______Al(填“>”、“<”或“=”)。
(2)计算镁片与稀盐酸反应产生氢气的质量(写出计算过程)。
(3)曲线BC段下降的原因是______。
三、推断题
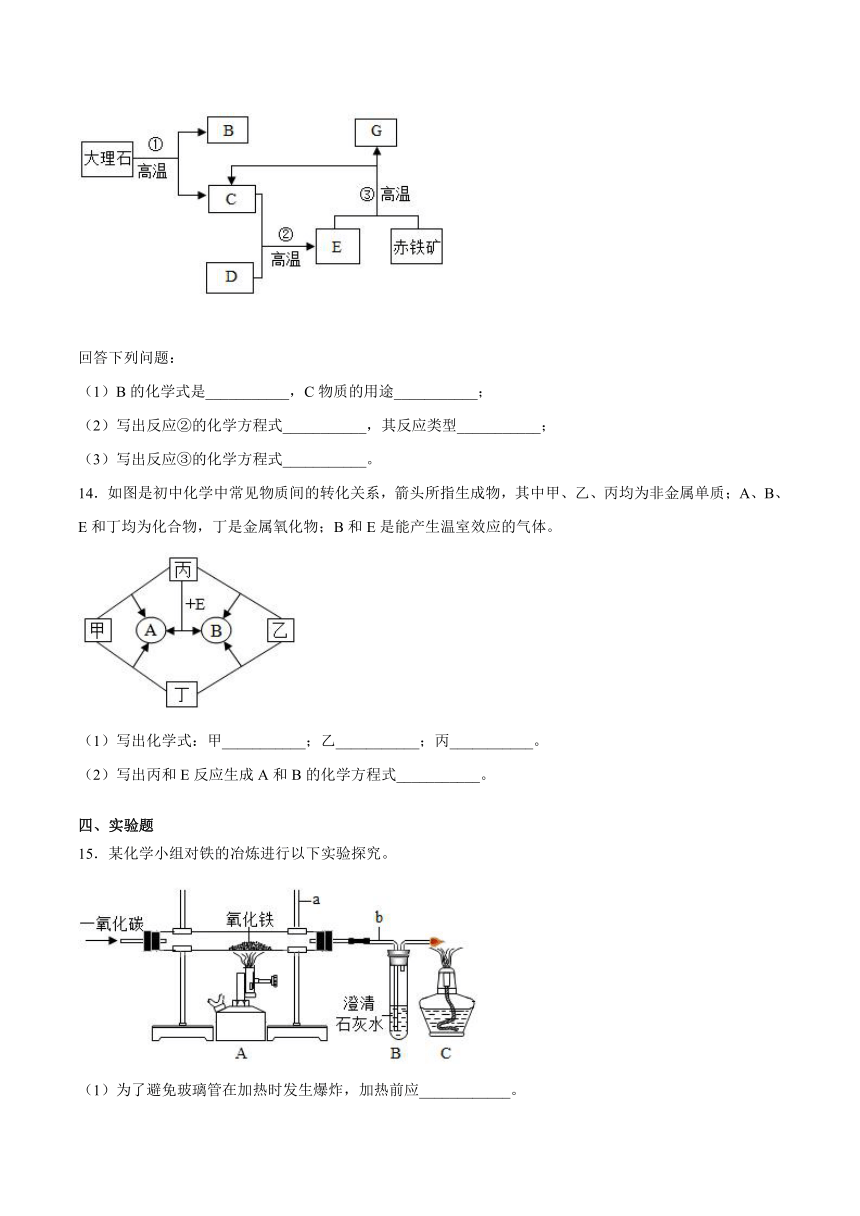
13.工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如下图所示,已知D、G为单质。
回答下列问题:
(1)B的化学式是___________,C物质的用途___________;
(2)写出反应②的化学方程式___________,其反应类型___________;
(3)写出反应③的化学方程式___________。
14.如图是初中化学中常见物质间的转化关系,箭头所指生成物,其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物,丁是金属氧化物;B和E是能产生温室效应的气体。
(1)写出化学式:甲___________;乙___________;丙___________。
(2)写出丙和E反应生成A和B的化学方程式___________。
四、实验题
15.某化学小组对铁的冶炼进行以下实验探究。
(1)为了避免玻璃管在加热时发生爆炸,加热前应____________。
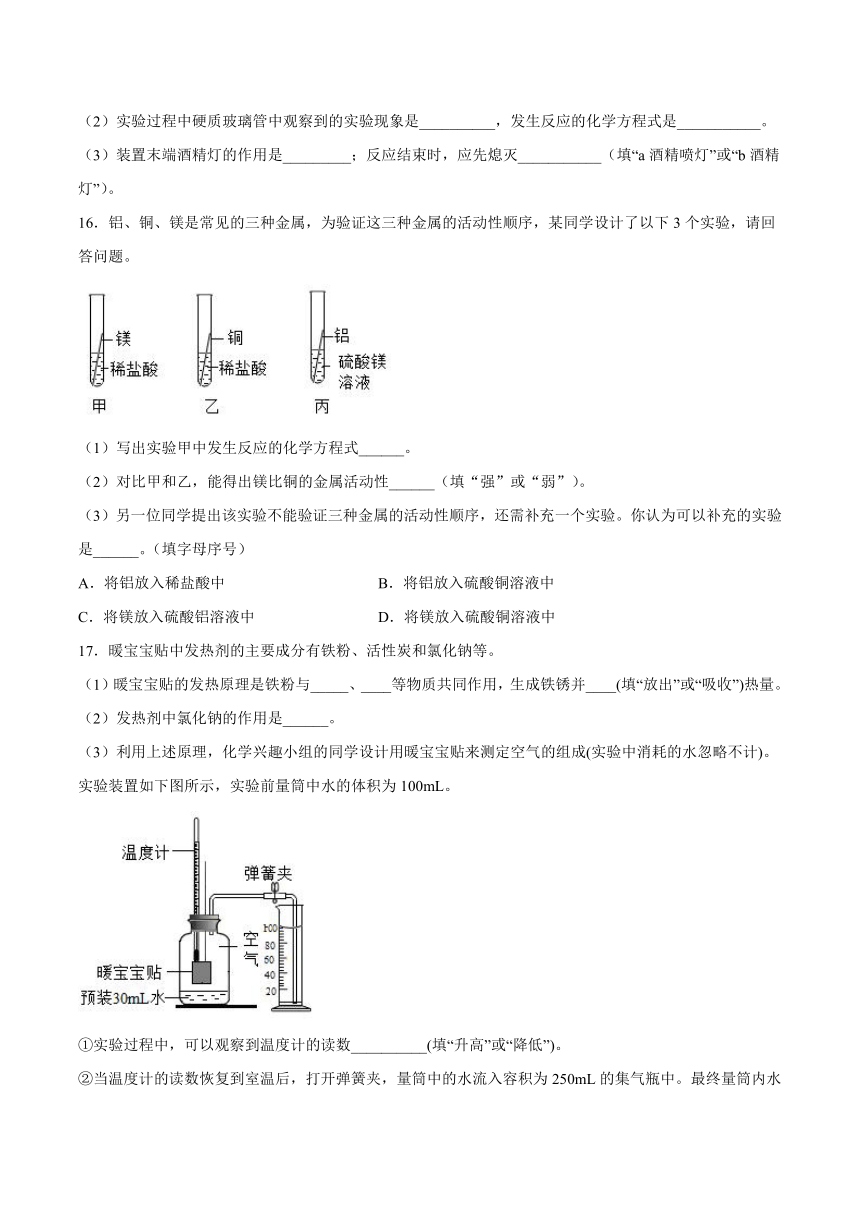
(2)实验过程中硬质玻璃管中观察到的实验现象是__________,发生反应的化学方程式是___________。
(3)装置末端酒精灯的作用是_________;反应结束时,应先熄灭___________(填“a酒精喷灯”或“b酒精灯”)。
16.铝、铜、镁是常见的三种金属,为验证这三种金属的活动性顺序,某同学设计了以下3个实验,请回答问题。
(1)写出实验甲中发生反应的化学方程式______。
(2)对比甲和乙,能得出镁比铜的金属活动性______(填“强”或“弱”)。
(3)另一位同学提出该实验不能验证三种金属的活动性顺序,还需补充一个实验。你认为可以补充的实验是______。(填字母序号)
A.将铝放入稀盐酸中 B.将铝放入硫酸铜溶液中
C.将镁放入硫酸铝溶液中 D.将镁放入硫酸铜溶液中
17.暖宝宝贴中发热剂的主要成分有铁粉、活性炭和氯化钠等。
(1)暖宝宝贴的发热原理是铁粉与_____、____等物质共同作用,生成铁锈并____(填“放出”或“吸收”)热量。
(2)发热剂中氯化钠的作用是______。
(3)利用上述原理,化学兴趣小组的同学设计用暖宝宝贴来测定空气的组成(实验中消耗的水忽略不计)。实验装置如下图所示,实验前量筒中水的体积为100mL。
①实验过程中,可以观察到温度计的读数__________(填“升高”或“降低”)。
②当温度计的读数恢复到室温后,打开弹簧夹,量筒中的水流入容积为250mL的集气瓶中。最终量筒内水的读数为45mL,则该实验测得空气中氧气的体积分数为______。
③上述结果与理论值相比,造成误差的原因可能是_____________(填标号)。
A.装置漏气 B.暖宝宝贴量不足 C.暖宝宝贴过量
D.最终读取量筒中剩余水的体积时俯视读数 E.最终读取量筒中剩余水的体积时仰视读数
五、计算题
18.铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的稀硫酸,充分反应后所得数据如下表。
项 目 第1次 第2次 第3次 第4次 第5次
加入稀硫酸的质量/g 5 5 5 5 5
每次产生气体的质量/g 0.01 0.01 0.01 0.005 m
请根据相关信息回答问题:(反应的化学方程式为:Fe+H2SO4═FeSO4 +H2↑)
(1)表中m的数值为______;
(2)铜粉中混有铁粉的质量是______g(保留两位小数);
(3)求稀硫酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
19.为了测定某铁合金样品中铁的含量,小樱同学取该样品11.5g,加入100g稀硫酸,充分反应后,称量得到的剩余物质总质量为111.1g,已知铁合金中的其他成分不与酸反应,且难溶于水。求:
(1)生成氢气的质量为___________g。
(2)该铁合金样品中铁的质量分数。(结果保留到小数点后一位)
20.为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取10g合金于烧杯中,将40g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 第二次 第三次 第四次
加入稀盐酸的质量(g) 10 10 10 10
烧杯中剩余物的质量(g) 19.96 29.92 39.90 49.90
(1)充分反应后产生气体的总质量______g。
(2)该铜、锌合金中铜的质量分数为多少?(写出计算过程)
参考答案
1.C 2.A 3.C 4.D 5.A 6.B 7.B 8.D 9.B 10.B 11.B 12.
(1)=
(2)设镁与稀盐酸反应产生氢气的质量为x
x=0.08g;
故镁片与稀盐酸反应产生氢气的质量为0.08g。
(3)热量散失
13.
(1) CaO 可以用来灭火
(2) CO2+C2CO 化合反应
(3)3CO+Fe2O3 2Fe+3CO2
14.
(1) H2 C O2
(2)
15.
(1)检验气体纯度,并且先通入一氧化碳排出装置中空气后再加热
(2) 红色固体逐渐变黑色
(3) 点燃一氧化碳,防止一氧化碳污染空气 a酒精喷灯
16.
(1)
(2)强
(3)AB
17.
(1) 氧气 水 放出
(2)加速铁粉生锈,更快放出热量
(3) 升高 25% E
18.
(1)0
(2)产生气体的总质量为:0.01g+0.01g+0.01g+0.005g=0.035g
解:设铜粉中混有铁粉的质量为x
x=0.98g
答:铜粉中混有铁粉的质量是0.98g
(3)解:设稀硫酸中溶质的质量分数为y
y=9.8%
答:稀硫酸中溶质的质量分数为9.8%
19.
(1)0.4
(2)设:铁的质量为x
答:铁合金样品中铁的质量分数为97.4%。
20.
(1)0.10
(2)解:设10克铜锌合金中锌的质量为x
x=3.25g
答:铜锌合金中铜的质量分数为67.5%。
一、单选题
1.将一定量铁粉置于AgNO3和Mg(NO3)2混合溶液中,充分反应完毕后,过滤所得滤液中一定含有的金属阳离子是
A.Fe3+、Mg2+ B.Mg2+ C.Fe2+、Mg2+ D.Fe2+、Mg2+、Ag+
2.中国诗词既蕴含人文思想,又焕发理性光辉。诗句“何意百炼钢,化为绕指柔”提到了古代将生铁煅烧捶打氧化变成钢的过程,下列化学解释不合理的是
A.生铁和钢是同种物质 B.煅打过程发生碳燃烧反应
C.钢的机械性能比生铁好 D.生铁和钢都是铁的合金
3.下列实验现象,描述正确的是
A.红热的铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.用火柴去点蜡烛刚熄灭时产生的白烟,蜡烛不能重新燃烧
C.将光亮的铁钉放入硫酸铜溶液中,铁钉表面变红
D.硫在空气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体
4.下列说法正确的是
A.黄铜的硬度比纯铜的硬度小 B.催化剂只能加快化学反应速率
C.活性炭吸附可降低水的硬度 D.溶液一定是混合物
5.向200.0gAgNO3溶液中加入mgAl和Cu的混合粉末,搅拌,充分反应后过滤、洗涤、干燥得到32.4g固体。向滤液中再次插入洁净光亮的细铜丝,铜丝表面产生银白色物质。下列说法正确的是
A.m的值可能为8.0 B.向过滤所得固体中加入稀盐酸可能会有气体生成
C.滤液的质量为167.6g D.原AgNO3溶液的溶质质量分数是25.5%
6.实验室现有硝酸银和硝酸铜的混合溶液,现要对其进行处理和回收。将过量的铁屑加入废液中,充分反应后过滤,得到滤液和滤渣。下列说法不正确的是
A.滤渣中一定有铁、铜、银 B.滤渣中一定有铜和银,可能含有铁
C.滤液中一定含有硝酸亚铁 D.滤液中一定没有硝酸铜和硝酸银
7.现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是
A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
8.下列实验的相关描述,合理的是
A.探究可燃物燃烧的条件 B.说明气体X中一定含有氢元素 C.探究铁钉生锈的条件 D.不能验证CO2与水反应
A.A B.B C.C D.D
9.下列有关物质的性质及其对应用途的说法正确的是
A.石墨有滑腻感,可用作电极 B.铜具有良好的导电性,可作导线
C.二氧化碳能与水反应,可用于灭火 D.氧气能支持燃烧,可用作火箭的燃料
10.下列物质的用途涉及化学变化的是
A.金刚石划玻璃 B.焦炭炼铁 C.活性炭净水 D.高铁石墨滑板
11.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
二、简答题
12.室温下足量镁片、铝片(已去除氧化膜)分别与40g溶质质量分数为7.3%的稀盐酸反应,用数据采集器测得装置内压强随时间的变化关系图(见如图)。
已知:相同温度下,装置内压强与产生气体的体积成正比。
(1)根据图乙可知,充分反应后产生氢气的质量:Mg______Al(填“>”、“<”或“=”)。
(2)计算镁片与稀盐酸反应产生氢气的质量(写出计算过程)。
(3)曲线BC段下降的原因是______。
三、推断题
13.工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如下图所示,已知D、G为单质。
回答下列问题:
(1)B的化学式是___________,C物质的用途___________;
(2)写出反应②的化学方程式___________,其反应类型___________;
(3)写出反应③的化学方程式___________。
14.如图是初中化学中常见物质间的转化关系,箭头所指生成物,其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物,丁是金属氧化物;B和E是能产生温室效应的气体。
(1)写出化学式:甲___________;乙___________;丙___________。
(2)写出丙和E反应生成A和B的化学方程式___________。
四、实验题
15.某化学小组对铁的冶炼进行以下实验探究。
(1)为了避免玻璃管在加热时发生爆炸,加热前应____________。
(2)实验过程中硬质玻璃管中观察到的实验现象是__________,发生反应的化学方程式是___________。
(3)装置末端酒精灯的作用是_________;反应结束时,应先熄灭___________(填“a酒精喷灯”或“b酒精灯”)。
16.铝、铜、镁是常见的三种金属,为验证这三种金属的活动性顺序,某同学设计了以下3个实验,请回答问题。
(1)写出实验甲中发生反应的化学方程式______。
(2)对比甲和乙,能得出镁比铜的金属活动性______(填“强”或“弱”)。
(3)另一位同学提出该实验不能验证三种金属的活动性顺序,还需补充一个实验。你认为可以补充的实验是______。(填字母序号)
A.将铝放入稀盐酸中 B.将铝放入硫酸铜溶液中
C.将镁放入硫酸铝溶液中 D.将镁放入硫酸铜溶液中
17.暖宝宝贴中发热剂的主要成分有铁粉、活性炭和氯化钠等。
(1)暖宝宝贴的发热原理是铁粉与_____、____等物质共同作用,生成铁锈并____(填“放出”或“吸收”)热量。
(2)发热剂中氯化钠的作用是______。
(3)利用上述原理,化学兴趣小组的同学设计用暖宝宝贴来测定空气的组成(实验中消耗的水忽略不计)。实验装置如下图所示,实验前量筒中水的体积为100mL。
①实验过程中,可以观察到温度计的读数__________(填“升高”或“降低”)。
②当温度计的读数恢复到室温后,打开弹簧夹,量筒中的水流入容积为250mL的集气瓶中。最终量筒内水的读数为45mL,则该实验测得空气中氧气的体积分数为______。
③上述结果与理论值相比,造成误差的原因可能是_____________(填标号)。
A.装置漏气 B.暖宝宝贴量不足 C.暖宝宝贴过量
D.最终读取量筒中剩余水的体积时俯视读数 E.最终读取量筒中剩余水的体积时仰视读数
五、计算题
18.铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的稀硫酸,充分反应后所得数据如下表。
项 目 第1次 第2次 第3次 第4次 第5次
加入稀硫酸的质量/g 5 5 5 5 5
每次产生气体的质量/g 0.01 0.01 0.01 0.005 m
请根据相关信息回答问题:(反应的化学方程式为:Fe+H2SO4═FeSO4 +H2↑)
(1)表中m的数值为______;
(2)铜粉中混有铁粉的质量是______g(保留两位小数);
(3)求稀硫酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
19.为了测定某铁合金样品中铁的含量,小樱同学取该样品11.5g,加入100g稀硫酸,充分反应后,称量得到的剩余物质总质量为111.1g,已知铁合金中的其他成分不与酸反应,且难溶于水。求:
(1)生成氢气的质量为___________g。
(2)该铁合金样品中铁的质量分数。(结果保留到小数点后一位)
20.为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取10g合金于烧杯中,将40g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 第二次 第三次 第四次
加入稀盐酸的质量(g) 10 10 10 10
烧杯中剩余物的质量(g) 19.96 29.92 39.90 49.90
(1)充分反应后产生气体的总质量______g。
(2)该铜、锌合金中铜的质量分数为多少?(写出计算过程)
参考答案
1.C 2.A 3.C 4.D 5.A 6.B 7.B 8.D 9.B 10.B 11.B 12.
(1)=
(2)设镁与稀盐酸反应产生氢气的质量为x
x=0.08g;
故镁片与稀盐酸反应产生氢气的质量为0.08g。
(3)热量散失
13.
(1) CaO 可以用来灭火
(2) CO2+C2CO 化合反应
(3)3CO+Fe2O3 2Fe+3CO2
14.
(1) H2 C O2
(2)
15.
(1)检验气体纯度,并且先通入一氧化碳排出装置中空气后再加热
(2) 红色固体逐渐变黑色
(3) 点燃一氧化碳,防止一氧化碳污染空气 a酒精喷灯
16.
(1)
(2)强
(3)AB
17.
(1) 氧气 水 放出
(2)加速铁粉生锈,更快放出热量
(3) 升高 25% E
18.
(1)0
(2)产生气体的总质量为:0.01g+0.01g+0.01g+0.005g=0.035g
解:设铜粉中混有铁粉的质量为x
x=0.98g
答:铜粉中混有铁粉的质量是0.98g
(3)解:设稀硫酸中溶质的质量分数为y
y=9.8%
答:稀硫酸中溶质的质量分数为9.8%
19.
(1)0.4
(2)设:铁的质量为x
答:铁合金样品中铁的质量分数为97.4%。
20.
(1)0.10
(2)解:设10克铜锌合金中锌的质量为x
x=3.25g
答:铜锌合金中铜的质量分数为67.5%。
