第10章金属检测题-2021-2022学年九年级化学京改版下册(word版有答案)
文档属性
| 名称 | 第10章金属检测题-2021-2022学年九年级化学京改版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 173.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-07 00:00:00 | ||
图片预览



文档简介
第10章《金属》检测题
一、单选题
1.下列描述与事实相符合的是
A.细铁丝伸入盛有空气的集气瓶中剧烈燃烧、火星四射
B.铜丝插入稀硫酸中,溶液由无色变为蓝色
C.镁带在空气中燃烧,发出耀眼的白光,生成白色固体
D.电解水实验,电源正极产生的气体燃烧时会发出淡蓝色火焰
2.下列说法正确的是
A.含有两种元素的物质一定是化合物
B.石蜡燃烧的过程中一定发生了物理变化
C.将带火星的木条伸入集气瓶中,用来检验氧气是否收满
D.活泼金属能与稀硫酸反应放出气体,能与稀硫酸反应放出气体的物质一定是活泼金属
3.下列实验现象的描述错误的是
A.铁丝在氧气中燃烧发出白光,生成白色固体
B.把铁粉放入稀硫酸中可以看到有气泡产生,溶液逐渐由无色变为浅绿色
C.将铜片在空气中加热,表面逐渐变黑
D.镁带在空气中燃烧,发出耀眼白光,生成白色固体
4.下列关于实验现象描述,正确的是
A.黄铜和铜互相刻画时,铜表面会出现划痕
B.双氧水和二氧化锰制氧气时黑色固体逐渐消失
C.电解水时正极生成的气体燃烧,产生淡蓝色火焰
D.红磷在空气中燃烧,产生大量白雾
5.生活离不开厨房、下列与厨房有关的说法不正确的是
A.洗洁精洗去油污是利用了乳化原理 B.油锅着火可以迅速用锅盖盖灭
C.家庭中用蒸馏的方法降低水的硬度 D.铝锅不宜用钢丝球擦洗
6.实验室现有硝酸银和硝酸铜的混合溶液,现要对其进行处理和回收。将过量的铁屑加入废液中,充分反应后过滤,得到滤液和滤渣。下列说法不正确的是
A.滤渣中一定有铁、铜、银 B.滤渣中一定有铜和银,可能含有铁
C.滤液中一定含有硝酸亚铁 D.滤液中一定没有硝酸铜和硝酸银
7.有x y z三种金属,如果把x和z分别放人稀硫酸中,x溶解并产生氢气,而z不反应;如果把y和z分别放入硝酸银溶液中,过一会儿,在z表面有银析出,而y没有变化。根据以上实验事实,判断x y和z的金属活动顺序正确的是
A.xyz B.xzy C.zyx D.zxy
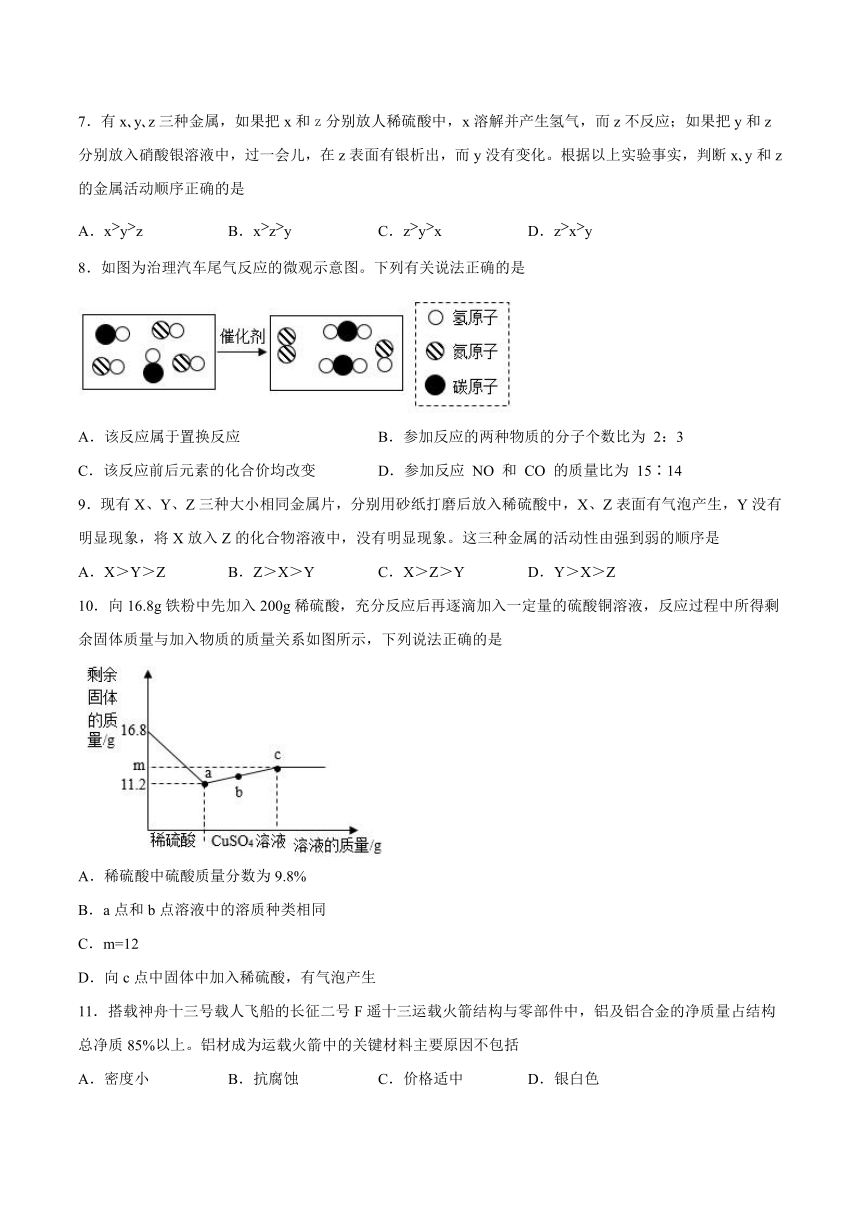
8.如图为治理汽车尾气反应的微观示意图。下列有关说法正确的是
A.该反应属于置换反应 B.参加反应的两种物质的分子个数比为 2:3
C.该反应前后元素的化合价均改变 D.参加反应 NO 和 CO 的质量比为 15∶14
9.现有X、Y、Z三种大小相同金属片,分别用砂纸打磨后放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,将X放入Z的化合物溶液中,没有明显现象。这三种金属的活动性由强到弱的顺序是
A.X>Y>Z B.Z>X>Y C.X>Z>Y D.Y>X>Z
10.向16.8g铁粉中先加入200g稀硫酸,充分反应后再逐滴加入一定量的硫酸铜溶液,反应过程中所得剩余固体质量与加入物质的质量关系如图所示,下列说法正确的是
A.稀硫酸中硫酸质量分数为9.8%
B.a点和b点溶液中的溶质种类相同
C.m=12
D.向c点中固体中加入稀硫酸,有气泡产生
11.搭载神舟十三号载人飞船的长征二号F遥十三运载火箭结构与零部件中,铝及铝合金的净质量占结构总净质85%以上。铝材成为运载火箭中的关键材料主要原因不包括
A.密度小 B.抗腐蚀 C.价格适中 D.银白色
12.下列实验数据可用图表示的是
A.加热高锰酸钾制取氧气;Y轴表示产生气体的质量
B.往澄清石灰水中通入 CO2;Y轴表示生成沉淀质量
C.向生铁中慢慢加入足量的稀硫酸;Y轴表示剩余固体的质量
D.高温灼烧氧化铁和足量炭粉的混合物;Y轴表示剩余固体中氧元素的质量
二、简答题
13.随着人们生活水平的提高,汽车已经走进了千家万户,成为许多家庭的代步工具。也许你的家庭就拥有一台不错的轿车,那就请根据你对汽车的了解及所学的化学知识回答下列问题:
(1)新能源电动汽车采用的电池为高铁蓄电池,其在行驶过程中能量转化是______。
(2)车体多用钢材制造,钢材生锈是铁与空气中的氧气、水蒸气等反应的结果,可以采取______的方法来防止钢材生锈。
(3)叠氮化钠{NaN3}被广泛应用于汽车气囊。制备工业级NaN3如下:将NaN2与N2O气体反应可生成NaN3、NaOH和溶于水呈碱性的刺激性气味气体,该反应的化学方程式是______。反应前氮元素的化合价分别为______。
14.生活中处处是化学,请用所学过的化学知识回答下列问题。
(1)在铁制品表面涂油刷漆等都能防止铁生锈,其原理是什么?
(2)金刚石和石墨都是碳元素组成的单质,但二者的物理性质差异却非常大,其原因是什么?
三、推断题
15.下图是初中化学中一些常见物质之间的转化(部分生成物已省路):其中A、C是无色气体,B、F是红色固体。
请回答问题:
(1)写出B的化学式_________,x溶液的名称_________(写一个即可)。
(2)反应①的现象___________,该反应在工业上常用于__________。
(3)反应③的化学方程式_________。
16.A~H是初中化学常见的物质,其中F是大理石的主要成分,A和D是气体,B是红棕色固体,它们之间的转化关系如图所示。请回答下列问题:
(1)F的化学式为_______。
(2)反应③属于基本反应类型________。
(3)反应④________(选填“放出”或“吸收”)热量。
(4)反应①的化学方程式为__________。
17.有A、B、C、D、E、F、N、M八种物质,其中A为一种应用最广泛的金属,B由三种元素组成,C、D为单质且C为红色金属,D为黑色固体。它们之间有如下转化关系:①A + MB + C;②A + NB + H2↑;③A +O2F;④D + FA + CO2↑;⑤D+CO2E;⑥E + FA + CO2↑。请回答下列问题
(1)E的用途__________;M为蓝色溶液,则其中含有的金属阳离子是_______(填化学符号)。
(2)用化学方程式表示下列转化,并填空:
①A + MB + C _________;
②A + NB + H2↑ __________,观察到的现象是__________。
③D + FA + CO2↑_________,其反应的基本类型是_________。
四、实验题
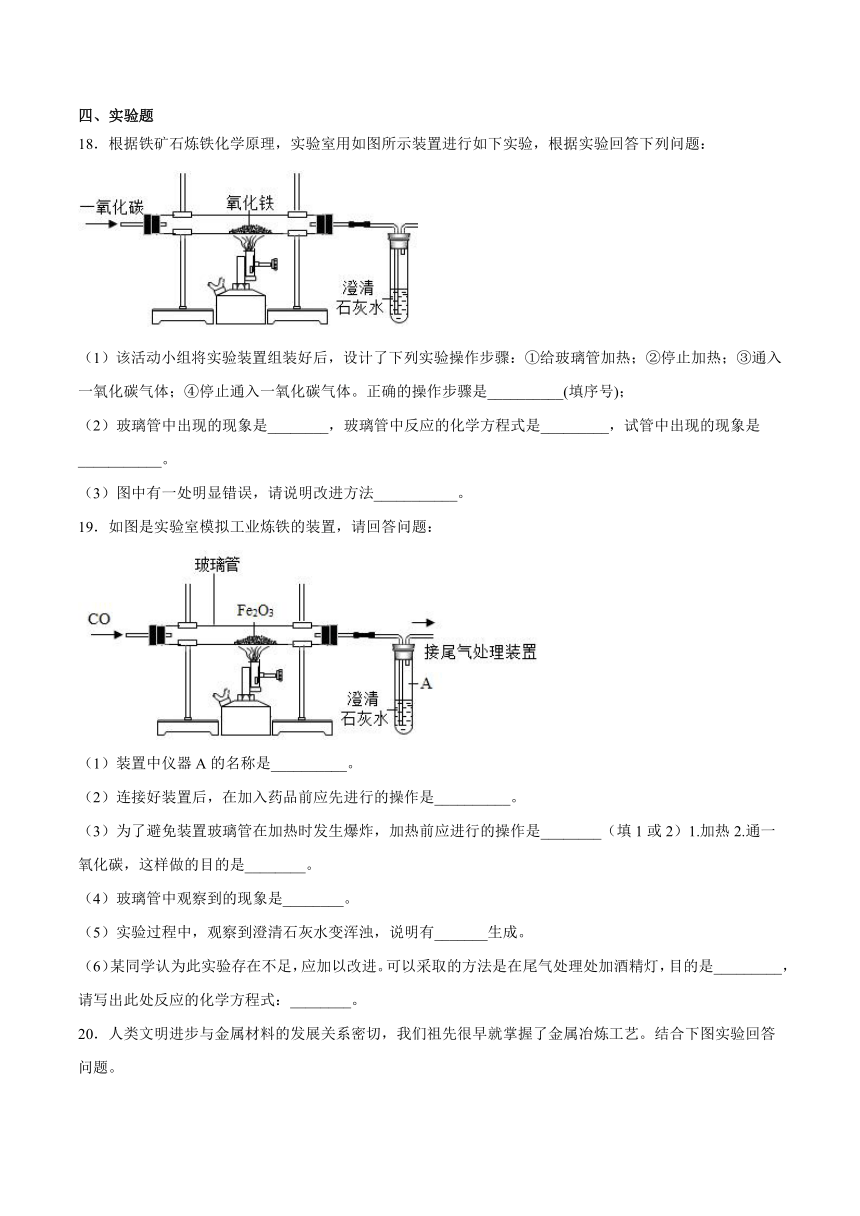
18.根据铁矿石炼铁化学原理,实验室用如图所示装置进行如下实验,根据实验回答下列问题:
(1)该活动小组将实验装置组装好后,设计了下列实验操作步骤:①给玻璃管加热;②停止加热;③通入一氧化碳气体;④停止通入一氧化碳气体。正确的操作步骤是__________(填序号);
(2)玻璃管中出现的现象是________,玻璃管中反应的化学方程式是_________,试管中出现的现象是___________。
(3)图中有一处明显错误,请说明改进方法___________。
19.如图是实验室模拟工业炼铁的装置,请回答问题:
(1)装置中仪器A的名称是__________。
(2)连接好装置后,在加入药品前应先进行的操作是__________。
(3)为了避免装置玻璃管在加热时发生爆炸,加热前应进行的操作是________(填1或2)1.加热2.通一氧化碳,这样做的目的是________。
(4)玻璃管中观察到的现象是________。
(5)实验过程中,观察到澄清石灰水变浑浊,说明有_______生成。
(6)某同学认为此实验存在不足,应加以改进。可以采取的方法是在尾气处理处加酒精灯,目的是_________,请写出此处反应的化学方程式:________。
20.人类文明进步与金属材料的发展关系密切,我们祖先很早就掌握了金属冶炼工艺。结合下图实验回答问题。
(1)图1实验结束时要先将导管移出试管,再停止加热,目的是___________。
(2)图2实验硬质玻璃管中反应的化学方程式为___________。
(3)下列关于图中两个实验的说法正确的有___________(填字母序号)。
A.两实验中酒精灯①、②加网罩的作用是使火焰集中,提高温度
B.加热过程中均出现黑色固体变为红色的实验现象
C.加热过程中均出现澄清石灰水变浑浊的实验现象
D.两实验中均发生了置换反应
E.两实验中均发生了金属氧化物还原反应
五、计算题
21.将13克的锌粒放入87.4克的稀盐酸中,当锌粒完全反应后:
(1)最多可以放出多少克的氢气?
(2)盐酸溶液中溶质的质量分数是多少?
22.古玩市场惊现“三星堆”遗址出土的同款假黄金面具。
(查阅资料)(1)铜锌合金(又称:假黄金)外观和黄金相似,常被不法商贩以假乱真。
(2)标准状况下,氢气密度
为进一步定量分析黄金面具中金属锌的质量分数,小明同学利用下图设计了如下实验::
(1)按图所示组装实验装置,并检查装置的气密性。
(2)向锥形瓶中加入5.0g黄金面具样品,注射器中吸入25mL稀硫酸。
(3)将注射器中的稀硫酸平均分5次推入锥形瓶中:每次推入稀硫酸、待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响),如下表。
次数 第1次 第2次 第3次 第4次 第5次
收集气体的总体积/mL 200 400 515 x 525
(1)上表中的数据x=___________
(2)分析数据,完全反应后生成氢气的体积V=___________mL
(数据处理)
(3)此黄金面具中锌的质量分数___________(写出计算过程)
23.中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。利用此原理,向160kg含硫酸铜的废液中加入足量的铁粉,得到金属铜6.4kg。请计算废液中硫酸铜的溶质质量分数。
参考答案
1.C 2.B 3.A 4.A 5.C 6.B 7.B 8.D 9.B 10.B 11.D 12.D 13.
(1)化学能→电能→机械能
(2)刷油漆
(3) -3,+1
14.
(1)隔绝水和氧气
(2)碳原子的排序不同
15.
(1) Fe2O3 硫酸铜溶液
(2) 红棕色固体逐渐变黑 炼铁
(3)
16.
(1)CaCO3
(2)分解反应
(3)放出
(4)
17.
(1) 在冶金工业中作还原剂或做气体燃料 Cu2+
(2) Fe+CuSO4=FeSO4+Cu Fe+H2SO4=FeSO4+H2↑ 有气泡产生,溶液由无色变浅绿色
置换反应
18.
(1)③①②④
(2) 固体由红棕色变成黑色 Fe2O3+3CO2Fe+3CO2 澄清石灰水变浑浊
(3)尾气点燃或收集
19.
(1)试管
(2)检查装置的气密性
(3) 2 排除空气,以防止爆炸
(4)红色粉末逐渐变成黑色
(5)二氧化碳CO2
(6) 因为一氧化碳有毒,防止扩散到空中污染空气
20.
(1)防止澄清石灰水倒流入热的试管,使试管炸裂
(2)
(3)ACE
21.
(1)设最多可以放出的氢气的质量为x
故最多可以放出0.4克的氢气。
(2)设参加反应的盐酸的质量为y
故盐酸溶液中溶质的质量分数是。
22.
(1)520
(2)500
(3)解:生成氢气的质量=500mL×0.09g/L=0.045g
设黄金面具中锌的质量为x
=
x=1.4625g
此黄金面具中锌的质量分数=×100%=29.25%
答:此黄金面具中锌的质量分数为29.25%。
23.解:设废液中硫酸铜的质量为x
x=16kg
废液中硫酸铜的质量分数为
答:废液中含硫酸铜的溶质质量分数为10%。
一、单选题
1.下列描述与事实相符合的是
A.细铁丝伸入盛有空气的集气瓶中剧烈燃烧、火星四射
B.铜丝插入稀硫酸中,溶液由无色变为蓝色
C.镁带在空气中燃烧,发出耀眼的白光,生成白色固体
D.电解水实验,电源正极产生的气体燃烧时会发出淡蓝色火焰
2.下列说法正确的是
A.含有两种元素的物质一定是化合物
B.石蜡燃烧的过程中一定发生了物理变化
C.将带火星的木条伸入集气瓶中,用来检验氧气是否收满
D.活泼金属能与稀硫酸反应放出气体,能与稀硫酸反应放出气体的物质一定是活泼金属
3.下列实验现象的描述错误的是
A.铁丝在氧气中燃烧发出白光,生成白色固体
B.把铁粉放入稀硫酸中可以看到有气泡产生,溶液逐渐由无色变为浅绿色
C.将铜片在空气中加热,表面逐渐变黑
D.镁带在空气中燃烧,发出耀眼白光,生成白色固体
4.下列关于实验现象描述,正确的是
A.黄铜和铜互相刻画时,铜表面会出现划痕
B.双氧水和二氧化锰制氧气时黑色固体逐渐消失
C.电解水时正极生成的气体燃烧,产生淡蓝色火焰
D.红磷在空气中燃烧,产生大量白雾
5.生活离不开厨房、下列与厨房有关的说法不正确的是
A.洗洁精洗去油污是利用了乳化原理 B.油锅着火可以迅速用锅盖盖灭
C.家庭中用蒸馏的方法降低水的硬度 D.铝锅不宜用钢丝球擦洗
6.实验室现有硝酸银和硝酸铜的混合溶液,现要对其进行处理和回收。将过量的铁屑加入废液中,充分反应后过滤,得到滤液和滤渣。下列说法不正确的是
A.滤渣中一定有铁、铜、银 B.滤渣中一定有铜和银,可能含有铁
C.滤液中一定含有硝酸亚铁 D.滤液中一定没有硝酸铜和硝酸银
7.有x y z三种金属,如果把x和z分别放人稀硫酸中,x溶解并产生氢气,而z不反应;如果把y和z分别放入硝酸银溶液中,过一会儿,在z表面有银析出,而y没有变化。根据以上实验事实,判断x y和z的金属活动顺序正确的是
A.xyz B.xzy C.zyx D.zxy
8.如图为治理汽车尾气反应的微观示意图。下列有关说法正确的是
A.该反应属于置换反应 B.参加反应的两种物质的分子个数比为 2:3
C.该反应前后元素的化合价均改变 D.参加反应 NO 和 CO 的质量比为 15∶14
9.现有X、Y、Z三种大小相同金属片,分别用砂纸打磨后放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,将X放入Z的化合物溶液中,没有明显现象。这三种金属的活动性由强到弱的顺序是
A.X>Y>Z B.Z>X>Y C.X>Z>Y D.Y>X>Z
10.向16.8g铁粉中先加入200g稀硫酸,充分反应后再逐滴加入一定量的硫酸铜溶液,反应过程中所得剩余固体质量与加入物质的质量关系如图所示,下列说法正确的是
A.稀硫酸中硫酸质量分数为9.8%
B.a点和b点溶液中的溶质种类相同
C.m=12
D.向c点中固体中加入稀硫酸,有气泡产生
11.搭载神舟十三号载人飞船的长征二号F遥十三运载火箭结构与零部件中,铝及铝合金的净质量占结构总净质85%以上。铝材成为运载火箭中的关键材料主要原因不包括
A.密度小 B.抗腐蚀 C.价格适中 D.银白色
12.下列实验数据可用图表示的是
A.加热高锰酸钾制取氧气;Y轴表示产生气体的质量
B.往澄清石灰水中通入 CO2;Y轴表示生成沉淀质量
C.向生铁中慢慢加入足量的稀硫酸;Y轴表示剩余固体的质量
D.高温灼烧氧化铁和足量炭粉的混合物;Y轴表示剩余固体中氧元素的质量
二、简答题
13.随着人们生活水平的提高,汽车已经走进了千家万户,成为许多家庭的代步工具。也许你的家庭就拥有一台不错的轿车,那就请根据你对汽车的了解及所学的化学知识回答下列问题:
(1)新能源电动汽车采用的电池为高铁蓄电池,其在行驶过程中能量转化是______。
(2)车体多用钢材制造,钢材生锈是铁与空气中的氧气、水蒸气等反应的结果,可以采取______的方法来防止钢材生锈。
(3)叠氮化钠{NaN3}被广泛应用于汽车气囊。制备工业级NaN3如下:将NaN2与N2O气体反应可生成NaN3、NaOH和溶于水呈碱性的刺激性气味气体,该反应的化学方程式是______。反应前氮元素的化合价分别为______。
14.生活中处处是化学,请用所学过的化学知识回答下列问题。
(1)在铁制品表面涂油刷漆等都能防止铁生锈,其原理是什么?
(2)金刚石和石墨都是碳元素组成的单质,但二者的物理性质差异却非常大,其原因是什么?
三、推断题
15.下图是初中化学中一些常见物质之间的转化(部分生成物已省路):其中A、C是无色气体,B、F是红色固体。
请回答问题:
(1)写出B的化学式_________,x溶液的名称_________(写一个即可)。
(2)反应①的现象___________,该反应在工业上常用于__________。
(3)反应③的化学方程式_________。
16.A~H是初中化学常见的物质,其中F是大理石的主要成分,A和D是气体,B是红棕色固体,它们之间的转化关系如图所示。请回答下列问题:
(1)F的化学式为_______。
(2)反应③属于基本反应类型________。
(3)反应④________(选填“放出”或“吸收”)热量。
(4)反应①的化学方程式为__________。
17.有A、B、C、D、E、F、N、M八种物质,其中A为一种应用最广泛的金属,B由三种元素组成,C、D为单质且C为红色金属,D为黑色固体。它们之间有如下转化关系:①A + MB + C;②A + NB + H2↑;③A +O2F;④D + FA + CO2↑;⑤D+CO2E;⑥E + FA + CO2↑。请回答下列问题
(1)E的用途__________;M为蓝色溶液,则其中含有的金属阳离子是_______(填化学符号)。
(2)用化学方程式表示下列转化,并填空:
①A + MB + C _________;
②A + NB + H2↑ __________,观察到的现象是__________。
③D + FA + CO2↑_________,其反应的基本类型是_________。
四、实验题
18.根据铁矿石炼铁化学原理,实验室用如图所示装置进行如下实验,根据实验回答下列问题:
(1)该活动小组将实验装置组装好后,设计了下列实验操作步骤:①给玻璃管加热;②停止加热;③通入一氧化碳气体;④停止通入一氧化碳气体。正确的操作步骤是__________(填序号);
(2)玻璃管中出现的现象是________,玻璃管中反应的化学方程式是_________,试管中出现的现象是___________。
(3)图中有一处明显错误,请说明改进方法___________。
19.如图是实验室模拟工业炼铁的装置,请回答问题:
(1)装置中仪器A的名称是__________。
(2)连接好装置后,在加入药品前应先进行的操作是__________。
(3)为了避免装置玻璃管在加热时发生爆炸,加热前应进行的操作是________(填1或2)1.加热2.通一氧化碳,这样做的目的是________。
(4)玻璃管中观察到的现象是________。
(5)实验过程中,观察到澄清石灰水变浑浊,说明有_______生成。
(6)某同学认为此实验存在不足,应加以改进。可以采取的方法是在尾气处理处加酒精灯,目的是_________,请写出此处反应的化学方程式:________。
20.人类文明进步与金属材料的发展关系密切,我们祖先很早就掌握了金属冶炼工艺。结合下图实验回答问题。
(1)图1实验结束时要先将导管移出试管,再停止加热,目的是___________。
(2)图2实验硬质玻璃管中反应的化学方程式为___________。
(3)下列关于图中两个实验的说法正确的有___________(填字母序号)。
A.两实验中酒精灯①、②加网罩的作用是使火焰集中,提高温度
B.加热过程中均出现黑色固体变为红色的实验现象
C.加热过程中均出现澄清石灰水变浑浊的实验现象
D.两实验中均发生了置换反应
E.两实验中均发生了金属氧化物还原反应
五、计算题
21.将13克的锌粒放入87.4克的稀盐酸中,当锌粒完全反应后:
(1)最多可以放出多少克的氢气?
(2)盐酸溶液中溶质的质量分数是多少?
22.古玩市场惊现“三星堆”遗址出土的同款假黄金面具。
(查阅资料)(1)铜锌合金(又称:假黄金)外观和黄金相似,常被不法商贩以假乱真。
(2)标准状况下,氢气密度
为进一步定量分析黄金面具中金属锌的质量分数,小明同学利用下图设计了如下实验::
(1)按图所示组装实验装置,并检查装置的气密性。
(2)向锥形瓶中加入5.0g黄金面具样品,注射器中吸入25mL稀硫酸。
(3)将注射器中的稀硫酸平均分5次推入锥形瓶中:每次推入稀硫酸、待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响),如下表。
次数 第1次 第2次 第3次 第4次 第5次
收集气体的总体积/mL 200 400 515 x 525
(1)上表中的数据x=___________
(2)分析数据,完全反应后生成氢气的体积V=___________mL
(数据处理)
(3)此黄金面具中锌的质量分数___________(写出计算过程)
23.中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。利用此原理,向160kg含硫酸铜的废液中加入足量的铁粉,得到金属铜6.4kg。请计算废液中硫酸铜的溶质质量分数。
参考答案
1.C 2.B 3.A 4.A 5.C 6.B 7.B 8.D 9.B 10.B 11.D 12.D 13.
(1)化学能→电能→机械能
(2)刷油漆
(3) -3,+1
14.
(1)隔绝水和氧气
(2)碳原子的排序不同
15.
(1) Fe2O3 硫酸铜溶液
(2) 红棕色固体逐渐变黑 炼铁
(3)
16.
(1)CaCO3
(2)分解反应
(3)放出
(4)
17.
(1) 在冶金工业中作还原剂或做气体燃料 Cu2+
(2) Fe+CuSO4=FeSO4+Cu Fe+H2SO4=FeSO4+H2↑ 有气泡产生,溶液由无色变浅绿色
置换反应
18.
(1)③①②④
(2) 固体由红棕色变成黑色 Fe2O3+3CO2Fe+3CO2 澄清石灰水变浑浊
(3)尾气点燃或收集
19.
(1)试管
(2)检查装置的气密性
(3) 2 排除空气,以防止爆炸
(4)红色粉末逐渐变成黑色
(5)二氧化碳CO2
(6) 因为一氧化碳有毒,防止扩散到空中污染空气
20.
(1)防止澄清石灰水倒流入热的试管,使试管炸裂
(2)
(3)ACE
21.
(1)设最多可以放出的氢气的质量为x
故最多可以放出0.4克的氢气。
(2)设参加反应的盐酸的质量为y
故盐酸溶液中溶质的质量分数是。
22.
(1)520
(2)500
(3)解:生成氢气的质量=500mL×0.09g/L=0.045g
设黄金面具中锌的质量为x
=
x=1.4625g
此黄金面具中锌的质量分数=×100%=29.25%
答:此黄金面具中锌的质量分数为29.25%。
23.解:设废液中硫酸铜的质量为x
x=16kg
废液中硫酸铜的质量分数为
答:废液中含硫酸铜的溶质质量分数为10%。
