第11章酸与碱检测题-2021-2022学年九年级化学京改版下册(word版有答案)
文档属性
| 名称 | 第11章酸与碱检测题-2021-2022学年九年级化学京改版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 114.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-07 00:00:00 | ||
图片预览

文档简介
第11章《酸与碱》检测题
一、单选题
1.水是生命之源,下列“水”可以使石蕊溶液变红的是
A.蒸馏水 B.糖水 C.氨水 D.柠檬水
2.下列物质的用途中,利用了物质的物理性质的是
A.活性炭吸附 B.氮气做保护气 C.酒精做燃料 D.生石灰做干燥剂
3.下列实验操作符合规范要求的是
A.“实验室制取二氧化碳”实验中,先装入药品再检查装置的气密性
B.“粗盐提纯操作”中,在蒸发结晶时,用玻璃棒不断搅拌
C.“配制一定溶质质量分数的溶液”实验中,多余的药品应放回原瓶
D.“探究酸碱中和”实验中,测定溶液的pH时应先将试纸用蒸馏水湿润
4.下列物质的用途能体现其物理性质的是
A.氢氧化铝用作中和胃酸 B.钨丝用作灯泡的灯丝
C.铁粉用作食品保鲜吸氧剂 D.用石英砂等物质为原料制玻璃
5.下列对实验现象的描述错误的是
A.红磷在空气中燃烧,产生大量白烟
B.镁与稀盐酸反应产生大量气泡,放出热量
C.硫在氧气中燃烧发出明亮的蓝紫色火焰,生成刺激性气味的气体
D.干燥蓝色石蕊试纸放入盛有二氧化碳的集气瓶中,试纸变红
6.根据你的生活经验,结合化学知识判断,下列说法错误的是
A.部分人到高原旅游时出现高原反应,是因为高原上空气稀薄
B.滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂能溶解油污
C.吃松花蛋时可加人少量食醋,因为食醋能消除蛋中所含碱性物质的涩味
D.稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应
7.下列有关物质的性质与用途具有对应关系的是
A.氮气常温下化学性质稳定,可用作保护气 B.天然气难溶于水,可用作燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多 D.活性炭具有吸附性,可使硬水软化
8.下列物质用途,主要利用其物理性质的是
A.用稀盐酸除去水垢 B.用氢气作高燃料 C.氧气用于气焊 D.用铝制作导线
9.下列实验现象描述正确的是
A.镁条在空气中燃烧发出耀眼的白光,生成白色固体
B.打开盛有浓盐酸的试剂瓶盖,瓶口上方会出现白烟
C.将CO2气体通入紫色石蕊溶液,溶液变蓝
D.将木炭在空气中点燃后伸至氧气瓶中,生成二氧化碳气体
10.下列物质能除去铁锈的是
A.盐酸 B.汽油 C.NaOH溶液 D.酒精
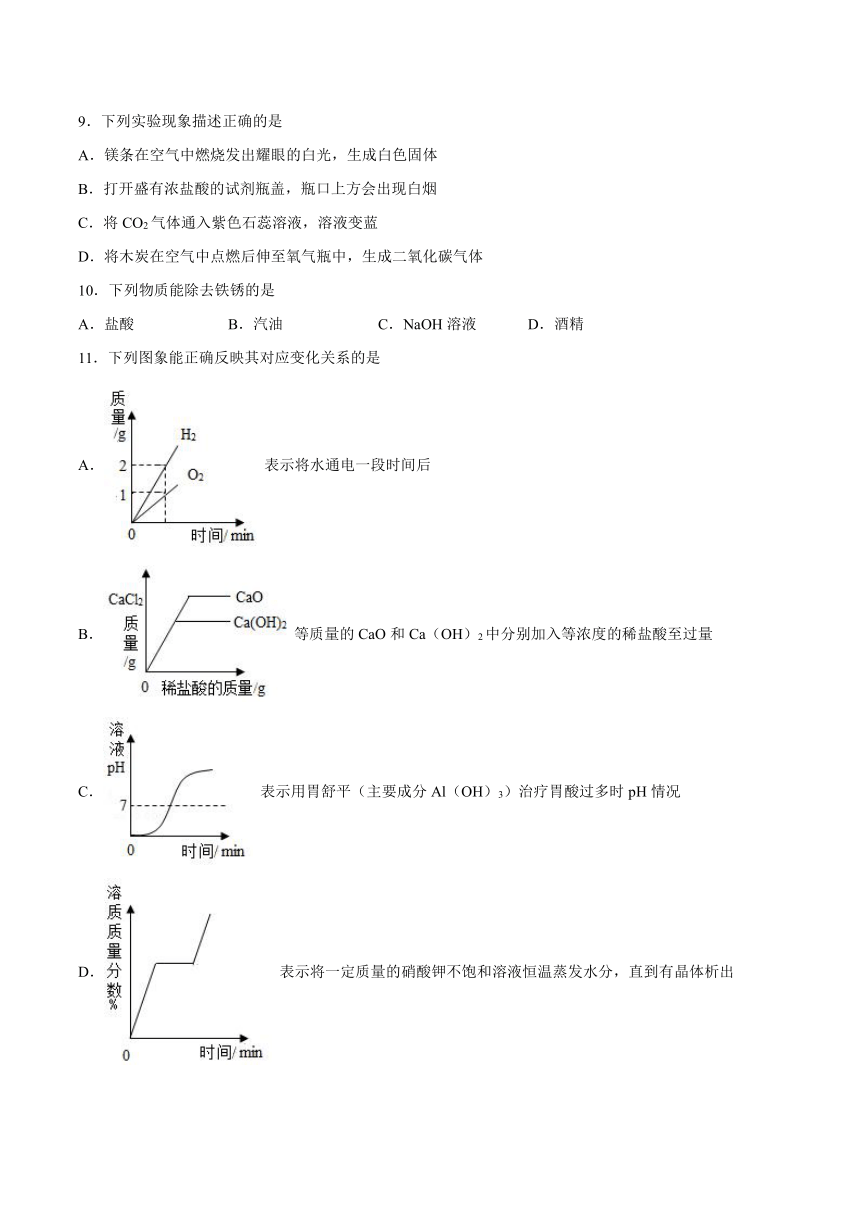
11.下列图象能正确反映其对应变化关系的是
A. 表示将水通电一段时间后
B. 等质量的CaO和Ca(OH)2中分别加入等浓度的稀盐酸至过量
C. 表示用胃舒平(主要成分Al(OH)3)治疗胃酸过多时pH情况
D. 表示将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直到有晶体析出
二、简答题
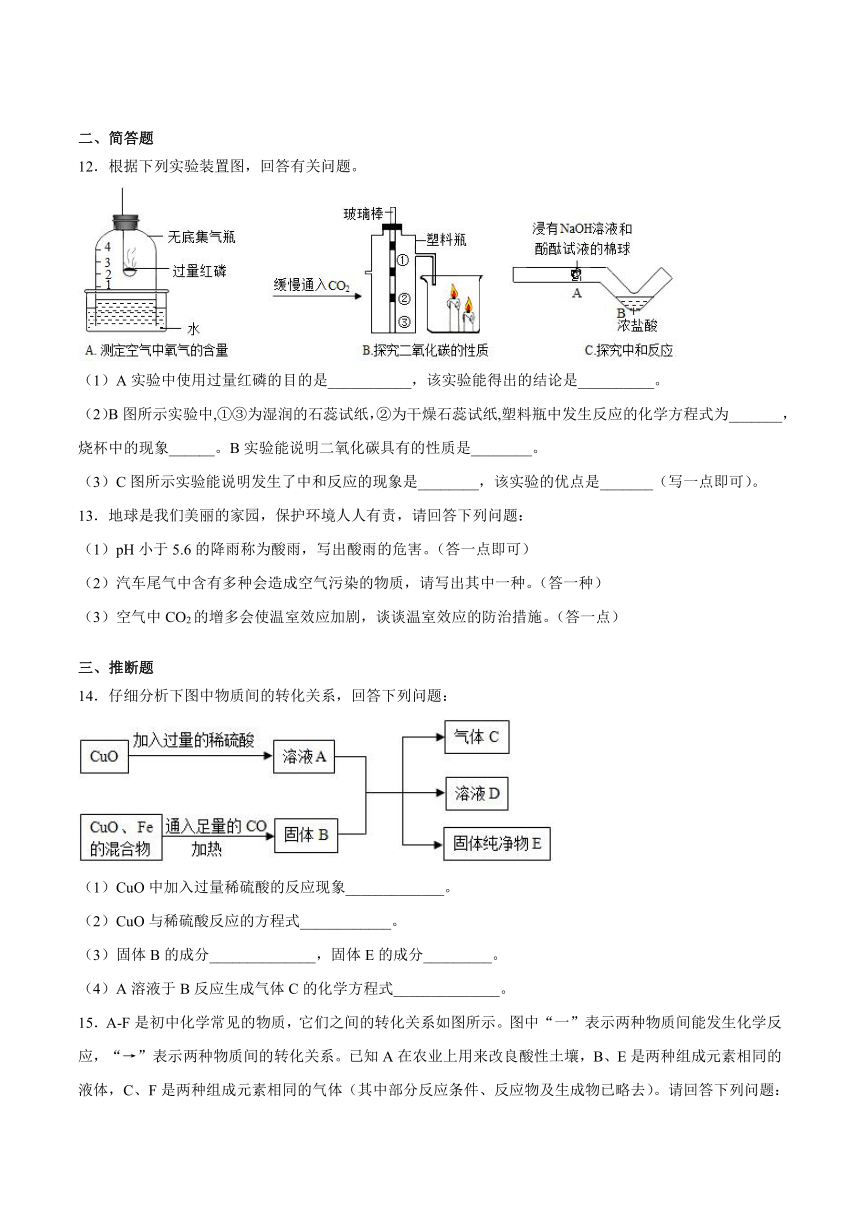
12.根据下列实验装置图,回答有关问题。
(1)A实验中使用过量红磷的目的是___________,该实验能得出的结论是__________。
(2)B图所示实验中,①③为湿润的石蕊试纸,②为干燥石蕊试纸,塑料瓶中发生反应的化学方程式为_______,烧杯中的现象______。B实验能说明二氧化碳具有的性质是________。
(3)C图所示实验能说明发生了中和反应的现象是________,该实验的优点是_______(写一点即可)。
13.地球是我们美丽的家园,保护环境人人有责,请回答下列问题:
(1)pH小于5.6的降雨称为酸雨,写出酸雨的危害。(答一点即可)
(2)汽车尾气中含有多种会造成空气污染的物质,请写出其中一种。(答一种)
(3)空气中CO2的增多会使温室效应加剧,谈谈温室效应的防治措施。(答一点)
三、推断题
14.仔细分析下图中物质间的转化关系,回答下列问题:
(1)CuO中加入过量稀硫酸的反应现象_____________。
(2)CuO与稀硫酸反应的方程式____________。
(3)固体B的成分______________,固体E的成分_________。
(4)A溶液于B反应生成气体C的化学方程式______________。
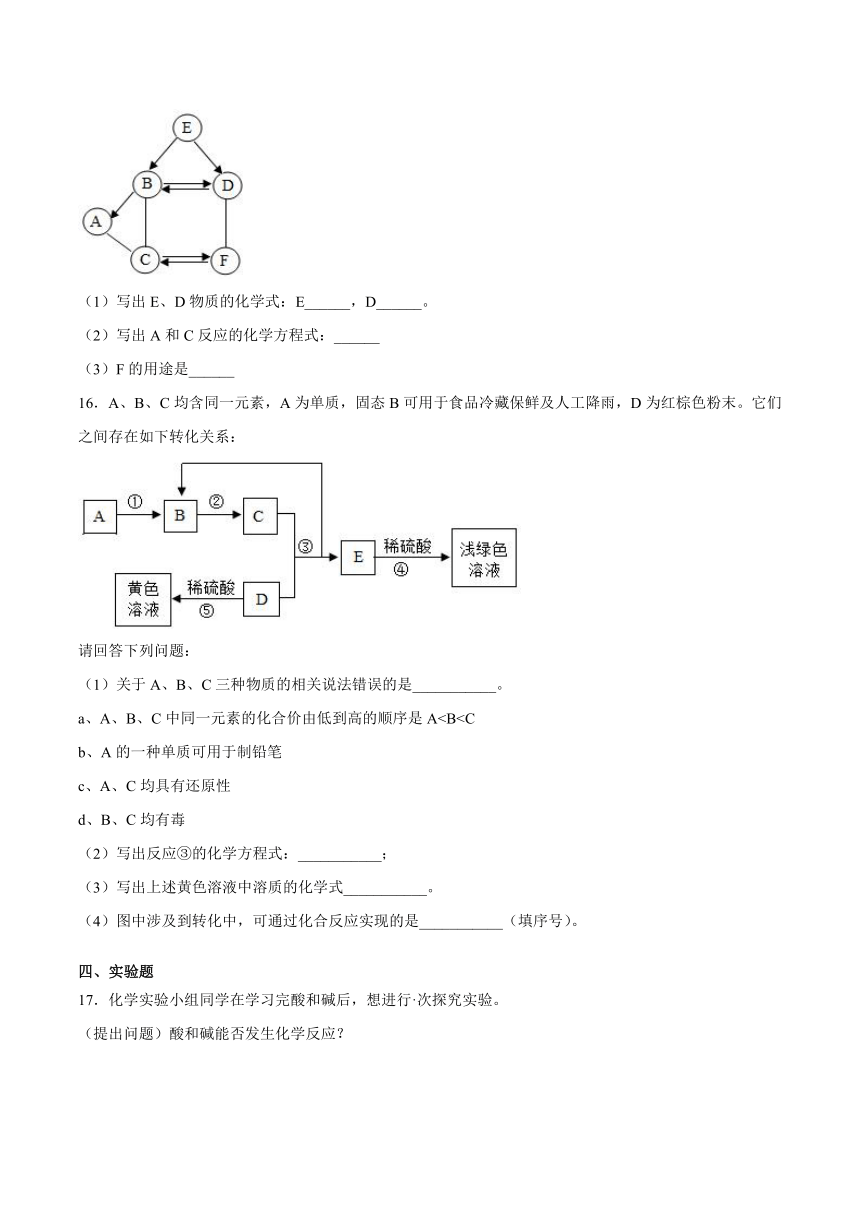
15.A-F是初中化学常见的物质,它们之间的转化关系如图所示。图中“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系。已知A在农业上用来改良酸性土壤,B、E是两种组成元素相同的液体,C、F是两种组成元素相同的气体(其中部分反应条件、反应物及生成物已略去)。请回答下列问题:
(1)写出E、D物质的化学式:E______,D______。
(2)写出A和C反应的化学方程式:______
(3)F的用途是______
16.A、B、C均含同一元素,A为单质,固态B可用于食品冷藏保鲜及人工降雨,D为红棕色粉末。它们之间存在如下转化关系:
请回答下列问题:
(1)关于A、B、C三种物质的相关说法错误的是___________。
a、A、B、C中同一元素的化合价由低到高的顺序是Ab、A的一种单质可用于制铅笔
c、A、C均具有还原性
d、B、C均有毒
(2)写出反应③的化学方程式:___________;
(3)写出上述黄色溶液中溶质的化学式___________。
(4)图中涉及到转化中,可通过化合反应实现的是___________(填序号)。
四、实验题
17.化学实验小组同学在学习完酸和碱后,想进行·次探究实验。
(提出问题)酸和碱能否发生化学反应?
实验一:向盛有氢氧化铜的试管中滴加稀盐酸 实验二:向盛有稀盐酸的试管中滴加氢氧化钠溶液
(实验记录)请帮助小组同学完成下面的内容:
实验一:
(1)同学们观察到了明显的实验现象,得出氢氧化铜与稀盐酸发生了化学反应的结论。请你写出发生反应的化学方程式_____。
实验二:
同学们没有观察到明显的实验现象,质疑二者是否发生了化学反应呢?于是又设计了实验三:
实验三:
(2)如图,向有酚酞的稀盐酸中滴加氢氧化钠溶液,观察到的实验现象是①_____从而证明稀盐酸和氢氧化钠溶液发生了化学反应,其中酚酞的作用是②_____。
(提出问题)实验三中稀盐酸和氢氧化钠溶液是否恰好完全反应呢?
(猜想与假设)分析反应后溶液中溶质成分进行猜想:
溶质成分:甲同学:氯化钠
乙同学:氯化钠、氢氧化钠
丙同学:氯化钠、氯化氢
(设计与交流)
(3)三位同学为了验证实验二是恰好完全反应,设计实验如下:取样,加入一种药品_____。即可得出二者恰好完全反应甲同学猜想正确的结论。如图,图像②中表示的是_____。(填离子符号)
(反思与总结)
(4)由上述探究可知,当我们分析两种物质恰好完全反应时,不是去验证有其他物质生成,而是验证_____来得出恰好完全反应的结论。
18.酸与碱作用生成盐和水的反应,叫中和反应。在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:
(1)要得到此变化曲线,所进行的操作是______(填序号)。
①将稀盐酸滴加到氢氧化钠溶液中 ②将氢氧化钠溶液滴加到稀盐酸中
(2)a点该溶液中的溶质为(写化学式)______。
五、计算题
19.向部分被氧化的镁带样品中,加入146g溶质质量分数为10%的稀盐酸,恰好完全反应,收集到氢气0.2g。
(1)根据化学方程式计算,该样品中金属镁的质量。
(2)计算反应后生成氯化镁的质量。
20.用溶质质量分数为5%的NaOH溶液中和115g的稀盐酸,反应过程中溶液的酸碱度变化如下图所示。请计算。
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g要水_____克。
(2)当a为80g时,所得溶液中溶质的质量分数是多少?
参考答案
1.D 2.A 3.B 4.B 5.D 6.B 7.A 8.D 9.A 10.A 11.B
12.使瓶中的氧气耗尽 氧气约占空气体积的五分之一 矮蜡烛先熄灭,高蜡烛后熄灭 二氧化碳的密度比空气大,不燃烧也不支持燃烧 棉球由红色变为白色 反应现象明显,节约药品
13.
(1)酸雨呈酸性,会腐蚀大理石建筑物;
(2)一氧化碳
(3)发展清洁能源以逐步替代化石能源
14.
(1)黑色粉末消失,溶液变成蓝色
(2)
(3) Cu Fe Cu
(4)
15.
(1) H2O2 O2
(2)
(3)作燃料或冶炼金属
16.
(1)acd
(2)
(3)Fe2(SO4)3
(4)①②
17.
(1)
(2) 加入一定量氢氧化钠溶液,溶液不变色,继续滴加后,溶液变成红色 通过溶液颜色由无色变成红色,证明氢氧化钠从无到有,证明稀盐酸和氢氧化钠溶液发生了化学反应(合理即可)
(3) 紫色石蕊试液 H+
(4)反应物是否有剩余
18.
(1)②
(2)NaCl、HCl
19.
(1)设:样品中金属镁的质量为x。
(2)盐酸中氯化氢的质量:146g×10%=14.6g
氯化氢中氯元素的质量:14.6g×=14.2g
生成氯化镁的质量: 14.2g÷=19g
答:金属镁的质量为2.4g,生成氯化镁的质量为19g。
20.
(1)50
(2)解:设所得溶液中溶质的质量分数是x,加入ag氢氧化钠时pH=7,则恰好完全反应,溶液质量=115g+80g=195g
解得x=3%
答:当a为80g时,所得溶液中溶质的质量分数是3%。
一、单选题
1.水是生命之源,下列“水”可以使石蕊溶液变红的是
A.蒸馏水 B.糖水 C.氨水 D.柠檬水
2.下列物质的用途中,利用了物质的物理性质的是
A.活性炭吸附 B.氮气做保护气 C.酒精做燃料 D.生石灰做干燥剂
3.下列实验操作符合规范要求的是
A.“实验室制取二氧化碳”实验中,先装入药品再检查装置的气密性
B.“粗盐提纯操作”中,在蒸发结晶时,用玻璃棒不断搅拌
C.“配制一定溶质质量分数的溶液”实验中,多余的药品应放回原瓶
D.“探究酸碱中和”实验中,测定溶液的pH时应先将试纸用蒸馏水湿润
4.下列物质的用途能体现其物理性质的是
A.氢氧化铝用作中和胃酸 B.钨丝用作灯泡的灯丝
C.铁粉用作食品保鲜吸氧剂 D.用石英砂等物质为原料制玻璃
5.下列对实验现象的描述错误的是
A.红磷在空气中燃烧,产生大量白烟
B.镁与稀盐酸反应产生大量气泡,放出热量
C.硫在氧气中燃烧发出明亮的蓝紫色火焰,生成刺激性气味的气体
D.干燥蓝色石蕊试纸放入盛有二氧化碳的集气瓶中,试纸变红
6.根据你的生活经验,结合化学知识判断,下列说法错误的是
A.部分人到高原旅游时出现高原反应,是因为高原上空气稀薄
B.滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂能溶解油污
C.吃松花蛋时可加人少量食醋,因为食醋能消除蛋中所含碱性物质的涩味
D.稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应
7.下列有关物质的性质与用途具有对应关系的是
A.氮气常温下化学性质稳定,可用作保护气 B.天然气难溶于水,可用作燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多 D.活性炭具有吸附性,可使硬水软化
8.下列物质用途,主要利用其物理性质的是
A.用稀盐酸除去水垢 B.用氢气作高燃料 C.氧气用于气焊 D.用铝制作导线
9.下列实验现象描述正确的是
A.镁条在空气中燃烧发出耀眼的白光,生成白色固体
B.打开盛有浓盐酸的试剂瓶盖,瓶口上方会出现白烟
C.将CO2气体通入紫色石蕊溶液,溶液变蓝
D.将木炭在空气中点燃后伸至氧气瓶中,生成二氧化碳气体
10.下列物质能除去铁锈的是
A.盐酸 B.汽油 C.NaOH溶液 D.酒精
11.下列图象能正确反映其对应变化关系的是
A. 表示将水通电一段时间后
B. 等质量的CaO和Ca(OH)2中分别加入等浓度的稀盐酸至过量
C. 表示用胃舒平(主要成分Al(OH)3)治疗胃酸过多时pH情况
D. 表示将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直到有晶体析出
二、简答题
12.根据下列实验装置图,回答有关问题。
(1)A实验中使用过量红磷的目的是___________,该实验能得出的结论是__________。
(2)B图所示实验中,①③为湿润的石蕊试纸,②为干燥石蕊试纸,塑料瓶中发生反应的化学方程式为_______,烧杯中的现象______。B实验能说明二氧化碳具有的性质是________。
(3)C图所示实验能说明发生了中和反应的现象是________,该实验的优点是_______(写一点即可)。
13.地球是我们美丽的家园,保护环境人人有责,请回答下列问题:
(1)pH小于5.6的降雨称为酸雨,写出酸雨的危害。(答一点即可)
(2)汽车尾气中含有多种会造成空气污染的物质,请写出其中一种。(答一种)
(3)空气中CO2的增多会使温室效应加剧,谈谈温室效应的防治措施。(答一点)
三、推断题
14.仔细分析下图中物质间的转化关系,回答下列问题:
(1)CuO中加入过量稀硫酸的反应现象_____________。
(2)CuO与稀硫酸反应的方程式____________。
(3)固体B的成分______________,固体E的成分_________。
(4)A溶液于B反应生成气体C的化学方程式______________。
15.A-F是初中化学常见的物质,它们之间的转化关系如图所示。图中“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系。已知A在农业上用来改良酸性土壤,B、E是两种组成元素相同的液体,C、F是两种组成元素相同的气体(其中部分反应条件、反应物及生成物已略去)。请回答下列问题:
(1)写出E、D物质的化学式:E______,D______。
(2)写出A和C反应的化学方程式:______
(3)F的用途是______
16.A、B、C均含同一元素,A为单质,固态B可用于食品冷藏保鲜及人工降雨,D为红棕色粉末。它们之间存在如下转化关系:
请回答下列问题:
(1)关于A、B、C三种物质的相关说法错误的是___________。
a、A、B、C中同一元素的化合价由低到高的顺序是A
c、A、C均具有还原性
d、B、C均有毒
(2)写出反应③的化学方程式:___________;
(3)写出上述黄色溶液中溶质的化学式___________。
(4)图中涉及到转化中,可通过化合反应实现的是___________(填序号)。
四、实验题
17.化学实验小组同学在学习完酸和碱后,想进行·次探究实验。
(提出问题)酸和碱能否发生化学反应?
实验一:向盛有氢氧化铜的试管中滴加稀盐酸 实验二:向盛有稀盐酸的试管中滴加氢氧化钠溶液
(实验记录)请帮助小组同学完成下面的内容:
实验一:
(1)同学们观察到了明显的实验现象,得出氢氧化铜与稀盐酸发生了化学反应的结论。请你写出发生反应的化学方程式_____。
实验二:
同学们没有观察到明显的实验现象,质疑二者是否发生了化学反应呢?于是又设计了实验三:
实验三:
(2)如图,向有酚酞的稀盐酸中滴加氢氧化钠溶液,观察到的实验现象是①_____从而证明稀盐酸和氢氧化钠溶液发生了化学反应,其中酚酞的作用是②_____。
(提出问题)实验三中稀盐酸和氢氧化钠溶液是否恰好完全反应呢?
(猜想与假设)分析反应后溶液中溶质成分进行猜想:
溶质成分:甲同学:氯化钠
乙同学:氯化钠、氢氧化钠
丙同学:氯化钠、氯化氢
(设计与交流)
(3)三位同学为了验证实验二是恰好完全反应,设计实验如下:取样,加入一种药品_____。即可得出二者恰好完全反应甲同学猜想正确的结论。如图,图像②中表示的是_____。(填离子符号)
(反思与总结)
(4)由上述探究可知,当我们分析两种物质恰好完全反应时,不是去验证有其他物质生成,而是验证_____来得出恰好完全反应的结论。
18.酸与碱作用生成盐和水的反应,叫中和反应。在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:
(1)要得到此变化曲线,所进行的操作是______(填序号)。
①将稀盐酸滴加到氢氧化钠溶液中 ②将氢氧化钠溶液滴加到稀盐酸中
(2)a点该溶液中的溶质为(写化学式)______。
五、计算题
19.向部分被氧化的镁带样品中,加入146g溶质质量分数为10%的稀盐酸,恰好完全反应,收集到氢气0.2g。
(1)根据化学方程式计算,该样品中金属镁的质量。
(2)计算反应后生成氯化镁的质量。
20.用溶质质量分数为5%的NaOH溶液中和115g的稀盐酸,反应过程中溶液的酸碱度变化如下图所示。请计算。
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g要水_____克。
(2)当a为80g时,所得溶液中溶质的质量分数是多少?
参考答案
1.D 2.A 3.B 4.B 5.D 6.B 7.A 8.D 9.A 10.A 11.B
12.使瓶中的氧气耗尽 氧气约占空气体积的五分之一 矮蜡烛先熄灭,高蜡烛后熄灭 二氧化碳的密度比空气大,不燃烧也不支持燃烧 棉球由红色变为白色 反应现象明显,节约药品
13.
(1)酸雨呈酸性,会腐蚀大理石建筑物;
(2)一氧化碳
(3)发展清洁能源以逐步替代化石能源
14.
(1)黑色粉末消失,溶液变成蓝色
(2)
(3) Cu Fe Cu
(4)
15.
(1) H2O2 O2
(2)
(3)作燃料或冶炼金属
16.
(1)acd
(2)
(3)Fe2(SO4)3
(4)①②
17.
(1)
(2) 加入一定量氢氧化钠溶液,溶液不变色,继续滴加后,溶液变成红色 通过溶液颜色由无色变成红色,证明氢氧化钠从无到有,证明稀盐酸和氢氧化钠溶液发生了化学反应(合理即可)
(3) 紫色石蕊试液 H+
(4)反应物是否有剩余
18.
(1)②
(2)NaCl、HCl
19.
(1)设:样品中金属镁的质量为x。
(2)盐酸中氯化氢的质量:146g×10%=14.6g
氯化氢中氯元素的质量:14.6g×=14.2g
生成氯化镁的质量: 14.2g÷=19g
答:金属镁的质量为2.4g,生成氯化镁的质量为19g。
20.
(1)50
(2)解:设所得溶液中溶质的质量分数是x,加入ag氢氧化钠时pH=7,则恰好完全反应,溶液质量=115g+80g=195g
解得x=3%
答:当a为80g时,所得溶液中溶质的质量分数是3%。
