鲁教版九年级化学上册 5.1化学反应中的质量守恒课件(33张PPT)
文档属性
| 名称 | 鲁教版九年级化学上册 5.1化学反应中的质量守恒课件(33张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-10 00:00:00 | ||
图片预览










文档简介
(共33张PPT)
第五单元
课题一
化学反应中的质量守恒定律
一天,福尔摩斯象往常一样滋滋有味地 抽着他的烟斗,房间里充满了刺鼻的烟味。华生问道:“敬爱的先生,别人都说你很聪明,那么你能告诉我你吐出的这些烟和气体有多重吗?”
福尔摩斯慢条斯理地说:“这个问题很简单,我只要称出抽烟前烟斗和烟丝的总重量,再减去抽完烟后烟斗和剩余烟灰的总重量,不就是我吐出烟和气体的重量了么!”
这些物质:火柴、蜡烛、酒精燃烧最后留下什么?
○火柴燃烧最后剩下灰烬
○蜡烛、酒精充分燃烧最后连灰烬都没有留下
难道物质从世界上消失了吗?
我们要对物质变化进行定量研究
化学反应中反应前各反应物的质量总和与反应后各生成物的质量总和之间可能有哪几种关系呢
提出问题:
作出假设:
生成物的质量总和 反应物的质量总和
等于
大于
小于
(3)将试管内的溶液倒入烧杯(试管仍留在烧杯中),
使二者反应,观察实验现象
产生蓝色沉淀
(4)称量烧杯及烧杯内物质的总质量
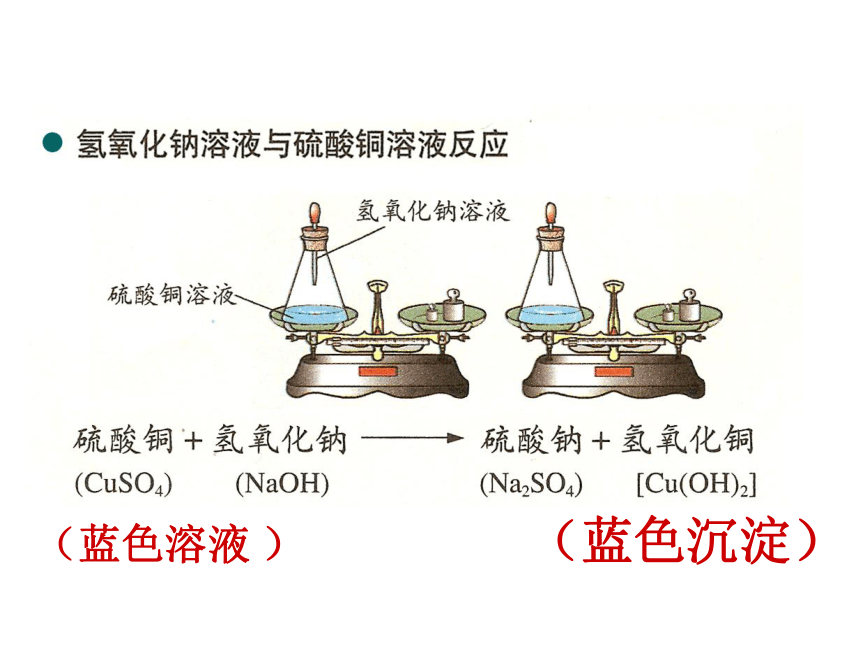
氢氧化钠溶液跟硫酸铜溶液反应前后质量的变化
实验一:
(1)将装有氢氧化钠溶液的小试管放入
装有蓝色硫酸铜溶液的烧杯中
(2)称量烧杯及烧杯内物质的总质量
(5)比较反应前后物质总质量的变化
(蓝色溶液 ) (蓝色沉淀)
烧杯
烧杯
对定义的理解
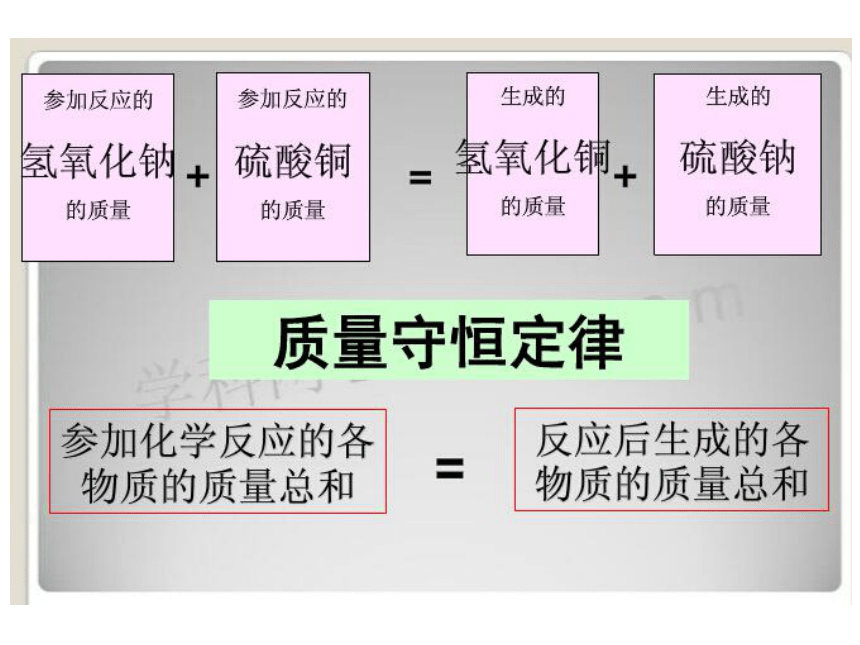
质量守恒定律
参加化学反应的各物质的质量总和,等于反应生成的各物质的质量总和
只适用于化学反应
没有参加化学反应的物质不符合定律
反应物和生成物的质量总和,而不是其他量的和
不能漏掉任何一种反应物和生成物
10克水加热后沸腾,变成10克水蒸气,此变化符合质量守恒定律。
你认为下列说法对吗?为什么?
1. 质量守恒定律仅适用于化学变化。
2.“质量”必须是真正参加化学反应的物质质量,而不是各物质质量的简单加和。
纸燃烧后,剩下的灰比原来的纸轻,此反应不符合质量守恒定律。
3、总和:不能忽略反应物或生成物中的气体
特别是“气体反应物O2”
“气体生成物CO2 H2 O2”
1升氢气和8升氧气反应生成9升水
4. 是“质量守恒”,不是体积守恒。
将稀盐酸倒入烧杯中
实验现象:
固体溶解,有大量的气泡产生;
碳酸钠+盐酸 氯化钠+二氧化碳+水
Na2CO3+HCl NaCl+ CO2 + H2O
反应原理:
实验5--1
天平指针向右倾斜(变轻)
天平平衡情况:
HCl + Na2CO3 NaCl+ H2O + CO2
(如何改进实验装置?)
总质量
总质量
怎么反应后天平不平衡了呢?
那么,这个反应遵守质量守恒定律吗?
反应后称量到的
A装置
B装置
碳酸钠粉末
稀盐酸
改进后的实验装置
镁 + 氧气
氧化镁
点燃
Mg + O2
MgO
点燃
观察:1、该实验的现象是什么?
发出耀眼的白光,放出热量,生成白色固体
思考:2、该反应的原理是什么?
同时还有白烟产生
实验5--2
小结:
在有气体参加或生成的化学变化中,验证质量守恒定律时候,必须在密闭容器中进行。
1.下列现象不能用质量守恒定律解释的是( )
A、蜡烛燃烧时慢慢变短内
B、打开盛酒精的瓶盖,酒精质量变小 C、镁带燃烧后,固体质量增加
D、澄清的石灰水露置在空气中变重
B
1673年,波义耳在一只敞口的容器中加热汞,结果发现反应后质量增加了。
波义耳--英国
拉瓦锡--法国
1777年,他在密闭容器中氧化汞的分解与合成实验,结果发现反应后质量不变。
失败
成功
质量守恒定律的发现
为什么参加化学反应的各物物质质量总和等于生成的各物质质量总和呢?能不能从微观角度分析质量守恒定律?
想一想
分解
结合
水分子
氢原子
氧原子
氢分子
氧分子
H2O H2 +O2
通电
分子
分解
原子
重组
新分子
化学变化的实质是:
思考:
原子的种类 ,原子的数目 。
原子的质量 。
不变
不变
不变
水电解微观示意图
氧原子
氢原子
质量守恒的原因
思考:化学反应前后,分子变化了吗?元素变化了吗?
分子的种类 ,物质的种类 。
元素的种类 ,
改变
改变
不变
水电解微观示意图
氧原子
氢原子
元素的种类 。
不变
原子质量
原子数目
原子种类
微观
元素质量
元素种类
不 变
物质种类
分子种类
改变
宏观
可能
改变
分子数目
元素化合价
质量守恒定律的适用范围是什么?学了该定律,对我们有什么用?
质量守恒定律适用于一切化学反应。
可运用定律 1. 进行有关的计算
2. 推测一些物质的组成
3. 解释一些实验事实
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应。
40
(1)
1、用质量差确定某反应物或生成物的质量
(2)6克碳与一定量的氧气恰好完全反应,生成二氧化碳22克,有______克氧气参加了反应。
16
1、用质量差确定某反应物或生成物的质量
(3) 将24.5 g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为15.9 g,则产生氧气____g。
9.6
练习:1、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
请根据质量守恒定律判断x的值:( )
A.50 B.30 C.10 D.70
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 50 50 10 x
D
哪种物质是反应物?
70
属于______反应.
2.在化学反应2XY2+Y2=2Z中Z的化学式为( )
A、X2Y3 B、XY3
C、X2Y6 D、 X2Y4
1.已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。
C、H
O
B
2、推断反应物或生成物的组成元素
点燃
4.该化学反应中,参加反应的 和
与反应后生成 的各微粒的个数比为: _____ 。
2∶1∶2
5、某有机物R在足量氧气中完全燃烧后的化学方程式如下:2R + 13O2 === 8CO2 +10H2O。根据质量守定律,R的化学式为( )
A.C4H10 B.CH4 C.C8H10 D.C2H4O2
6、亚硝酸钠(NaNO2)外观与食盐很相似,有咸味,误食易中毒。区别它们的一种方法是:隔绝空气加热。没有明显变化的是食盐。能分解放出有刺激性气味气体的是亚硝酸钠。此气体可能是( )
A.SO2 B.NO2 C.N2 D.NH3
A
B
7.镁带在耐高温的容器中密封(内含空气)加热,在图中,能正确表示容器里所盛的物质总质量变化的是( )
B
8.某化合物在空气中完全燃烧,需要4.8g氧气,同时生成4.4g二氧化碳和2.7g水,则该化合物中:( )
A、只含有C元素
B、只含有C、H元素
C、一定含有C、H元素,可能含有O元素
D、只含有C、H、O三种元素
D
9、某物质2.3g在氧气中完全燃烧生成4.4g二氧化碳和2.7g水,则关于这种物质的组成描述正确的是( )
A.该物质一定有碳元素和氢元素 ,可能含有氧元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素、氢元素和氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰2
C
你知道该物质的化学式可能会是怎样的吗?
10.某物质在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的是( )
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰2
C
第五单元
课题一
化学反应中的质量守恒定律
一天,福尔摩斯象往常一样滋滋有味地 抽着他的烟斗,房间里充满了刺鼻的烟味。华生问道:“敬爱的先生,别人都说你很聪明,那么你能告诉我你吐出的这些烟和气体有多重吗?”
福尔摩斯慢条斯理地说:“这个问题很简单,我只要称出抽烟前烟斗和烟丝的总重量,再减去抽完烟后烟斗和剩余烟灰的总重量,不就是我吐出烟和气体的重量了么!”
这些物质:火柴、蜡烛、酒精燃烧最后留下什么?
○火柴燃烧最后剩下灰烬
○蜡烛、酒精充分燃烧最后连灰烬都没有留下
难道物质从世界上消失了吗?
我们要对物质变化进行定量研究
化学反应中反应前各反应物的质量总和与反应后各生成物的质量总和之间可能有哪几种关系呢
提出问题:
作出假设:
生成物的质量总和 反应物的质量总和
等于
大于
小于
(3)将试管内的溶液倒入烧杯(试管仍留在烧杯中),
使二者反应,观察实验现象
产生蓝色沉淀
(4)称量烧杯及烧杯内物质的总质量
氢氧化钠溶液跟硫酸铜溶液反应前后质量的变化
实验一:
(1)将装有氢氧化钠溶液的小试管放入
装有蓝色硫酸铜溶液的烧杯中
(2)称量烧杯及烧杯内物质的总质量
(5)比较反应前后物质总质量的变化
(蓝色溶液 ) (蓝色沉淀)
烧杯
烧杯
对定义的理解
质量守恒定律
参加化学反应的各物质的质量总和,等于反应生成的各物质的质量总和
只适用于化学反应
没有参加化学反应的物质不符合定律
反应物和生成物的质量总和,而不是其他量的和
不能漏掉任何一种反应物和生成物
10克水加热后沸腾,变成10克水蒸气,此变化符合质量守恒定律。
你认为下列说法对吗?为什么?
1. 质量守恒定律仅适用于化学变化。
2.“质量”必须是真正参加化学反应的物质质量,而不是各物质质量的简单加和。
纸燃烧后,剩下的灰比原来的纸轻,此反应不符合质量守恒定律。
3、总和:不能忽略反应物或生成物中的气体
特别是“气体反应物O2”
“气体生成物CO2 H2 O2”
1升氢气和8升氧气反应生成9升水
4. 是“质量守恒”,不是体积守恒。
将稀盐酸倒入烧杯中
实验现象:
固体溶解,有大量的气泡产生;
碳酸钠+盐酸 氯化钠+二氧化碳+水
Na2CO3+HCl NaCl+ CO2 + H2O
反应原理:
实验5--1
天平指针向右倾斜(变轻)
天平平衡情况:
HCl + Na2CO3 NaCl+ H2O + CO2
(如何改进实验装置?)
总质量
总质量
怎么反应后天平不平衡了呢?
那么,这个反应遵守质量守恒定律吗?
反应后称量到的
A装置
B装置
碳酸钠粉末
稀盐酸
改进后的实验装置
镁 + 氧气
氧化镁
点燃
Mg + O2
MgO
点燃
观察:1、该实验的现象是什么?
发出耀眼的白光,放出热量,生成白色固体
思考:2、该反应的原理是什么?
同时还有白烟产生
实验5--2
小结:
在有气体参加或生成的化学变化中,验证质量守恒定律时候,必须在密闭容器中进行。
1.下列现象不能用质量守恒定律解释的是( )
A、蜡烛燃烧时慢慢变短内
B、打开盛酒精的瓶盖,酒精质量变小 C、镁带燃烧后,固体质量增加
D、澄清的石灰水露置在空气中变重
B
1673年,波义耳在一只敞口的容器中加热汞,结果发现反应后质量增加了。
波义耳--英国
拉瓦锡--法国
1777年,他在密闭容器中氧化汞的分解与合成实验,结果发现反应后质量不变。
失败
成功
质量守恒定律的发现
为什么参加化学反应的各物物质质量总和等于生成的各物质质量总和呢?能不能从微观角度分析质量守恒定律?
想一想
分解
结合
水分子
氢原子
氧原子
氢分子
氧分子
H2O H2 +O2
通电
分子
分解
原子
重组
新分子
化学变化的实质是:
思考:
原子的种类 ,原子的数目 。
原子的质量 。
不变
不变
不变
水电解微观示意图
氧原子
氢原子
质量守恒的原因
思考:化学反应前后,分子变化了吗?元素变化了吗?
分子的种类 ,物质的种类 。
元素的种类 ,
改变
改变
不变
水电解微观示意图
氧原子
氢原子
元素的种类 。
不变
原子质量
原子数目
原子种类
微观
元素质量
元素种类
不 变
物质种类
分子种类
改变
宏观
可能
改变
分子数目
元素化合价
质量守恒定律的适用范围是什么?学了该定律,对我们有什么用?
质量守恒定律适用于一切化学反应。
可运用定律 1. 进行有关的计算
2. 推测一些物质的组成
3. 解释一些实验事实
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应。
40
(1)
1、用质量差确定某反应物或生成物的质量
(2)6克碳与一定量的氧气恰好完全反应,生成二氧化碳22克,有______克氧气参加了反应。
16
1、用质量差确定某反应物或生成物的质量
(3) 将24.5 g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为15.9 g,则产生氧气____g。
9.6
练习:1、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
请根据质量守恒定律判断x的值:( )
A.50 B.30 C.10 D.70
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 50 50 10 x
D
哪种物质是反应物?
70
属于______反应.
2.在化学反应2XY2+Y2=2Z中Z的化学式为( )
A、X2Y3 B、XY3
C、X2Y6 D、 X2Y4
1.已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。
C、H
O
B
2、推断反应物或生成物的组成元素
点燃
4.该化学反应中,参加反应的 和
与反应后生成 的各微粒的个数比为: _____ 。
2∶1∶2
5、某有机物R在足量氧气中完全燃烧后的化学方程式如下:2R + 13O2 === 8CO2 +10H2O。根据质量守定律,R的化学式为( )
A.C4H10 B.CH4 C.C8H10 D.C2H4O2
6、亚硝酸钠(NaNO2)外观与食盐很相似,有咸味,误食易中毒。区别它们的一种方法是:隔绝空气加热。没有明显变化的是食盐。能分解放出有刺激性气味气体的是亚硝酸钠。此气体可能是( )
A.SO2 B.NO2 C.N2 D.NH3
A
B
7.镁带在耐高温的容器中密封(内含空气)加热,在图中,能正确表示容器里所盛的物质总质量变化的是( )
B
8.某化合物在空气中完全燃烧,需要4.8g氧气,同时生成4.4g二氧化碳和2.7g水,则该化合物中:( )
A、只含有C元素
B、只含有C、H元素
C、一定含有C、H元素,可能含有O元素
D、只含有C、H、O三种元素
D
9、某物质2.3g在氧气中完全燃烧生成4.4g二氧化碳和2.7g水,则关于这种物质的组成描述正确的是( )
A.该物质一定有碳元素和氢元素 ,可能含有氧元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素、氢元素和氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰2
C
你知道该物质的化学式可能会是怎样的吗?
10.某物质在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的是( )
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰2
C
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
