第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 159.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-10 00:00:00 | ||
图片预览


文档简介
第5章《初识酸和碱》检测题
一、单选题
1.下列实验操作能达到实验目的的是
实验目的 实验操作
A 除去CO2中混有的少量氯化氢气体 将气体通过足量的氢氧化钠溶液
B 鉴别 H2SO4溶液和 NaCl溶液 取样,滴加酚酞溶液,观察现象
C 区别硬水和软水 取样,加肥皂水,振荡,观察现象
D 分离Fe和CuSO4固体混合物 加入足量的水溶解,过滤
A.A B.B C.C D.D
2.物质的用途与性质密切相关,下列叙述正确的是
A.由于活性炭具有吸附性,故可用活性炭将硬水变为软水
B.由于氢氧化钠是一种强碱,故可用于改良酸性土壤
C.由于一氧化碳易溶于水,故在室内放一盆水能预防煤气中毒
D.由于镁在空气中燃烧会发出耀眼的白光,故可用于制作照明弹
3.物质的用途只体现其物理性质的是
A.N2:作保护气 B.稀有气体:作电光源
C.CO2:作灭火器 D.CaO:加热食品
4.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2OB.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2D.O2、Fe2O3、H2SO4、NH3·H2O
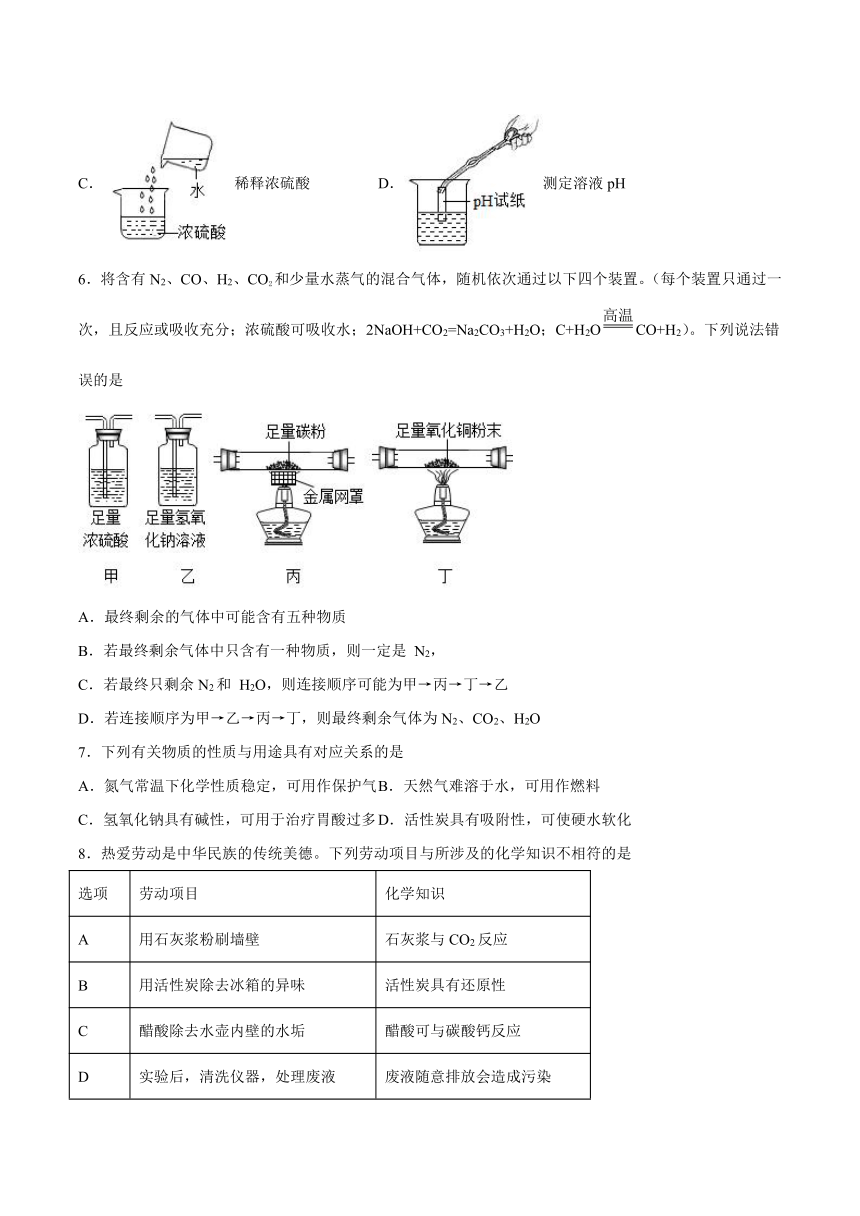
5.下列实验基本操作规范的是
A.称量氢氧化钠 B.蒸发氯化钠溶液
C.稀释浓硫酸 D.测定溶液pH
6.将含有N2、CO、H2、CO2和少量水蒸气的混合气体,随机依次通过以下四个装置。(每个装置只通过一次,且反应或吸收充分;浓硫酸可吸收水;2NaOH+CO2=Na2CO3+H2O;C+H2OCO+H2)。下列说法错误的是
A.最终剩余的气体中可能含有五种物质
B.若最终剩余气体中只含有一种物质,则一定是 N2,
C.若最终只剩余N2和 H2O,则连接顺序可能为甲→丙→丁→乙
D.若连接顺序为甲→乙→丙→丁,则最终剩余气体为N2、CO2、H2O
7.下列有关物质的性质与用途具有对应关系的是
A.氮气常温下化学性质稳定,可用作保护气 B.天然气难溶于水,可用作燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多 D.活性炭具有吸附性,可使硬水软化
8.热爱劳动是中华民族的传统美德。下列劳动项目与所涉及的化学知识不相符的是
选项 劳动项目 化学知识
A 用石灰浆粉刷墙壁 石灰浆与CO2反应
B 用活性炭除去冰箱的异味 活性炭具有还原性
C 醋酸除去水壶内壁的水垢 醋酸可与碳酸钙反应
D 实验后,清洗仪器,处理废液 废液随意排放会造成污染
A.A B.B C.C D.D
9.逻辑推理是一种重要的化学思维方法。下列说法中合理的是
A.洗洁精去除油污是利用了乳化作用,则汽油去除油污也是应用了乳化作用
B.活泼金属加入稀盐酸能产生气体,则能与稀盐酸反应产生气体的一定是活泼金属
C.将酚酞滴入碱性溶液后显红色,则能使酚酞变红色的溶液一定是碱性溶液
D.酸碱中和反应能生成盐和水,则生成盐和水的反应一定是中和反应
10.已知生活用品中厕所清洁剂的pH=1,厨房清洁剂的pH=12。下列说法错误的是
A.两者混合使用能提高清洁效果
B.厕所清洁剂中可能含有酸性物质
C.厨房清洁剂加水稀释溶液pH减小
D.厕所清洁剂可能使铁制下水道腐蚀
二、简答题
11.归纳总结是学习化学的一种方法。某同学整理的氢氧化钠的化学性质如图。结合此图回答下列问题:
(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,反应的化学方程式为:_____,所以要密封保存。实验室须密封保存的物质还有_____填一种。
(2)写出能与氢氧化钠溶液反应的X中的一种物质的化学式:_____。
(3)写出氢氧化钠溶液与稀硫酸反应的化学方程式_____。
三、推断题
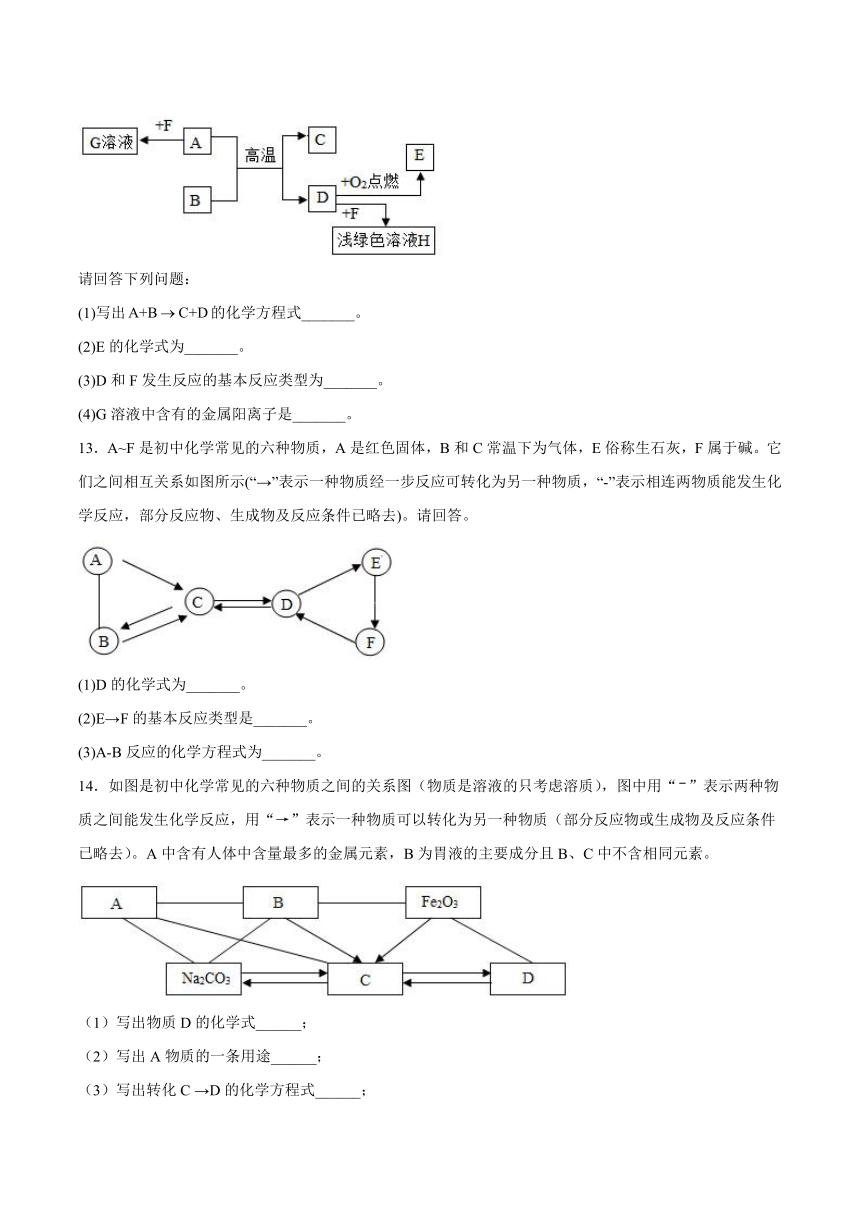
12.A、B、C、D、E、F、G、H都是初中化学中常见的物质,它们存在如下的转化关系(部分反应的生成物已经略去),其中A是由两种元素组成的红棕色粉末,C是一种造成温室效应的气体,E是一种黑色固体且和A含有的元素种类相同,A、B、C、E在物质的分类中属于同类物质。
请回答下列问题:
(1)写出的化学方程式_______。
(2)E的化学式为_______。
(3)D和F发生反应的基本反应类型为_______。
(4)G溶液中含有的金属阳离子是_______。
13.A~F是初中化学常见的六种物质,A是红色固体,B和C常温下为气体,E俗称生石灰,F属于碱。它们之间相互关系如图所示(“→”表示一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答。
(1)D的化学式为_______。
(2)E→F的基本反应类型是_______。
(3)A-B反应的化学方程式为_______。
14.如图是初中化学常见的六种物质之间的关系图(物质是溶液的只考虑溶质),图中用“”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。A中含有人体中含量最多的金属元素,B为胃液的主要成分且B、C中不含相同元素。
(1)写出物质D的化学式______;
(2)写出A物质的一条用途______;
(3)写出转化C →D的化学方程式______;
(4)写出B与Fe2O3反应的化学方程式______。
四、实验题
15.根据下列实验回答问题。
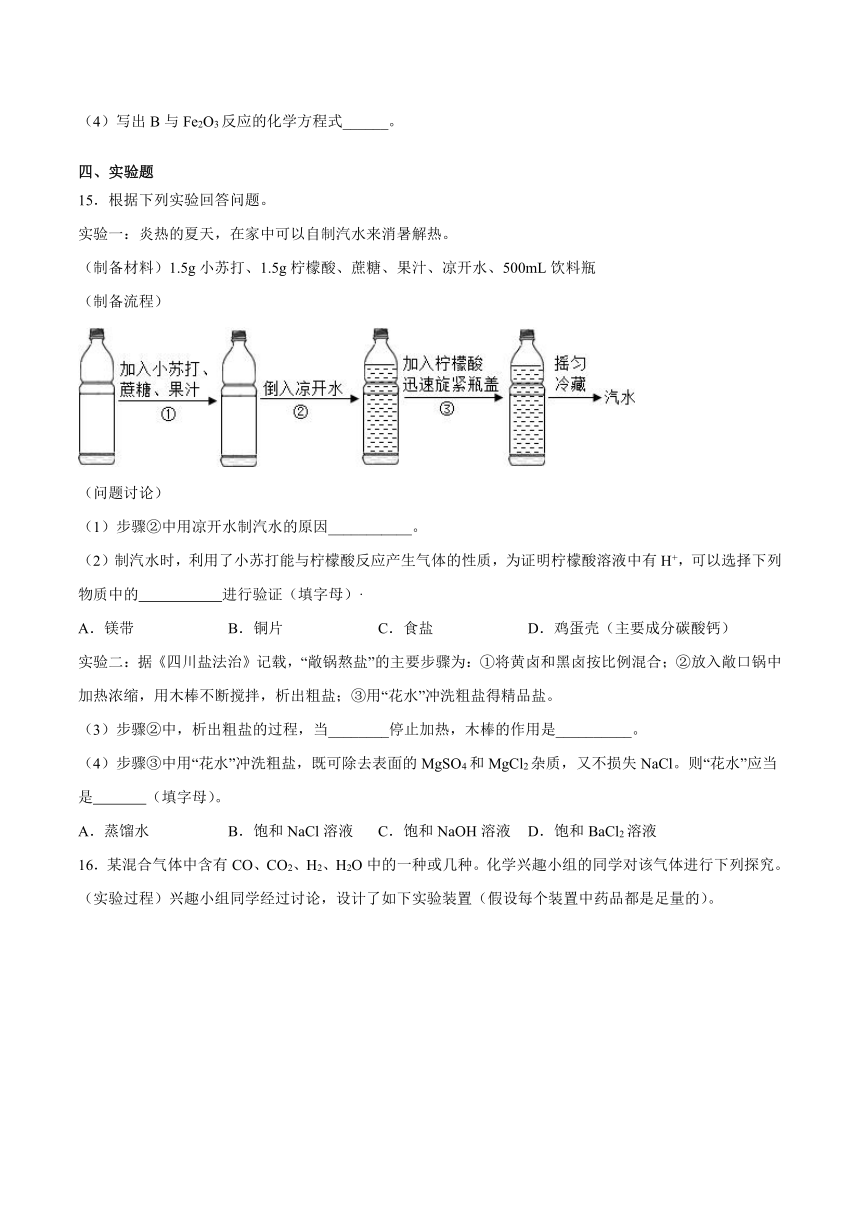
实验一:炎热的夏天,在家中可以自制汽水来消暑解热。
(制备材料)1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
(制备流程)
(问题讨论)
(1)步骤②中用凉开水制汽水的原因___________。
(2)制汽水时,利用了小苏打能与柠檬酸反应产生气体的性质,为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母)·
A.镁带 B.铜片 C.食盐 D.鸡蛋壳(主要成分碳酸钙)
实验二:据《四川盐法治》记载,“敞锅熬盐”的主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,用木棒不断搅拌,析出粗盐;③用“花水”冲洗粗盐得精品盐。
(3)步骤②中,析出粗盐的过程,当________停止加热,木棒的作用是__________。
(4)步骤③中用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是 (填字母)。
A.蒸馏水 B.饱和NaCl溶液 C.饱和NaOH溶液 D.饱和BaCl2溶液
16.某混合气体中含有CO、CO2、H2、H2O中的一种或几种。化学兴趣小组的同学对该气体进行下列探究。
(实验过程)兴趣小组同学经过讨论,设计了如下实验装置(假设每个装置中药品都是足量的)。
(实验现象)A和F中的白色粉末变为蓝色,B中的澄清石灰水变浑浊,E中的黑色粉末变红,其他装置中未观察到明显的实验现象。
根据以上实验过程和实验现象,回答下列问题:
(1)装置D中盛放的试剂是_______,装置G中盛放的试剂是________。
(2)装置B和C不能颠倒顺序的原因是_________。
(3)写出装置E中发生反应的化学方程式:_________。
(实验结论)
(4)混合气体中含有的气体是_______ (填化学式)。
17.请结合下图回答问题:
(1)仪器名称:②___________。
(2)实验室用氯酸钾和二氧化锰制取并收集O2,可选用发生装置___________(选序号)和收集装置D组合,反应的化学方程式为___________。
(3)实验室制取CO2,CO2可用装置E收集,理由是___________。
(4)实验室使用B或C装置,用块状固体FeS和稀H2SO4反应制取硫化氢:。H2S是有毒气体,能溶于水,其水溶液为氢硫酸。
①“尾气吸收装置”应选择___________(选填“甲”或“乙”)。
②氢氧化钠溶液的作用是___________。
五、计算题
18.为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸恰好完全反应,测得剩余固体的质量为2g(杂质不溶于水也不与酸反应)。请计算:
(1)该赤铁矿中Fe2O3的纯度为_______。
(2)稀盐酸中溶质的质量分数_____。
19.过氧乙酸是一种常用的消毒剂,其说明书的一部分如图所示,回答下列问题:
(1)保存和配制过氧乙酸不宜使用__(填“铁”“玻璃”或“陶瓷”)材料制成的容器。
(2)双氧水和乙酸反应可得到过氧乙酸,该反应的化学方程式为CH3COOH+H2O2=CH3COOOH+X,则X的化学式为__。
(3)用质量分数为40%的过氧乙酸溶液配制8000g质量分数为0.5%的过氧乙酸溶液来浸泡消毒,需要取水__mL(水的密度为1g/mL)。
20.某实验小组同学从碳酸钙、碳酸钠和氯化钠的固体混合物中提取氯化钠,实验操作的一部分流程如下图。请根据图中所提供的数据,回答下列问题:
(1)本实验生成二氧化碳的质量是______g,原固体混合物中碳酸钠的质量是______g。
(2)本实验最终所得不饱和溶液的溶质质量分数是多少?
参考答案
1.C 2.D 3.B 4.D 5.B 6.A 7.A 8.B 9.C 10.A
11. 浓硫酸
12. Fe3O4 置换反应 Fe3+
13.CaCO3 化合反应
14.
改良酸性土壤
15.
(1)CO2的溶解度随温度的降低而增大,凉开水温度低,溶解的CO2较多
(2)AD
(3) 敞口锅中出现较多量晶体 搅拌,防止液体因局部温度过高,造成液滴飞溅
(4)B
16.浓硫酸
17.
(1)集气瓶
(2) A
(3)二氧化碳的密度大于空气
(4) 乙 吸收H2S,防止污染空气
18.
(1)80%
(2)解:设稀盐酸中氯化氢的质量为x。
x=10.95g
稀盐酸中溶质的质量分数为:×100%=10.95%
答:稀盐酸中溶质的质量分数是10.95%。
19.
(1)铁
(2)H2O
(3)7900
20.解:生成二氧化碳质量为20g-5.6g+90g+100g-200g=4.4g
设碳酸钠质量为x,生成氯化钠质量为y
答:(1)4.4;10.6
(2)所得溶液的溶质质量分数为7.75%。
一、单选题
1.下列实验操作能达到实验目的的是
实验目的 实验操作
A 除去CO2中混有的少量氯化氢气体 将气体通过足量的氢氧化钠溶液
B 鉴别 H2SO4溶液和 NaCl溶液 取样,滴加酚酞溶液,观察现象
C 区别硬水和软水 取样,加肥皂水,振荡,观察现象
D 分离Fe和CuSO4固体混合物 加入足量的水溶解,过滤
A.A B.B C.C D.D
2.物质的用途与性质密切相关,下列叙述正确的是
A.由于活性炭具有吸附性,故可用活性炭将硬水变为软水
B.由于氢氧化钠是一种强碱,故可用于改良酸性土壤
C.由于一氧化碳易溶于水,故在室内放一盆水能预防煤气中毒
D.由于镁在空气中燃烧会发出耀眼的白光,故可用于制作照明弹
3.物质的用途只体现其物理性质的是
A.N2:作保护气 B.稀有气体:作电光源
C.CO2:作灭火器 D.CaO:加热食品
4.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2OB.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2D.O2、Fe2O3、H2SO4、NH3·H2O
5.下列实验基本操作规范的是
A.称量氢氧化钠 B.蒸发氯化钠溶液
C.稀释浓硫酸 D.测定溶液pH
6.将含有N2、CO、H2、CO2和少量水蒸气的混合气体,随机依次通过以下四个装置。(每个装置只通过一次,且反应或吸收充分;浓硫酸可吸收水;2NaOH+CO2=Na2CO3+H2O;C+H2OCO+H2)。下列说法错误的是
A.最终剩余的气体中可能含有五种物质
B.若最终剩余气体中只含有一种物质,则一定是 N2,
C.若最终只剩余N2和 H2O,则连接顺序可能为甲→丙→丁→乙
D.若连接顺序为甲→乙→丙→丁,则最终剩余气体为N2、CO2、H2O
7.下列有关物质的性质与用途具有对应关系的是
A.氮气常温下化学性质稳定,可用作保护气 B.天然气难溶于水,可用作燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多 D.活性炭具有吸附性,可使硬水软化
8.热爱劳动是中华民族的传统美德。下列劳动项目与所涉及的化学知识不相符的是
选项 劳动项目 化学知识
A 用石灰浆粉刷墙壁 石灰浆与CO2反应
B 用活性炭除去冰箱的异味 活性炭具有还原性
C 醋酸除去水壶内壁的水垢 醋酸可与碳酸钙反应
D 实验后,清洗仪器,处理废液 废液随意排放会造成污染
A.A B.B C.C D.D
9.逻辑推理是一种重要的化学思维方法。下列说法中合理的是
A.洗洁精去除油污是利用了乳化作用,则汽油去除油污也是应用了乳化作用
B.活泼金属加入稀盐酸能产生气体,则能与稀盐酸反应产生气体的一定是活泼金属
C.将酚酞滴入碱性溶液后显红色,则能使酚酞变红色的溶液一定是碱性溶液
D.酸碱中和反应能生成盐和水,则生成盐和水的反应一定是中和反应
10.已知生活用品中厕所清洁剂的pH=1,厨房清洁剂的pH=12。下列说法错误的是
A.两者混合使用能提高清洁效果
B.厕所清洁剂中可能含有酸性物质
C.厨房清洁剂加水稀释溶液pH减小
D.厕所清洁剂可能使铁制下水道腐蚀
二、简答题
11.归纳总结是学习化学的一种方法。某同学整理的氢氧化钠的化学性质如图。结合此图回答下列问题:
(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,反应的化学方程式为:_____,所以要密封保存。实验室须密封保存的物质还有_____填一种。
(2)写出能与氢氧化钠溶液反应的X中的一种物质的化学式:_____。
(3)写出氢氧化钠溶液与稀硫酸反应的化学方程式_____。
三、推断题
12.A、B、C、D、E、F、G、H都是初中化学中常见的物质,它们存在如下的转化关系(部分反应的生成物已经略去),其中A是由两种元素组成的红棕色粉末,C是一种造成温室效应的气体,E是一种黑色固体且和A含有的元素种类相同,A、B、C、E在物质的分类中属于同类物质。
请回答下列问题:
(1)写出的化学方程式_______。
(2)E的化学式为_______。
(3)D和F发生反应的基本反应类型为_______。
(4)G溶液中含有的金属阳离子是_______。
13.A~F是初中化学常见的六种物质,A是红色固体,B和C常温下为气体,E俗称生石灰,F属于碱。它们之间相互关系如图所示(“→”表示一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答。
(1)D的化学式为_______。
(2)E→F的基本反应类型是_______。
(3)A-B反应的化学方程式为_______。
14.如图是初中化学常见的六种物质之间的关系图(物质是溶液的只考虑溶质),图中用“”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。A中含有人体中含量最多的金属元素,B为胃液的主要成分且B、C中不含相同元素。
(1)写出物质D的化学式______;
(2)写出A物质的一条用途______;
(3)写出转化C →D的化学方程式______;
(4)写出B与Fe2O3反应的化学方程式______。
四、实验题
15.根据下列实验回答问题。
实验一:炎热的夏天,在家中可以自制汽水来消暑解热。
(制备材料)1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
(制备流程)
(问题讨论)
(1)步骤②中用凉开水制汽水的原因___________。
(2)制汽水时,利用了小苏打能与柠檬酸反应产生气体的性质,为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母)·
A.镁带 B.铜片 C.食盐 D.鸡蛋壳(主要成分碳酸钙)
实验二:据《四川盐法治》记载,“敞锅熬盐”的主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,用木棒不断搅拌,析出粗盐;③用“花水”冲洗粗盐得精品盐。
(3)步骤②中,析出粗盐的过程,当________停止加热,木棒的作用是__________。
(4)步骤③中用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是 (填字母)。
A.蒸馏水 B.饱和NaCl溶液 C.饱和NaOH溶液 D.饱和BaCl2溶液
16.某混合气体中含有CO、CO2、H2、H2O中的一种或几种。化学兴趣小组的同学对该气体进行下列探究。
(实验过程)兴趣小组同学经过讨论,设计了如下实验装置(假设每个装置中药品都是足量的)。
(实验现象)A和F中的白色粉末变为蓝色,B中的澄清石灰水变浑浊,E中的黑色粉末变红,其他装置中未观察到明显的实验现象。
根据以上实验过程和实验现象,回答下列问题:
(1)装置D中盛放的试剂是_______,装置G中盛放的试剂是________。
(2)装置B和C不能颠倒顺序的原因是_________。
(3)写出装置E中发生反应的化学方程式:_________。
(实验结论)
(4)混合气体中含有的气体是_______ (填化学式)。
17.请结合下图回答问题:
(1)仪器名称:②___________。
(2)实验室用氯酸钾和二氧化锰制取并收集O2,可选用发生装置___________(选序号)和收集装置D组合,反应的化学方程式为___________。
(3)实验室制取CO2,CO2可用装置E收集,理由是___________。
(4)实验室使用B或C装置,用块状固体FeS和稀H2SO4反应制取硫化氢:。H2S是有毒气体,能溶于水,其水溶液为氢硫酸。
①“尾气吸收装置”应选择___________(选填“甲”或“乙”)。
②氢氧化钠溶液的作用是___________。
五、计算题
18.为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸恰好完全反应,测得剩余固体的质量为2g(杂质不溶于水也不与酸反应)。请计算:
(1)该赤铁矿中Fe2O3的纯度为_______。
(2)稀盐酸中溶质的质量分数_____。
19.过氧乙酸是一种常用的消毒剂,其说明书的一部分如图所示,回答下列问题:
(1)保存和配制过氧乙酸不宜使用__(填“铁”“玻璃”或“陶瓷”)材料制成的容器。
(2)双氧水和乙酸反应可得到过氧乙酸,该反应的化学方程式为CH3COOH+H2O2=CH3COOOH+X,则X的化学式为__。
(3)用质量分数为40%的过氧乙酸溶液配制8000g质量分数为0.5%的过氧乙酸溶液来浸泡消毒,需要取水__mL(水的密度为1g/mL)。
20.某实验小组同学从碳酸钙、碳酸钠和氯化钠的固体混合物中提取氯化钠,实验操作的一部分流程如下图。请根据图中所提供的数据,回答下列问题:
(1)本实验生成二氧化碳的质量是______g,原固体混合物中碳酸钠的质量是______g。
(2)本实验最终所得不饱和溶液的溶质质量分数是多少?
参考答案
1.C 2.D 3.B 4.D 5.B 6.A 7.A 8.B 9.C 10.A
11. 浓硫酸
12. Fe3O4 置换反应 Fe3+
13.CaCO3 化合反应
14.
改良酸性土壤
15.
(1)CO2的溶解度随温度的降低而增大,凉开水温度低,溶解的CO2较多
(2)AD
(3) 敞口锅中出现较多量晶体 搅拌,防止液体因局部温度过高,造成液滴飞溅
(4)B
16.浓硫酸
17.
(1)集气瓶
(2) A
(3)二氧化碳的密度大于空气
(4) 乙 吸收H2S,防止污染空气
18.
(1)80%
(2)解:设稀盐酸中氯化氢的质量为x。
x=10.95g
稀盐酸中溶质的质量分数为:×100%=10.95%
答:稀盐酸中溶质的质量分数是10.95%。
19.
(1)铁
(2)H2O
(3)7900
20.解:生成二氧化碳质量为20g-5.6g+90g+100g-200g=4.4g
设碳酸钠质量为x,生成氯化钠质量为y
答:(1)4.4;10.6
(2)所得溶液的溶质质量分数为7.75%。
